Single Chromatin Stre t ching Reveals Physically Distinct Population of Dis as sembly Events
description
Transcript of Single Chromatin Stre t ching Reveals Physically Distinct Population of Dis as sembly Events

Single Chromatin StreSingle Chromatin Strettching ching Reveals Physically Reveals Physically
Distinct Population of Distinct Population of DisDisasassembly Eventssembly Events
L. H. Pope, M. L. Bennink, K. A. van Leijenhorst-Groener, D. Nikova, J. Greve, und J. F. Marko
wird präsentiert von Anil Demirata

Gliederung
Hintergrundwissen und Einführung
Material und Methoden
Ergebnisse und Diskussion
Zusammenfassung und Ausblick

GrundkenntisseGrundkenntisse
DNA + Proteine Chromatin Kompaktierung: 104 – 105
Grundeinheit: Nukleosom Es besteht aus:
NCP: nucleosome core particle
Linkerhistonen Linker DNA
Höher geordnete Chromatin Strukturen
http://micro.magnet.fsu.edu/cells/nucleus/images/chromatinstructurefigure1.jpg

Nukleosom
NCP: ist ein Oktamer 1x (H3-H4)2 Tetramer 2x (H2A-H2B) Dimere DNA: ~146 bp um 1,65 mal
Linkerhiston: bindet ein/ausgehende DNA(~160 bp)
Linker DNA: Abstandhalter: (~200 bp)
Chromatin Breite: 11 nm
http://www.bio.miami.edu/dana/104/nucleosome.jpg
http://www.mun.ca/biochem/courses/3107/images/Stryer/Stryer_F37-08.jpg

Höher geordnete Chromatin Strukturen
Auch 30 nm-Fiber genannt Zwei Modelle
Reguläre Spirale Irregulärer Zick Zack
Aktive Form
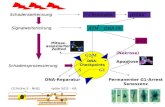
Dynamisch für Rekombination Transkription Reparationsmaschinerie
http://edoc.hu-berlin.de/dissertationen/seitz-stefanie-2004-10-20/HTML/seitz_html_21996ee1.png

wird erreicht durch...
Posttranslationale Modifikationen an den Ausläufern von Histonen: acetyliert (A) phosphoryliert (P) Ändert NCP-NCP
Wechselwirkung (WW) der Grad der
Kompaktierung ist regulierbar durch Schlüsselenzyme
http://chemistry.gsu.edu/faculty/Zheng/nucleosome.jpg

wird erreicht durch (2)...
Änderungen in Ionenkonzentrationen Linkerhistone
die Abschirmung der negativen Ladung des DNA-Rückgrats auch durch basische
nicht-Histon Proteine: HMGs
Polyamine in Chromatin
http://academic.brooklyn.cuny.edu/biology/bio4fv/page/molecular%20biology/dsDNA.jpg

EinführungEinführung
Vorteil der Forschung mit einzelnen Molekülen Untersucht werden
Struktur, Dynamik, Kinetik und Mechanik
von DNA-Protein WW in Zusammenhang mit DNA-Kompaktierung mit den Methoden: AFM, Optical Tweezer und
flow generated forces

drei wichtige Studien Extrahierte individuelle
Chromatinfäden Native
Chromatinfäden Untersucht wird
mechanische Eigenschaften
Bei verschiedenen Salzkonzentrationen
Weniger kompaktes Chromatin in niedrigeren Salzkonzentrationen
Rekonstruierte Chromatinfäden
präzis und reproduzierbar
Strukturelle Informationen
Stretching Zerreißen von
einzelnen Nukleosomen
Individuelle DNA MoleküleDefinierte kurze NukleosomenarrayKeine Linkerhistone
Nukleosomen werden schrittweise gespaltet

Ziel dieser Arbeit
Bestehende Frage: “Wie wird der genetische Code organisiert und zugegriffen?”
Erwartungen: Die Stretching-Bedingungen beeinflussen Zerreißkraft
Hier: bestimmt wird Zerreißkraft (F) und Längenunterschied (ΔL)
jeweils pro mechanisches Zerreißen von Chromatinfaden (Event)
Zerreißkraft Energiebarrieren Längenunterschied Typ des Nukleosomsunterbrechen

Ziel dieser Arbeit (2)
Bestehende Frage: “Wie wird der genetische Code organisiert und zugegriffen?”
Überlegung: DNA-Protein WW müssen irgendwie geändert und/oder unterbrochen werden
Durch Kraftgenerierende Motoren: Polymerasen

MaterialMaterial
12 bp Überhänge von λ-DNA werden ergänzt in der PCR mit bio-11-dUTP und bio-14-dATP Streptavidin bekleidete Polystyrene beads
(Ø=2,6μm)

Methode Methode
1 DNA Molekül zwischen 2 Beads + Xenopus Oozytenextrakt Kompaktion von DNA von 16,4 μm zu 2 μm

Optical trapping 1064 nm
Infrarotlaser O
Micropipette: erlaubt das Bewegen von nicht “getrappten” bead
piezzo-Streckung
Quadrant Detektor: notiert Ablenkung des transmittierten Laserlichts
Kraft ist Direkt proportional zu Δx
Optical trapping

ErgebnisseErgebnisse
Vergrößerung: Einzelne Events
(DNA-Protein WW) ΔL Indiz: welche WW ist
unterbrochen(später)
Hier: Dabei steigt die Kraft F steigt stetig an und dann fällt plötzlich ab
Genereller Verlauf: 1.& 2. Streckung von
rekonstutierter Chromatinfaden
Kraft / Extensions-Kurve Plateau bei 65pN
(wie bei nackten DNA)
Fig2

Statistik
Kraft-Extensions-Kurven mit verschiedenen Chromatinfasern Mit verscheidenen Piezo-
Streckgeschwindigkeiten
Zerreißkraft (F) und Längenunterschied (ΔL)

Analyse
ΔL pro Event Histogramme Multi Gauss Fitting
3 peaks bei 30, 59, und 117 nm
30nm Abwickeln halbes Nukleosoms 59nm und 117nm 1-2 Nukleosom Abwickeln

Fig 3

Applied Dynamic Force Spectroscopy Theory
Betrachtungen: Für jedes Zerreißen: dF/dt aus
dF/dx und Streckgeschwindigkeit v Chromatin: Kette von N in Serie
geschalteten Ereignissen folgende Strecken:
weniger Ereignisse mit höherer Kraft sichtbar
3 Energiebarrieren

Fig 4
Alle
WeitereStrecken
ErstesStrecken

Korrelationen
Um eine Korrelation zwischen Energiebarrieren und Typ von Zerreißen der Nukleosome zu bestimmen
Daten (F) werden sortiert Für korrespondierende Energiebarrieren Graphen F vs ΔL
Eine kleine Korrelation sichtbar

Fig5
25 kBT
28 kBT

DiskussionDiskussion
Chromatin DNA + Xenopus Oozytenextrakt Hier: statt somatischem Linkerhiston H1
embryonisches Linkerhiston B4 Weniger basisch im C-Terminus geöffnete aktive Form
in vitro : physiologisch angeordnete Nuckleosomen (mit 62 nm Abstand)
Längenunterschied korreliert nur mit Abwicklung der Nukleosomen

Warum zwei verteilte Kräfte?Warum verschwindet eine nach der ersten Strecken?
schrittweise 1. B4 sehr mobile, schwach gebundene Proteine 2. H2A-H2B Dimere 3. (H3-H4)2 Tetramer
Höhere Kraft im ersten Strecken: alle Linkerhistone eine Energiebarriere (28kBT)
Niedrige Kräfte 2 Energiebarrieren (25kBT & 20kBT)
gleiche Anzahl von Events für hohe und niedrige Kraft in Natur 28kBT und 25kBT Barrieren möglich
Differenz: 3kBT: Energiebeitrag von B4

Abwicklung von DNA
60 nm: ganzes Nukleosom
30 nm:partielle Abwicklung
3 Modelle
ändert die Konturlänge zwei diskräte ΔL: bei 30nm und 60nm

neues Modell
zuerst: Linkerhiston und schwachgebunde Teile der NCP
dann: übrige Oktamere
zweites Modell
zuerst: Linkerhistone und (H2A-H2B) Dimer dann: übriges Hexamer
K. Klenin, T. Wocjan, J. Langowski (2006)K. Klenin, T. Wocjan, J. Langowski (2006)

zusätzlich
Zuerst Chromatinfaden vollständig strecken (bis auf nackte DNA-Länge)
dann Relaxation, Chromatinfaden zieht sich auf intermediäre Konturlänge zusammen
NCP-Teile nicht vollständing abgelöst
keine Korrelation in der Abfolge der 30nm und 60 nm-Schritte

ZusammenfassungZusammenfassung
Abwicklung von Nukleosomen verläuft in Schritten
30 nm “Halbschritte” in rekonstutiertem Chromatinfaden (hier) und kurzen Nukleosomenarrays (Brower-Toland et al.)
3 Energiebarrieren Für folgende Streckzyklen: Events zu 28kBT Energiebeitrag des B4 Linkerhistons: 3kBT

Zusammenfassung 2
diese Barrieren Hindernis beim Zugriff auf den genetischen Code
kraftausübende Motoren (Polymerasen) Torsionkräfte auf DNA durch Polymerasen
können zum Öffnen des Chromatins beitragen
Nukleosomen können abgewickelt und dann wieder hergestellt werden.
Traskription ist bei (H3-H4)2 nicht gestört

AusblickAusblick
Ersetzen oder Ausnehmen von Faktoren im Extrakt
B4 gegen H1 tauschen oder “abschalten” Rekombinante Histone
Effekte von (A) & (P) vortäuschen Histone ohne Ausläufer(tails) Effekt von HMGs? Studien mit einzelnen Molekülen: erweitert den
Einblick

Vielen Dank für Ihre Aufmerksamkeit
Fragen??
Anregungen??
Beschwerden??