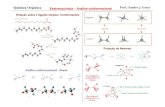
Isomería conformacional Carmen Coronel Química Orgánica I Instituto de Química Orgánica Fac. de...
-
Upload
ximenez-la-madrid -
Category
Documents
-
view
229 -
download
0
Transcript of Isomería conformacional Carmen Coronel Química Orgánica I Instituto de Química Orgánica Fac. de...

Isomería conformacional
Carmen CoronelQuímica Orgánica I
Instituto de Química OrgánicaFac. de Bioquímica, Química y Farmacia Universidad
Nacional de Tucumán

Isómeros
Son compuestos que presentan la misma fórmula molecular, pero propiedades físicas y/o químicas distintas.

Cis-trans
Clasificación
Isomería
Constitucional o estructural
Estereoisomería
De cadena
De posición
De función
En C=C
Conformacional
Óptica
En ciclos

Isómeros constitucionales
Los isómeros constitucionales o
estructurales son los compuestos que a
pesar de tener la misma fórmula molecular
difieren en el orden en que están conectados
los átomos, es decir, tienen los mismos
átomos conectados de forma diferente
(distinta fórmula estructural).

Isómeros de cadena
Los isómeros de cadena son compuestos
que tienen distribuidos los átomos de
carbono de la molécula de forma
diferente. Por ejemplo, existen 3
isómeros de fórmula molecular C5H12.
pentano CH3CH2CH2CH2CH3
2-metilbutano (isopentano)
CH3CHCH2CH3
CH3CH3 C CH3
CH3
CH3
2,2-dimetilpropano (neopentano)

Isómeros de posición
Son compuestos que tienen las mismas
funciones químicas, pero sobre átomos de
carbono con números localizadores
diferentes.
CH3CH2CH2CH2OH
1-butanol
CH3CHCH2CH3
OH
2-butanol
CH3CCH2CH2CH3 O
2-pentanona
CH3CH2CCH2CH3
O
3-pentanona

Isómeros de función
Son compuestos de igual fórmula molecular
que presentan funciones químicas
diferentes.
C3H8O O CH2CH3 CH3
etil metil éter
CH3CH2CH2OH
1-propanol
C3H6O C CH3CH3
O
propanona
C HCH2
OCH3
propanal

Estereoisómeros
Los estereoisómeros son los isómeros cuyos átomos están conectados en el mismo orden, pero con disposición espacial diferente.
La estereoquímica estudia a las moléculas en tres dimensiones.

Conformaciones
Conformaciones son las distintas estructuras de
un mismo compuesto que surgen como resultado
de la “libre rotación” de los enlaces simples y la
flexilibilidad de los ángulos de enlace.
O O
H
H
O O
H H

Análisis conformacional
El análisis conformacional es el estudio de las energías de las diferentes conformaciones. (Wade)
El análisis conformacional es el estudio de la forma en la que los factores conformacionales afectan la estructura de una molécula y sus propiedades físicas y biológicas.
(Carey)

Proyecciones de Newman
Representaciones de moléculas orgánicas
H
HHH
H H
Carbono frontal
Carbono posterior

H
H H
HH
HH
HHH
HH
Caballete Tridimensional
Representaciones de moléculas orgánicas

Conformaciones del etano
H
HHH
H H
Enlace sp3-sp3
“Libre rotación” alrededor del enlace diferentes conformaciones

Estructura de los alcanos lineales
Debido a la estructura del átomo de carbono los alcanos lineales adoptan la conformación más estable que es la alternada (forma de zig-zag) porque es la más estable.

Quiralidad

Quiralidad
Quiralidad (del griego Cheir que significa mano) es la propiedad que tienen ciertos objetos de poder existir bajo dos formas que son imágenes especulares una de otra y que no se pueden superponer.

Quiralidad
Pendiente (+)
Pendiente (-)
a)

Quiralidad
El término quiral se aplica también a las moléculas. Las moléculas quirales se diferencian de las aquirales en que presentan actividad óptica. La actividad óptica es la propiedad de desviar el plano de la luz polarizada. Este tema es de gran interés debido a que en los seres vivos las moléculas quirales se encuentran ampliamente distribuidas.

Quiralidad
Son quirales los hidratos de carbono, los aminoácidos (excepto la glicina) que forman las proteínas, algunos lípidos, etc.
En la naturaleza se encuentra presente generalmente una de las formas quirales. Por lo tanto, las consecuencias pueden ser impre-visibles cuando un ser vivo se enfrenta a una molécula que tiene la forma opuesta a la que existe en la naturaleza o para la que está preparado. Se recuerda el caso tristemente célebre de la talidomida.

Quiralidad
N
O
O
N
O
O
H
H
N
O
O
N
O
O
H
H
(S) (R)
Enantiómeros de la Talidomida.

Quiralidad
La importancia del tema es tal que en el año 2001 el premio Nobel de Química le dieron a W. Knowles y R. Noyori por el desarrollo de catalizadores para hidrogenaciones asimétricas y a K. Sharpless por la oxidación asimétrica de alcoholes alílicos.

La actividad óptica es una propiedad que se mide en el polarímetro.
Si el estereoisómero hace girar el plano de la luz hacia la derecha (sentido horario) se denomina dextrógiro, y si lo hace girar hacia la izquierda (sentido antihorario) se denomina levógiro.
Quiralidad
Dextrógiro: del latín dexter, “derecho”Levógiro: del latín laevus, “izquierdo”

No sólo se puede determinar el sentido del giro sino también la magnitud del mismo, que es el número de grados que se debe rotar el analizador.
Según las reglas de la IUPAC, se emplean los símbolos + para indicar que una sustancia es dextrógira y – para indicar que es levógira. Se utilizan también los símbolos d y l respectiva-mente.
Quiralidad

Ácido D-(-)-lácticoÁcido (R)-2-hidroxipropanoico
Quiralidad
Ácido L-(+)-lácticoÁcido (S)-2-hidroxipropanoico

La rotación específica [] de un compuesto se define como la rotación que se observa cuando se utiliza una celda para la muestra de 10 cm (1 dm) de camino óptico y una concentración de 1 g/mL. Se puede utilizar otras longitudes de celdas y otras concentraciones, pero la rotación observada () se divide entre el producto de la longitud de la celda (l) y la concentración (c).
Rotación específica
[] = (observada)l . c

Un haz luminoso se propaga en diferentes ángulos o planos con respecto a la dirección de propagación, y si se observara en forma frontal en el sentido de la propagación, se vería como la figura A .
Cuando se eliminan todos los planos, excepto uno de ellos , entonces se obtiene luz polarizada en el plano (Fig. B).
Luz normal y Luz polarizada

Luz natural
Luz polarizada

Polarímetro
Un polarímetro mide la rotación de la luz polarizada.

La luz se origina en una fuente (generalmente una lámpara de sodio), y pasa a través de un polarizador y la celda de muestra. La luz de una lámpara de sodio pasa a través de un filtro que selecciona la luz amarilla de emisión (la línea D) El filtro analizador es otro polarizador equipado con un transportador angular; se gira hasta que se observa la máxima cantidad de luz y la rotación se lee en el transportador.
Diagrama esquemático de un polarímetro

Esta luz polarizada pasa por la celda de muestra que contiene una solución del compuesto que se está analizando. Solamente los compuestos quirales tienen actividad óptica y pueden girar el plano de la luz polarizada. La luz que atraviesa la celda de muestra pasa a continuación a través de un segundo filtro polarizador y se determina la magnitud y la dirección de la rotación óptica.
Diagrama esquemático de un polarímetro

Elementos de simetría
Los elementos de simetría son entes geométricos, como ser un punto, una recta o un plano alrededor del cual se puede efectuar una operación de simetría.
Una operación de simetría consiste en mover un cuerpo respecto de alguno de los elementos de simetría de manera de llevarlo a una configuración indistinguible de la original.

Elementos de simetría
Plano ()
La operación de simetría asociada a un plano de simetría es la reflexión. Un plano de simetría divide en dos partes iguales a una molécula.
CH3
CH3CH3
CH3

Una molécula es aquiral cuando posee alguno de los elementos de simetría: plano (), centro de inversión (i) o eje impropio (Sn)
Una molécula quiral no posee dichos elementos.
Condiciones de quiralidad

Para la mayoría de las moléculas orgánicas basta una sola prueba para comprobar si existe o no quiralidad: la presencia del plano de simetría.
Condiciones de quiralidad
Las moléculas quirales no tienen ningún plano de simetría.

Condiciones de quiralidad
Elementos de simetría: 1
Molécula simétrica: Tiene un plano de simetría, por lo tanto es aquiral.
Bromoclorometano
Cl
12
Br

Condiciones de quiralidad
No tiene elementos de simetría. Molécula asimétrica, no tiene plano de simetría, por lo tanto es quiral.
Bromocloroyodometano

La presencia de un carbono quiral no es condición necesaria ni suficiente para la quiralidad de una molécula.
Átomos estereogénicos
Carbono quiral o estereogénico (C*): Se encuentra unido a 4 sustituyentes distintos.
Carbono quiral

Enantiómeros
Los estereoisómeros que son imágenes especulares no superponibles reciben el nombre de enantiómeros.
enantiómeros
espejo

Enantiómeros
Aunque pueda superponer algunos átomos, siempre hay otros que no se superponen.

Enantiómeros
Los enantiómeros tienen las mismas propiedades físicas (p.f., p.eb.), excepto en el sentido hacia el que hacen girar el plano de luz polarizada.
Los enantiómeros hacen girar el plano de luz polarizada la misma cantidad de grados (igual magnitud), pero en sentido contrario. (R)-2-bromobutano (S)-2-bromobutano
Punto de ebullición ºC 91,2 91,2
Punto de fusión ºC -112 -112
Índice de refracción 1,436 1,436
Densidad 1,253 1,253
[] +23,1 -23,1

Nomenclatura R,S
La Nomenclatura R,S se utiliza para determinar la configuración absoluta de los carbonos quirales. Para determinar si una molécula es R ó S se procede de la siguiente manera:

1. Se observan los átomos que están directamente unidos a cada carbono quiral y se establece un orden de prioridad siguiendo las reglas de Cahn, Ingold y Prelog (reglas CIP).
Nomenclatura R,S
F
H ClBr 1
2
3
4

Nomenclatura R,S
2. Una vez determinadas las prioridades, se dispone la molécula (mentalmente, en el papel o mediante modelos moleculares) de manera que el sustituyente de menor prioridad se encuentre lo más alejado posible del observador.
F
H ClBr 1
2
3
4
F
BrCl12
3

Nomenclatura R,S
3. Si al recorrer con la vista los sustituyentes se lo hace siguiendo el sentido de las agujas del reloj la configuración es R, si es en sentido contrario a las agujas de reloj la configuración es S.
R S
Sentido horario
R: Del latín rectus, “derecha”.S: Del latín sinister, “izquierda”
Sentido antihorario
F
BrCl12
3F
Br Cl1 2
3

Reglas de Cahn, Ingold y Prelog
1. De los átomos unidos directamente al carbono quiral tiene prioridad el de mayor número atómico (Z).
Así por ejemplo:
I > Br > Cl > S > P > Si > F > O > N > C > H
En caso de isótopos tiene prioridad el de mayor masa atómica.
3H > 2H > 1H

Reglas de Cahn, Ingold y Prelog
Ejemplo:
CH3
H IBr 2
1
3
4
Cl
F HCH3
3
1
2
4

HO H
*2
Reglas de Cahn, Ingold y Prelog
2. Si hay átomos iguales unidos directamente al carbono quiral se consideran los átomos siguientes hasta que se encuentre una diferencia.
C CH3
CH3
H
C CH2
H
H
CH3>
1
3
4
(S)-2-metil-3-hexanol Este carbono tiene unido 2 C (mayor
Z) y 1 H
Este carbono tiene unido 1 C y 2 H

Reglas de Cahn, Ingold y Prelog
3. Se considera que los átomos unidos con enlaces múltiples son equivalentes al mismo número de átomos unidos con enlaces sencillos.
C CH
H
C
C
H
CH2 CH equivale a
C C H equivale a C C
C
C
H
C
C

Reglas de Cahn, Ingold y Prelog
Como si estuvieraunido a O, O, H
Como si estuvieraunido a C, C
equivale aC O
H
C O
O
H
C
21
3
4 R12
3
CH2OH
CHOH
HO
OH
CH2OH
H
C H
O CH2OH
OHOHC

Ejemplos
CBr
H
COOH
CH3
ácido (S)-2-bromopropanoico
C
Br
H COOHH3C
ácido (R)-2-bromopropanoico
2
13
43
1
24
OH
COOH
Ácido (2S,3E)-3-metil-3-hidro- xi-2-pentenoico
C CHO
CH3
H2N
H
(R)-2-aminopropanal
2
1
3
4 2
1
3
4

Configuración y rotación
En el laboratorio se puede medir una rotación y ver si una sustancia es (+) o (-). En el papel, se puede determinar si a una representación determinada se nombra como (R) o (S). No se puede predecir si una estructura que llamamos (R) será dextrógira o levógira. De la misma manera no se puede predecir si una sustancia dextrógira en un matraz tendrá configuración (R) o (S).

Si una molécula tiene un único carbono
quiral, sólo puede existir un par de
enantiómeros.
En general, una molécula con n carbonos
quirales tiene un número máximo de 2n
estereoisómeros posibles, donde n es el
número de carbonos quirales.
Número de estereoisómeros

Compuestos con más de un centro quiral
C
C
HO CH3
CH3Br
H
H
C
C
OHH3C
H3C Br
H
H
El 3-bromo-2-butanol tiene 2 carbonos quirales por lo que el número máximo de estereoisómeros es 4 (22 = 4).
S
R S
R
Los enantiómeros tienen configuraciones opuestas en todos los centros quirales.
enantiómeros
(2S,3R)-3-bromo-2-butanol
(2R,3S)-3-bromo-2-butanol

Compuestos con más de un centro quiral
Para dibujar los otros estereoisómeros se deja igual un centro quiral y se modifica el otro.
C
C
HO CH3
CH3H
H
Br
C
C
OHH3C
H3C H
H
Br
S R
S R
enantiómeros
(2S,3S)-3-bromo-2-butanol
(2R,3R)-3-bromo-2-butanol

Diastereómeros
Los estereoisómeros que no son imágenes especulares se denominan diastereómeros.
Los diastereómeros tienen propieda-des físicas diferentes.
Tienen por lo menos un centro quiral con configuración diferente.

Diastereómeros
Flechas horizontales: enantiómerosFlechas verticales y oblicuas: diastereómeros
C
C
HO CH3
CH3Br
H
H
C
C
OHH3C
H3C Br
H
H
C
C
HO CH3
CH3H
H
Br
C
C
OHH3C
H3C H
H
Br
S
R S
R
R
R
S
S

Compuestos meso
Se denominan compuestos meso a
aquéllos que, a pesar de tener carbonos
quirales, son aquirales (no tienen
actividad óptica) porque poseen un
plano de simetría.

Compuestos meso
Estas dos estructuras del 2,3-butanodiol son imágenes especulares y no pueden superponerse, por lo tanto, son enantiómeros
C
C
HO CH3
CH3H
H
HO
C
C
OHH3C
H3C H
H
OH
SRS
R
(2S,3S)-2,3-butanodiol (2R,3R)-2,3-butanodiol

Compuestos meso
Estas dos estructuras del 2,3-butanodiol son imágenes especulares, pero pueden superponerse, por lo tanto, NO son enantiómeros, sino que se trata del mismo compuesto. Es el compuesto meso.
Por lo tanto, sólo hay 3 estereoisómeros del 2,3-butanodiol: el par de enantiómeros y el compuesto meso.
C
C
HO CH3
CH3HO
H
H
C
C
OHH3C
H3C OH
H
H
Plano de simetría
S
R
Rotación de 180º en el plano del papel.

Mezcla racémica
Se denomina mezcla racémica o racemato, a aquélla que contiene un par de enantiómeros en una proporción del 50% de cada uno. Esta mezcla no tiene actividad óptica.
Por ejemplo: El 2-butanol racémico se denomina (±)-2-butanol o (d,l)-2-butanol.

Proyecciones de Fischer
Los cuatro enlaces de un carbono quiral se representan por una cruz.
El carbono quiral queda en el centro del plano del papel.
Líneas horizontales: enlaces delante del plano.Líneas verticales: enlaces detrás del plano.
equivale a

Transformación de fórmulas en perspectivas a proyecciones en el plano
OH
COOH
CH3
H
Ácido D-láctico
C OHH
COOH
CH3
COOH
COHH3C
H
D-gliceraldehído L-gliceraldehído
CHO
COHHOH2C
H
OH
CHO
CH2OH
H=
CHO
CHO CH2OH
H
HO
CHO
CH2OH
H=

Nomenclatura D,L
• Se utiliza para describir la estereoquímica (configuración) inherente a las proyecciones de Fischer.• La cadena principal de átomos de C se dispone verticalmente y de manera que el átomo de carbono en el estado de oxidación más alto quede situado en el extremo superior .
R
R'
Carbono en estado de oxidación más alto.

Nomenclatura D,L
• Si el grupo -X del último C quiral está a la derecha el compuesto es D y si está a la izquierda es L.
CHO
H OH
CH2OH
+1
-1D-gliceraldehído
COOH
H2N H
CH3
+3
-3L-alanina
D-manosa
CHO
HHO
HHO
OHH
OHH
CH2OH
CHO
H OH
HO H
HO H
CH2OHL-arabinosa

Epímeros
Son los estereoisómeros que difieren en la configuración de un sólo centro quiral.
CHO
HHO
HHO
OHH
OHH
CH2OH
CHO
HHO
HHO
HHO
OHH
CH2OHD-manosa D-talosa
Epímeros de C 4
Epímeros de C 3
CHO
HHO
OHH
OHH
CH2OH
CHO
HHO
HHO
OHH
CH2OH

Estereoisómeros
Estereoisómeros
Enantiómeros
Diastereómeros
Epímeros
Anómeros

Por ejemplo, los isómeros configuracionales de la carvona poseen diferente olor.
Consecuencias de la estereoquímica molecular
El (-)-monoglutamato de sodio es un agente químico que se usa para dar sabor a la carne, pero el isómero (+) no tiene sabor.
O
()-carvona
COOH
H2N H
CH2CH2COO-Na+
(-)-monoglutamato

Penicilium glaucum sólo metaboliza a la forma dextrógira de los ácidos tartáricos.
Consecuencias de la estereoquímica molecular
COOH
H OH
COOH
HO H
COOH
HHO
COOH
OHH
Ácido (+)-tartárico Ácido (-)-tartárico
Las sales de ácido tartárico fueron los primeros compuestos quirales aislados porque es una de las pocas especies químicas que cristaliza en forma de imágenes especulares para cada enantiómero. Este descubrimiento fue realizado por Pasteur.

Bibliografía
Carey, F. Química Orgánica. Ed. Mc Graw Hill. 6° ed. 2006.
Vollhardt, K., Schore, N. Química Orgánica. Ed. Omega, S.A. 3° ed. 2000.
Wade, L.G. Jr Química Orgánica.Ed. Pearson, 5º Ed. 2004.