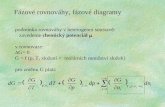Chemické a fázové rovnováhy v heterogenních systémech
description
Transcript of Chemické a fázové rovnováhy v heterogenních systémech

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
1
Chemické a fázové rovnováhyChemické a fázové rovnováhyv heterogenních systémechv heterogenních systémech
http://www.vscht.cz/ipl/osobni/leitner/prednasky/fchr/FCHR.htmhttp://www.vscht.cz/ipl/osobni/leitner/prednasky/fchr/FCHR.htm
33.1 Podmřížkový model – základní modelové představy.1 Podmřížkový model – základní modelové představy
33.2 Roztoky stechiometrických sloučenin – substituce na jedné .2 Roztoky stechiometrických sloučenin – substituce na jedné podmřížce (typ (A,B)podmřížce (typ (A,B)aaCCcc) )
33.3 Roztoky stechiometrických sloučenin – substituce na dvou .3 Roztoky stechiometrických sloučenin – substituce na dvou podmřížkách (typ (A,B)(C,D)) podmřížkách (typ (A,B)(C,D))
33.4 Intersticiální tuhé roztoky (typ AC.4 Intersticiální tuhé roztoky (typ AC1-1-δδ))
33.5 Příklady.5 Příklady

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
2
Podmřížkový modelPodmřížkový modelpro popis uspořádaných pevných roztokůpro popis uspořádaných pevných roztoků
Wagner & Schottky (1930), Bragg & Williams (1934,1935)Sublattice Model – SM (Hillert & Staffansson, 1970)
Compound Energy Model – CEM (Hillert et al., 1986)
PoužitíPoužití Uspořádané intermetalické fáze: γ’-Ni3Al, σ-fáze v systémech Cr-Fe, Re-W, …, Lavesovy fáze v systémech Cu-Mg, Mg-Ni, … Roztoky stechiometrických sloučenin: (Ca,Sr)O, (Ni,Fe)Cr2O4, (Ga,In)(As,Sb), … Nestechiometrické sloučeniny: “makro” - SrMnO3-δ, “mikro” – bodové defekty v GaAs, Intersticiální pevné roztoky: TiC1-δ, (U,Pu)N1-δ, …

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
3
Základní modelové představy: Krystalová mřížka je rozdělena na tzv. podmřížky (sublattices), které
jsou obsazovány různými atomy resp. ionty. Při vzniku pevného roztoku se mísí na jednotlivých podmřížkách
ekvivalentní atomy resp. ionty, jejichž koncentrace je vyjádřena tzv. podmřížkovými molárními zlomky (site fractions).
Každou z podmřížek lze chápat jako běžný substituční roztok, přičemž uspořádání atomů resp. iontů v rámci podmřížek je zcela nahodilé.
Makroskopickými složkami roztoku (end-members) jsou reálné či hypotetické “sloučeniny“ (compounds), vytvořené kombinací atomů resp. iontů na jednotlivých pormřížkách.
NaCl(B1)NaCl(B1) 2 x FCC2 x FCC((A1A1))

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
4
Dále jsou odvozeny vztahy pro integrální a parciální molární Gibbsovu energii různých typů pevných
roztoků. Pro lepší orientaci je vždy dodrženonásledující schéma:
1. Jsou definovány podmřížky, mikro- a makrosložky roztoku.2. Je provedena látková bilance (celková látková množství
mikrosložek na jedné a druhé podmřížce jsou označována n’ resp. n’’, látková množství makrosložek n) a odvozeny vztahy mezi podmřížkovými molárními zlomky (y resp. z) a molárními zlomky makrosložek (x).
3. Jsou zapsány vztahy pro integrální Gibbsovu energii (celkovou a molární) ve tvaru
4. Jsou odvozeny vztahy pro parciální molární Gibbsovy energie (chemický potenciál) jednotlivých složek roztoku.
Poznámka: pro vyjádření dodatkové Gibbsovy energie je pro jednoduchost vždy použit model regulárního roztoku.
ref M,id EG G G G

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
5
I.I. Roztok typu (A,B) – běžný substituční roztok Roztok typu (A,B) – běžný substituční roztok
11
22
33
44
Jedna podmřížka, mikrosložky A a B na jedné podmřížce, makrosložky A a B
A A B B
A A B B
n n n n n n
x y x y
ref M,id E
o oA m B m A A B B A-B A B(A) (B) + ln ln
G G G G
n G n G RT n y n y n L y y
m
o oA m B m A A B B A-B A B(A) (B) + ln ln
G G n
x G x G RT x x x x L x x
2oA m A A-B A(A) (A) ln 1G G RT x L x

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
6
II.II. Roztok typu (A,B)C Roztok typu (A,B)C
11
22
33
44
Dvě podmřížky, mikrosložky A a B na jedné podmřížce, C na druhé podmřížce, makrosložky AC a BC
AC A BC B AC BC C
AC A BC B
n n n n n n n n n n
x y x y
ref M,id E
o o CAC m BC m A A B B A-B A B(AC) (BC) + ln ln
G G G G
n G n G RT n y n y n L y y
m
o o CAC m BC m AC AC BC BC A-B AC BC(AC) (BC) + ln ln
G G n
x G x G RT x x x x L x x
2o CAC m AC A-B AC(AC) (AC) ln 1G G RT x L x

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
7
III.III. Roztok typu (A,B) Roztok typu (A,B)aaCCcc
11
22
33
44
Dvě podmřížky, mikrosložky A a B na jedné podmřížce, C na druhé podmřížce, makrosložky AaCc a BaCc
a c a c a c a c
a c a c
A C A B C B A C B C
A C A B C B
Cn n a n n a n n n c n n a n c
x y x y
a c a c
ref M,id E
o o CA C m a c B C m a c A A B B A-B A B(A C ) (B C ) + ln ln
G G G G
n G n G RT n y n y n L y y
a c a c a c a c a c a c a c a c
m
o o CA C m a c B C m a c A C A C B C B C A-B A C B C(A C ) (B C ) ln ln
G G n
x G x G aRT x x x x aL x x
a c a c a c
2o Ca c A C m a c A C A-B A C(A C ) (A C ) ln 1G G aRT x aL x

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
8
III.III. Roztok typu (A,B) Roztok typu (A,B)aaCCcc - - pokračovánípokračování
a c
a c a c
M,ida c A C
idA C A C
(A C ) lna
G aRT x
a x
Při míšení na jedné podmřížce pro a = 1 jsou vztahy pro termodynamické funkce odvozené v rámci podmřížkového modelu formálně shodné se vztahy pro substituční roztok složek ACc, BCc, …
0.0 0.2 0.4 0.6 0.8 1.00.0
0.2
0.4
0.6
0.8
1.0
A4C
c
A2C
c
ACc
a(A
aC)
x(AaC)

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
9
IIVV.. Roztok typu (A,B) Roztok typu (A,B) ((CC,D),D)tzv. reciproké systémytzv. reciproké systémy
11
22
Dvě podmřížky, mikrosložky A a B na jedné, mikrosložky C a D na druhé podmřížce, makrosložky AC, AD, BC a BD
AC AD A BC BD B AC BC C AD BD D
A AC AD B BC BD C AC BC D AD BD
n n n n n n n n n n n n
n n n
y x x y x x z x x z x x
Problém:
Přepočtové vztahy mezi xij (tři nezávislé proměnné) a yi, zj (dvě nezávisle proměnné) nejsou jednoznačné
M ( , )mG f y z

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
10
IIVV.. Roztok typu (A,B) Roztok typu (A,B) ((CC,D) - ,D) - pokračovánípokračování
0 10
1
(A1-y
By)(C
1-zD
z)
BC
AD BD
AC
z (z
D)
y (yB)
0 10
1
(A1-y
By)(C
1-zD
z)
BC
AD BD
AC
z (z
D)
y (yB)
0 10
1
(A1-y
By)(C
1-zD
z)
BC
AD BD
AC
z (z
D)
y (yB)
1- 1-AC BD (A B )(C D )y y z z
1- 1-AD BC+BD (A B )(C D )y y z z
1- 1-AC+AD BC+BD (A B )(C D )y y z z

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
11
IIVV.. Roztok typu (A,B) Roztok typu (A,B) ((CC,D),D)tzv. reciproké systémytzv. reciproké systémy
22 AC AD A BC BD B AC BC C AD BD D
A AC AD B BC BD C AC BC D AD BD
AC BC
AD BD
AC A C BC B C AD A D BD B D
volíme:
n n n n n n n n n n n n
n n n
y x x y x x z x x z x x
x x
x x
x y z x y z x y z x y z

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
12
IIVV.. Roztok typu (A,B) Roztok typu (A,B) ((CC,D) - ,D) - pokračovánípokračování
0 10
1
(A1-y
By)(C
1-zD
z)
BC
AD BD
AC
z (z
D)
y (yB)

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
13
IIVV.. Roztok typu (A,B) Roztok typu (A,B) ((CC,D) - ,D) - pokračovánípokračování
33
ref M,id E
o o o oAC m BC m AD m BD m
A A B B C C D D
C D A BC A-B A B D A-B A B A C-D C D B C-D C D
(AC) (BC) (AD) (BD)
ln ln ln ln
G G G G
n G n G n G n G
RT n y n y RT n z n z
n z L y y z L y y n y L z z y L z z
m
o o o oA C m B C m A D m B D m
A A B B C C D D
C D A BC A-B A B D A-B A B A C-D C D B C-D C D
(AC) (BC) (AD) (BD)
ln ln ln ln
G G n
y z G y z G y z G y z G
RT y y y y RT z z z z
z L y y z L y y y L z z y L z z
Z důvodů zjednodušení dalších matematických úprav vyjádříme molární Gibbsovu energii jako funkci podmřížkových molárních zlomků y a z místo molárních zlomků makrosložek x.
NGa-In
PGa-In
AsGa-In
SbGa-In
31,5 kJ/mol
14,6 kJ/mol
12,6 kJ/mol
7,9 kJ/mol
L
L
L
L

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
14
IIVV.. Roztok typu (A,B) Roztok typu (A,B) ((CC,D) - ,D) - pokračovánípokračování
44
m mAC m
m m mAD m AC
m m mBC m AC
m m mBD m AC
(AC)
(AD) 1
(BC) 1
(BD) 1 1
G GG G y z
y z
G G GG G y z
y z z
G G GG G y z
y z y
G G GG G y z
y z
mG
y z
Označme y = yB (yA = 1- y), z = zD (zC = 1- z). Platí:
m m mm m( ) ij
ij ij ij ij
G G GG y zG ij G n G n
n n y n z n

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
15
IIVV.. Roztok typu (A,B) Roztok typu (A,B) ((CC,D) - ,D) - pokračovánípokračování
o o EAC m r
o o EAD m r
o o EBC m r
o o EBD m r
(AC) (AC) ln(1 ) ln(1 ) (AC)
(AD) (AD) 1 ln ln(1 ) (AD)
(BC) (BC) 1 ln(1 ) ln (BC)
(BD) (BD) 1 1 ln ln (BD)
G G yz G RT y RT z G
G G y z G RT y RT z G
G G y z G RT y RT z G
G G y z G RT y RT z G
Označme Platí:
E C A D BA-B C-D A-B C-D
E D A C BA-B C-D A-B C-D
E C B D AA-B C-D A-B C-D
E
(AC) 1 1 1 2 1 2
(AD) 1 1 1 1 2 1 2 1
(BC) 1 1 1 1 1 2 2 1
(
G z y y z yL zL yz y L z L
G z y yz yL z L y z y L z L
G yz z y y L zL y z y L z L
G
D B C AA-B C-D A-B C-DBD) 1 1 1 1 1 1 1 2 1 2y z y z y L z L y z y L z L
o o o o or m m m m(AC) (BD) (AD) (BC)G G G G G

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
16
IV.IV. Roztok typu (A,B) Roztok typu (A,B) (C,D) - (C,D) - pokračovánípokračování
termodynamická stabilitatermodynamická stabilita
2or
or
1
1 1
4
G
RT y y z z
G
RT
Podmínka termodynamické stability:2 2
m m2
2 2m m
2
0
G G
y y z
G G
z y z
Předpoklad ideálního směšovánína obou podmřížkách:
2or 1
1 1
G
RT y y z z
Spinodála 0 10
1
rGo/RT = 10
rGo/RT = 5
rGo/RT = 4,1
BC
AD BD
AC
z
y

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
17
V.V. Intersticiální rIntersticiální roztok typu ACoztok typu AC1-1-δδ
Intersticiální pevné roztoky vznikají tak, že v definovaných polohách (dutinách) mřížky prvku s většími atomy se zabudovávají menší atomy rozpouštěného prvku. Tyto polohy lze chápat jako podmřížku, na které dochází k nahodilému míšení atomů a vakancí (označení Va).
Dvě podmřížky, mikrosložky A na jedné podmřížce, C a Va na druhé podmřížce – A(C,Va), makrosložky AC a A
1 mol roztoku AC1-δ představuje:
{{1 mol A + (1-1 mol A + (1-δδ) mol C) mol C}} resp. resp. {{δδ mol A + mol A + (1-(1-δδ) mol AC) mol AC}}
11
22 AC C A Va
AC C A Va
n n n n n n
x y x y

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
18
V.V. Intersticiální rIntersticiální roztok typu ACoztok typu AC1-1-δδ - - pokračovánípokračování
33
ref M,id E
o o AAC m A m C C Va Va C-Va C Va(AC) (A) + ln ln
G G G G
n G n G RT n y n y n L y y
m AC A
o o AAC m A m AC AC A A C-Va AC A(AC) (A) + ln ln
G G n n
x G x G RT x x x x L x x
Molární Gibbsova energie vztažená na 1 mol (AC+A):
Molární Gibbsova energie vztažená na 1 mol (A+C):
Platí: 1 mol (AC+C) = (1 + xAC) mol (A+C)
AC Cm A C m m AC
A C
o o AAC AC AC AA Am m AC A C-Va
AC AC AC AC AC
1
(AC) (A) + ln ln1 1 1 1 1
n nG G n n G G x
n n
x x x xx xG G RT x x L
x x x x x

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
19
V.V. Intersticiální rIntersticiální roztok typu ACoztok typu AC1-1-δδ - - pokračovánípokračování
44
A
AC
2o AAC m AC C-Va AC
AC , ,
2o AA m A C-Va A
A , ,
(AC) (AC) ln 1
(A) (A) ln 1
T p n
T p n
GG G RT x L x
n
GG G RT x L x
n
Chemické potenciály složek v roztoku (AC+A):
A
C
2o o ACC m m C-Va C
C C, ,
o A 2A m C C-Va C
A , ,
(C) (AC) (A) ln 1 21
(A) (A) ln 1
T p n
T p n
yGG G G RT L y
n y
GG G RT y L y
n
Chemické potenciály složek v roztoku (A+C):

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
20
Příklad Příklad 11::Komplexní spinel (FeKomplexní spinel (Fe22++)(Fe)(Fe3+3+,Cr,Cr3+3+))22OO44
11Ideální strukturu spinelu lze interpretovat jako FCC mřížku obsazenou anionty O2-, ve které je každá osmá tetraedrická dutina obsazena kationtem Me2+ a každá druhá oktaedrická dutina kationtem Me3+. Skutečnost, že magnetit, jako jedna z dále uvedených makrosložek, vykazuje tzv. inverzní strukturu v dalším odvození zanedbáme.
Tři podmřížky, mikrosložky Fe3+ a Cr3+ na jedné podmřížce, Fe2+ na druhé podmřížce a O2- na třetí podmřížce, makrosložky FeFe2O4 (magnetit) a FeCr2O4 (chromit).
22
FFO F3 FCO C3
FFO F3 FCO C3
2 2 2n n n n n n
x y x y
Označení: Fe2+ = F2, Fe3+ = F3, Cr3+ = C3 FeFe2O4 = FFO, FeCr2O4 = FCO
KomentářKomentář

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
21
0,0 0,2 0,4 0,6 0,8 1,00,0
0,2
0,4
0,6
0,8
1,0
a = x2
A. Petric, K.T. JacobJ. Am. Ceram. Soc. 65 (1982) 117-123
T = 1673 K
a(F
e 3O4)
x(Fe3O
4)
Příklad Příklad 1 - 1 - pokračovánípokračování
Komplexní spinel (FeKomplexní spinel (Fe22++)(Fe)(Fe3+3+,Cr,Cr3+3+))22OO44
33
44
ref M,id E
o o FeFFO m FCO m F3 F3 C3 C3 Fe-Cr F3 C3(FFO) (FCO) + ln ln
G G G G
n G n G RT n y n y n L y y
m
o o FeFFO m FCO m FFO FFO FCO FCO Fe-Cr FFO FCO(FFO) (FCO) 2 ln ln 2
G G n
x G x G RT x x x x L x x
2o FeFFO m FFO Fe-Cr FFO(FFO) (FFO) 2 ln 2 1G G RT x L x
2o FeFCO m FCO Fe-Cr FCO(FCO) (FCO) 2 ln 2 1G G RT x L x
V případě ideálního chování platí: 2 2
FFO FFO FCO FCOa x a x

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
22
Příklad 2:Příklad 2:Nestechiometrická fáze SrMnONestechiometrická fáze SrMnO3-3-δδ
11Nestechiometrickou fázi SrMnO3-δ můžeme zapsat na základě podmřížkového modelu vzorcem (Sr2+)(Mn3+,Mn4+)(O2-,Va)3. Jedna podmřížka je obsazována kationty Mn3+ a Mn4+, druhá anionty kyslíku s vakancemi, jejichž koncentrace je s ohledem na elektroneutralitu systému dána obsahem Mn3+. Třetí podmřížka je zcela zaplněna ionty Sr2+.Podmřížkový model se substitucí na dvou podmřížkách formálně vede ke čtyřem makrosložkám. Ty jsou v tomto případě hypotetické (nejsou elektroneutrální), a proto je další postup zjednodušen volbou pouze dvou reálných makrosložek: SrMnO2,5 a SrMnO3, přičemž v prvním případě je veškerý mangan přítomen jako Mn3+, v druhém jako Mn4+. (Sr
2+)(Mn
3+)(O
2-)
2.5
(Sr2+
)(Mn4+
)(O2-)
3(Sr2+
)(Mn4+
)(Va)3
(Sr2+
)(Mn3+
)(O2-)
3
(Sr2+
)(Mn3+
)(Va)3
KomentářKomentář

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
23
Příklad 2 - Příklad 2 - pokračovánípokračování
Nestechiometrická fáze SrMnONestechiometrická fáze SrMnO3-3-δδ
22
SMO2.5 M3 SMO3 M4
SMO2.5 M3 SMO3 M4
O Va O
2δ 1 2δ
5 11
6 6
n n n n n n
x y x y x
x xz z z
Označení: Mn3+ = M3, Mn4+ = M4, SrMnO2,5 = SMO2,5, SrMnO3 = SMO3
M,idm
5 5 1 1ln (1 ) ln(1 ) 3 ln ln
6 6 6 6
x x x xG RT x x x x RT
Předpoklad: ideální míšení na obou podmřížkách33
44 SMO3
5 3 δln ln 3ln ln 1 2 3ln
6 3
xa x
SMO2,5
5 5 1 1 5 3 δ 1 δln ln 1 ln ln ln 2 ln ln
2 6 2 6 2 3 2 3
x xa x
+
o o M,idm m m m(SMO3) 1 (SMO2,5)G xG x G G

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
24
Příklad 3:Příklad 3:Kvaternární pevné roztoky typu (AKvaternární pevné roztoky typu (AIIIIII,A,AIIIIII)(B)(BVV,B,BVV))
Vypočtené oblasti omezené mísitelnosti (binodální křivky a konody) pevných roztoků (Ga,In)(As,P) a (Al,In)(As,P), H. Ohtani et al.: Phase equilibria in III-V Quaternary alloy semiconductors, Part II: III-III-V-V systems, Computer Aided Innovation of New Materials II, (M. Doyama et al., Eds.), Elsevier 1993.
KomentářKomentář

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
25
Bond Energy Model (BME) - Alternativní přístup navržený Braggem a Williamsem (1934) k popisu uspořádání v binárních slitinách kovových prvků. Vychází rovněž z konceptu podmřížek, přičemž celkovou vnitřní energii dané fáze (U) popisuje jako sumu interakčních energií dvojic nejbližších sousedních atomů (εij):
Parametr Wij je označován jako párová výměnná energie (pair exchange energy). V případě dvou podmřížek náleží každý atom z páru jedné podmřížce.
BME, v původní podobě (Bragg-Williams zero approximation) nebo v generalizované podobě (Chen et al. 1995) byl užit např. pro popis uspořádaných intermetalických fází strukturních typů CsCl(B2), AuCu(L10), Cu3Au(L12), pevných roztoků sloučenin typu AIIIBV aj.
Compound Energy Model vs. Bond EneCompound Energy Model vs. Bond Enerrgy Modelgy Model
M
2ii jj
ij ij i j ijij
U n U x x W kde W

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
26
LiteraturaLiteratura
5.1 Sublattice model (SM)5.1 Sublattice model (SM) M. Hillert, L.I. Staffansson: The regular solution model for stoichiometric phases and ionic melts, Acta Chem. Scand. 24 (1970) 3618-3626. B. Sundman, J. Ågren: A regular solution model for phases with several components and sublattices, suitable for computer applications, J. Phys. Chem. Solids 42 (1981) 297-301.
5.2 Compound energy model (CEM)5.2 Compound energy model (CEM) J.-O. Andersson et al.: A compound energy model of ordering in a phase with sites of different coordination numbers, Acta Metall. 34 (1986) 437-445. M. Hillert, B. Jansson, B. Sundman: Application of the Compound energy model to oxide systems, Z. Metallkde. 79 (1988) 81-87. T.I. Barry et al. : The Compound energy model for ionic solutions with applications to solid oxides, J. Phase Equilibria 13 (1992) 459-475. M. Hillert: Some properties of the compound energy model, CALPHAD 20 (1996) 333-341. Q. Chen, M. Hillert: The compound energy model for compound semiconductors, J. Alloys Compounds 245 (1996) 125-131. M. Hillert: The compound energy formalism, J. Alloys Compounds 320 (2001) 161-167.
5.3 Bond energy model (BEM)5.3 Bond energy model (BEM) W.A. Oates, H. Wenzl: The bond energy model for ordering in a phase with sites of different coordination numbers, CALPHAD 16 (1992) 73-78. W.A. Oates, H. Wenzl: Bond energy model of multiple sublattices solutions using species chemical potentials, CALPHAD 17 (1993) 35-46. F. Zhang et al.: Equivalence of the generalized bond-energy model, the Wagner-Schottky-type model and the compound-energy model for ordered phases, CALPHAD 21 (1997) 337-348.

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
27
Propracovanější model komplexního Fe-Cr spinelu je navržen v práci J.R. Taylor, A.T. Dinsdale:A thermodynamic assessment of the Cr-Fe-O system,Z. Metallkd. 84 (1993) 335-345.
Doplňující komentářeDoplňující komentáře
11.10.2005 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
17
PPřřííklad klad 11::KomplexnKomplexníí spinel spinel (Fe(Fe22++)()(FeFe33++,Cr,Cr3+3+))22OO44
11Ideální strukturu spinelu lze interpretovat jako FCC mřížku obsazenou anionty O2-, ve které je každá osmá tetraedrická dutina obsazena kationtem Me2+ a každá druhá oktaedrická dutina kationtem Me3+. Skutečnost, že magnetit, jako jedna z dále uvedených makrosložek, vykazuje tzv. inverzní strukturu v dalším odvození zanedbáme.
Tři podmřížky, mikrosložky Fe3+ a Cr3+ na jedné podmřížce, Fe2+ na druhé podmřížce a O2- na třetí podmřížce, makrosložky FeFe2O4
(magnetit) a FeCr2O4 (chromit).
22
FFO F3 FCO C3
FFO F3 FCO C3
2 2 2n n n n n n
x y x y
Označení: Fe2+ = F2, Fe3+ = F3, Cr3+ = C3FeFe2O4 = FFO, FeCr2O4 = FCO
KomentářKomentář

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
28
Doplňující komentářeDoplňující komentáře
Komplexnější termodynamický model pro fázi SrMnO3-δ je prezentován v následující přednášce T5. Termodynamický popis oxidických systémů.
11.10.2005 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
19
PPřřííklad 2:klad 2:NestechiometrickNestechiometrickáá ffááze SrMnOze SrMnO33--δδ
11Nestechiometrickou fázi SrMnO3-δ můžeme zapsat na základěpodmřížkového modelu vzorcem (Sr2+)(Mn3+,Mn4+)(O2-,Va)3. Jedna podmřížka je obsazována kationty Mn3+ a Mn4+, druhá anionty kyslíku s vakancemi, jejichž koncentrace je s ohledem na elektroneutralitu systému dána obsahem Mn3+. Třetí podmřížka je zcela zaplněna ionty Sr2+.
Podmřížkový model se substitucí na dvou podmřížkách formálně vede ke čtyřem makrosložkám. Ty jsou v tomto případě hypotetické (nejsou elektroneutrální), a proto je další postup zjednodušen volbou pouze dvou reálných makrosložek: SrMnO2,5 a SrMnO3, přičemž v prvním případě je veškerý mangan přítomen jako Mn3+, v druhém jako Mn4+. (Sr2+)(Mn3+)(O2-)
2.5
(Sr2+)(Mn4+)(O2-)3(Sr2+)(Mn4+)(Va)
3
(Sr2+)(Mn3+)(O2-)3
(Sr2+)(Mn3+)(Va)3
KomentářKomentář

6.10.2011 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
29
Doplňující komentářeDoplňující komentáře
Pro výpočet fázových diagramů byly použity následující parametry (K. Ishida et al.: Data base for calculating phase diagrams of III-V alloy semiconductors, J. Cryst. Growth 98 (1989) 140-147.):
11.10.2005 J. Leitner - Ústav inženýrství pevných látek, VŠCHT Praha
21
PPřřííklad 3:klad 3:KvaternKvaternáárnrníí pevnpevnéé roztoky typu (Aroztoky typu (AIIIIII,A,AIIIIII)(B)(BVV,B,BVV))
Vypočtené oblasti omezené mísitelnosti (binodální křivky a konody) pevných roztoků (Ga,In)(As,P) a (Al,In)(As,P), H. Ohtani et al.: Phase equilibria in III-V Quaternary alloy semiconductors, Part II: III-III-V-V systems, Computer Aided Innovation of New Materials II, (M. Doyama et al., Eds.), Elsevier 1993.
KomentářKomentář
PAl-In
AsAl-In
PGa-In GaP InP
AsGa-In
AlP-As
GaP-As
InP-As
15520 J/mol
10450 J/mol
16500 2,0 2550 J/mol
12500 J/mol
4072 J/mol
0
2000 J/mol
L
L
L T x x
L
L
L
L