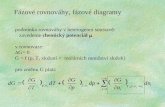Fázové rovnováhy v jednozložkových sústavách
description
Transcript of Fázové rovnováhy v jednozložkových sústavách

Katedra chémie, Technická univerzita v Košiciach
1
Fázové rovnováhy v jednozložkových sústavách
Clapeyronova rovnica
Clausius-Clapeyronova rovnica
Fázové diagramy

Katedra chémie, Technická univerzita v Košiciach
2
Fázová rovnováha: Definícia fázyDefinícia:
Fáza: Časť sústavy, ktorá je od ostatných častí fyzicky oddelená hranicou.
Hranicou je fázové rozhranie.
Jednofázová sústava vody
voda
Dvojfázová sústava vody
Trojfázová sústava vody
ľad
vodavoda
ľad
para

Katedra chémie, Technická univerzita v Košiciach
3
Homogénna: obsahuje len jednu fázu.
Heterogénna: obsahuje viac fáz.
Fázová rovnováha:
Homogénna a heterogénna sústava
Jednofázová sústava vody
Dvojfázová sústava vody
ľad
voda
Trojfázová sústava vody
voda
para
ľad
voda

Katedra chémie, Technická univerzita v Košiciach
4
Dvojfázová rovnováha:
• Vyparovanie: A(l) A(g)
• Kondenzácia: A(g) A(l)
• Topenie: A(s) A(l)
• Tuhnutie: A(l) A(s)
• Rekryštalizácia: A(s1) A(s2)

Katedra chémie, Technická univerzita v Košiciach
5
Clapeyronova rovnica
• Popisuje dvojfázové rovnováhy: s-s, s-l
VT
H
dT
dP
ΔH je entalpia fázovej premeny (J/K.mol)
T je teplota fázovej premeny (K)
Δ V je zmena mólového objemu pri fázovej premene (m³)

Katedra chémie, Technická univerzita v Košiciach
6
Rovnováha solidus-likvidus
• Je množinou bodov topenia
• S rastúcim tlakom bod topenia.
Rastie, ak je ΔV>0Klesá, ak je ΔV<0

Katedra chémie, Technická univerzita v Košiciach
7
Rovnováha solidus-likvidus Fázový diagram vodyVlastnosti:
Záporný sklon krivky topenia.
Zvýšený tlak pri konštantnej teplote spôsobí topenie.
Pri topení ľadu sa zmenšuje jeho objem
Teplota
P(Pa)
Ľad Voda
Para

Katedra chémie, Technická univerzita v Košiciach
8
Fázová rovnováha: Tlak pár a fázový diagramVyparovanie: A(l) A(g) KondenzáciaA(g) A(l)
Fázová rovnováha: dve fázy koexistujú v dynamickej rovnováhe
Kvapalina
Para
G
Teplota
G

Katedra chémie, Technická univerzita v Košiciach
9
Dvojfázové rovnováhy s prítomnosťou pary: sublimácia a vyparovanie
• Sublimácia : (s) → (g)
• Tuhý oxid uhličitý známy ako „suchý ľad“ nejestvuje pri normálnom tlaku v kvapalnom stave. Suchý ľad sa netopí, ale sublimuje.
Suchý ľad

Katedra chémie, Technická univerzita v Košiciach
10
Body sublimácie niektorých látok
Látka Bod sublimácie (ºC)
Acetylén - 84
Oxid uhličitý - 78.5
Grafit 3825
Fosfor (červený) 416

Katedra chémie, Technická univerzita v Košiciach
11
Vyparovanie: (l) → (g)
• K vyparovaniu dochádza vtedy keď je počet molekúl, ktoré opúšťajú kvapalinu väčší ako počet molekúl, ktorý vstupujú do kvapaliny.
• Ku kondenzácii dochádza vtedy ak viac molekúl vstupuje do kvapaliny ako kvapalinu opúšťa.
• Hnacou silou toho je koncentrácia molekúl látky v atmosfére.

Katedra chémie, Technická univerzita v Košiciach
12
Vyparovanie: (l) → (g)
• Ak je koncentrácia vysoká, prevláda kondenzácia
• Ak ani jeden proces neprevláda je to preto, že v v plynnej fáze je správna koncentrácia molekúl – nie je to ani viac a ani menej ako treba.
• Plynná fáza je vtedy NASÝTENÁ • Tlak pary nad kvapalinou sa nazýva TLAK
NASÝTENEJ PARY• Tlak nasýtenej pary sa zvyšuje s rastúcou
teplotou

Katedra chémie, Technická univerzita v Košiciach
13
Tlak nasýtenej paryJe tlak pary, ktorá je v rovnováhe s kvapalnou fázou pri konštantnej teplote
Pnas

Katedra chémie, Technická univerzita v Košiciach
14
Vyparovanie
• Vyparovanie kvapaliny v uzavretej nádobe prebieha dovtedy kým je počet molekúl, ktoré sa za jednotku času vyparia z povrchurovnaký ako počet molekúl, ktoré skondenzujú.
• Vtedy je para NASÝTENÁ a jej tlak sa nazýva tlak nasýtenej pary.
• Pri vyššej teplote uniká z povrchu kvapaliny viac molekúl a preto je tlak nasýtenej pary vyšší.
• Ak je kvapalina v otvorenej nádoby je tlak pary parciálnym tlakom v zmesi plynov vo vzduchu.
• Teplota, pri ktorej je tlak pary rovný atmosférickému tlaku sa nazýva bod varu.

Katedra chémie, Technická univerzita v Košiciach
15
Vyparovanie a var
Bubliny nevznikajú,lebo tlak je nižší ako
atmosferický tlak
Bubliny vznikajú,pretože tlak pary je väčší ako atmosférický
tlak
Vyparovanie Var

Katedra chémie, Technická univerzita v Košiciach
16
Dvojfázové rovnováhy s prítomnosťou pary
• Clausiusova-Clapeyronova rovnica
121
2 11ln
TTR
H
P
P
P2 je tlak pary pri teplote T 2
P 1 je tlak pary pri teplote T 1
ΔH je mólová entalpia vyparovania/sublimácie
R je plynová konštanta

Katedra chémie, Technická univerzita v Košiciach
17
Clausius

Katedra chémie, Technická univerzita v Košiciach
18
Denis Papin (1647-1712)

Katedra chémie, Technická univerzita v Košiciach
19

Katedra chémie, Technická univerzita v Košiciach
20
Tlakový hrniec
Tlak pary vždy rastie ak sa zvyšuje teplota!
Pri zvýšenom tlaku sa zvyšuje bod varu!

Katedra chémie, Technická univerzita v Košiciach
21
Tlakový hrniec
• Tlakový hrniec skracuje dobu varenia tak, že voda zostáva v kvapalnom stave pri oveľa vyššej teplote ako v obyčajnom hrnci.
• Pri zvýšenom tlaku sa zvyšuje bod varu vody.

Katedra chémie, Technická univerzita v Košiciach
22
Bod varu pri zníženom tlaku okolia
• Pokles vonkajšieho tlaku spôsobuje zníženie bodu varu

Katedra chémie, Technická univerzita v Košiciach
23
Všeobecný rovnovážny diagram jednej zložky
Vysoké P a nízke T :Tuhá Vysoká T a nízke P
:plyn/para
Topenie s-l
Vyparovanie l-g
Sublimácia s-g
Trojný bod T
Kritický bod C
P
Teplota
Tuhá
Kvapalná
Para

Katedra chémie, Technická univerzita v Košiciach
24
Rovnováhy vo fázovom diagrame
• Topenie: s-l univariantná rovnováha: v=1-2+2= 1
• Vyparovanie l-v univariantná rovnováha: v=1-2+2= 1
• Sublimácia s-v univariantná rovnováha: v=1-2+2= 1 • Trojný bod T nonvariantná rovnováha: v=1-3+2= 0

Katedra chémie, Technická univerzita v Košiciach
25
Fázová rovnováha: Fázový diagram CO2Vlastnosti:
Trojný bod je pri tlaku vyššom ako 101325 Pa.
Zvýšenie T pri atmosferickomtlaku vedie k sublimácii,
t.j. Suchý ľad sa netopí.
s l
g
Teplota
P10325 Pa

Katedra chémie, Technická univerzita v Košiciach
26
Koniec