Bahan Bakar
-
Upload
feriizco-ramadhan -
Category
Documents
-
view
30 -
download
4
Transcript of Bahan Bakar
DIKTAT
BAB I
PENDAHULUAN
1.1 Latar Belakang
Bahan-bahan yang berdasarkan pertimbangan teknis ekonomis dapat di bakar untuk menghasilkan panas dalam mesin-mesin industri disebut dengan bahan bakar. Pembakaran adalah suatu proses reaksi kimia antara unsur-unsur bahan bakar dengan oksigen disertai pelepasan panas dengan temperatur tinggi.
Setiap jenis bahan bakar mempunyai nilai pembakaran yang berbeda dan kandungan unsur-unsur atau komponen-komponen yang terkandung di dalamnya juga berbeda-beda, sehingga dimungkinkan pada suatu jenis bahan bakar dapat terjadi pembakaran sempurna dan pada jenis lainnya terjadi pembakaran sempurna, tetapi hal ini tidak mutlak karena ada beberapa faktor yang mempengaruhinya.
Pembakaran sempurna terjadi bila semua unsur-unsur bahan bakar terbakar dan semua panas dilepaskan dan hal ini hanya dapat terjadi secara teoritis. Ada dua hal yang mendorong mengapa pembakaran harus sempurna mungkin yaitu:
Bahan bakar mahal, sehingga pembakaran yang tidak efisien berarti pemborosan
Pembakaran yang tidak sempurna akan menimbulkan polusi udara
1.2 Perumusan Masalah
Bagaimana cara untuk dapat menghasilkan pembakaran yang sesempurna mungkin sehingga mendapatkan hasil effesiensi yang optimal. Karena untuk bahan bakar yang berbeda akan menghasilkan nilai kalor yang berbeda pula.
BAB II
PEMBAKARAN
2.1Bahan Bakar
Pada prinsipnya bahan bakar adalah suatu material yang pada kondisi tertentu dapat membentuk reaksi pembakaran dengan oksigen dan dari reaksi tersebut dihasilkan panas yang cukup besar. Syarat-syarat bahan bakar yang baik adalah :
a. Mempunyai titik pengapian yang rendah
b. Mempunyai nilai kalor yang tinggi
c. Harus terbakar dengan baik sekali diapikan
d. Tidak mengandung gas-gas yang berbahaya
e. Menghasilkan asap dan gas seminimal mungkin
f. Harus ekonomis, mudah penyimpanannya serta mudah transportasinya
2.2Klasifikasi Bahan Bakar
a. Bahan Bakar Cair (Liquid Fuel)
- Minyak Berat (Heavy Oil)
- Minyak Diesel (Diesel Oil)
- Kerosin
- Minyak Mentah / Minyak Bumi (Crude Oil)
b. Bahan Bakar Gas (Gas Fuel)
- Gas Batu Bara (Coal Gas)
- Gas Alam Cair (LNG)
- Gas Petroleum Cair (LPG)
c.Bahan Bakar Padat (Solid Fuel)
- Batu Bara (Coal)
- Lignit (Lignite)
- Kokos (Coke)
- Kayu (Wood)
Selain bahan-bahan bakar tersebut diatas, ada juga bahan-bahan khusus yang dapat digunakan sebagai bahan bakar Ketel Uap, yaitu:
Sekam atau kulit padi kering (Husk)
Ampas tebu (Bagasse)
Serbuk kayu hasil penggergajian (Wood Tip)
Potongan potongan kecil kayu (Bark) dan
Sampah sampah kota (City Refuse)
Jenis bahan bakar yang banyak dipakai di PLTU adalah bahan bakar padat (batu bara) dan bahan bakar minyak (residu dan solar).
Perbadaan komposisi kedua jenis bahan bakar tersebut terutama pada kandungan Carbon dan Hidrogen.
Komposisi Batu Bara
Komposisi Residu
Carbon = 56,8 %
84,4 %
Hidrogen = 3,7 %
11,5 %
Sulfur
= 2 %
3 %
Oksigen= 7,4 %
0,2 %
Nitrogen= 1,3 %
0,3 %
Ash
= 16,7 %
0,1 %
Moisture= 12,5 %
0,5 %
---------------
--------------
100 %
100 %
NATURAL GAS
Hydrocarbon Methane
CH4
93,3 %
Ethane
C2H6
3,3 %
Propane
C3H8
0,7 %
Butane
C4H10
0,2 %
Pentane
C5H12
0,5 %
Hydrogen SulphideH2S
--
Carbondioxide
CO2
0,3 %
Nitrogen
N2
1,7 %
-----------
100 %
Diantara unsur-unsur yang terkandung dalam suatu komposisi bahan bakar, unsur yang dapat terbakar adalah Carbon, Hidrogen dan Sulfur.
2.3Komposisi Udara
Udara yang ada di alam ini umumnya terdiri dari dua unsur utama yaitu Nitrogen dan Oksigen. Selain kedua unsur tersebut, sebenarnya udara juga mengandung gas-gas lain seperti CO, CO2 dan sebagainya. Tetapi karena persentasenya sangat kecil dibandingkan kedua unsur utama tersebut, maka biasanya unsur-unsur lain dapat diabaikan.
Selanjutnya persentase oksigen dan nitrogen dalam udara dapat dinyatakan baik dalam satuan berat maupun dalam satuan volume.
Dalam satuan persen berat, Udara mengandung :
Oksigen = 23,2 %
Nitrogen = 76,8 %
Dalam satuan persen volume, Udara mengandung :
Oksigen = 21 %
Nitrogen = 79 %
Perbedaan persentase satuan berat dan satuan volume ini disebabkan oleh perbedaan berat atom antara oksigen dengan nitrogen. Nitrogen tidak memberikan kontribusi apapun terhadap proses pembakaran. Selain akan membawa sejumlah panas kecerobong, nitrogen juga dapat menghalangi kontak antara oksigen dengan partikel-partikel bahan bakar.
2.4 Reaksi Pembakaran
Seperti diketahui bahwa unsur-unsur dalam bahan bakar yang dapat membentuk reaksi pembakaran dengan oksigen adalah Carbon, Hidrogen dan Sulfur. Oleh karena itu proses pembakaran bahan bakar tidak lain adalah terbentuknya reaksi pembakaran antara ketiga unsur tersebut dengan Oksigen.
Reaksi pembakaran untuk ketiga unsur tersebut adalah sebagai berikut :
- Reaksi Pembakaran Carbon
C + O2 CO2(Pembakaran Carbon Sempurna)
C + O CO(Pembakaran Carbon Tak Sempurna)
- Reaksi Pembakaran Hidrogen
H2 + O2 H2O
2H2 + O2 2H2O
- Reaksi Pembakaran Sulfur
S + O2 SO2
2.5Menghitung Kebutuhan Oksigen Dan Udara Teoritis Untuk Proses Pembakaran Bahan Bakar
Untuk dapat menghitung kebutuhan oksigen dan udara teoritis bagi proses pembakaran bahan bakar, maka perlu diingat berat atom masing-masing unsur yang terlibat dalam reaksi pembakaran. Agar lebih mudah mengingat, dapat digunakan daftar berikut :
Nama UnsurSimbolB.A
CarbonC12
HidrogenH1
SulfurS32
OksigenO16
NitrogenN14
Berdasarkan daftar berat atom tersebut, kebutuhan Oksigen dapat dihitung sebagai berikut :
- Oksigen yang diperlukan untuk membakar Carbon, adalah :
C + O2 CO2
12 + 32 44
1 Kg C + Kg O2 Kg CO2
1 Kg C + Kg O2 Kg CO2
Jadi untuk setiap Kg Carbon memerlukan Kg Oksigen
- Oksigen yang diperlukan untuk membakar Hidrogen, adalah :
H2 + O2 H2O
2H2 + O2 2H2O
4 Kg H + 32 Kg O2 36 Kg H2O
1 Kg H + 8 Kg O2 9 Kg H2O
Jadi untuk setiap Kg Hidrogen memerlukan 8 Kg Oksigen
- Oksigen yang diperlukan untuk membakar Sulfur, adalah :
S + O2 SO2
32 Kg S + 32 Kg O2 64 Kg SO2
1 Kg S + 1 Kg O2 2 Kg SO2
Jadi 1 Kg Sulfur memerlukan 1 Kg Oksigen
Kebutuhan Oksigen Total :
Kebutuhan oksigen untuk membakar (Carbon+Hidrogen+Sulfur)
Oksigen Total = C + 8 H + S
Tetapi biasanya di dalam bahan bakar juga terdapat sedikit oksigen. Oksigen dalam bahan bakar dianggap akan bereaksi dengan hidrogen di dalam bahan bakartersebut. Karena itu hidrogen yang akan bereaksi dengan oksigen yang berasal dari udara akan berkurang sebanyak .
Dengan demikian kebutuhan oksigen total menjadi : C + 8 ( H - ) + SBerhubung dalam satuan berat udara mengandung 23,2 %, maka kebutuhan udara teoritis = Oksigen total
atau udara teoritis = ..................
Keterangan :C = %
H = %
O = %
S = %
Contoh : 1 Kg Bahan Bakar dengan komposisi sebagai berikut :
Carbon : 56,8 %
Hidrogen: 3,7 %
Nitrogen: 1,3 %
Sulfur
: 2,0 %
Oksigen : 7,0 %
Abu
: 16,7 %
Moisture: 12,5 %
--------------
100 %
Hitung kebutuhan udara minimum untuk membakar sempurna bahan bakar tersebut.
Udara Minimum = .............
=
= 4,31 [1,515 + 0,226 + 0,02]
= 4,31 x 1,761
= 7,59
Udara 1 nm3 pada 0 oC beratnya 1,29 Kg sehingga jumlah udara minimum / teoritis dalam satuan adalah Udara minimum / teoritis = = 5,88 .
Unsur C, H dan S masing-masing memerlukan 1 Kg mol Oksigen atau 2,24 nm3 Oksigen, sehingga dapat dihitung dengan cara :
O2 =
=
= 1,288 nm3O2
Telah ada sebanyak 0,07 Kg O2 dalam 1 Kg bahan bakar atau sebanyak:
0,07 x ( 22,4 : 32 ) nm3O2 = 0,049 nm3O2
Sehingga O2 yang dibutuhkan hanya :
O2 = 1,288 0,049 = 1,239 nm3O2
Dengan demikian jumlah udara minimum / teoritis yang dibutuhkan dalam satuan nm3O2 adalah :
Udara minimum / teoritis = 100/21 x 1,239 = 5,9 nm3/ kgbb
2.6Kendala Kendala Dalam Proses Pembakaran
Meskipun udara pembakaran telah di hitung dengan cermat, namun bila dilakukan pemantauan yang teliti terhadap gas asap, tetap masih terdapat unsur-unsur bahan bakar yang tidak terbakar sama sekali ataupun terbakar tidak sempurna. Hal ini terjadi bukan karena kekurangan oksigen tetapi di sebabkan oleh kendala-kendala praktis yang sulit dihindari.
Kendala yang ditemui dalam proses pembakaran diantaranya adalah :
- Pencampuran yang tidak homogen antara bahan bakar dengan oksigen.
Ini akan mengakibatkan oksigen tidak bertemu dan bereaksi dengan partikel-partikel sampai keduanya keluar lagi kecerobong.
- Terlalu singkatnya waktu pembakaran sehingga tidak semua bahan bakar terbakar
-Adanya interpose dari partikel-partikel seperti nitrogen dan abu yang menyusup diantara oksigen dan atom/molekul dari unsur dalam bahan sehingga dapat menghalangi proses reaksi pembakaran.
Kendala-kendala tersebut dapat mengakibatkan pembakaran tidak sempurna yang ditandai munculnya CO dalam Gas Asap meskipun dalam Gas Asap tersebut juga terdapat O2, hal ini tentunya merupakan kerugian.
Untuk mengatasi kendala-kendala tersebut, maka dalam praktek selalu diberikan jumlah udara yang lebih besar dari jumlah udara teoritis. Hal ini dimaksudkan untuk memperoleh pembakaran yang sempurna. Oleh karena itu dalam praktek pembakaran pada ketel uap, udara actual yang diberikan selalu lebih besar dari kebutuhan udara teoritis. Selisih antara jumlah udara actual dengan udara teoritis disebut udara lebih (Excess Air).
2.7Pengaruh Udara Lebih (Excess Air)
Seperti telah diuraikan diatas bahwa tanpa udara lebih sulit memperoleh pembakaran yang sempurna. Oleh karena itu dalam proses pembakaran selalu diperlukan udara lebih.
Presentase udara lebih dapat dihitung dengan :
% udara lebih =
Besarnya udara lebih yang diperlukan untuk bahan bakar batubara tidak sama dengan yang diperlukan oleh bahan bakar minyak. Besarnya udara lebih harus tepat karena sebenarnya udara lebih ini akan membawa sejumlah panas keluar ke cerobong. Jadi sebenarnya udara lebih ini merupakan suatu kerugian bila ditinjau dari segi efisiensi.
Sekalipun demikian, tanpa udara lebih juga merupakan kerugian bila ditinjau dari segi efisiensi. Karena itu jumlah udara lebih harus tepat dan ini merupakan kompromi antara besarnya kerugian karena udara lebih dengan kerugian karena pembakaran tak sempurna. Dengan kata lain, jumlah udara lebih harus dibuat pada suatu harga tertentu dimana pada harga tersebut besarnya kerugian yang diakibatkannya berada pada tingkat minimum.
Sebagai ilustrasi perhatikan Gambat 1 berikut :
Gambar 1. Pengaruh Excess Air terhadap Efisiensi
Gambar 1 A memperlihatkan proses pembakaran pada ketel tanpa udara lebih, Gambar 1 B dengan 15% udara lebih sedang dan pada Gambar 1 C dengan 100% udara lebih.
Pada Gambar1 A terlihat bahwa tanpa udara lebih, kerugian karena pembakaran tak sempurna mencapai sekitar 25% yang terdiri dari 15% kerugian pada gas asap sedang, 10% pada abu dan debu. Dengan 15% udara lebih seperti pada Gambar1 B, kerugian karena pembakaran tak sempurna akan berkurang menjadi sekitar 3% tetapi kerugian gas asap bertambah besar.
Pada Gambar 1 C dengan 100% udara lebih, kerugian karena pembakaran tak sempurna turun menjadi sekitar 0,5% tetapi kerugian gas asap menjadi besar. Jadi dengan naiknya udara lebih, kerugian karena pembakaran tak sempurna turun tetapi kerugian karena panas yang dibawa oleh gas keluar cerobong bertambah. Kurva besarnya kedua kerugian tersebut dapat dilihat pada Gambar 2 dibawah ini.
Gambar 2. Kurva Excess Air versus Kerugian
Pada Gambar 2, terlihat bahwa kerugian minimum terjadi pada harga udara lebih sekitar 22%. Untuk pengoperasian yang efisien, maka ketel harus dioperasikan dengan jumlah udara lebih dimana harga kerugian minimum. Karena itu memonitor % udara lebih menjadi hal yang cukup penting. Selain dengan rumus diatas, % udara lebih juga dapat ditentukan bila % O2 atau % CO2 dalam gas asap diketahui. Bila dengan menggunakan % CO2 maka :
% udara lebih =
Bila dengan menggunakan % O2, maka :
% udara lebih =
% CO2 dan % O2 dalam gas asap dapat diukur dengan menggunakan alat Orsat atau O2 analizer. Pada ketel modern, O2 dimonitor secara kontinyu dan ditunjukkan pada alat ukur atau recorder. Dengan demikian % udara lebih dapat diketahui setiap saat sehingga operator dapat mengatur sesuai dengan harga yang dikehendaki.
2.8Nilai Kalor Bahan Bakar
Setiap unsur dalam bahan bakar yang dapat membentuk reaksi dengan oksigen akan melepaskan sejumlah panas ketika reaksi-reaksi tersebut berlangsung. Banyaknya panas yang dilepaskan berbeda antara unsur yang satu dengan unsur yang lain. Misalnya:
- Pembakaran Carbon :
C + O2 CO2 + 33.820
- Pembakaran Hidrogen :
2H2 + O2 2 H2 O + 144.000
- Pembakaran Sulfur :
S + O2 SO2 + 9720
Bila panas yang dihasilkan dari reaksi masing-masing unsur tersebut dijumlahkan, maka akan diperoleh panas total yang dapat dihasilkan oleh setiap Kg bahan bakar bila dibakar. Panas ini disebut nilai kalor. Nilai kalor bahan bakar bervariasi dan berbeda antara bahan bakar yang satu dengan bahan bakar lainnya.
Nilai kalor bahan bakar dapat diukur dengan menggunakan alat yang disebut Bomb Calorimeter. Bahan bakar dibakar dalam Bomb Calorimeter untuk selanjutnya jumlah panas yang dilepaskan dapat diukur. Nilai kalor yang diperoleh dengan cara seperti ini disebut nilai kalor atas (High Heating Value).
Selain menggunakan Bomb Calorimeter, nilai kalor bahan bakar juga dapat diketahui bila komposisi bahan bakar diketahui, maka nilai kalor dapat diketahui melalui perhitungan dengan menggunakan rumus Dulong dan Petit. Rumus Dulong untuk Nilai Kalor Atas adalah :
HHV = 33.820 C + 144000 ( H - ) + 9270 S
LHV = HHV ( 9.H2Ox 2442 ) ( nilai kalor bawah )
Dimana :C = Carbon
H = Hidrogen
S = Sulfur
O = Oksigen
2.9Pengaruh Kandungan Sulfur Dalam Bahan Bakar
Telah diuraikan bahwa sulfur akan terbakar dengan reaksi :
S + O2 SO2
Dalam proses pembakaran ketel, selalu diberikan udara lebih. Dengan demikian maka juga terdapat oksigen lebih. Selanjutnya bila gas sulfur dioksida ini bertemu dengan oksigen yang berasal dari udara lebih, maka akan terjadi reaksi :
2 SO2 + O2 2 SO3
Hasil pembakaran Hidrogen adalah 2H + O2 2 H2 O. Selain itu dalam gas sisa pembakaran juga terdapat air yang berasal dari udara pembakaran maupun dari bahan bakar. Apabila H2O ini bertemu dengan SO3 akan terjadi reaksi :
SO3 + H2O H2 SO4(Asam Sulfat)
Asam sulfat ini bersifat sangat korosif terhadap logam sehingga sering dijumpai terjadinya korosi pada saluran-saluran gas asap pada daerah yang temperaturnya cukup rendah dimana terjadi pengembunan H2 SO4. Kerusakan ini terutama sering dijumpai pada elemen A/H sisi dingin. Selain itu, bila terbuang ke atmosfir melalui cerobong akan dapat mengakibatkan pencemaran lingkungan serta hujan asam yang dapat membunuh tanaman.
Dengan demikian meskipun sulfur memberikan kontribusi panas dalam proses pembakaran, tetapi sulfur juga menimbulkan dampak negatif yang merugikan. Karena itu kandungan sulfur dalam bahan bakar dibatasi dan kita tentunya akan memilih bahan bakar yang tidak mengandung sulfur bila hal ini memungkinkan. Tetapi kenyataannya hampir tidak ada bahan bakar fosil yang bebas dari sulfur. Jadi meskipun dalam jumlah yang kecil, dampak negatif sulfur harus tetap kita tanggung.
2.10Desulphurizaiton Plant
Dampak yang disebabkan sulfur dalam masalah korosi dapat diperkecil dengan mengorbankan sedikit efisiensi yaitu dengan menaikkan temperatur gas keluar A/H untuk mencegah pembekuan sulfur. Tetapi bila sulfur ini dibiarkan lolos dari cerobong, dampak pencemaran lingkungan akan sulit ditanggulangi.
Sejalan dengan meningkatnya kesadaran tentang kelestarian alam serta makin ketatnya peraturan mengenai pencemaran lingkungan, maka sebaiknya produk dari pembakaran sulfur jangan dibuang ke atmosfir. Untuk memenuhi tuntutan lingkungan ini, maka pusat-pusat pembangkit pada masa mendatang harus dilengkapi dengan suatu perangkat yang dapat menyerap produk pembakaran sulfur. Perangkat ini disebut Desulphurizaiton Plant
Pada prinsipnya Desulphurizaiton Plant adalah suatu perangkat yang merubah SO2 menjadi Gypsum dengan cara mencampur SO2 tersebut dengan Lymstone.
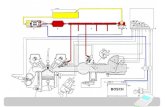
Desulphurizaiton Plant dipasang pada laluan gas asap sebelum cerobong. Dengan demikian maka gas asap yang keluar dari cerobong tidak lagi mengandung produk. Pembakaran sulfur yang dapat mencemari lingkungan. Secara skematik, Desulphurizaiton Plant dapat dilihat pada Gambar 3 dibawah ini:
Gambar 3. Desulphurizaiton Plant
Secara singkat, prinsip kerja Desulphurizaiton Plant adalah sebagai berikut. Gas bekas dari Electrosatic Precipitator dialirkan ke Desulphurizaiton Plant melalui Booster Fan. Selanjutnya gas akan masuk dalam tangki penyerap (Absorption Unit) dan dalam tangki ini, SO2 akan diikat oleh lumpur limestone untuk membentuk Gypsum. Sebelum masuk tangki penyerap, temperatur gas harus diturunkan tetapi dinaikkan kembali setelah keluar dari tangki penyerap agar gas memiliki cukup buoyancy sehingga dapat keluar dari cerobong. Untuk keperluan ini maka dipasang alat penukar panas tipe regeneratif yang mengambil panas dari gas sebelum masuk tangki penyerap, untuk selanjutnya menyerahkan kembali panas tersebut kepada gas yang keluar dari tangki.
Limestone yang digiling dicampur dengan air di dalam tangki sehingga membentuk lumpur Limestone untuk selanjutnya lumpur limestone ini dipompakan ke tangki penyerap. Lumpur ini kemudian dispraykan dalam tangki penyerap SO2. Gypsum yang merupakan produk selanjutnya dipompakan dari bagian bawah tangki penyerap SO2 yang merupakan lumpur kasar dengan 30 60 % padat menuju unit pemisah (Primary Hydrocyclone).
Pada Primary Hydrocyclone terjadi pemisahan antara partikel lumpur yang halus dengan yang kasar. Lumpur kasar selanjutnya dimasukkan dalam tangki Gypsum. Partikel yang halus selanjutnya dialirkan ke pemisah tingkat dua (Secondary Hydrocyclone). Setelah terlebih dahulu ditampung dalam tangki penampung lumpur halus (Secondary Hydrocyclone Feed Tank).
Lumpur Gypsum dari tangki Gypsum dipompakan ke dalam tangki centrifuge untuk selanjutnya dipompakan ke pengering sentrifugal (Centrifuge). Pada unit Centrifuge, Gypsum dikeringkan hingga kadar airnya tinggal 8 - 10% saja. Gypsum ini selanjutnya dikirim ke tempat penyimpanan atau ke tempat pemrosesan lebih lanjut dengan menggunakan konveyor. Air dari unit Centrifuge ditampung dalam tangki (Concrate Tank) untuk selanjutnya dipompakan kembali tangki lumpur Limestone. Partikel halus dari pemisah kedua (Secondary Hydrocyclone) diencerkan dalam tangki pengencer untuk selanjutnya dipompakan ke unit pengolahan air limbah. Gypsum ini dapat dibuat bricket-bricket untuk dibuat dinding / bata.
2.11Terbentuknya Asap
Gas bekas adalah merupakan material tak terlihat yang disebarkan melalui cerobong. Secara umum, Gas Asap berwarna hitam yang keluar dari cerobong menunjukkan bahwa proses pembakaran di dalam ketel berlangsung secara kurang sempurna. Penyebab terbentuknya asap yang berwarna hitam ada beberapa faktor, seperti :
a. Terbawanya debu dengan jumlah yang cukup banyak dalam gas asap.
b. Terdapat Carbon yang tak terbakar pada gas asap dalam bentuk jelaga (soot)
c. Adanya gas-gas berwarna seperti SO2, NOx terutama pada saat pembakaran minyak.
d. Adanya uap volatile matter.
Tetapi gas asap yang keluar dari cerobong juga dapat berwarna hitam meskipun hanya mengandung sedikit carbon yang tak terbakar yang bila ditinjau dari segi efisiensi, hal ini sebenarnya dapat diabaikan.
Sebaliknya, asap yang berwarna jernih secara umum menyatakan bahwa proses pembakaran berlangsung secara sempurna. Terutama pada proses pembakaran minyak. Asap yang jernih biasanya dapat diperoleh dengan cara menurunkan % CO2 pada suatu harga tertentu dimana udara lebih berada sedikit diatas harga optimum. Selain berkaitan dengan masalah efisiensi, kepekatan gas asap juga berkaitan dengan masalah lingkungan.
Asap yang pekat akan mencemari lingkungan dengan kadar pencemaran yang lebih besar. Oleh sebab itu, pengukuran kepekatan gas asap menjadi faktor yang perlu diperhatikan oleh pengelola PLTU terutama di negara-negara yang telah menjalankan peraturan mengenai lingkungan hidup yang ketat. Pengukuran kepekatan gas asap dapat dilakukan dengan menggunakan kartu Ringelmann atau dengan menggunakan meter asap tipe photo cell.
2.11.1Pengukuran Kepekatan Asap Dengan Kartu Ringlemann
Kartu Ringelmann terdiri dari 6 buah kartu yang diberi nomor mulai dari 0 5. Kartu-kartu tersebut berwarna putih sampai hitam pekat, selanjutnya kartu-kartu tersebut juga diberi skala dengan % kepekatan (obscuration). Untuk jelasnya perhatikan Gambar 4 dibawah ini:
Gambar 4. Kartu RinglemannNo. Kartu
Warna
Skala % Kepekatan0
Putih
0 %
1
Abu Abu Muda
20 %
2
Abu Abu
40 %
3
Abu Abu Tua
60 %
4
Hitam
80 %
5
Hitam Pekat
100 %
Cara menggunakan kartu ini sederhana saja yaitu dengan melihat asap yang keluar dari cerobong serta menyamakan warna asap dengan salah satu warna dari kartu Ringelmann sehingga % kepekatannya dapat diketahui.
Asap yang masih dianggap aman terhadap lingkungan adalah asap dengan kepekatan dibawah 40 %. Kartu ini hanya dapat dipakai mengukur kepekatan asap secara insidental.
2.11.2Pengukuran Kepekatan Asap dengan Meter Asap
Pada PLTU modern, pemantauan kepekatan asap tidak hanya dilakukan secara insidental, tetapi secara terus menerus dan bahkan dilengkapi dengan recorder. Untuk keperluan ini biasanya digunakan alat pengukur kepekatan asap tipe Photo Cell. Tipe alat ini dapat dilihat pada Gambar 5.
Prinsip pengukuran asap dengan alat ini adalah dengan cara memancarkan sinar melintasi saluran asap dimana pada sisi lintasan yang lain ditempatkan cell cahaya (Photo Cell) yang akan menyerap sinar yang dipancarkan tadi. Kepekatan gas asap akan mempengaruhi intensitas cahaya yang diterima.photo cell yang selanjutnya dipakai sebagai signal pengukuran. Sinyal listrik ini setelah dikuatkan kemudian dipakai untuk menggerakkan jarum penunjuk pada sebuah alat ulur yang diberi skala % kepekatan. Dengan cara ini, kepekatan asap dapat dimonitor setiap saat dan bahkan juga dilengkapi dengan recorder serta alarm.
Gambar 5. Meter Asap Tipe Photo Cell
2.12Efisiensi Ketel Uap
Perbandingan panas sebenarnya yang digunakan untuk menghasilkan uap terhadap panas yang dilepaskan dalam dapur. Efisiensi ini juga dikenal dengan Efisiensi Thermal Ketel Uap.
Secara matematis ditulis
Dimana :
We = Berat air sebenarnya yang diuapkan untuk menghasilkan uap terhadap
panas yang dilepaskan dalam dapur
LHV= Nilai Kalor Bawah Bahan Bakar
H = Panas Total
h1= Panas Sensibel Air Pengisi
Ws= Berat Uap yang dihasilkan
Wf= Berat Bahan Bakar yang digunakan
Maka :
# EXCESS AIR (Udara Lebih)
Excess Air = 25 50 % untuk Bahan Bakar Padat
= 5 10 % untuk Bahan Bakar Cair & Gas
(Wa)EXC = (Wa)th x Excess Air
# Udara Actual
(Wa)ACT = (Wa)EXC + (Wa)th
BAB III
CONTOH SOAL
1. Diketahui :
Sebuah Ketel Uap dapat menghasilkan uap kering = 2500
dengan tekanan kerja = 12 ban
Temperatur air pengisi t1 = 70 0C
Effisiensi Ketel = 80 %
Excess Air = 25 % (diambil)
Dengan komposisi Bahan Bakar:
C = 68,8 % = 0,688 Kg
H = 4,2 % = 0,042 Kg
S = 3 % = 0,03 Kg
O = 9 % = 0,09 Kg
Ash= 9 % = 0,09 Kg
Moist= 6 % = 0,06 Kg
Ditanya :
a. Jumlah bahan bakar yang dibutuhkan
b. Jumlah udara teoritis dinyatakan dalam Kg dan nm3
c. Jumlah udara actual
Jawab :
* Nilai Kalor Atas (HHV)
HHV = 33800 . C + 144000 (H2 - ) + 9270 . S
= 33800 . 0,688 + 144000 (0,042 - ) + 9270 . 0,03
= 23254,4 + 144000 . 0,03075 + 278,1
= 23254,4 + 4428 + 278,1
HHV= 27960,5
* Nilai Kalor Bawah (LHV)
LHV= HHV ( 9 H2 2442 )
= 27960,5 ( 9 0,042 2442 )
= 27960,5 923,076
LHV= 27037,424
a) Jumlah Bahan Bakar Yang Dibutuhkan (Wf)
..
Dimana :
Wf = Banyaknya bahan bakar yang dibutuhkan .()
Ws= Kapasitas Uap yang dihasilkan( Kg/jam )
hfg (Hsat)= Enthalphy uap saturasi pada tekanan dan temperature kerja ketel (Boiler) lihat pada diagram mollier atau table uap ()
h1= Enthalphy air pengisi ketel / air umpan ketel ()
Catatan: Khusus untuk air pengisi ketel besarnya Enthalhpy tergantung pada besarnya temperature air pengisi dengan besaran yang sama pada satuan berbeda.
Contoh : Temperatur air pengisi / air umpan
: 70 0C
Maka Enthalphy nya (tabel uap)=
: 70
k = Effisiensi ketel ( 70 90)
LHV = Nilai kalor bahan bakar tergantung bahan bakar yang
digunakan ()
Wf = hg : 2782,7
Tabel uap pada p = 12 bar
Wf=
Wf= 313,535
b) Jumlah Udara Teoritis Dalam Satuan Kg dan nm3
Udara Teoritis =
=
= 4,31 (1,835 + 0,03075) + 0,03
= 4,31 1,86575 + 0,03
= 8,07
Udara 1 nm3 pada 0 0C beratnya 1,29 Kg
Udara teoritis =
= 6,256
Dari unsur kimia C, H dan S masing-masing memerlukan 1 Kg mol oksigen atau 22,4 nm3 oksigen.
O2 = nm3O2
= ( 0,057 + 0,0105 + 0,00094 ) 22,4 nm3O2
= 0,0684 22,4 nm3O2
= 1,53 nm3O2
Telah ada sebanyak 0,09 Kg O2 dalam 1 Kg bahan bakar atau sebanyak : 0,09 (2,4 : 32) nm3O2 = 0,063 nm3O2 .
sehingga O2 yang dibutuhkan hanya : 1,53 0,063 = 1,467 nm3
Dengan demikian jumlah udara teoritis yang dibutuhkan dalam satuan
Udara teoritis =
c) Jumlah Udara Actual
(Wa)ACT = (Wa)EXC + (Wa)th (Wa)EXC = EXC (Wa)th
= 0,25 8,07
= 2,0175
(Wa)ACT = 2,0175 + 8,07
= 10,09
DAFTAR PUSTAKA
[1]R.S Khurmi, Heat Engine Thermal Engineering.
[2]Pusdiklat PLN, Pembakaran
[3] Syamsir A. Muin, Ir., Pesawat pesawat Konversi Energi I (Ketel Uap), Rajawali Pers, Jakarta.
[4]M.J.Djoko Setyardjo, Ketel Uap, PT.Pradaya Paramita Jakarta.
.........................................................................................
PAGE 12
_1609205200.unknown
_1611284696.unknown
_1611287576.unknown
_1612077148.unknown
_1612078428.unknown
_1612865760.unknown
_1612866400.unknown
_1612867040.unknown
_1612867360.unknown
_1612866720.unknown
_1612866080.unknown
_1612078748.unknown
_1612077788.unknown
_1612078108.unknown
_1612077468.unknown
_1612075548.unknown
_1612076508.unknown
_1612076828.unknown
_1612075868.unknown
_1611288216.unknown
_1612075228.unknown
_1611287896.unknown
_1611286296.unknown
_1611286936.unknown
_1611287256.unknown
_1611286616.unknown
_1611285656.unknown
_1611285976.unknown
_1611285336.unknown
_1610220692.unknown
_1610221972.unknown
_1610222612.unknown
_1610223252.unknown
_1610222292.unknown
_1610221332.unknown
_1610221652.unknown
_1610221012.unknown
_1609207440.unknown
_1610220052.unknown
_1610220372.unknown
_1610219732.unknown
_1609206480.unknown
_1609207120.unknown
_1609205520.unknown
_1605335752.unknown
_1605986380.unknown
_1609203920.unknown
_1609204560.unknown
_1609204880.unknown
_1609204240.unknown
_1605987660.unknown
_1605987980.unknown
_1605986700.unknown
_1605984460.unknown
_1605985420.unknown
_1605985740.unknown
_1605984780.unknown
_1605336392.unknown
_1605336712.unknown
_1605336072.unknown
_1605333192.unknown
_1605334472.unknown
_1605335112.unknown
_1605335432.unknown
_1605334792.unknown
_1605333832.unknown
_1605334152.unknown
_1605333512.unknown
_1586191044.unknown
_1586191684.unknown
_1586192004.unknown
_1586191364.unknown
_1314647756.unknown
_1586190404.unknown
_1586190724.unknown
_1314701704.unknown
_1314648050.unknown
_1314647319.unknown
_1314647479.unknown
_593421032.unknown