ZIELGERICHTETE THERAPIE DES FORTGESCHRITTENEN ALK ...€¦ · ALK-vermittelter Signalwege bewirken...
Transcript of ZIELGERICHTETE THERAPIE DES FORTGESCHRITTENEN ALK ...€¦ · ALK-vermittelter Signalwege bewirken...
-
- 1 -
PD Dr. med. Niels Reinmuth Asklepios-Kliniken München-Gauting
VNR: 2760909010521940013 | Gültigkeit: 15.07.2020 – 31.12.2020
ZIELGERICHTETE THERAPIE DES FORTGESCHRITTENEN ALK-POSITIVEN
NICHT-KLEINZELLIGEN LUNGENKARZINOMS MIT ALK-INHIBITOREN
1. EINLEITUNG
Im deutschsprachigen Raum ist Lungenkrebs bei Frauen die dritthäufigste und bei Männern die zweit-häufigste maligne Tumorerkrankung [Griesinger et al. 2019, RKI 2019]. Hierbei stellen mit 80 – 85 % nicht-kleinzellige Lungenkarzinome (NSCLC) die häufigste Form von Lungentumoren dar [Baik et al. 2015], davon sind je etwa 40 % Adenokarzinome oder Plattenzell-epithelkarzinome [Getman et al. 2004].
Ein kleiner Anteil der NSCLC-Patienten, etwa 2 – 7 %, zeigen Veränderungen am anaplastischen Lymphom-Kinase(ALK)-Gen, die ursächlich für das Krebswachs-tum sind [Economopoulou und Mountzios 2016]. Bei Diagnosestellung weisen dabei bis zu 30 % dieser ALK-positiven (ALK+) NSCLC-Patienten Metastasen im zentralen Nervensystem (ZNS) auf [Hofer 2017], was mit einer schlechten Prognose sowie einer redu-zierten Lebensqualität assoziiert ist. Ein wirksamer Behandlungsansatz bei diesem Patientenkollektiv ist die Hemmung der in Tumorzellen konstitutiv aktivierten ALK mittels ALK-Inhibitoren (ALKi). Für eine solche ziel-gerichtete Therapie stehen seit einigen Jahren diverse Wirkstoffe zur Verfügung, weitere ALKi befinden sich in der klinischen Entwicklung. Durch die Behandlung mit ALKi kann im Vergleich zur klassischen Chemotherapie ein deutlich längeres medianes progressionsfreies Überleben (PFS) erreicht werden, bei gleichzeitig bes-
serer Verträglichkeit [Spagnuolo et al. 2018]. Für eine optimale Therapiesteuerung ist es daher entscheidend, ALK+ Patienten möglichst frühzeitig zu identifizieren.
Zu beachten ist, dass es beim Einsatz von allen ALKi im Therapieverlauf zu einer Resistenzbildung der Tu-morzellen und zum Progress kommt [Rothenstein und Chooback 2018]. Im Rahmen der Progression treten bei etwa 70 % (Hirnmetastasen zum Diagnosezeitpunkt) bzw. 20 % (keine Hirnmetastasen zum Diagnose-zeitpunkt) der Patienten unter Crizotinib-Behandlung Tumoren im ZNS auf [Costa et al. 2015]. Im Vergleich zu Crizotinib, dem ALKi der ersten Generation, zeigen ALKi der neuen Generation (Ceritinib, Alectinib, Brigatinib und Lorlatinib) eine deutlich bessere Wirksamkeit bei ZNS-Metastasen [Remon und Besse 2018]. Außerdem weisen die verfügbaren ALKi individuelle Resistenz-profile auf, die relevant für die Therapieplanung sind [Gainor et al. 2016].
Ziel dieser Fortbildung ist es, einen Überblick über die aktuell verfügbaren Therapieoptionen beim ALK+ NSCLC zu geben und wichtige Aspekte, wie die Wirk-samkeit von ALKi bei ZNS-Metastasen, das Auftreten von Resistenzmutationen sowie die Verträglichkeit und deren Auswirkungen auf die Lebensqualität der Patienten näher zu beleuchten.
-
- 2 -
ALK
EML4-ALK
EML4
ALK-EML4
Chromosom 2pA
C
BInaktive ALK Konstitutiv
aktivierte ALK bei EML4-ALK-Fusion
Aktivierte ALK
Ligand
EML4-ALK v1TD TAPE TK
EML4-ALK v3TD TK
EML4-ALK v5TD TK
EML4-ALK v2TD TAPE TK
ZIELGERICHTETE THERAPIE DES FORTGESCHRITTENEN ALK-POSITIVEN NICHT-KLEINZELLIGEN LUNGENKARZINOMS MIT ALK-INHIBITOREN
2. PATHOLOGIE
Das ALK-Gen kodiert für einen Tyrosinkinase-Rezeptor der Insulinrezeptor-Familie und wird durch eine Ligan-den-abhängige Dimerisierung aktiviert (Abbildung 1). Die durch ALK vermittelten Signalwege sind in zahl-reiche zelluläre Prozesse, wie Zellvermehrung, Zellin-vasion, Metastasenbildung und Apoptose-Resistenz, involviert [Spagnuolo et al. 2018]. Eine Veränderung des ALK-Gens durch Punktmutation, Amplifikation oder Translokation kann eine konstitutive Aktivierung ALK-vermittelter Signalwege bewirken und damit zu ungebremstem Tumorwachstum führen [Du et al. 2018, Nix und Brown 2015].
Die bei NSCLC auftretende Fusion eines ALK-Gen-abschnittes mit dem Echinoderm microtubule-asso-ciated protein-like(EML4)-Gen wurde erstmals 2007 nachgewiesen [Bayliss et al. 2016]. Beide Gene sind in entgegengesetzter Richtung auf dem kurzen Arm des Chromosom 2 lokalisiert, wobei das EML4-ALK-
Fusionsgen durch eine parazentrische Inversion in diesem Genabschnitt entsteht (Abbildung 1) [Bayliss et al. 2016]. Der Bruchpunkt des ALK-Gens ist stark konserviert [Katayama et al. 2015]. In der Regel trans-loziert ausschließlich der Genabschnitt für die intra-zelluläre Domäne, welche die Kinasefunktion erfüllt [Bayliss et al. 2016]. Die Fusionsstelle innerhalb des EML4-Gens ist jedoch variabel, sodass verschiedene Fusionsgene entstehen können (Abbildung 1). Bislang wurden 15 verschiedene Varianten identifiziert, wobei die Varianten 1, 2 und 3 am häufigsten vorkommen [Bayliss et al. 2016, Christopoulos et al. 2018]. Welche der Varianten vorliegt, spielt eine Rolle für die Prognose der NSCLC-Patienten. So kommt es bei Patienten mit der Variante 3 schneller zu einem Therapieversagen [Christopoulos et al. 2018]. Tritt neben der ALK-Mu-tation zusätzlich noch eine Mutation im Tumor-Sup-pressor-Gen Tp53 auf, verschlechtert dies zusätzlich die Prognose [Christopoulos et al. 2019].
Abb. 1: A) Das EML4-ALK-Fusionsgen entsteht durch eine parazentrische Inversion eines Genabschnitts auf dem kurzen Arm von Chromosom 2. B) Die im EML4-Anteil enthaltene Coiled-Coil-Domäne (TD) induziert eine Liganden-unabhängige Dimerisierung des EML4-ALK-Fusions-proteins und führt in Folge zu einer konstitutiven Aktivierung nachgeschalteter Signalwege. C) Häufige Varianten des EML4-ALK-Fusions-gens. Modifiziert nach [Bayliss et al. 2016, Rosenbaum et al. 2018]. TD, Trimerisation domain; TAPE, Tandem atypical propeller domain; TK, Tyrosinkinasedomäne; ALK, Anaplastische Lymphom-Kinase; EML4, Echinoderm microtubule-associated protein-like 4.
-
- 3 -
ZIELGERICHTETE THERAPIE DES FORTGESCHRITTENEN ALK-POSITIVEN NICHT-KLEINZELLIGEN LUNGENKARZINOMS MIT ALK-INHIBITOREN
3. DIAGNOSTIK
Nach Leitlinienempfehlung sollten neben anderen therapierelevanten Genveränderungen wie EGFR- und BRAF-V600-Mutationen sowie ROS1-Fusionen alle nicht kurativ behandelbaren NSCLC-Patienten, ins-besondere beim nicht-squamösen NSCLC, hinsichtlich ALK-Fusionen analysiert werden. Als Probenmaterial werden hierbei meist Gewebeproben, jedoch auch Blutproben (Liquid Biopsy) verwendet, z. B. wenn nicht ausreichend Gewebematerial zur Verfügung steht oder eine Entnahme mit zu hohen Risiken verbunden ist [Leitlinienprogramm Onkologie 2018].
Eine molekularpathologische Charakterisierung des Tumorgewebes ist dabei nicht nur vor der Erstlinie indiziert, sondern sollte auch bei Progression unter einer ALKi-Therapie erneut durchgeführt werden. Grund dafür ist die Resistenzbildung, die während der Behandlung bei nahezu allen Patienten auftritt [Griesinger et al. 2019]. Zukünftig wird die Testung auf Resistenzmutationen höchstwahrscheinlich an Be-deutung gewinnen, um die optimale Therapiesequenz der Wirkstoffe zu ermitteln.
TESTVERFAHREN
Zum Nachweis molekularpathogener Veränderungen können grundsätzlich unterschiedliche Testverfahren eingesetzt werden. Hierzu gehören die Fluoreszenz-in-situ-Hybridisierung (FISH), die Immunhistochemie (IHC), die Reverse-Transkriptase-PCR (RT-PCR) und das Next-Generation-Sequencing (NGS) [Du et al. 2018].
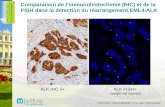
FISH ist die derzeit am häufigsten eingesetzte und zuverlässigste Methode zum Nachweis von ALK-Trans-lokationen [Du et al. 2018]. Das Prinzip beruht auf der getrennten Detektion des 5‘- und des 3‘-Endes im ALK-Gen mittels fluoreszenzmarkierter Nukleinsäure-Sonden [Du et al. 2018, Weickhardt et al. 2013]. Mittels FISH lassen sich ALK-Umlagerungen unabhängig von der Variante und dem Fusionspartner nachweisen und es wird nur wenig Probenmaterial (ca. 100 Tumorzellen) benötigt. Nachteil der Methode ist der relativ hohe Aufwand (benötigt u. a. ein Fluoreszenz-Mikroskop und speziell ausgebildetes Personal), spezifische
ALK-Fusionspartner bzw. die Fusionsvariante oder seltene komplexe Umlagerungen können mit FISH nicht detektiert werden [Weickhardt et al. 2013].
Im Gegensatz zu FISH oder der RT-PCR ist mit der IHC ein Nachweis von pathogen verändertem ALK auf Proteinebene möglich. Im Vergleich zum funktionellen ALK-Protein in gesundem Gewebe ist die Expression der katalytischen ALK-Domäne im Tumorgewebe deutlich stärker ausgeprägt. Dies kann mit einem ALK-spezi-fischen Antikörper schnell und einfach nachgewiesen werden. Die IHC ist sehr kostengünstig und liefert in der Regel sehr zuverlässige Ergebnisse [Du et al. 2018].
RT-PCR-basierte Assays werden für die Testung auf ALK-Translokationen weniger häufig angewendet als FISH oder IHC. Sie besitzen jedoch einige Vorteile gegenüber den anderen Methoden. Während der Nachweis einer ALK-Translokation bei FISH und IHC indirekt erfolgt, kann mit der RT-PCR die Genfusion direkt nachgewiesen und die exakte Variante der Um-lagerung identifiziert werden. Darüber hinaus besitzt diese Methode eine hohe Sensitivität und Spezifität und ist schnell und einfach durchführbar. Durch die hohe Sensitivität besteht jedoch auch ein höheres Risiko für falsch-positive Ergebnisse [Du et al. 2018, Niu et al. 2017].
Das NGS gewinnt als Analyseverfahren zunehmend an Bedeutung. Der große Vorteil besteht darin, dass mittels Multiplexverfahren neuartige ALK-Fusionspartner und andere Genveränderungen, die im Zusammenhang mit Lungenkarzinomen stehen, parallel detektiert werden können [Du et al. 2018]. Die klinisch relevanteste Me-thode ist das Targeted-Exome-Sequencing, bei dem gezielt Genabschnitte im Exom analysiert werden. Noch ist die Methode jedoch nicht Analyse-Standard [Du et al. 2018].
BILDGEBENDE DIAGNOSTIK
Neben der molekularpathologischen Charakterisierung sollte eine gezielte Ausbreitungsdiagnostik erfolgen. Beim NSCLC können Metastasen in nahezu allen
-
- 4 -
ZIELGERICHTETE THERAPIE DES FORTGESCHRITTENEN ALK-POSITIVEN NICHT-KLEINZELLIGEN LUNGENKARZINOMS MIT ALK-INHIBITOREN
Körperregionen auftreten. Am häufigsten betroffen sind Lymphknoten, ipsi- oder kontralaterale Lunge, Skelett, Leber, Nebennieren und ZNS [Griesinger et al. 2019]. Hirn-metastasen kommt dabei eine besondere Bedeutung zu, da sie mit einer hohen Mortalität und einer erheblichen
Verschlechterung der Lebensqualität assoziiert sind [Economopoulou und Mountzios 2016]. Laut Leitlinien ist bei klinischen Symptomen, die auf ZNS-Metastasen hindeuten, eine bildgebende Diagnostik mittels Magnet-resonanztomografie (MRT) indiziert [Griesinger et al. 2019].
4. ZIELGERICHTETE THERAPIE MIT ALK-INHIBITOREN
Durch die Hemmung der ALK-Aktivität mittels ALKi kann die Erkrankung bei ALK+ Patienten über einen relativ langen Zeitraum kontrolliert werden. Der Vor-teil dieser zielgerichteten Therapie ist, dass aufgrund der niedrigen Expression von ALK in gesunden Zellen nahezu ausschließlich Tumorzellen angesprochen werden [Spagnuolo et al. 2018].
Für die Erstlinien-Behandlung erwachsener ALK+ NSCLC-Patienten stehen mittlerweile eine ganze Reihe von ALKi zur Verfügung: Crizotinib, Ceritinib, Alectinib und seit 2020 auch Brigatinib. In der Zweitlinie können Crizotinib sowie Ceritinib, Alectinib und Brigatinib (je-weils nach Crizotinib-Vorbehandlung) oder Lorlatinib (nach Alectinib oder Ceritinib bzw. nach Crizotinib und mindestens einem weiteren ALKi) eingesetzt werden [EMA 2020a, EMA 2020b, EMA 2020c, EMA 2020d, EMA 2020e].
4.1 CRIZOTINIB
ErstlinientherapieCrizotinib erhielt 2015 als erster ALKi die EU-Zulas-sung für die Erstlinientherapie [EMA 2020d] bei ALK+ fortgeschrittenem NSCLC und ist darüber hinaus auch bei ROS1 + NSCLC wirksam. In der offenen Phase-III-Studie PROFILE 1014 war Crizotinib einer intravenösen Chemotherapie mit Pemetrexed plus Cisplatin bzw. Carboplatin bezüglich des medianen PFS überlegen (10,9 Monate vs. 7,0 Monate, Hazard Ratio [HR]: 0,45; 95 % Konfidenzintervall [KI]: 0,35 – 0,60; p
-
- 5 -
ZIELGERICHTETE THERAPIE DES FORTGESCHRITTENEN ALK-POSITIVEN NICHT-KLEINZELLIGEN LUNGENKARZINOMS MIT ALK-INHIBITOREN
lag unter Crizotinib ebenfalls signifikant höher (65 % vs. 20 %; p
-
- 6 -
ZIELGERICHTETE THERAPIE DES FORTGESCHRITTENEN ALK-POSITIVEN NICHT-KLEINZELLIGEN LUNGENKARZINOMS MIT ALK-INHIBITOREN
dreimal so lang (33,1 Monate vs. 11,1 Monate). Im Ver-gleich zu Crizotinib reduzierte Alectinib das Risiko für eine Krankheitsprogression um 57 % und verlängerte das mediane PFS (gemäß Prüfarzt) auf 34,8 Monate gegenüber 10,9 Monate (HR: 0,43, 95 % KI: 0,32 – 0,58). Eine abschließende Analyse für das OS steht noch aus, da die Daten zum Zeitpunkt der Studienauswertung noch unreif waren [Camidge et al. 2018b]. Außerdem erwies sich die Therapie mit Alectinib gegenüber einer Crizotinib-Therapie hinsichtlich einer klinisch relevanten Verbesserung der Symptome als überlegen und war mit einer höheren Lebensqualität assoziiert [Perol et al. 2018].
Die häufigsten unter Alectinib auftretenden Nebenwir-kungen in der ALEX-Studie waren Obstipation (34 %), Anämie (20 %) und Fatigue (19 %). Erhöhte Leber-werte (Alanin- und Aspartat-Aminotransferase) sowie Anämie gehörten mit jeweils 5 % zu den häufigsten unerwünschten Ereignissen mit Grad ≥ 3. Insgesamt führte Alectinib auch bei längerer Behandlung zu weniger schweren (Grad 3 – 5) Nebenwirkungen als Crizotinib [Peters et al. 2017].
ZweitlinientherapieZur Zweitlinientherapie wurde Alectinib 2017 zugelassen [EMA 2020a]. Maßgeblich hierfür waren die Ergebnisse von zwei Phase-II-Studien mit 138 (globale Studie) bzw. 87 (nordamerikanische Studie) Crizotinib-refraktären Patienten. In einer gepoolten Analyse der Studiendaten betrug die ORR 51,3 % und die DCR 78,8 %. Die mediane Ansprechdauer lag bei 14,9 Monaten und das mediane PFS betrug 8,3 Monate [Yang et al. 2017].
Die multizentrische Phase-III-Studie ALUR evaluierte die Wirksamkeit und Verträglichkeit von Alectinib im Vergleich zu einer Chemotherapie mit Pem/Doce bei Crizotinib-refraktären/rezidiven Patienten. Sowohl hin-sichtlich der ORR als auch der DCR war Alectinib der Chemotherapie hier deutlich überlegen (ORR: 37,5 % vs. 2,9 %; DCR: 80,6 % vs. 28,6 %). Die Studienteilnehmer erreichten in der Alectinib-Gruppe ein medianes PFS von 9,6 Monaten vs.1,4 Monaten im Vergleichsarm (HR: 0,15; 95 % KI: 0,08 – 0,29; p
-
- 7 -
ZIELGERICHTETE THERAPIE DES FORTGESCHRITTENEN ALK-POSITIVEN NICHT-KLEINZELLIGEN LUNGENKARZINOMS MIT ALK-INHIBITOREN
ZweitlinientherapieFür die Zweitlinientherapie (nach Crizotinib-Vorbehand-lung) erhielt Brigatinib 2018 die EU-Zulassung, basierend auf den Ergebnissen der Phase-II-Studie [EMA 2020b]. Die Studie evaluierte die Wirksamkeit und Sicherheit des ALKi in zwei Dosierungsschemata: 90 mg täglich bzw. 180 mg mit einer siebentägigen Einleitungsphase von 90 mg täglich. Für den Patientenarm mit der sie-bentägigen Einleitungsphase lagen die ORR bei 56 % und die DCR bei 84 %, mit einer medianen Ansprech-dauer von 13,8 Monaten. Das mediane PFS betrug 16,7 Monate und das mediane OS lag in der letzten Auswertung bei 34,1 Monaten [Huber et al. 2018]. In den ersten sieben Monaten stieg die Lebensqualität der mit Brigatinib behandelten Patienten stetig an und nahm anschließend leicht ab, blieb jedoch durchgehend über dem Niveau zu Studienbeginn [Kim et al. 2017].
4.5 LORLATINIB
ZweitlinientherapieLorlatinib ist seit 2019 in der EU für die Zweitlinien- therapie von ALK+ fortgeschrittenem NSCLC zugelas-sen, nach vorangegangener Therapie mit Alectinib oder Ceritinib bzw. nach Crizotinib und mindestens einem weiteren ALKi [EMA 2020c]. Die Anti-Tumor-Aktivität und Sicherheit von Lorlatinib wurde in einer Phase-II-Studie mit insgesamt 276 ALK+-Patienten mit und ohne ALKi-Vortherapie untersucht. Hierbei betrug die
ORR bei ALKi-naiven Patienten 90 % und 70 % bei mit Crizotinib vorbehandelten Patienten. Für Studienteil-nehmer, die mit einem anderen ALKi vorbehandelt wurden, lag die ORR bei 32 %, bei Vorbehandlung mit zwei oder mehr ALKi betrug sie 39 %. Zu den häufigsten Nebenwirkungen zählten Hypercholesterinämie (81 %) und Hypertriglyceridämie (60 %) [Solomon et al. 2018a].
Die Wirksamkeit und Sicherheit einer Lorlatinib- Monotherapie im Vergleich zu Crizotinib bei ALKi-naiven Patienten mit fortgeschrittenem ALK+ NSCLC wird derzeit in einer aktuell laufenden Phase-III-Studie evaluiert (NCT03052608). Primärer Endpunkte der Studie ist das PFS nach verblindetem unabhängigem Review-Komitee [NIH 2020].
4.6 RESISTENZMUTATIONEN UNTER ALK-INHIBITOREN
Unter ALKi-Therapie kommt es in der Regel zu einer Selektion von Mutationen, die zu Resistenzen gegen-über dem eingesetzten ALKi führen. Hierzu gehö-ren Mutationen im ALK-Gen (Punktmutationen oder Genamplifikationen), aber auch ALK-unabhängige Mutationen, die zur Aktivierung alternativer Signal-wege führen. Je nach ALKi herrschen dabei typische Resistenzmutationen vor (Abbildung 2). Häufig tritt z. B. die G1202R-Mutation unter Behandlung von ALKi der zweiten Generation auf [Gainor et al. 2016].
Abb. 2: Chemische Struktur und häufige Resistenzmutationen von ALK-Inhibitoren; modifiziert nach [Latif et al. 2018]. *Nach Fachinformation der jeweiligen Arzneistoffe, abrufbar unter www.fachinfo.de
F
CI
CINH2
N
N
NH
N
O
Crizotinib ALK-Inhibitor der 1. Generation Dosierung*: 250 mg (1 Tablette) 2x tgl.
Resistenzmutationen L1196M, G1269A C1156Y, L1152R I1171T, F1174L E1210K, 1151T-ins S1206Y, G1202R D1203N, V1180L
CI N
N
NH NH
OO
O
S
N H
Ceritinib ALK-Inhibitor der 2. Generation Dosierung*: 450 mg (3 Tabletten) 1x tgl. zu einer Mahlzeit
Resistenzmutationen F1174C, G1202R G1202del, C1156Y 1151Tins, L1152R F1174V, F1174L
Alectinib ALK-Inhibitor der 2. Generation Dosierung*: 600 mg (4 Tabletten) 2x tgl. zusammen mit einem Nahrungsmittel
Resistenzmutationen I1171T/N/S, G1202R V1180L
Lorlatinib ALK-Inhibitor der 3. Generation Dosierung*: 100 mg (1 Tablette) 1x tgl.
Resistenzmutationen L1198F, C1156Y/L1198F C1156Y
Brigatinib ALK-Inhibitor der 3. Generation Dosierung*: 90 mg (1 Tablette) 1x tgl. während der 7-tägigen Einleitungsphase, anschließend 180 mg (1 Tablette) 1x tgl.
Resistenzmutationen G1202R E1210K + S1206C E1210K + D1203N
O
O
N
NH N
NC
O
N
NN
H2N
NF
O
N O
N
N
N
CI N
N
HN
OP
N H
-
- 8 -
Tab. 1: Wirkspektrum der ALK-Inhibitoren gegenüber typischen ALK-Resistenzmutationen. Angegeben sind mittlere inhibitori-sche Konzentrationen (IC50) des jeweiligen Wirkstoffs in BA/F3-Zellen mit der EML4-ALK-Fusionsvariante 1 (A) und der EML4-ALK- Fusionsvariante 3 (B); modifiziert nach [Horn et al. 2019].
A B
ZIELGERICHTETE THERAPIE DES FORTGESCHRITTENEN ALK-POSITIVEN NICHT-KLEINZELLIGEN LUNGENKARZINOMS MIT ALK-INHIBITOREN
Bei den meisten Patienten kommt es aufgrund der Resistenzbildung unter der ALKi-Behandlung schließ-lich zu einem Progress [Gainor et al. 2016]. Für die weitere Therapieplanung ist es daher entscheidend zu bestimmen, welche Mutationen auftreten und welche ALKi in diesem Fall noch wirksam sind. Zur Beurteilung der Wirksamkeit von ALKi hinsichtlich bestimmter Mutationen stehen bislang lediglich In- vitro-Daten und einige Fallberichte zur Verfügung [Gai-nor et al. 2016]. Hiernach weisen die ALKi Brigatinib und Lorlatinib das breiteste Wirkungsspektrum gegenüber
häufigen Resistenzmutationen auf (Tabelle 1) [Gainor et al. 2016, Horn et al. 2019]. Die Wirksamkeit von ALKi gegenüber bestimmten Resistenzmutationen wird zukünftig wahrscheinlich zunehmend Einfluss auf die Therapiesequenz nehmen. Ein wichtiges Diagnosetool zur Bestimmung von Resistenzmutationen ist das NGS (siehe Kapitel 3), das zukünftig an Bedeutung für die Steuerung der Therapie und die Sequenz der ALKi gewinnen könnte. Zur Beurteilung der klinischen Relevanz der Resistenzen sind klinische Untersuchun-gen jedoch unabdingbar.
Crizotinib Certinib Ensartinib Alectinib Brigantinib Lorlatinib
WT 23,30 16,23–33,46
12,47 7,813–19,92
1,281 1,073–1,530
1,377 1,044–1,818
0,959 0,794–1,158
0,267 0,212–0,337
G1123S 27,17 16,75–44,09
661,6 271,7–1611
0,983 0,711–1,358
1,559 1,167–2,082
11,14 7,082–17,53
2,855 2,238–3,642
L1152R 361,3 205,5–635,1
167,3 145,2–968,4
34,75 23,42–51,56
3,501 3,110–3,943
0,798 0,640–0,995
7,402 8,190–20,24
C1156Y 306,0 100,6–931,3
199,7 54,09–737,4
27,27 9,057–82,12
13,61 5,461–33,91
7,659 3,999–14,67
8,938 4,206–18,99
I1171T 471,9 190,3–1171
165,1 59,20–460,4
69,25 339,21–122,3
379,8 126,4–1141
25,85 10,58–63,14
52,53 23,42–117,8
F1174C 294,4 72,52–1196
205,1 69,89–601,6
58,55 24,82–138,1
19,22 9,222–40,05
29,10 12,31–68,78
9,786 5,047–18,98
F1174V 57,91 33,13–100,7
51,28 24,74–106,3
6,992 5,689–8,593
1,988 1,700–2,325
5,165 4,110–6,491
2,100 1,732–2,545
V1180L 114,5 44,44–295,0
11,87 7,962–17,70
4,436 3,401–5,786
1902 1186–3051
1,563 1,233–1,983
1,650 1,394–1,953
L1196M 637,1 246,7–1645
133,8 59,24–302,4
59,53 31,25–113,4
58,74 23,75–145,3
20,09 8,841–45,65
56,52 30,07–106,2
L1198F 27,97 14,30–54,73
1722 587,6–5045
0,323 0,199–,524
201,9 125,2–325,5
48,53 29,15–80,80
56,61 26,51–120,9
G1202del 179,9 59,72–541,6
319,1 165,9–614,0
138,9 68,17–283,0
963 614,7–1509
25,02 14,85–42,15
11,15 5,858–21,21
G1202R 289,5 197,4–424,4
252,4 147,7–413,3
316,0 212,4–470,2
1918 1151–3197
30,92 233,47–40,72
31,18 26,41–36,81
S1206Y 177,5 65,38–482,0
53,14 25,64–110,1
31,45 21,92–45,14
7,216 3,878–13,43
17,56 8,543–36,10
4,704 2,795–7,918
E1210K 4027 887,6–20981
345,6 147,4–809,1
3010 1015–9077
5065 2991–8557
299,2 144,7–622
38,04 10,67–139,3
F1245C 197,6 68,43–571,3
216,3 87,17–536,6
22,03 11,88–40,85
13,62 6,995–26,53
26,00 12,48–54,18
7,357 4,538–11,93
G1269A 699,3 176,9–2765
67,13 29,22–154,3
221,8 97,82–503,1
58,66 42,83–80,35
11,41 5,492–23,72
76,39 31,93–182,7
Crizotinib Certinib Ensartinib Alectinib Brigantinib Lorlatinib
WT 205,3 70,5–597,9
75,1 29,72–189,8
24,92 9,450–65,70
29,51 15,53–56,05
16,75 10,10–27,77
4,456 2,376–8,357
G1123S 54,50 23,65–125,6
651,2 179,3–2365
1,309 0,701–2,446
3,000 1,424–6,319
25,79 9,503–69,99
3,557 2,111–5,992
L1152R 124,3 66,44–232,6
165,7 533,61–511,9
14,80 7,863–27,86
3,300 2,502–4,354
0,190 0,126–0,287
4,246 2,228–8,091
C1156Y 110,4 69,28–176,1
58,66 38,68–88,98
10,92 7,338–16,25
5,266 3,842–7,218
2,263 3,842–7,218
2,313 1,570–3,407
I1171T 152,8 79,26–294,5
17,60 13,11–23,62
13,84 6,726–28,50
24,78 14,50–42,36
3,135 2,297–4,278
7,450 4,528–12,26
F1174C 257,7 85,86–773,5
248,5 110,2–560,4
64,79 23,95–175,3
286,2 123,0–665,8
28,06 13,40–58,75
13,11 6,494–26,48
F1174V 238,8 170,4–1003
157,4 60,73–408,0
33,28 22,67–48,86
38,43 21,25–69,52
31,92 20,08–50,75
8,258 5,731–11,90
V1180L 98,12 43,35–222,6
18,63 7,693–45,10
9,423 5,058–17,56
2166 601,8–7798
3,523 1,950–6,365
2,653 1,569–4,484
L1196M 924,5 415,4–2057
205,9 58,74–721,6
81,31 37,03–178,6
929,6 422,2–2047
26,66 11,10–64,04
69,81 28,04–173,8
L1198F 46,52 17,84–121,3
2072 382,2–11228
3,807 2,080–6,966
1205 494,7–2933
157,0 59,32–415,5
59,47 313,53–112,2
G1202del 322,0 125,6–765,0
586,7 173,2–1988
474,7 169,0–1333
>10000 N/A
104,6 337,6–290,8
26,19 12,51–54,86
G1202R 440,5 175,7–1105
405,6 189,5–868,1
315,9 194,1–514,1
>10000 N/A
83,82 50,43–139,3
35,72 20,46–62,36
D1203N 332,0 170,1–648,2
329,2 172,0–630,1
21,10 11,73–37,98
142,7 46,29–439,7
33,42 20,19–55,30
19,73 12,16–32,01
S1206Y 175,7 60,74–508,3
90,5 24,02–337,6
48,24 23,47–99,14
9,804 6,057–15,87
16,29 8,313–31,94
3,238 3,042–5,134
E1210K 482,6 170,5–1366
178,2 83,58–380,1
527,6 198,5–1402
759,3 255,7–2255
162,9 58,92–450,3
7,565 3,780–15,14
F1245C 289,9 119,2–704,8
208,0 63,52–680,9
52,90 23,83–117,5
65,55 27,22–157,9
46,16 21,58–98,70
14,82 6,451–34,00
G1269A 511,4 169,3–1544
52,65 23,98–115,6
123,1 65,00–268,6
100,4 45,83–220,0
10,02 5,337–18,82
42,70 20,85–87,42
1000nM
–800nM
–600nM
–400nM
–200nM
0nM
1000nM
–800nM
–600nM
–400nM
–200nM
0nM
-
- 9 -
ZIELGERICHTETE THERAPIE DES FORTGESCHRITTENEN ALK-POSITIVEN NICHT-KLEINZELLIGEN LUNGENKARZINOMS MIT ALK-INHIBITOREN
5. ZNS-WIRKSAMKEIT DER ALK-INHIBITOREN
Metastasen im ZNS treten beim ALK+ NSCLC häufig auf, bei bis zu 30 % der Patienten sind bereits zum Zeitpunkt der Diagnose Hirnmetastasen nachweisbar [Hofer 2017]. Im Verlauf einer Therapie mit einem Tyro-sinkinaseinhibitor kommt es darüber hinaus bei über der Hälfte der Patienten zu einer ZNS-Progression, die mit einer verringerten Lebensqualität und einer schlechten Prognose assoziiert ist [Remon und Besse 2018].
Hinsichtlich der Wirksamkeit im ZNS unterscheiden sich die ALKi zum Teil deutlich (Tabelle 2). So besitzt der ALKi der ersten Generation, Crizotinib, nur eine geringe ZNS-Aktivität und bei 70 % der mit diesem behandelten Patienten tritt eine Progression mit Metas- tasenbildung im ZNS auf [Remon und Besse 2018]. Eine verbesserte Wirksamkeit zeigen hingegen ALKi der zweiten Generation. In der ASCEND-3-Studie konnte unter Ceritinib eine intrakranielle DCR von 80 % er-reicht werden [Felip et al. 2015]. Die ASCEND-4-Studie demonstrierte ebenfalls eine gute ZNS-Wirksamkeit von Ceritinib, die intrakranielle ORR lag hier bei 72,7 % bei Patienten mit messbaren Hirnmetastasen (gegen-über 27,3 % im Chemotherapie-Arm). Die mediane intrakranielle DOR betrug 16,6 Monate [Soria et al. 2017]. In der ASCEND-5-Studie profitierten Patienten mit Hirnmetastasen hinsichtlich des medianen PFS ähnlich gut von einer Ceritinib-Therapie wie Patienten ohne Hirnmetastasen [Shaw et al. 2017b].
Eine hohe intrakranielle Wirksamkeit besitzt auch Alecti-nib. Im Gegensatz zu Crizotinib und Ceritinib ist Alectinib kein Substrat des Effluxtransporters P-Glykoprotein, der den aktiven Transport aus dem ZNS vermittelt, daher wird eine vergleichsweise hohe Alectinib-Konzentration im ZNS erreicht [Zhang et al. 2015]. In einer Analyse zur intrakraniellen Wirksamkeit von Alectinib in der Erstlinie lag die intrakranielle ORR bei Patienten mit messbaren oder nicht-messbaren Hirnmetastasen mit 59 % (95 % KI: 46 – 71) etwa doppelt so hoch wie in der Kontroll-gruppe (26 %; 95 % KI: 15 – 39). Alectinib zeigte hier eine kumulative Inzidenz der ZNS-Progression über zwölf Monate von 9,4 % im Vergleich zu 41,4 % unter Crizotinib [Peters et al. 2017]. Auch in der Zweitlinie zeigte Alectinib eine sehr gute Wirksamkeit hinsichtlich des intrakraniellen Ansprechens [Novello et al. 2018].
Die ALKi der dritten Generation, Brigatinib und Lorlati-nib, weisen ebenfalls eine hohe ZNS-Wirksamkeit auf. Nach den Ergebnissen der zweiten Interimsanalyse der ALTA-1L-Studie profitierten insbesondere Patienten mit Hirnmetastasen bei Behandlungsbeginn von einer Brigatinib-Therapie. Das Risiko für eine Krankheits-progression oder Tod war hier um ca. 75 % reduziert, mit einem medianen PFS von 24,0 unter Brigatinib vs. 5,6 bei Crizotinib (HR: 0,25 [0,14 – 0,46]) bewertet durch ein verblindetes unabhängiges Review-Komitee (BIRC) (Abbildung 3). Das mediane PFS nach Prüfarzt-beurteilung war unter Brigatinib noch nicht erreicht vs. 5,9 unter Crizotinib-Behandlung (HR: 0,24 [0,12 – 0,45]). Die intrakranielle ORR lag im Brigatinib-Arm mit 66 % ebenfalls deutlich höher als im Crizotinib-Arm mit 16 %. Hinsichtlich des medianen PFS wiesen Patienten mit und ohne Hirnmetastasen keinen Unterschied auf (je 24,0 Monate bei Bewertung durch ein verblindetes unabhängiges Review-Komitee [Camidge et al. 2019]. Auch in der Zweitlinie ist die intrakranielle ORR (67 %) und die intrakranielle DCR (83 %) hoch [Huber et al. 2018]. Eine ähnlich hohe ORR zeigte auch Lorlatinib. Hier lag die intrakranielle ORR abhängig von der Vor-behandlung der Patienten zwischen 53 % und 87 % [Solomon et al. 2018a].
Abb. 3: Krankheitsprogression bei Patienten mit ZNS-Metasta-sen zu Studienbeginn in der ALTA-1L Studie (zweite Interimsana-lyse) beurteilt durch BIRC; modifiziert nach [Camidge et al. 2019].
100 –
80 –
60 –
40 –
20 –
0 –
PFS
(% P
atie
nten
)
Zeit (Monate)
Hazard Ratio für Progression oder Tod 0,25 (95 % KI, 0,14 – 0,46)
p
-
- 10 -
ZIELGERICHTETE THERAPIE DES FORTGESCHRITTENEN ALK-POSITIVEN NICHT-KLEINZELLIGEN LUNGENKARZINOMS MIT ALK-INHIBITOREN
ALK- Inhibitor
Studie [Ref.]
Vorbehandlung
Patientenanzahl mit ZNS-Metastasen zu Studienbeginn
Patientenanzahl mit messbaren ZNS-Metastasen
icRR (%)
icTTP (Monate)
s/ic PFS (Monate)
icDOR (Monate)
Crizotinib PROFILE 1005 + 1007 gepooled [Costa et al. 2015]ALK-naiv mit vorheriger CT
275 22/18b 18/33b 7,0/13,2 NA 26,4/NRb
PROFILE 1014 Phase III [Solomon et al. 2016]ALK-naiv
79 79 185c 15,7 sPFS: 9 NA
Ceritinib ASCEND 5, Phase III [Shaw et al. 2017b] Crizotinib + CT-resistent
133 17 35 72,7
NA sPFS: 4,4 6,9 16,6
ASCEND 4, Phase III [Soria et al. 2017]ALK-naiv
121 22 62 NA sPFS: 10,7 NA
ASCEND 3, Phase II [Felip et al. 2015]ALK-TKI-naiva
49 13 39,4 NA sPFS: 10,8 9,2
ASCEND 2, Phase II [Crino et al. 2016]Crizotinib-resistent
100 33 63 NA sPFS: 5,4 8,2
ASCEND 1, Phase I [Kim et al. 2017]Naiv/ vorbehandelt
94 36 61d NA NA 11,1d
Alectinib Gepoolte Analyse Phase II [Gadgeel et al. 2016]Crizotinib-resistent
136 50 64
9,2 NA 10,8
ALUR, Phase II [Novello et al. 2018]Crizotinib- und CT-resistent
76 40 54 NA sPFS: 9,6 17,3
ALEX, Phase III [Gadgeel et al. 2018, Peters et al. 2017]ALK TKI-naiv
122 21 81 NA sPFS: 25,7 ?
Lorlatinib Phase I [Shaw et al. 2017a]ALK-positiv (11 % Crizotinib-naiv)
41 19 42 NA sPFS: 9,6 12,4
Phase II [Solomon et al. 2018a]ALK/ROS1-positiv 12 5 60 NA sPFS: 7,0 12,0ALK-TKI-naiv 8 8 75 NA NR NACrizotinib oder Crizotinib + 1 – 2 CT
37 37 68 NA NR NA
TKI außer Crizotinib ± CT 12 12 42 NA sPFS: 5,5 NA2 – 3 ALK-TKI ± CT 83 83 48 NA sPFS: 6,9 NA
Brigatinib Phase I [Gettinger et al. 2016]ALK-naiv und Crizotinib-resistent
46 15 53
NA icPFS: 15,6 18,9
ALTA Phase II [Huber et al. 2018, Kim et al. 2017]Crizotinib-resistent
153 18 67e NA icPFS: 18,4e
NRe
ALTA-1L, Phase III [Camidge et al. 2019]CT
40 18 78 NA sPFS/ icPFS: 24,0f (NRg)
NR
icRR, intrakranielle Ansprechrate; icTTP, intrakranielle Zeit bis zur Progression; s/icPFS,systemisches/intrakranielles progressionsfreies Überleben; icDOR, intrakranielle Ansprechdauer; CT, Chemotherapie; NA, nicht verfügbar; NR, nicht erreicht ; TKI, Tyrosinkinaseinhibitor. aALKi-naiv und Chemotherapie-naiv oder bis zu drei Chemotherapien mit Progression während oder nach der letzten Chemotherapie. baufgrund von Hirnmetastasen vorbehandelt/nicht vorbehandelt. cintrakranielle DOR nach zwölf Wochen. dGesamtwert für ALKi-naive und ALK-Inhi-bitor-vorbehandelte Patienten. ePatienten mit 180 mg/Tag. fBewertung durch unabhängiges Review-Komitee. gBewertung durch Prüfarzt.
Tab. 2: Ausgewählte Studiendaten zur Wirksamkeit von ALK-Inhibitoren bei ZNS-Metastasen; modifiziert nach [Remon und Besse 2018].
-
- 11 -
ZIELGERICHTETE THERAPIE DES FORTGESCHRITTENEN ALK-POSITIVEN NICHT-KLEINZELLIGEN LUNGENKARZINOMS MIT ALK-INHIBITOREN
6. FAZIT Das ALK+ Patientenkollektiv stellt unter den NSCLC-Patienten mit 2 – 7 % eine Minderheit dar. Dennoch ist die Identifizierung der betroffenen Patienten besonders wichtig, damit diese von einer zielgerichteten Therapie in Form von ALKi profitieren können. In der molekular-pathologischen Diagnostik finden derzeit FISH, IHC, RT-PCR und NGS als Nachweisverfahren Anwendung. Mit der Neuzulassung von Brigatinib 2020 stehen nun insgesamt vier ALKi für die Erstlinientherapie bei ALK+
Patienten zur Verfügung. Neben der systemischen Wirksamkeit und Sicherheit der ALKi spielen ihre Akti-vität gegenüber ALK-Resistenzmutationen sowie ihre intrakranielle Wirksamkeit für die Therapieplanung eine große Rolle. In-vitro-Daten und Fallstudien geben erste Hinweise auf mögliche günstige Therapiesequenzen. Auf diesem Gebiet sind jedoch noch weitere, vor allem klinische Studien essenziell, um optimale Therapie- sequenzen für jeden einzelnen Patienten zu identifizieren.
7. LITERATUR Baik CS, Chamberlain MC, Chow LQ. Targeted therapy for brain metasta-
ses in EGFR-mutated and ALK-rearranged non-small-cell lung cancer. J Thorac Oncol 2015;10(9):1268 – 78
Bayliss R, Choi J, Fennell DA, et al. Molecular mechanisms that underpin EML4-ALK driven cancers and their response to targeted drugs. Cell Mol Life Sci 2016;73(6):1209 – 24
Blackhall F, Ross Camidge D, Shaw AT, et al. Final results of the large-scale multinational trial PROFILE 1005: efficacy and safety of crizotinib in previously treated patients with advanced/metastatic ALK-positive non-small-cell lung cancer. ESMO Open 2017;2(3):e000219
Camidge D, Kim HR, M. Ahn M, et al. Brigatinib vs crizotinib in ALK inhibi-tor–naive advanced ALK+ NSCLC: updated results from the phase 3 ALTA-1L trial, oral presentation at ESMO ASIA congress in Singapore, 23 November 2019. 2019. https://oncologypro.esmo.org/meeting-resources/esmo-asia-congress-2019/brigatinib-vs-crizotinib-in-patients-with-alk-inhibitor-naive-advanced-alk-nsclc-updated-results-from-the-phase-iii-alta-1l-trial, abgerufen am: 29.04.2020
Camidge DR, Kim HR, Ahn MJ, et al. Brigatinib versus crizotinib in ALK-posi-tive non-small-cell lung cancer. N Engl J Med 2018a;379(21):2027-39
Camidge DR, Peters S, Mok T, et al. Updated efficacy and safety data from the global phase III ALEX study of alectinib (ALC) vs crizotinib (CZ) in un-treated advanced ALK+ NSCLC. J Clin Oncol 2018b;36(suppl.):abstr 9043
Christopoulos P, Endris V, Bozorgmehr F, et al. EML4-ALK fusion variant V3 is a high-risk feature conferring accelerated metastatic spread, early treatment failure and worse overall survival in ALK(+) non-small cell lung cancer. Int J Cancer 2018;142(12):2589 – 98
Christopoulos P, Kirchner M, Bozorgmehr F, et al. Identification of a highly lethal V3(+) TP53(+) subset in ALK(+) lung adenocarcinoma. Int J Cancer 2019;144(1):190 – 9
Costa DB, Shaw AT, Ou SH, et al. Clinical experience with crizotinib in patients with advanced ALK-rearranged non-small-cell lung cancer and brain metastases. J Clin Oncol 2015;33(17):1881 – 8
Crino L, Ahn MJ, De Marinis F, et al. Multicenter phase II study of whole-body and intracranial activity with ceritinib in patients with ALK-rearranged non-small-cell lung cancer previously treated with chemotherapy and crizotinib: Results from ASCEND-2. J Clin Oncol 2016;34(24):2866 – 73
Du X, Shao Y, Qin HF, et al. ALK-rearrangement in non-small-cell lung cancer (NSCLC). Thorac Cancer 2018;9(4):423 – 30
Economopoulou P, Mountzios G. Non-small cell lung cancer (NSCLC) and central nervous system (CNS) metastases: role of tyrosine kinase in-hibitors (TKIs) and evidence in favor or against their use with concurrent cranial radiotherapy. Transl Lung Cancer Res 2016;5(6):588 – 98
EMA. European Medical Agency Human medicine European public as-sessment report (EPAR): Alecensa (Alectinib). 2020a. https://www.ema.europa.eu/en/medicines/human/EPAR/alecensa, abgerufen am: 10.06.2020
EMA. European Medical Agency Human medicine European public as-sessment report (EPAR): Alunbrig (Brigatinib). 2020b. https://www.ema.europa.eu/en/medicines/human/EPAR/alunbrig, abgerufen am: 10.06.2020
EMA. European Medical Agency Human medicine European public as-sessment report (EPAR): Lorviqua (Lorlatinib). 2020c. https://www.ema.europa.eu/en/medicines/human/EPAR/lorviqua abgerufen am: 10.06.2020
EMA. European Medical Agency Human medicine European public assess-ment report (EPAR): Xalkori (Crizotinib). 2020d. https://www.ema.europa.eu/en/medicines/human/EPAR/xalkori, abgerufen am: 10.06.2020
EMA. European Medical Agency Human medicine European public assess-ment report (EPAR): Zykadia (Ceritinib). 2020e. https://www.ema.europa.eu/en/medicines/human/EPAR/zykadia, abgerufen am: 10.06.2020
Felip E, Orlov S, Park K, et al. ASCEND-3: A single-arm, open-label, multi-center phase II study of ceritinib in ALKi-naïve adult patients (pts) with ALK-rearranged (ALK+) non-small cell lung cancer (NSCLC). J Clin Oncol 2015;33(15_suppl):8060
FI. Fachinformation Alunbrig. 2020
Gadgeel S, Peters S, Mok T, et al. Alectinib versus crizotinib in treatment-naive anaplastic lymphoma kinase-positive (ALK+) non-small-cell lung cancer: CNS efficacy results from the ALEX study. Ann Oncol 2018;29(11):2214 – 22
Gadgeel SM, Shaw AT, Govindan R, et al. Pooled analysis of CNS response to alectinib in two studies of pretreated patients with ALK-positive non-small-cell lung cancer. J Clin Oncol 2016;34(34):4079 – 85
Gainor JF, Dardaei L, Yoda S, et al. Molecular mechanisms of resistance to first- and second-generation ALK inhibitors in ALK-rearranged lung cancer. Cancer Discov 2016;6(10):1118 – 33
Getman VV, Dekan G, Mueller MR. Histological classification and TNM staging of lung cancer. European Surgery 2004;36(2):66 – 9
Gettinger SN, Bazhenova LA, Langer CJ, et al. Activity and safety of brigatinib in ALK-rearranged non-small-cell lung cancer and other malignancies: a single-arm, open-label, phase 1/2 trial. Lancet Oncol 2016;17(12):1683 – 96
Griesinger F, Eberhardt W, Früh M, et al. Leitlinie der DGHO: Lungenkarzinom, nicht-kleinzellig (NSCLC) Stand: Oktober 2019. 2019
-
- 12 -
ZIELGERICHTETE THERAPIE DES FORTGESCHRITTENEN ALK-POSITIVEN NICHT-KLEINZELLIGEN LUNGENKARZINOMS MIT ALK-INHIBITOREN
Hida T, Nokihara H, Kondo M, et al. Alectinib versus crizotinib in patients with ALK-positive non-small-cell lung cancer (J-ALEX): an open-label, randomised phase 3 trial. Lancet 2017;390(10089):29 – 39
Hofer S. Info@onkologie 2017;2:10 – 3
Horn L, Whisenant JG, Wakelee H, et al. Monitoring therapeutic response and resistance: analysis of circulating tumor DNA in patients with ALK+ lung cancer. J Thorac Oncol 2019;14(11):1901 – 11
Huber RM, Kim DW, Ahn M-J. Brigatinib (BRG) in crizotinib (CRZ)-refrac-tory ALK+ non–small cell lung cancer (NSCLC): Efficacy updates and exploratory analysis of CNS ORR and overall ORR by baseline (BL) brain lesion status. J Clin Oncol 2018;36(suppl.):abstract 9061
Katayama R, Lovly CM, Shaw AT. Therapeutic targeting of anaplastic lym-phoma kinase in lung cancer: a paradigm for precision cancer medicine. Clin Cancer Res 2015;21(10):2227 – 35
Kim DW, Tiseo M, Ahn MJ, et al. Brigatinib in patients with crizotinib-refrac-tory anaplastic lymphoma kinase-positive non-small-cell lung cancer: A randomized, multicenter phase II trial. J Clin Oncol 2017;35(22):2490 – 8
Leitlinienprogramm Onkologie. Prävention, Diagnostik, Therapie und Nach-sorge des Lungenkarzinoms. AWMF-Registernummer: 020/007OL. 2018. http://leitlinienprogramm-onkologie.de/Lungenkarzinom.98.0.html, abgerufen am: 16.11.2018
NIH. A study of lorlatinib versus crizotinib in first line treatment of patients with ALK-positive NSCLC. 2020. https://www.clinicaltrials.gov/ct2/show/NCT03052608, abgerufen am: 22.05.2020
Niu X, Chuang JC, Berry GJ, et al. Anaplastic lymphoma kinase testing: IHC vs. FISH vs. NGS. Curr Treat Options Oncol 2017;18(12):71
Nix NM, Brown KS. Ceritinib for ALK-rearrangement-positive non-small cell lung cancer. J Adv Pract Oncol 2015;6(2):156 – 60
Novello S, Mazieres J, Oh IJ, et al. Alectinib versus chemotherapy in crizotinib-pretreated anaplastic lymphoma kinase (ALK)-positive non-small-cell lung cancer: results from the phase III ALUR study. Ann Oncol 2018;29(6):1409 – 16
Perol M, Peters S, Pavlakis N, et al. 138PD_PR Patient-reported outcomes (PROs) in ALEX: A phase III study of alectinib (ALEC) vs crizotinib (CRIZ) in non-small-cell lung cancer (NSCLC). J Thorac Oncol 2018;13(4):S80-S1
Peters S, Camidge DR, Shaw AT, et al. Alectinib versus crizotinib in un-treated ALK-positive non-small-cell lung cancer. N Engl J Med 2017;377(9):829 – 38
Ramiro S, Sepriano A, Chatzidionysiou K, et al. Safety of synthetic and biological DMARDs: a systematic literature review informing the 2016 update of the EULAR recommendations for management of rheumatoid arthritis. Ann Rheum Dis 2017;76(6):1101 – 36
Remon J, Besse B. Brain metastases in oncogene-addicted non-small cell lung cancer patients: Incidence and treatment. Front Oncol 2018;8:88
RKI. Zentrum für Krebsregisterdaten, Stand: 17.12.2019. 2019. https://www.krebsdaten.de/Krebs/DE/Content/Krebsarten/krebsarten_node.html, abgerufen am: 21. 04. 2020
Rothenstein JM, Chooback N. ALK inhibitors, resistance development, clinical trials. Curr Oncol 2018;25(Suppl 1):S59 – s67
Shaw AT, Felip E, Bauer TM, et al. Lorlatinib in non-small-cell lung cancer with ALK or ROS1 rearrangement: an international, multicentre, open-label, single-arm first-in-man phase 1 trial. Lancet Oncol 2017a;18(12):1590 – 9
Shaw AT, Kim DW, Nakagawa K, et al. Crizotinib versus chemotherapy in advanced ALK-positive lung cancer. N Engl J Med 2013;368(25):2385 – 94
Shaw AT, Kim TM, Crino L, et al. Ceritinib versus chemotherapy in patients with ALK-rearranged non-small-cell lung cancer previously given chemot-herapy and crizotinib (ASCEND-5): a randomised, controlled, open-label, phase 3 trial. Lancet Oncol 2017b;18(7):874 – 86
Solomon BJ, Besse B, Bauer TM, et al. Lorlatinib in patients with ALK-positive non-small-cell lung cancer: results from a global phase 2 study. Lancet Oncol 2018a;19(12):1654 – 67
Solomon BJ, Cappuzzo F, Felip E, et al. Intracranial efficacy of crizotinib versus chemotherapy in patients with advanced ALK-positive non-small-cell lung cancer: Results from PROFILE 1014. J Clin Oncol 2016;34(24):2858 – 65
Solomon BJ, Kim DW, Wu YL, et al. Final overall survival analysis from a study comparing first-line crizotinib versus chemotherapy in ALK-mutation-positive non-small-cell lung cancer. J Clin Oncol 2018b;36(22):2251 – 8
Solomon BJ, Mok T, Kim DW, et al. First-line crizotinib versus chemother-apy in ALK-positive lung cancer. N Engl J Med 2014;371(23):2167 – 77
Soria JC, Tan DSW, Chiari R, et al. First-line ceritinib versus platinum-ba-sed chemotherapy in advanced ALK-rearranged non-small-cell lung cancer (ASCEND-4): a randomised, open-label, phase 3 study. Lancet 2017;389(10072):917 – 29
Spagnuolo A, Maione P, Gridelli C. Evolution in the treatment landscape of non-small cell lung cancer with ALK gene alterations: from the first- to third-generation of ALK inhibitors. Expert Opin Emerg Drugs 2018;23(3):231 – 41
Weickhardt AJ, Aisner DL, Franklin WA, et al. Diagnostic assays for iden-tification of anaplastic lymphoma kinase-positive non-small cell lung cancer. Cancer 2013;119(8):1467 – 77
Yang JC, Ou SI, De Petris L, et al. Pooled systemic efficacy and safety data from the pivotal phase II studies (NP28673 and NP28761) of alectinib in ALK-positive non-small cell lung cancer. J Thorac Oncol 2017;12(10):1552 – 60
Zhang I, Zaorsky NG, Palmer JD, et al. Targeting brain metastases in ALK-re-arranged non-small-cell lung cancer. Lancet Oncol 2015;16(13):e510 – 21
-
- 14 -
LERNKONTROLLFRAGENBitte kreuzen Sie jeweils nur eine Antwort an.
ZIELGERICHTETE THERAPIE DES FORTGESCHRITTENEN ALK-POSITIVEN NICHT-KLEINZELLIGEN LUNGENKARZINOMS MIT ALK-INHIBITOREN
1. Wie hoch ist der Anteil von nichtkleinzelligen Lun-genkarzinomen (NSCLC) bei Lungentumoren?A) 15 – 20 %B) 25 – 30 %C) 40 – 45 %D) 65 – 70 %E) 80 – 85 %
2. Welche der folgenden Aussagen zum NSCLC ist richtig?A) Bei etwa 10 – 15 % der NSCLC-Patienten ist
das anaplastische Lymphom-Kinase(ALK)-Gen verändert.
B) Etwa 5 % der NSCLC-Patienten entwickeln im Krankheitsverlauf ZNS-Metastasen.
C) ZNS-Metastasen wirken sich nur geringfügig auf die Prognose von NSCLC-Patienten aus.
D) ALK-positive Patienten können von einer Therapie mit ALK-Inhibitoren (ALKi) profitieren.
E) Die Verträglichkeit einer ALKi-basierten Thera-pie ist vergleichbar mit der Verträglichkeit einer Chemotherapie.
3. Was ist bei der Therapie mit ALKi zu berück-sichtigen?A) Im Verlauf der Therapie kommt es in der Regel
zu einer Resistenzbildung der Tumorzellen.B) Unter ALKi-Therapie kommt es nur bei wenigen
Patienten zu einem Progress.C) Der ALKi Crizotinib zeigt die beste Wirksamkeit
bei ZNS-Metastasen.D) Alle ALKi besitzen eine vergleichbare Wirksamkeit
hinsichtlich ZNS-Metastasen.E) Die Resistenzprofile von ALKi unterscheiden sich
nicht wesentlich.
4. Veränderungen des ALK-Gens spielen eine wich-tige Rolle bei der Pathologie des NSCLC. Welche Aussage hinsichtlich des ALK- bzw. des EML4-ALK-Fusionsgens ist falsch?A) Das ALK-Gen kodiert für einen Tyrosinkinase-
Rezeptor der Insulinrezeptor-Familie.B) Bei NSCLC kann ein EML4-ALK-Fusionsgen
nachgewiesen werden.C) Welche Variante des EML4-Fusionsgens vorliegt,
spielt keine Rolle für die Prognose der NSCLC-Patienten.
D) Es existieren mindestens 15 verschiedene Varianten des EML4-ALK-Fusionsgens.
E) Die EML4-ALK-Fusionsgenvarianten 1, 2 und 3 kommen am häufigsten vor.
5. Welche Aussage bezüglich der Diagnostik beim NSCLC ist richtig?A) Die Leitlinien empfehlen eine Testung auf ALK-
Fusionen bei allen nicht kurativ behandelbaren NSCLC-Patienten, insbesondere bei nicht-squa-mösem NSCLC.
B) Es sollten ausschließlich Gewebeproben analysiert werden, um die Diagnose zu sichern.
C) Es sollten ausschließlich Blutproben (Liquid Biopsies) analysiert werden, um die Diagnose zu sichern.
D) Beim NSCLC ist es ausreichend, eine molekular-pathologische Analyse des Tumorgewebes vor Beginn der Erstlinientherapie durchzuführen.
E) Zukünftig wird die Testung auf Resistenzmutatio-nen höchstwahrscheinlich an Be deutung verlieren.
-
- 15 -
ZIELGERICHTETE THERAPIE DES FORTGESCHRITTENEN ALK-POSITIVEN NICHT-KLEINZELLIGEN LUNGENKARZINOMS MIT ALK-INHIBITOREN
6. Was gilt für die Testverfahren, die für die Detektion von ALK-Genfusionen eingesetzt werden?A) Die Fluoreszenz-in-situ-Hybridisierung (FISH)
wird nur selten zum Nachweis einer ALK-Trans-lokation eingesetzt.
B) Mit FISH lassen sich auch EML4-ALK-Fusions-varianten eindeutig identifizieren.
C) Die Immunhistochemie ist die einzige Methode, bei der die pathogen veränderte ALK auf Protein-ebene nachgewiesen wird.
D) Die RT-PCR liefert einen indirekten Nachweis für EML4-ALK-Genfusionen.
E) Das Next-Generation-Sequencing (NGS) gilt seit einigen Jahren als Goldstandard für den Nach-weis von EML4-ALK-Genfusionen.
7. Was gehört nicht zu den beim NSCLC am häufig-sten von Metastasen betroffenen Körperregionen?A) ZNSB) PankreasC) LymphknotenD) LeberE) Nebennieren
8. Welche Aussage zur zielgerichteten Therapie bei ALK-positivem NSCLC ist falsch?A) Der Vorteil der ALKi-Therapie ist, dass sie sich in
erster Linie gegen Tumorzellen richtet.B) Für die Erstlinienbehandlung sind die ALKi Crizoti-
nib, Ceritinib, Alectinib und Brigatinib zugelassen.C) Brigatinib ist für die Zweitlinie nach Vorbehandlung
mit Crizotinib zugelassen.D) Lorlatinib ist für die Zweitlinie nach Vorbehandlung
mit Crizotinib zugelassen.E) Lorlatinib ist für die Zweitline nach Vorbehandlung
mit Alectinib oder Ceritinib zugelassen.
9. Bei Behandlung mit ALKi kommt es in der Regel nach einiger Zeit zu einer Resistenzbildung gegen-über dem eingesetzten ALKi. Welche der folgenden Aussagen zur Resistenzbildung ist falsch?A) Ursachen einer Resistenzbildung sind Mutationen
im ALK-Gen (Punktmutationen oder Genamplifika-tionen), aber auch ALK-unabhängige Mutationen.
B) Bei ALKi der zweiten Generation tritt häufig die G1202R-Mutation auf.
C) Die Wirksamkeit von ALKi bei bestimmten Muta-tionen wurde in klinischen Studien nachgewiesen.
D) Brigatinib und Lorlatinib weisen das breiteste Wirkungsspektrum gegenüber häufigen Resis-tenzmutationen auf.
E) NGS ist die wichtigste Methode für den Nachweis von Resistenzmutationen.
10. Metastasen im ZNS treten bei der Mehrheit der Patienten mit NSCLC im Krankheitsverlauf auf. Was lässt sich hinsichtlich der ZNS-Wirksamkeit bei ALKi feststellen?
A) Bei etwa 30 % der mit Crizotinib behandelten Patienten kommt es zum Progress mit Hirn-metastasen.
B) In der Studie ASCEND-5 profitierten Patienten mit Hirnmetastasen hinsichtlich des progres-sionsfreien Überlebens weniger stark von einer Ceritinib-Behandlung als Patienten ohne Hirn-metastasen.
C) Alectinib ist ein Substrat des Effluxtransporters P-Glykoprotein, wodurch es zu einer vergleichs-weise niedrigen Wirkstoffkonzentration im ZNS kommt.
D) Lorlatinib weist nach Crizotinib die geringste ZNS-Aktivität auf.
E) In der Studie ALTA-1L reduzierte Brigatinib das Risiko für eine Krankheitsprogression/Tod um 75 % bei Patienten mit Hirnmetastasen zu Stu-dienbeginn.
-
VNR: 2760909010521940013 | Gültigkeitsdauer: 15.07.2020 – 31.12.2020
Bitte die Angaben zur Person leserlich ausfüllen:
Frau Herr
Titel, Vorname, Name
Straße, Hausnummer
PLZ, Ort
Zusätzliche Daten (Angabe ist freiwillig): niedergelassener Arzt angestellt – Klinik angestellt – sonst. Arbeitgeber
Fachgebiet
Bitte informieren Sie mich über neue Fortbildungen per E-Mail. : E-Mail-Adresse (freiwillig)
Datenschutz: Ihre Daten werden ausschließlich für die Auswertung der Antworten verwendet. Als Veranstalter sind wir verpflichtet, ihre Ergebnisse für zehn Jahre zu speichern und auf Verlangen der zertifizierenden Ärztekammer vorzulegen. Es erfolgt keine Speicherung darüber hinaus. Namens- und Adressangaben dienen nur dem Versand der Teilnahmebescheinigungen. Ihre Punkte werden über Ihre EFN-Nummer an den elektronischen Informationsverteiler (EIV) gemeldet, der die Punkte an die Ärztekammern weiterleitet.
Erklärung: Mit meiner Unterschrift versichere ich, dass ich die Beantwortung der Fragen selbstständig und ohne fremde Hilfe durchgeführt habe. Der Zustellung der Teilnahmebescheinigung durch den Sponsor stimme ich zu.
LERNERFOLGSKONTROLLE
·· a b c d e123456789
10
Evaluation (freiwillig): Bitte bewerten Sie nach dem Schulnoten-System (1 = ja, sehr; 6 = gar nicht) 1 2 3 4 5 6
A Meine Erwartungen hinsichtlich der Fortbil-dung haben sich erfüllt.
B Während des Durcharbeitens habe ich fach-lich gelernt.
C Der Text hat Relevanz für meine praktische Tätigkeit.
D Die Didaktik, die Eingängigkeit und die Quali-tät des Textes sind sehr gut.
E Der Aufwand für die Bearbeitung (zeitlich und organisatorisch) hat sich gelohnt.
F In der Fortbildung wurde die Firmen- und Produktneutralität gewahrt.
G Diese Form der Fortbildung möchte ich auch zukünftig erhalten.
ZIELGERICHTETE THERAPIE DES FORTGESCHRITTENEN ALK-POSITIVENNICHT-KLEINZELLIGEN LUNGENKARZINOMS MIT ALK-INHIBITOREN
Außendienst-Stempel (optional)
Arzt-Stempel
EFN-Nummer eintragen oder Aufkleber aufkleben
CME MEDIPOINT, Fax-Nr.: 0821 – 27 14 00 06, E-Mail: [email protected]
Ort, Datum Unterschrift
Auswertung der Lernerfolgskontrolle (PN: 2623)
-
- 3 -
IMPRESSUM
AUTORPD Dr. med. Niels ReinmuthAsklepios-Kliniken München-Gauting
REDAKTION & LAYOUTDr. Martina Reitz & Dominik KudelaKW MEDIPOINT, Bonn
VERANSTALTERCME MEDIPOINT, Neusäß | www.cme-medipoint.de
SPONSORDiese Fortbildung wurde von Takeda Pharma Vertrieb GmbH & Co. KG mit insgesamt 12.859 € finanziell unterstützt.Die Inhalte der Fortbildung werden durch den Sponsor nicht beeinflusst.
Diese Fortbildung ist auf www.cme-medipoint.de online verfügbar.Die Transparenzinformationen sind dort einsehbar.