UNIVERSIDADE FEDERAL RURAL DO SEMI-ÁRIDO CAMPUS … Pablo... · óleo de coco bruto na produção...
Transcript of UNIVERSIDADE FEDERAL RURAL DO SEMI-ÁRIDO CAMPUS … Pablo... · óleo de coco bruto na produção...
PABLO VINÍCIUS SOARES DA SILVA
ESTUDO DA PRODUÇÃO DE BIODIESEL DE ÓLEO DE COCO BRUTO VIA
CATÁLISE BÁSICA
ANGICOS-RN
2013
UNIVERSIDADE FEDERAL RURAL DO SEMI-ÁRIDO CAMPUS ANGICOS DEPARTAMENTO DE CIÊNCIAS EXATAS, TECNOLÓGICAS E HUMANAS CURSO DE BACHARELADO EM CIÊNCIA E TECNOLOGIA
PABLO VINÍCIUS SOARES DA SILVA
ESTUDO DA PRODUÇÃO DE BIODIESEL DE ÓLEO DE COCO BRUTO VIA
CATÁLISE BÁSICA
Monografia apresentada à Universidade Federal Rural do Semi-Árido – UFERSA, Campus Angicos para a obtenção do título de Bacharel em Ciência e Tecnologia. Orientador (a): Profª. Dra. Elisângela Lopes Galvão – (UFERSA/ Angicos). Coorientador: Prof. Me. Ricardo Henrique Rocha de Carvalho (UFERSA/ Mossoró)
ANGICOS-RN 2013
PABLO VINÍCIUS SOARES DA SILVA
ESTUDO DA PRODUÇÃO DE BIODIESEL DE ÓLEO DE COCO BRUTO VIA
CATÁLISE BÁSICA
Monografia apresentada à Universidade Federal Rural do Semi-Árido- UFERSA, Campus Angicos para a obtenção do título de Bacharel em Ciência e Tecnologia.
Dedico este trabalho aos meus pais
MARIA DA CONCEIÇÃO SOARES DA
SILVA e PEDRO PAULO FERREIRA DA
SILVA, por estarem do meu lado em
todos os momentos de minha vida
fazendo com que eu não desistisse dos
meus objetivos, tenho-os não só como
pais, mais também como meus exemplos
de vida.
AGRADECIMENTOS
A Deus, por ter me dado forças para terminar mais uma etapa da minha vida,
proporcionando-me luz e muita paciência, para conseguir lidar com os percalços do
trajeto.
A toda a minha família, pelo apoio a mim conferido. E especial a meu tio HAMILTON
CÉSAR GABRIEL SOARES, por ser a minha fonte de inspiração durante a minha
caminhada.
A minha namorada ALDILENE BEZERRA PINHEIRO, pelo seu amor, carinho,
compreensão e, principalmente, paciência nos momentos que estive ao seu lado.
A minha orientadora Prof.ª Dra. ELISÂNGELA LOPES GALVÃO, que me
proporcionou uma grande oportunidade, acreditando em meu potencial, tendo
paciência e disponibilizando do seu tempo para que esse trabalho acontecesse.
Ao meu coorientador Prof. RICARDO HENRIQUE ROCHA DE CARVALHO por
disponibilizar de seu tempo para demonstrar as etapas de síntese do biodiesel.
Ao ANTÔNIO ANDRÉ DE SOUZA e família, pela ajuda muito importante na
produção do óleo de coco, tanto na doação da matéria-prima, como no processo de
fabricação do mesmo.
À UFRPE e a professora Suzana Pedroza, pela ajuda com a realização das análises
cromatográficas.
A banca examinadora desse trabalho Prof.ª Ma. ANDRÉA GALINDO CARNEIRO
ROSAL e o Prof. Me. FRANCISCO SOUTO DE SOUSA JÚNIOR, aceitando o
convite e disponibilizando o seu tempo para colaborar com este trabalho.
A todos os professores da UFERSA – Campus Angicos, pelos ensinamentos
passados ao longo do curso.
A todos o meus colegas da turma de 2010.1, que fizeram parte desse capítulo da
minha vida.
A UFERSA – Campus Angicos, por ter me ensinado a ver o mundo com outros olhos
e a tantos outros que colaboraram para a realização deste trabalho.
RESUMO
Nos últimos anos, as pesquisas no sentido de fornecer fontes de energia
alternativas ao petróleo e que possam suprir as necessidades energéticas da
população mundial tem recebido bastante atenção. O biodiesel é uma destas novas
fontes de energia; além de renovável e menos poluente que o combustível de
origem fóssil, quando produzido a partir de fontes vegetais, contribui com a retirada
de dióxido de carbono da atmosfera. Nesse trabalho objetivou-se estudar o uso do
óleo de coco bruto na produção de biodiesel, avaliando o efeito das variáveis: razão
molar óleo/álcool, temperatura do sistema reacional e percentagem de catalisador
no rendimento da reação de transesterificação. O biodiesel de coco foi produzido via
catálise básica, tendo como catalisador o hidróxido de sódio. O rendimento da
reação variou de 36,2 a 84,1% e os resultados mostraram que as variáveis que
apresentaram maior efeito sobre o rendimento da reação de transesterificação do
óleo de coco foram o percentual de catalisador e a razão molar óleo/álcool.
Palavras-chave: Biodiesel. Óleo de Coco. Transesterificação. Catálise básica.
LISTA DE FIGURAS
FIGURA 1- POTENCIALIDADE BRASILEIRA PARA PRODUÇÃO DE OLEAGINOSAS POR REGIÃO. .......................................................................... 18
FIGURA 2 - REAÇÃO DE TRANSESTERIFICAÇÃO PARA PRODUÇÃO DO
BIODIESEL. ........................................................................................................ 23 FIGURA 3 – FLUXOGRAMA DE PRODUÇÃO DO ÓLEO DE COCO BRUTO ......... 28 FIGURA 4 - APARATO UTILIZADO NA SÍNTESE DO BIODIESEL. ........................ 30 FIGURA 5 - ETAPA DE LAVAGEM DO BIODIESEL. ............................................... 32 FIGURA 6 - AMOSTRA DE BIODIESEL ENVIADA PARA ANÁLISE E AMOSTRA DA
GLICERINA (SUBPRODUTO DA REAÇÃO). ..................................................... 32 FIGURA 7 - VISUALIZAÇÃO DO ASPECTO DO BIODIESEL OBTIDO. .................. 37
LISTA DE TABELAS
TABELA 1 - DADOS DE PRODUTIVIDADE E RENDIMENTO DE ALGUMAS CULTURAS OLEAGINOSAS DE ACORDO COM AS REGIÕES PRODUTORAS ............................................................................................................................ 17
TABELA 2 - ESPECIFICAÇÃO DO BIODIESEL ....................................................... 21 TABELA 3 - INTERVALO DE ESTUDO DAS VARIÁVEIS DO PLANEJAMENTO
EXPERIMENTAL ................................................................................................. 33 TABELA 4 - PLANEJAMENTO EXPERIMENTAL UTILIZADO NA SÍNTESE DO
BIODIESEL DE ÓLEO DE COCO. ...................................................................... 33 TABELA 5 - VALORES DE RENDIMENTO BRUTO OBTIDO PARA CADA
CONDIÇÃO EXPERIMENTAL. ........................................................................... 38
LISTA DE GRÁFICOS
GRÁFICO 1 - COMPOSIÇÃO EM ÁCIDOS GRAXOS DO ÓLEO DE COCO BRUTO ............................................................................................................................ 36
GRÁFICO 2 - RENDIMENTO BRUTO EM FUNÇÃO DA RAZÃO MOLAR
ÓLEO/ÁLCOOL UTILIZADA. ............................................................................... 39 GRÁFICO 3 - RENDIMENTO BRUTO EM FUNÇÃO DA TEMPERATURA
REACIONAL UTILIZADA. ................................................................................... 40 GRÁFICO 4 - RENDIMENTO BRUTO EM FUNÇÃO DO PERCENTUAL DE
CATALISADOR UTILIZADO. .............................................................................. 40
LISTA DE ABREVIATURAS E SIGLAS
ANP – Agência Nacional do Petróleo;
CG – Cromatografia gasosa;
HA – Hectare;
INT – Instituto Nacional de Tecnologia;
KOH – Hidróxido de potássio;
NaOH – Hidróxido de sódio;
nbiodiesel – número de mols do biodiesel produzido;
nóleo – número de mols do óleo de coco
PRÓ-ALCOOL – Programa Nacional do Álcool
Rbruto – rendimento bruto;
TON – tonelada;
UFC – Universidade Federal do Ceará.
SUMÁRIO
1 INTRODUÇÃO ....................................................................................................... 12
2 OBJETIVOS ........................................................................................................... 14
3 FUNDAMENTAÇÃO TEÓRICA ............................................................................. 15
3.1 BIODIESEL .......................................................................................................... 15 3.1.1 Breve histórico ............................................................................................... 15 3.1.2 Distribuição geográfica das principais oleaginosas no Brasil ................... 17 3.2 MATÉRIA-PRIMA ................................................................................................ 19 3.2.1 O óleo de coco ................................................................................................ 19 3.2.2 Extração do óleo de coco .............................................................................. 20 3.3 PROPRIEDADES FÍSICO-QUÍMICAS DO BIODIESEL ....................................... 21 3.3.1 Especificação brasileira do biodiesel ........................................................... 21 3.4 PROCESSOS DE PRODUÇÃO DE BIODIESEL ................................................. 23 3.4.1 Transesterificação por Catálise Básica Homogênea .................................. 23 3.4.2 Transesterificação por Catálise Ácida Homogênea .................................... 24 3.4.3 Transesterificação por Catálise Heterogênea .............................................. 24 3.4.4 Transesterificação por Catálise Enzimática ................................................. 24 3.5 FATORES QUE AFETAM A REAÇÃO DE TRANSESTERIFICAÇÃO ................. 25 3.5.1 Presença de ácidos graxos livres e umidade .............................................. 25 3.5.2 Tipo de álcool e razão molar óleo/álcool utilizado ...................................... 25 3.5.3 Tipo e concentração do catalisador ............................................................. 26 3.5.4 Tempo e temperatura de reação ................................................................... 26 3.5.5 Intensidade da agitação ................................................................................. 27
4 MATERIAL E MÉTODOS ...................................................................................... 28
4.1 OBTENÇÃO DA MATÉRIA-PRIMA (ÓLEO DE COCO BRUTO). ......................... 28 4.2 ANÁLISE CROMATOGRÁFICA DO ÓLEO DE COCO ........................................ 29 4.3 PRODUÇÃO DO BIODIESEL .............................................................................. 30 4.4 VARIÁVEIS ANALISADAS .................................................................................. 33 4.5 ANÁLISE CROMATOGRÁFICA DO BIODIESEL PARA CÁLCULO DO
RENDIMENTO .......................................................................................................... 34
5 RESULTADOS E DISCUSSÕES ........................................................................... 36
5.1 COMPOSIÇÃO EM ÁCIDOS GRAXOS DO ÓLEO DE COCO BRUTO ................ 36 5.2 PRODUÇÃO DO BIODIESEL A PARTIR DO ÓLEO DE COCO BRUTO .............. 37 5.3 RENDIMENTO BRUTO DA REAÇÃO DE TRANSESTERIFICAÇÃO .................. 38 5.4 INFLUÊNCIA DAS VARIÁVEIS NO RENDIMENTO............................................. 39
6 CONCLUSÕES ...................................................................................................... 42
REFERÊNCIAS ......................................................................................................... 43
12
1 INTRODUÇÃO
Na atualidade, a sociedade tem se preocupado cada vez mais com a questão
ambiental, principalmente motivada pelas transformações climáticas que vem
ocorrendo em nosso planeta nas últimas décadas. Tais transformações tem
resultado em desastres naturais, agravados pelo crescente aquecimento global, o
qual é decorrente de diversas causas, entre elas, a emissão de gases poluentes
oriundos da queima de combustíveis, tanto na indústria quanto na crescente frota de
veículos automotores (MACHADO NETO, 2011).
É conhecido que a queima dos combustíveis derivados do petróleo,
denominados de combustíveis fósseis, são um dos maiores contribuintes para a
emissão dos gases que poluem o nosso planeta. Além disso, o petróleo é não
renovável, o que põe em risco a dependência dessa fonte de energia. Estes fatores
levam a busca de pesquisas para fornecer fontes de energia alternativas que
possam suprir as necessidades energéticas da população mundial.
Neste aspecto, os biocombustíveis apresentam vantagens frente aos
combustíveis fósseis uma vez que, além de renováveis e menos poluentes, quando
produzidos a partir de fontes vegetais ainda podem contribuir com a retirada de
dióxido de carbono da atmosfera. Tal efeito é resultado do processo natural de
fotossíntese da planta, que consome CO2 para ocorrer. Além disso, os
biocombustíveis podem ser produzidos a partir de diferentes culturas vegetais, o que
aumenta consideravelmente as alternativas para a produção destes combustíveis
alternativos (FONTANA, 2011; MACHADO NETO, 2011).
No Brasil, a criação do Programa Nacional do Álcool (PRÓ-ALCOOL) pelo
governo foi a primeira tentativa para impulsionar o desenvolvimento da produção de
combustíveis renováveis, porém os veículos comerciais, como os caminhões, ainda
continuaram a utilizar o diesel mineral como combustível (ARAÚJO, 2008).
Embora as pesquisas com a produção de combustíveis renováveis tenham se
iniciado na década de 1920, somente há poucos anos é que o uso de
biocombustíveis em motores de ciclo diesel começaram a ser implementados. O
impulso na produção e comercialização do biodiesel começou após a implantação
de plantas industriais nos Estados Unidos no final da década de 1990. No Brasil, os
primeiros passos para a regulamentação do uso do biodiesel se deram em setembro
13
de 2004, o que tem estimulado as pesquisas de produção do biodiesel utilizando
diversas oleaginosas nacionais, como a soja, milho, algodão, mamona, girassol,
coco e dendê (ARAÚJO, 2008).
Nesse sentido pretende-se estudar o uso do óleo de coco bruto na produção
de biodiesel, com vistas a fornecer dados de rendimento da reação do biodiesel
produzido a partir desta cultura oleaginosa, a qual é bastante comum na região
nordeste.
14
2 OBJETIVOS
2.1 GERAL
Ampliar o conhecimento da produção de biodiesel obtido a partir do óleo de
coco bruto.
2.2 ESPECÍFICOS
Identificar a composição em ácidos graxos do óleo de coco (matéria-prima);
Produzir o biodiesel via catálise básica utilizando o óleo de coco como
matéria-prima;
Verificar a influência dos parâmetros de processo: razão molar óleo/álcool,
percentual de catalisador e temperatura sobre o rendimento da reação de
produção do biodiesel.
Analisar o biodiesel produzido através da cromatografia gasosa para avaliar o
rendimento da reação de produção do biodiesel.
15
3 FUNDAMENTAÇÃO TEÓRICA
3.1 BIODIESEL
Por possuir características físico-químicas semelhantes às do diesel mineral,
o biodiesel é considerado seu substituto natural, com a vantagem de ser um
combustível que pode ser produzido a partir de fontes renováveis, como óleos
vegetais, gorduras animais e óleos usados para a cocção de alimentos (fritura)
(FONTANA, 2011).
Segundo Lima Neto et al., (2006) o biodiesel é definido quimicamente como
éster monoalquílico de óleos vegetais e ou gordura animal, que pode ser produzido
a partir de uma reação de transesterificação tendo a glicerina como subproduto.
O biodiesel apresenta algumas vantagens quando comparado aos
combustíveis fósseis: além de seu caráter renovável, seu uso possibilita uma
expressiva capacidade de redução da emissão de matéria particulada e gases
poluentes causadores do efeito estufa, sendo ainda biodegradável e não tóxico
(FONTANA, 2011).
Ao contrário dos derivados de petróleo, o biodiesel é produzido desde o
princípio pelo homem, com matérias-primas oriundas de práticas agrícolas, ou seja,
de fontes renováveis. Além disso, todo o gás carbônico emitido na queima do
combustível é capturado pelas plantas, tornando sua produção segura do ponto de
vista ambiental (MACHADO NETO, 2011; ARAÚJO, 2008).
3.1.1 Breve histórico
Não é de hoje que a humanidade busca fontes alternativas de energia. A
utilização de óleo vegetal como fonte combustível para uso em motores vem de
outrora. Em 1900, Rudolph Diesel apresentou uma patente de motor na Exposição
Universal em Paris, tendo como combustível óleo de amendoim, cultura bastante
difundida nas colônias francesas na África. No entanto, a abundância na oferta de
petróleo na época e o seu preço acessível favoreceram a utilização dos derivados
de petróleo nos motores de combustão (MACHADO NETO, 2011).
Devido a sua elevada viscosidade, que impedia uma injeção adequada nos
motores, além dos depósitos de carbono nos cilindros e nos injetores, o combustível
de origem vegetal utilizado apresentou dificuldades nos motores por compressão.
16
Para minimizar os problemas acarretados pela utilização do óleo vegetal in natura,
os pesquisadores chegaram a descoberta da transesterificação, que é a reação da
molécula de óleo (ácido graxo) com o álcool, transformando-o em glicerina
(separados após a reação) e ésteres (utilizado como o combustível). De acordo com
Fontana (2011), o registro da primeira patente de fabricação do biodiesel está
documentado como uma patente belga de 31 de agosto de 1937 em favor do
pesquisador C. G. Chavanne, da Universidade de Bruxelas (FONTANA, 2011 p. 83).
No Brasil, desde a década de 20, o Instituto Nacional de Tecnologia – INT já
estudava e testava combustíveis alternativos e renováveis. Nos anos 60, buscaram
produzir óleo através dos grãos de café. Para lavar o café de forma a retirar suas
impurezas (impróprias para o consumo humano) foi usado o álcool da cana de
açúcar. A reação entre o álcool e o óleo de café resultou na liberação de glicerina, e
formação do éster etílico, produto que hoje é chamado de biodiesel (PRESTES,
2007).
Entretanto, o precursor dos biocombustíveis no Brasil foi o etanol, quando na
década de 70 o governo Brasileiro implementou o Programa Nacional do Álcool
(PRÓ-ALCOOL) devido a grande crise mundial do petróleo iniciada em 1973.
Apostaram nessa nova fonte de energia, inicialmente por ser mais barata, e diminuir
a quantidade de gases poluentes, podendo ser utilizado integralmente ou misturado
com a gasolina (FONTANA, 2011. 83).
Quanto ao biodiesel, patentes registradas no INPI (Instituto Nacional da
Propriedade industrial) em 1980 atestam o Engenheiro Químico e professor da UFC
Expedito José de Sá Parente, como sendo o pioneiro na síntese e aplicação do
biodiesel no Brasil (FONTANA, 2011). Ainda segundo Fontana (2011), embora tenha
sido anunciado no mesmo ano em cerimônia realizada em Fortaleza-CE na
presença do Presidente da República, o biodiesel nordestino não recebeu a devida
atenção, sobretudo devido a ênfase que se dava ao embrionário PRÓ-ÁLCOOL.
Somente recentemente, em setembro de 2004, o governo brasileiro deu o
primeiro passo para regularizar o uso do biodiesel no Brasil (ARAÚJO, 2008).
De acordo com a Lei Nº 12.490, de Setembro de 2011 e regulamentada pela
ANP (Agencia Nacional do Petróleo, Gás Natural e Biocombustíveis), define
biocombustível como: uma substância derivada de biomassa renovável, incluindo o
etanol e o biodiesel, que podem ser empregada diretamente ou mediante alterações
em motores a combustão interna ou para outro tipo de geração de energia, podendo
17
substituir parcialmente ou totalmente o combustíveis de origem fóssil.
3.1.2 Distribuição geográfica das principais oleaginosas no Brasil
As oleaginosas são plantas cultivadas das quais é possível extrair óleo, usado
como matéria-prima na produção de biodiesel. Cada oleaginosa, dependendo da
região na qual é cultivada e segundo as condições de clima e de solo, apresenta
características específicas na produtividade por hectare e na percentagem de óleo
obtida da amêndoa ou grão. A produtividade obtida também está diretamente
associada às tecnologias de cultivo, à qualidade da semente e às tecnologias de
processamento praticadas (SEBRAE, 2013). A Tabela 1 ilustra a relação das
espécies, produtividade e rendimento de acordo com as regiões produtoras.
Tabela 1 - Dados de produtividade e rendimento de algumas culturas oleaginosas de acordo com as regiões produtoras
ESPÉCIE PRODUTIVIDADE
(TON/HA)
PORCENTAGEM
DE ÓLEO
REGIÕES
PRODUTORAS
RENDIMENTO
(TON ÓLEO /HA)
Algodão
1
0,86 a 1,4
15
MT, GO, MS, BA e MA
0,1 a 0,2
Amendoim1 1,5 a 2 40 a 43 SP 0,6 a 0,8
Dendê
2
15 a 25
20
BA e PA
3 a 6
Girassol
1
1,5 a 2
28 a 48
GO, MS, SP, RS e PR
0,5 a 0,9
Mamona
1
0,5 a 1,5
43 a 45
Nordeste
0,5 a 0,9
Pinhão
manso2
2 a 12
50 a 52
Nordeste e MG
1 a 6
Soja
1
2 a 3
17
MT, PR, RS, GO, MS,
MG e SP
0,2 a 0,4
Fonte: SEBRAE (2013) 1. Ciclo de vida anual 2. Ciclo de vida perene
18
A Figura 1 apresenta as potencialidades brasileiras para produção de culturas
oleaginosas nas diversas regiões do Brasil. Na região Norte destacam-se o babaçu
e o dendê; na região Nordeste: o algodão e a mamona; na região Centro-Oeste: o
algodão e a soja; na região Sudeste: a soja e o girassol e na Região Sul: o girassol.
Figura 1- Potencialidade brasileira para produção de oleaginosas por região.
Fonte: Salvador et al. (2009)
Embora, o coco não figure entre as principais fontes oleaginosas no Brasil, o
presente trabalho ressalta importantes características que tornam esta cultura
merecedora de atenção, como modo de torná-la mais uma alternativa na produção
brasileira de biodiesel.
19
3.2 MATÉRIA-PRIMA
3.2.1 O óleo de coco
O coqueiro (Cocos Nucifera L.) é uma espécie de origem asiática, que foi
introduzida no Brasil em 1553. Atualmente se apresenta naturalizado em longas
áreas da costa nordestina (SOBRAL, 1976 apud Souza et al., 2012). Dentre os
estados brasileiros, os principais produtores são a Bahia, Sergipe e o Rio Grande do
Norte, que aparece como o terceiro maior produtor do país.
As variedades mais comuns no Brasil são o coqueiro gigante, o anão e o
híbrido, o qual é proveniente do cruzamento natural ou artificial entre as variedades
gigante e anão. Entretanto a variedade gigante é predominante no país (ARAÚJO,
2008).
A produção existente proporciona abundante matéria-prima tanto para as
agroindústrias regionais quanto para uso alimentício. Porém, talvez em função do
clima tropical, no Brasil o coco é bastante consumido imaturo para o aproveitamento
da água (SOUZA et al., 2012), entretanto o mesmo constitui-se numa fonte
oleaginosa perene de grande potencial, uma vez que o conteúdo de óleo na polpa é
superior a 60%, o que equivale a uma produção de 500 a 3000 Kg de óleo/ha
(MAZZANI, 1963 apud ARAÚJO, 2008).
Em geral, o óleo de coco possui os seguintes ácidos graxos: caprílico 5,0 -
10,0%, cáprico 4,5 – 8,0%, mirístico 16 – 21%, palmítico 7,5 - 10%, esteárico 2,0 –
4,0%, oléico 5 – 10% e linoléico 1,0 – 2,5%, com destaque para o ácido láurico 43 -
51% (ANVISA, 1999). Segundo Balachandran et al. (1985 apud Araújo, 2008), o
endosperma do fruto do coqueiro é a principal fonte mundial de ácido láurico, usado
na indústria de alimentos, cosméticos, sabões e na fabricação de álcool.
Dependendo da qualidade da copra, o óleo de coco apresenta-se incolor ou de
coloração acastanhada e com teor de ácidos graxos livres (calculado como ácido
láurico) variando de 1 a 6 % (SOUZA et al., 2012).
Uma importante característica na utilização do óleo de coco para a produção
de biodiesel é que o rendimento em óleo é de aproximadamente 60%, sendo
superior ao de outras oleaginosas já em uso na produção de biodiesel comercial
(ARAÚJO, 2008).
20
3.2.2 Extração do óleo de coco
O óleo de coco pode ser extraído de diferentes formas, sendo as mais
comuns a extração por prensagem mecânica, extração com uso de solventes
orgânicos e através de fervura com água (XAVIER, 2008).
A extração por prensagem é a mais utilizada nas indústrias, podendo alcançar
rendimentos de até 72%. Entretanto, também é possível extrair o óleo de coco
ralando a polpa e fervendo-a em água. Nesse processo, após ralar a polpa, a
mesma deve ser triturada juntamente com água até formar uma mistura homogênea
e pastosa, dessa forma haverá maior rendimento do óleo quando o mesmo for
levado para cozinhar. Depois de processado, deve-se levar o mesmo para ser
filtrado a fim de separar o leite de coco do resíduo (bagaço). Logo em seguida, o
leite de coco deve ser levado ao fogo para ferver por algumas horas até evaporar
completamente a água. Após a evaporação da água, se obtém o óleo de coco bruto
e um resíduo do cozimento, que devem ser filtrados para a obtenção de um óleo
com aspecto mais límpido.
21
3.3 PROPRIEDADES FÍSICO-QUÍMICAS DO BIODIESEL
De acordo com Parente (2003), a determinação da qualidade de um biodiesel
depende da avaliação de diversas propriedades físico-químicas, entre elas:
viscosidade, densidade, ponto de fulgor, poder calorífico, tensão superficial, e índice
de cetano.
3.3.1 Especificação brasileira do biodiesel
A Tabela 2 apresenta os parâmetros básicos estabelecidos pela ANP para
especificação do Biodiesel.
Tabela 2 - Especificação do Biodiesel
PROPRIEDADE UNIDADE LIMITE
MÉTODO
ABNT NBR ASTM D EN/ISO
Aspecto - LII (1) - - -
Massa específica a 20º C kg/m³ 850-
900
7148 14065
1298 4052
EN ISO 3675 - EN ISO
12185
Viscosidade Cinemática a 40ºC Mm²/s 3,0-6,0 10441 445 EN ISO 3104
Teor de Água, máx. (2) mg/kg 500 - 6304 EN ISO 12937
Contaminação Total, máx. mg/kg 24 - - EN ISO 12662
Ponto de fulgor, mín. (3) ºC 100,0 14598 93 EN ISO 3679
Teor de éster, mín % massa 96,5 15764 - EN 14103
Resíduo de carbono (4) % massa 0,050 15586 4530 -
Cinzas sulfatadas, máx. % massa 0,020 6294 874 EN ISO 3987
Enxofre total, máx. mg/kg 50 - 5453 EN ISO 20846- EN ISO
20884
22
Sódio + Potássio, máx. mg/kg 5 15554 15555 15553 15556
-
EN 14108 - EN 14109 -
EN 14538
Cálcio + Magnésio, máx. mg/kg 5 15553 15556
- EN 14538
Fósforo, máx. mg/kg 10 15553 4951 EN 14107
Corrosividade ao cobre, 3h a 50 ºC,
máx. - 1 14359 130 EN ISO 2160
Número de Cetano (5) - Anotar - 613 6890 (6)
EN ISO 5165
Ponto de entupimento de filtro a frio,
máx. ºC 19 (7) 14747 6371 EN 116
Índice de acidez, máx. mg
KOH/g 0,50 14448
- 664
- EN 14104 (8)
Glicerol livre, máx. % massa 0,02 15341 15771
- -
6584 (8) -
EN 14105 (8)- EN 14106
(8)
Glicerol total, máx. % massa 0,25 15344 -
6584 (8) -
EN 14105 (10)
Mono, di, triacilglicerol (5) % massa Anotar 15342 15344
6584 (8) EN 14105 (8)
Metanol ou Etanol, máx. % massa 0,20 15343 - EN 14110
Índice de Iodo (5) g/100g Anotar - - EN 14111
Estabilidade à oxidação a 110ºC,
mín.(2) h 6 - - EN 14112 (8)
Nota: (1) Límpido e isento de impurezas com anotação da temperatura de ensaio. (2) O limite indicado deve ser atendido na certificação do biodiesel pelo produtor ou importador. (3) Quando a análise de ponto de fulgor resultar em valor superior a 130ºC, fica dispensada a análise de teor de metanol ou etanol. (4) O resíduo deve ser avaliado em 100% da amostra. (5) Estas características devem ser analisadas em conjunto com as demais constantes da tabela de especificação a cada trimestre civil. Os resultados devem ser enviados pelo produtor de biodiesel à ANP, tomando uma amostra do biodiesel comercializado no trimestre e, em caso de neste período haver mudança de tipo de matéria-prima, o produtor deverá analisar número de amostras correspondente ao número de tipos de matérias-primas utilizadas. (6) Poderá ser utilizado como método alternativo o método ASTM D6890 para número de cetano. (7) O limite máximo de 19ºC é válido para as regiões Sul, Sudeste, Centro-Oeste e Bahia, devendo ser anotado para as demais regiões. O biodiesel poderá ser entregue com temperaturas superiores ao limite supramencionado, caso haja acordo entre as partes envolvidas. Os métodos de análise indicados não podem ser empregados para biodiesel oriundo apenas de mamona. (8) Os métodos referenciados demandam validação para as matérias-primas não previstas no método e rota de produção etílica.
Fonte: ANP (2008).
23
3.4 PROCESSOS DE PRODUÇÃO DE BIODIESEL
Na tentativa de melhorar o rendimento da reação de conversão da matéria-
prima em biodiesel, diversas pesquisas tem ocorrido com o intuito de se otimizar as
condições de reação (REIS et al 2007; EEVERA et al. 2008; CARVALHO, 2009;
SOUZA et al. 2012). Vários também são os métodos que vem sendo testados,
destacando-se a transesterificação, na qual um triacilglicerídeo reage com um álcool
de cadeia curta na presença de um catalisador para formar ésteres monoalquilícos
(biodiesel) e glicerol (Ver Figura 2).
Figura 2 - Reação de transesterificação para produção do biodiesel.
Fonte: Souza, et al. (2012)
O catalisador usado na reação de transesterificação pode ter caráter ácido, ou
básico e isso define o mecanismo da reação (Fontana, 2011).
3.4.1 Transesterificação por Catálise Básica Homogênea
O processo de transesterificação via catalisa básica é usado quando a
quantidade de ácidos graxos livres não é elevada, pois o alto teor desses ácidos
favorece as reações de saponificação, diminuindo assim a eficiência da conversão.
Trata-se de um processo economicamente mais atrativo para as indústrias de
produção de biodiesel, devido às bases usadas terem baixo custo, e por ser mais
eficiente e menos corrosivo que a catálise ácida, entretanto, possui problemas
quanto à separação de fases (BENEVIDES, 2011).
Os catalisadores mais utilizados são os hidróxidos de sódio (NaOH) e de
potássio (KOH), por serem mais baratos. Para ter uma reação de transesterificação
mais viável, comumente utiliza-se os alcoóis com menores pesos moleculares, como
o metanol e etanol. Mas pelo fato de o metanol ser mais barato que o etanol, isento
24
de água e ter uma maior polaridade, torna mais fácil a separação entre os ésteres e
a glicerina.
3.4.2 Transesterificação por Catálise Ácida Homogênea
Na produção de biodiesel um dos processos mais usados é a catálise ácida
homogênea, onde a transesterificação é catalisada por um ácido, geralmente ácido
sulfúrico ou sulfônico. Esse processo é mais utilizado quando os ésteres de glicerina
possuem alto teor de ácidos graxos livres. O processo por catálise ácida esterifica os
ácidos graxos livres e não forma sabões, fazendo com que o rendimento da reação
aumente, facilitando a separação e purificação das fases (BENEVIDES, 2011).
A transesterificação por catalise ácida comparada com a básica é mais lenta,
porém tem um maior rendimento. Por outro lado, devido aos ácidos empregados,
tem alto poder de corrosão que pode vir a danificar os equipamentos.
3.4.3 Transesterificação por Catálise Heterogênea
A utilização de catalisadores heterogêneos permite uma redução significativa
do número de etapas de purificação do biodiesel, facilita a reutilização do catalisador
e consequentemente, reduz o custo do processo de produção ( FUKUDA et al., 2001
apud CARTONI, 2009, p. 43).
A presença de ácidos graxos livres em alguns óleos e gorduras usados como
matérias-primas, dificulta a síntese do biodiesel devido à formação de sabão,
quando usada a catálise básica. Dessa forma, os catalisadores heterogêneos
ácidos, que promovem simultaneamente reações de alcoólise de triacilglicerídeos e
de esterificações dos ácidos graxos livres, apresentam-se como substitutos
promissores dos catalisadores homogêneos básicos (KRAUSE, 2008).
3.4.4 Transesterificação por Catálise Enzimática
Em processos enzimáticos, são utilizadas as lipases (glicerol éster hidrolases),
que são enzimas cuja função biológica é a de catalisar a hidrólise de gorduras e de
25
óleos vegetais, com a subsequente liberação de ácidos graxos livres, diacilgliceróis,
monoacilgliceróis e glicerol livre. Como biocatalisadores, apresentam algumas
vantagens importantes sobre os catalisadores clássicos, como a especificidade, a
regiosseletividade e a enantiosseletividade, que permitem a catálise de reações com
um número reduzido de subprodutos necessitando de condições brandas de
temperatura e pressão (FACIOLI et al., 1998 apud CARTONI, 2009, p.43).
3.5 FATORES QUE AFETAM A REAÇÃO DE TRANSESTERIFICAÇÃO
3.5.1 Presença de ácidos graxos livres e umidade
O teor de ácidos graxos livres e a umidade são elementos importantes para
determinar a viabilidade do processo de transesterificação, principalmente de
gorduras animais ou qualquer outro tipo de matéria-prima apropriada para
transesterificação básica. Para produzir uma reação catalisada por uma base, o teor
de ácidos graxos livres precisa estar abaixo de 1%. Quanto maior a acidez da
matéria-prima, menor é a eficiência de conversão. A presença de ácidos graxos
livres e de umidade no catalisador, em excesso ou não, ocasionam a formação de
sabões (KRAUSE, 2008).
3.5.2 Tipo de álcool e razão molar óleo/álcool utilizado
O álcool usado na reação de transesterificação normalmente é um álcool de
cadeia curta, os mais comuns são o metanol e o etanol. Tais álcoois, por serem
polares, são imiscíveis em triglicerídeos à temperatura ambiente. Em função disso,
as reações são normalmente agitadas mecanicamente para aumentar a
transferência de massa, que formam emulsões durante a reação. As emulsões são
em parte causadas pela formação de intermediários mono e diacilgliceróis, os quais
possuem grupos hidroxilas e cadeias de hidrocarbonetos não polares. Entretanto, a
produção de ésteres etílicos por catálise básica torna-se mais difícil quando
comparada com a produção de ésteres metílicos, devido à formação de emulsão
estável e indesejável durante a etanólise. Porém, nas metanólises, as emulsões são
26
facilmente separadas em duas camadas, uma inferior (glicerol) e outra superior rica
em ésteres, e na etanólise elas são mais estáveis e severas dificultando a
separação e purificação dos ésteres (KRAUSE, 2008).
Uma das variáveis mais importantes que afetam o rendimento do éster na
reação de transesterificação é a razão molar óleo /álcool. A relação estequiométrica
requer três moles de álcool para um mol de triacilglicerol (óleo), com um rendimento
de três moles de ésteres graxos (biodiesel) e um mol de glicerol (glicerina). A
transesterificação é uma reação reversível em equilíbrio, portanto exige um excesso
de álcool para direcionar a reação no sentido de formação dos ésteres (FONTANA,
2011). Para uma máxima conversão de ésteres, a relação molar óleo /álcool deve
ser maior ou igual a 1:6 (BENEVIDES, 2011).
3.5.3 Tipo e concentração do catalisador
A reação de transesterificação por catálise básica de um triacilglicerol ocorre
mais rapidamente do que a transesterificação por catálise ácida (FONTANA, 2011).
Os catalisadores mais utilizados na catálise básica são os alcoóxidos e hidróxidos.
Sendo que, os alcoóxidos são os catalisadores mais reativos, e apresentam
rendimentos elevados em pequeno tempo reacional. Já os hidróxidos são mais
acessíveis em preço do que os alcoóxidos, mas são menos reativos. Apresentam-se
como uma boa alternativa, desde que as concentrações sejam aumentadas, para
que a conversão seja equivalente ao uso dos catalisadores alcoóxidos. Mas se a
mistura óleo/álcool usada contiver um pouco de água ocorre a indesejável formação
de sabão, o que reduz o rendimento dos ésteres. Logo, os catalisadores básicos
podem ser utilizados tanto com álcool metílico como etílico, porém, se a matéria-
prima graxa tiver um maior teor de ácidos graxos livres e de água, a
transesterificação por catálise ácida é mais adequada (BENEVIDES, 2011).
3.5.4 Tempo e temperatura de reação
A taxa de conversão normalmente aumenta com o tempo de reação.
Entretanto, em suas pesquisas Freedman et al. (1984 apud BENEVIDES, 2011)
estudando o processo de transesterificação de alguns óleos vegetais (amendoim,
27
algodão, óleo de girassol e soja) com o metanol, obtiveram um rendimento
aproximado de 80% após 1 min de reação, para os óleos de soja e girassol e
perceberam que após 1 hora de reação, as conversões eram praticamente as
mesmas (93% a 98%) para todos os óleos (BENEVIDES, 2011).
Quanto ao fator temperatura, estudos de produção de biodiesel para diferentes
matérias-primas mostraram que o percentual de conversão em ésteres varia em
função do tipo óleo utilizado (EEVERA et al., 2009), ou seja, nem sempre altas
temperaturas garantem altas conversões em biodiesel. Além disso, deve-se atentar
para o fato de que a temperatura de reação não deve ultrapassar o ponto de
ebulição do álcool utilizado, uma vez que isso provocaria a evaporação do mesmo,
prejudicando o processo, mesmo com reciclo do álcool.
3.5.5 Intensidade da agitação
A intensidade da agitação é um dos fatores mais importantes no processo de
transesterificação, pois sofre interferência da viscosidade do óleo usado. A agitação
deve ser intensa, para poder transferir quantidades de massa de triglicerídeos da
fase óleo para a interface com o álcool, pois a mistura da reação é heterogênea
consistindo em duas fases (KRAUSE, 2008).
28
4 MATERIAL E MÉTODOS
4.1 OBTENÇÃO DA MATÉRIA-PRIMA (ÓLEO DE COCO BRUTO).
O coco (da variedade gigante) utilizado para produção do óleo foi fornecido
por um produtor do município de Angicos-RN. A produção do óleo de coco seguiu o
fluxograma apresentado na Figura 3.
Figura 3 – Fluxograma de produção do óleo de coco bruto
Fonte: Autoria própria (2013).
29
Para produzir o óleo de coco, inicialmente ralou-se a polpa, adicionou-se água
e em seguida triturou-se a mesma em um processador de alimentos até formar uma
mistura homogênea e pastosa. Depois de processada, a mistura foi filtrada (em
tecido de algodão) para separar o leite de coco do bagaço. Em seguida, o leite de
coco foi levado ao fogo para ferver por 8 horas, até evaporar completamente a água.
Após a evaporação da água, se obteve o óleo de coco e um resíduo do cozimento,
que foram filtrados para remoção das impurezas a fim de se obter um óleo límpido.
4.2 ANÁLISE CROMATOGRÁFICA DO ÓLEO DE COCO
A análise do óleo de coco foi realizada no Laboratório de Análises do
Departamento de Engenharia Química da UFRN e seguiu a metodologia descrita por
Araújo (2008), onde para a identificação e quantificação dos componentes presentes
no óleo de coco foi utilizado o seguinte procedimento:
A composição química do óleo de coco foi determinada utilizando um
cromatógrafo gasoso equipado com um detector de ionização de chama Varian
STAR 3400 CX e coluna capilar DB-23 Agilent (50% cyanopropyl –
metlhylpolysiloxane; 30m x 0,25m x 0,25μm). O volume de injeção foi de 2μL
(sensibilidade do injetor em 12), taxa de split 1:50, temperatura do detector e injetor
igual a 280°C e 250°C, respectivamente. A temperatura da coluna foi iniciada em
110°C permanecendo por 5 minutos nesta condição com taxa de aquecimento de
5°C/min até 215°C e assim permanecendo por 24 minutos.
A identificação dos componentes foi acompanhada pela injeção dos padrões
dos componentes majoritários do óleo de coco (conforme ANVISA, 1999)1 e pela
determinação do tempo de retenção de cada composto.
1 ANVISA (1999). Disponível em:<
http://portal.anvisa.gov.br/wps/wcm/connect/a2190900474588939242d63fbc4c6735/RDC_482_1999.pdf?MOD
=AJPERES >Acesso em : 20 de fevereiro de 2013.
30
4.3 PRODUÇÃO DO BIODIESEL
O biodiesel foi sintetizado via catálise básica no Laboratório de Química II da
UFERSA (Campus Angicos).
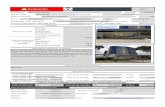
O aparato experimental para a síntese do biodiesel consistiu em um balão de
fundo chato de 250 mL (imerso em um banho-maria), acoplado a um condensador
tipo espiral de aproximadamente 45 cm (Figura 4). A reação foi agitada
mecanicamente através de um agitador mecânico com medidor de temperatura
acoplado (LOGEN SCIENTIFIC, Modelo: LS59D-220-400-VC), através do qual a
agitação da mistura e a temperatura reacional foram monitoradas.
Figura 4 - Aparato utilizado na síntese do biodiesel.
Fonte: Autoria própria (2013).
Como estequiometricamente a reação entre o triacilglicerídeo (óleo) e o álcool
é de 1:3, foi usado excesso de álcool para deslocar o equilíbrio da reação no sentido
da formação dos produtos. As razões molares óleo/álcool adotadas foram: 1:4, 1:6 e
1:8. No sistema reacional, o óleo, o álcool (metanol) e o catalisador (NaOH)
reagiram de acordo com as condições determinadas pelo planejamento experimental
(ver Tabela 4).
A quantidade de álcool, de catalisador (NaOH) e a temperatura do sistema
também seguiram os valores pré-determinados no planejamento experimental, para
31
o estudo das variáveis.
A massa do metanol (g) necessária para se obter cada razão molar do
planejamento experimental (1:4, 1:6 e 1:8) foi calculada levando em consideração a
massa molar do metanol (32 g/mol), a massa molar do óleo de coco e a massa de
óleo utilizada (100g) nos experimentos.
O percentual de catalisador utilizado foi definido em função da massa de óleo
(%m/m), tendo sido adotados neste trabalho os percentuais de 1%, 1,5% e 2% com
base em dados da literatura.
Após a montagem do aparato experimental, o óleo de coco foi pesado (100 g)
e introduzido no balão, permanecendo sob agitação mecânica até a estabilização da
temperatura operacional. Alcançada a temperatura de interesse (conforme o
planejamento experimental), os demais reagentes (metanol + NaOH) foram
previamente misturados e introduzidos no balão e após acoplar o condensador (cuja
função é evitar a perda de álcool por evaporação), iniciou-se a contagem do tempo
de reação (fixo em 90 minutos).
Depois de decorrido o tempo de reação programado, a mistura reacional foi
transferida para um funil de separação e deixada em repouso por 24 h até a total
separação das fases (superior- biodiesel + impurezas e inferior- glicerina +
impurezas). Ao término da separação de fases, a fase inferior foi removida do funil,
restando apenas o biodiesel bruto.
Em seguida, o biodiesel foi submetido a um processo de purificação, onde os
ésteres formados na reação foram lavados com água destilada quente
(aproximadamente 80 °C), com o intuito de eliminar o álcool remanescente, os
resquícios de catalisador e o sabão formado (ver Figura 5). A etapa de lavagem foi
repetida até que a água de lavagem atingisse pH neutro (para isso foram realizadas
em média 10 lavagens).
Após a etapa de purificação, foi realizado o processo de secagem do
biodiesel, que ocorreu em duas etapas: na primeira, o biodiesel foi colocado em
contato com o sulfato de sódio anidro para que toda ou parte da água remanescente
fosse absorvida. O sulfato de sódio anidro foi colocado diretamente dentro do funil
de separação, formado uma espécie de “filtro” para reter as moléculas de água
durante o escoamento do biodiesel (que foi coletado em um béquer).
A segunda etapa da secagem foi realizada numa estufa, onde o biodiesel foi
colocado para secar a 100°C durante 30 minutos, a fim de eliminar traços de
32
umidade remanescentes no biodiesel. Em seguida, o mesmo foi pesado, colocado
em frasco âmbar e armazenado em freezer até a realização das análises (Figura 6).
Figura 5 - Etapa de lavagem do biodiesel.
Fonte: Autoria própria (2013).
Figura 6 - Amostra de biodiesel enviada para análise e amostra da glicerina (subproduto da reação).
Fonte: Autoria própria (2013).
.
33
4.4 VARIÁVEIS ANALISADAS
Entre as variáveis que interferem no rendimento da reação de produção do
biodiesel, algumas foram escolhidas para serem analisadas no presente trabalho:
razão molar óleo/álcool, temperatura do sistema reacional e porcentagem de
catalisador utilizada. Com o intuito de se avaliar o efeito destas variáveis no
rendimento da reação, os experimentos foram realizados obedecendo a um
planejamento experimental fatorial 2³ (de 3 variáveis variando em dois níveis), com
triplicata no ponto central. A Tabela 3 apresenta o intervalo de estudo das variáveis
e a Tabela 4 os dados do planejamento experimental. O intervalo de estudo das
variáveis foi definido com base nos estudos de Araújo (2008) e Eevera et al, (2009),
que também pesquisaram o uso do óleo de coco para produção de biodiesel.
Tabela 3 - Intervalo de estudo das variáveis do planejamento experimental
VARIÁVEL INTERVALO
Razão molar óleo/álcool (metanol) [R] 1:4 -1:8
Temperatura [T] (°C) 40-60
Percentual de catalisador [C] (%) 1-2
Ponto central: R= 1:6; T=50°C; C=1,5%
Tabela 4 - Planejamento experimental utilizado na síntese do biodiesel de óleo de coco.
EXPERIMENTO RAZÃO ÓLEO/ÁLCOOL T (°C) % CATALISADOR
1 1:4 40 1
2 1:8 40 1
3 1:4 60 1
4 1:8 60 1
5 1:4 40 2
6 1:8 40 2
7 1:4 60 2
8 1:8 60 2
9 1:6 50 1,5
10 1:6 50 1,5
11 1:6 50 1,5
Os experimentos foram realizados de forma aleatória e o tempo de reação foi
mantido fixo em 90 minutos, com base em estudos de produção de biodiesel de óleo
de coco realizados por Eevera et al. (2009), que obteve melhores resultados para
este tempo de extração.
34
4.5 ANÁLISE CROMATOGRÁFICA DO BIODIESEL PARA CÁLCULO DO
RENDIMENTO
As amostras de biodiesel obtidas em cada experimento foram diluídas em
hexano na concentração de 8mg/mL (40 mg em 5 mL). Esta mistura foi analisada
por cromatografia gasosa no Laboratório de Cromatografia Instrumental, no
Departamento de Engenharia Química da Universidade Federal de Pernambuco. As
condições da análise cromatográfica estão resumidas a seguir.
4.5.1 Condições cromatográficas
Para as análises cromatográficas foi utilizado um cromatógrafo gasoso CG,
(modelo CG-Master), dotado de detector de ionização de chama, coluna capilar
(megabore) de sílica fundida contendo um filme com 0,25 μm de polietilenoglicol
(Carbowax 20 M), com 30 m de comprimento e 0,54 mm de diâmetro. A temperatura
do detector foi ajustada para 200°C e a do vaporizador para 150°C. A análise foi
realizada em condições isotérmicas à uma temperatura de 180°C durante 3 minutos.
A fase móvel foi o hidrogênio (5 mL/min), com uma razão de divisão (split) de 1/20.
O volume de amostra injetado no cromatógrafo foi de 2 μL para todas as amostras.
4.5.2 Cálculo do rendimento bruto de biodiesel produzido
O rendimento bruto de cada reação de transesterificação foi calculado a partir
da equação 1.
Em que:
A equação 1 se baseia na estequiometria da reação de transesterificação,
Equação (1)
35
que produz 3 mols de ésteres metílicos (biodiesel) para cada mol de óleo utilizado.
O número de mols do óleo de coco (nóleo) foi calculado a partir da razão entre
a massa de óleo de coco utilizada na reação (100g) e a massa molar média do óleo
de coco.
A massa molar média do óleo de coco foi determinada com base na sua
composição centesimal determinada por cromatografia gasosa, de acordo com a
metodologia de Hartman e Lago (1973).
Já o número de mols do biodiesel (nbiodiesel) foi calculado a partir da razão
entre a massa de biodiesel produzida em cada reação e a massa molar média do
biodiesel produzido em cada experimento, a qual também foi calculada com base
nos resultados das análises cromatográficas das amostras de biodiesel obtidas.
36
5 RESULTADOS E DISCUSSÕES
5.1 COMPOSIÇÃO EM ÁCIDOS GRAXOS DO ÓLEO DE COCO BRUTO
O óleo de coco analisado apresentou como componentes majoritários, o ácido
láurico (40,8%), o ácido mirístico (20,3%) e o ácido palmítico (12,3%) e mais alguns
outros ácidos graxos em percentuais menores, conforme pode ser visto no Gráfico 1,
que apresenta o perfil de ácidos graxos do óleo de coco analisado.
Gráfico 1 - Composição em ácidos graxos do óleo de coco bruto
Fonte: Autoria própria (2013).
Os ácidos láuricos possuem cadeias carbônicas curtas que permitem uma
interação mais efetiva com agentes transesterificantes, de modo que pode obter-se
um produto com excelentes características físico-químicas para síntese de biodiesel
(LIMA et al., 2007).
Pela análise do Gráfico 1 é possível observar que a maior parte dos ácidos
graxos do óleo de coco são saturados (85%), conferindo ao mesmo elevada
resistência a oxidação, o que contribui para utilização desse óleo como matéria-
prima para produção de biodiesel. Atualmente, grande parte dos óleos utilizados
para produção de biodiesel possuem predominantemente ácidos graxos insaturados,
o que torna esse combustível susceptível a oxidação (FERRARI; SOUZA, 2009).
4,7 4,1
40,8
20,3
12,3
2,8
9,9
3,6
0
5
10
15
20
25
30
35
40
45
50
Te
or
em
ácid
os
gra
xo
s(%
)
37
No presente trabalho, os ácidos graxos insaturados mais representativos
detectados foram o ácido oléico (9,9%) e o linoléico (3,6%). Os resultados obtidos
para o perfil de ácidos graxos do óleo de coco foram compatíveis com os
encontrados por Souza et al. (2012).
Após a obtenção da composição centesimal do óleo de coco foi possível
calcular a sua massa molar média, o resultado obtido foi 707,03 g/mol. A
determinação da massa molar do óleo era necessária previamente ao início dos
experimentos de síntese do biodiesel, pois só com essa informação era possível
determinar a massa de álcool (em gramas) a ser usada em cada experimento e
assim se obter as razões molares utilizadas neste trabalho, ou seja, 1:4, 1:6 e 1:8.
5.2 PRODUÇÃO DO BIODIESEL A PARTIR DO ÓLEO DE COCO BRUTO
Após a definição das massas de todos os reagentes, o biodiesel foi
sintetizado seguindo o planejamento experimental mostrado na Tabela 4.
A Figura 7 mostra o aspecto do biodiesel obtido após a etapa de purificação.
Figura 7 - Visualização do aspecto do biodiesel obtido.
Fonte: Autoria própria (2013).
38
O biodiesel de coco apresentou uma coloração mais clara que o óleo de coco
de origem, se aproximando de uma tonalidade incolor. A formação de sabão foi
observada em todos os experimentos, o que era esperado, em virtude de se ter
trabalhado com a transesterificação básica, entretanto, a quantidade de sabão
formado sugere que o óleo de coco bruto contém uma alta concentração de ácidos
graxos livres.
5.3 RENDIMENTO BRUTO DA REAÇÃO DE TRANSESTERIFICAÇÃO
A Tabela 5 apresenta o rendimento bruto da reação de transesterificação em
função dos parâmetros investigados.
Tabela 5 - Valores de rendimento bruto obtido para cada condição experimental.
EXPERIMENTO RAZÃO MOLAR
ÓLEO/ÁLCOOL
TEMPERATURA
(°C)
CATALISADOR
(%)
RENDIMENTO
(%)
1 1:4 40 1 70,7
2 1:8 40 1 78,7
3 1:4 60 1 57,4
4 1:8 60 1 84,0
5 1:4 40 2 42,8
6 1:8 40 2 53,3
7 1:4 60 2 36,2
8 1:8 60 2 52,5
9 1:6 50 1,5 84,1
10 1:6 50 1,5 80,8
11 1:6 50 1,5 57,7
Fonte: Autoria própria (2013).
Como pode ser visto na Tabela 5, o rendimento da reação de produção do
biodiesel variou de 36,2 a 84,1%. A melhor condição de síntese foi obtida para razão
molar 1:6, na temperatura de reação de 50°C, e com 1,5% de catalisador
(experimento 9).
Os experimentos 9, 10 e 11 foram realizados nas mesmas condições, pois
serviriam para cálculo do desvio-padrão dos ensaios. Entretanto foi constatada uma
discrepância no resultado das análises cromatográficas do experimento 11, o que
39
impossibilitou um tratamento mais apurado dos resultados, logo o desvio-padrão dos
ensaios foi calculado com base apenas nos experimentos 9 e 10, obtendo-se um
valor de desvio-padrão de 2,33.
5.4 INFLUÊNCIA DAS VARIÁVEIS NO RENDIMENTO
O Gráfico 2 apresenta, de forma comparativa, o efeito da razão molar sobre o
rendimento bruto da reação de produção do biodiesel.
Gráfico 2 - Rendimento bruto em função da razão molar óleo/álcool utilizada.
Fonte: Autoria própria (2013).
Comparando os experimentos 1 e 2 (que foram realizados nas mesmas
condições de temperatura e percentual de catalisador) foi possível observar que
maiores rendimentos foram obtidos para a razão molar mais alta (1:8), ou seja, uma
maior razão molar óleo/álcool contribuiu para o aumento do rendimento da reação
de transesterificação. O mesmo comportamento foi observado nos demais
experimentos.
O Gráfico 3 ilustra, também de forma comparativa, a influência da
temperatura reacional sobre o rendimento bruto da reação de produção do biodiesel.
O efeito da temperatura sobre o rendimento não apresentou um comportamento
linear. Comparando-se os experimentos 1 e 3, 5 e 7 e também 6 e 8, (realizados nas
mesmas condições de razão molar e % de catalisador) observa-se que a
70,7
57,4
42,8 36,2
78,7 84,0
53,3 52,5
0,0
20,0
40,0
60,0
80,0
100,0
1 e 2 3 e 4 5 e 6 7 e 8
Re
nd
ime
nto
bru
to (
%)
Experimentos
Razão molar o/a (1:4) Razão molar o/a (1:8)
40
temperatura de 40°C proporcionou melhores resultados, com rendimentos na a faixa
de 42,8% a 70,7%. Já para os ensaios 2 e 4 o comportamento se inverteu,
apresentando rendimentos mais altos na temperatura de 60°C (84%) que na de
40°C (78,7%).
Gráfico 3 - Rendimento bruto em função da temperatura reacional utilizada.
Fonte: Autoria própria (2013).
A influência do percentual de catalisador sobre o rendimento bruto da reação
de produção do biodiesel está ilustrado no Gráfico 4.
Gráfico 4 - Rendimento bruto em função do percentual de catalisador utilizado.
70,7 78,7
42,8 53,3
57,4
84,0
36,2
52,5
0,0
10,0
20,0
30,0
40,0
50,0
60,0
70,0
80,0
90,0
1 e 3 2 e 4 5 e 7 6 e 8
Re
nd
ime
nto
bru
to (
%)
Experimentos
T=40°C T=60°C
70,7 78,7
57,4
84,0
42,8
53,3
36,2
52,5
0,0
10,0
20,0
30,0
40,0
50,0
60,0
70,0
80,0
90,0
1 e 5 2 e 6 3 e 7 4 e 8
Re
nd
ime
nto
bru
to (
%)
Experimentos
1% de catalisador 2% de catalisador
41
Fonte: Autoria própria (2013).
Pela análise do Gráfico 4 observa-se que maiores rendimentos foram obtidos
ao se trabalhar com um percentual de 1% de catalisador.
Durante a síntese do biodiesel de coco observou-se que ao utilizar o
percentual mais elevado, ou seja, 2% de catalisador, sempre ocorria a formação de
uma maior quantidade de glicerina, o que resultava numa menor quantidade de
biodiesel.
No presente trabalho, os experimentos 9 e 10, apresentaram resultados
compatíveis com os de Eevera et al (2009), que também sintetizou biodiesel de
coco, além de outros óleos como: óleo de palma, algodão, farelo de arroz e
amendoim. Em seus estudos de síntese de biodiesel Eevera et al (2009), avaliaram
as variáveis: percentual de catalisador (0,5 a 2,5%), temperatura (40 a 60°C) e
tempo de reação (30 a 150 min). Tais pesquisadores obtiveram maiores rendimentos
nas seguintes condições: 1,5% de catalisador, temperatura de 50°C e 90 minutos de
reação, o que corrobora com o resultado do presente trabalho.
42
6 CONCLUSÕES
O presente trabalho apresentou os procedimentos que envolvem a reação de
transesterificação via catálise básica para a produção de biodiesel, utilizando como
matéria-prima o óleo de coco. Além disso, analisou a influência de algumas variáveis
(razão molar óleo/álcool, temperatura reacional e percentual de catalisador) sobre o
rendimento da reação de transesterificação.
O óleo de coco bruto utilizado na síntese do biodiesel apresentou o ácido
láurico (40,8%), o ácido mirístico (20,3%) e o ácido palmítico (12,3%) como
componentes majoritários.
O rendimento da reação de produção do biodiesel a partir do óleo de coco
bruto variou de 36,2 a 84,1%, com melhores resultados para as seguintes
condições: razão molar 1:6, temperatura reacional de 50°C, e percentual de
catalisador igual a 1,5%.
Os resultados também mostraram que as variáveis que apresentaram maior
influência sobre o rendimento da reação de transesterificação do óleo de coco foram
o percentual de catalisador e a razão molar óleo/álcool.
43
REFERÊNCIAS
ANP. Glossário. Disponível em: <http://www.anp.gov.br/?id=582>. Acesso em: 07 de março de 2013.
ANVISA. 1999. Disponível em: <http://portal.anvisa.gov.br/wps/wcm/connect/a2190900474588939242d63fbc4c6735/RDC_482_1999.pdf?MOD=AJPERES >. Acesso em: 20 de fevereiro de 2013.
ARAÚJO, G. S. Produção de biodiesel a partir de óleo de coco (Cocos nucifera L.). 2008. 104f. Dissertação (Mestrado em Engenharia Química), Universidade Federal do Rio Grande do Norte, Natal, 2008.
BENEVIDES, M. S. L. Estudo sobre a produção de biodiesel a partir de oleaginosas e análise de modelos cinéticos do processo de transesterificação via catálise homogênea. 2011. 75 f. Monografia (Bacharelado em Ciência e Tecnologia). Universidade Federal Rural do Semi-Árido, Angicos, 2011.
CARTONI, C. R. Avaliação de catalisadores alcalinos na produção de biodiesel metílico derivado do óleo de soja: análise técnica, econômica e ambiental. 2009. 83 f. Dissertação (Mestrado em Engenharia Química) - Universidade de São Paulo, Lorena, 2009.
CARVALHO, R. H. R. Avaliação da eficiência de catalisadores comerciais na obtenção de biodiesel de algodão(Gossipium hisutum L.) 2009. 110f. Dissertação (Mestrado em Engenharia Química), Universidade Federal do Rio Grande do Norte, Natal, 2009.
EEVERA, T. et al. Biodiesel production process optimization and characterization to assess the suitability of the product for varied environmental conditions. Renewable Energy, p. 1-4, 2008.
FERRARI, R. A.; SOUZA, W. L. Avaliação da estabilidade oxidativa de biodiesel de óleo de girassol com antioxidantes. Química Nova, v. 32, n.1, p. 106-111, 2009.
FONTANA, José Domingos. Biodiesel: para leitores de 9 a 90 anos. Curitiba: Ed. UFPR, 2011, 253 p.
HARTMAN, L.; LAGO, R. C. A., Laboratory Practices, 1973, 22, 475.
KRAUSE, L. C. Desenvolvimento do processo de produção de biodiesel de origem animal. 2008. 130 f. Tese (Doutor em Química) - Departamento do Instituto de Química, Universidade Federal do Rio Grande do Sul, Porto Alegre, 2008.
44
LIMA NETO et al., Anais do I Congresso da rede Brasileira de tecnologia de Biodiesel, 96-99, 2006.
LIMA, J. R. O et al. Biodiesel de babaçu (Orbignya sp.) obtido por via etanólica. Química Nova, v. 30, n. 3, p.600-603, 2007.
MACHADO NETO, A. S. Estudo da influência de blendas de óleo residual de frituras na viscosidade do biodiesel. 2011. 77 f. Monografia (Licenciatura em Química) – Universidade Federal Rural de Pernambuco, Serra Talhada, 2011.
MOURAD, A. L. Avaliação da cadeia produtiva de biodiesel obtido a partir da soja. 2008. 123 f. Tese (Doutorado em Planejamento de Sistemas Energéticos) - Faculdade de Engenharia Mecânica, Universidade Estadual de Campinas, Campinas, 2008.
PARENTE, E. J. S. Biodiesel: uma aventura tecnológica num país engraçado. Tecbio, 68 p. 2003.
PRESTES, I. A. F. Introdução do biodisel na matriz energética do Ceará. Disponível em <
http://www.ecoeco.org.br/conteudo/publicacoes/encontros/vii_en/mesa5/resumos/introducao_do_biodiesel_na_matriz.pdf> Acesso em: 01 de mar de 2013.
REIS, M. C. et al. Transesterificação dó óleo de castanha do Pará e coco de babaçu catalisada por ácido.In: CONGRESSO BRASILEIRO DE CATÁLISE, Anais...Porto de Galinhas: PE, 2007.
SALVADOR, A. A. et al. Biodiesel: aspectos gerais e produção enzimática. Trabalho de Graduação, Departamento de Engenharia de Alimentos e Engenharia Química, Universidade Federal de Santa Catarina, 2009.
SEBRAE. Biodiesel. Disponível em: <http://www.agencia.cnptia.embrapa.br/Repositorio/NT00035116_000gihb7tn102wx5ok05vadr1szzvy3n.pdf> Acesso em: 01 de abril de 2013.
SOUZA, L. S. S. et al. Obtenção dos ésteres etílicos a partir da transesterificação do óleo de coco (Cocos nucifera L.). In: XIX CONGRESSO BRASILEIRO DE ENGENHARIA QUÍMICA, 2012, Búzios, Rio de Janeiro, Anais..., Búzios:RJ, 2012.
XAVIER, C. H. Processo de beneficiamento do coco. 2008. 68 f. Monografia (Graduação em Engenharia Química) – Universidade Federal do Rio Grande do Norte, Natal, 2008.