Struttura e reattivita del particolato atmosferico Mauro CAUSA', Marco Trifuoggi, unina, modelling,...
-
Upload
giovanna-biondi -
Category
Documents
-
view
225 -
download
2
Transcript of Struttura e reattivita del particolato atmosferico Mauro CAUSA', Marco Trifuoggi, unina, modelling,...

Struttura e reattivita’ del particolato atmosferico
Mauro CAUSA' , Marco Trifuoggi, unina, modelling, analisi chimicheGlauco Tonachini, unito, modellingEnrico Ferrero, unipmn, Guido Pirovano, CESI, modelli regionali fluidodinamici Enrico Boccaleri, Aldo Arrais, Giorgio Gatti, unipmn, spettroscopie ottiche Luca Pardi, cnr ipcf, epr.Maria Cristina Paganini, unito, epr
Simona Silvia Merola, Bianca Maria Vaglieco, cnr im, studi su motoriHinrich Grothe, TU Wien, misure spettroscopiche Mike Pilling, Uni Leeds, atmospheric chemistry
Tone Kokalj, I Stefan, Ljubliana, modellingClaus Nielsen, Uni Oslo, spettroscopie ottiche
Torino 21 ottobre 2008

• Un punto debole dei modelli
fotochimici atmosferici e’ il
trattamento del particolato organico ed
inorganico
• L’informazione relativa al particolato
e’ molto piu’ parziale ed approssimata

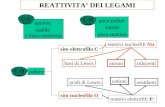
Aerosol organico e inorganico: il problema strutturale
La reattivita’,
E quindi gli effetti
locali e globali
possono essere studiati
solo attraverso la struttura

Segnale epr di particolato carbonioso
3450 3460 3470 3480 3490 3500 3510 3520 3530

I grafeni dispari: radicali
intrinseci
C14H10 e’ closed shellE’ stabile (Eatom/C: 210 kcal)Non reagisce con NO2
C13H9 e’ open shell (radicale )E’ stabile (Eatom/C: 208 kcal)E’ molto reattivo con NO2

La vacanza di carbonio: stato di tripletto
sc5=0.09
sc5=0.34
sc=1.16sc5=1.12
••

Misure epr ad alto campofuliggine modello: PRINTEX U
-0.03
-0.02
-0.01
0
0.01
0.02
0.03
0.04
6.78 6.785 6.79 6.795 6.8 6.805 6.81
tq_006
f300_002
f700_003
particolato diesel
-0.04
-0.03
-0.02
-0.01
0
0.01
0.02
0.03
0.04
0.05
6.74 6.76 6.78 6.8 6.82 6.84 6.86
diesel_004

Fig. 5: TPD-MS curves of Printex U - (trace) mass fragment.
OH
CO2
CO
CO2 desorption from -COOH?
Interpretazione teorica degli esperimenti TPD
Desorption maxima in TPD spectra assigned to functional groups
300 400 500 600 700 800 900 1000 1100 1200 1300 1400 1500 1600
T (K)
acid (6)
acid (5)
acid (3)
lactone (6)
lactone, 5 types (2) carbonyl, 3 types (2)
anhydride (6) carbonyl (6)
anhydride (3) and (4)
anhydride (1)
ketone K1 (CO)
carboxylic acids / CA1, CA2 and CA3
(monomolecular, CO2)
lactones L2, L1 (CO)
(lactoneL3)
computed data:
bicarboxylic acids DCA4, DCA2, DCA1
(cooperative, CO2)
OH from PA OH from SA
(bimolecular, CO2) OH from P
|aldehyde A (CO)
(AN1anhydride)
4 lactones and
3 lactones (CO2) (8) CO2+HO ?
acid (8)
(CO2 + HO)
2 anhydrides (CO2 + CO)(8)
--- Monarch--- Printex U
"all anhydrides removed" (7)
\ "all lactones and phenols removed" (7)/
\ "all carbonyls and ethers removed" (7)
summary of the experimental data:
lactones (7)
carbonyl (7)
phenol (CO) (6)
--- NORIT ROX 0.8
--- carbon fibers
--- PhOH/H 2 CO char
--- PhOH/H 2 CO char
--- polycrystalline graphite
--- Sorbonorit B 4
| ketone K3 (CO)
lactone L3/
AN2 anhydrides AN1
| (CO+CO2) |
anhydride? (CO2)
carboxyl group(strong acidic)
phenol group(acidic)
lactol group(weak acidic)
coincidecarbonyl group(weak acidic)
pyron group(basic)

Analisi cinetica del desorbimento
• Ea = RTmax.[ln(Tmax
./) – ln(Ea/RTmax)]
(T) = e.kT/h. exp[S‡(T)/R] ; =0.17 K s-1
(derivate dell’equazione di Polany-Wigner)
-35,0
-30,0
-25,0
-20,0
-15,0
-10,0
-5,0
0,0
5,0
E (kcal mol-1)OHO
+ HO
OHOHO
H OOHO
OH H
O O
OO
+ H2O
+ CO2
OOHHO
A
B
E
F
G
Bimolecular mechanism for Ar-COOH
D
C
O O
OHO OHOHO
OO
OH
O
HO H
Tmax=779°K Tmax=476°K
Tmax=556°K
Tmax=336°K
Tmax=550°K

spettroscopia raman (micro)
1000 2000 3000 40000
1000
2000
3000
4000
0
1000
2000
3000
4000
In
ten
sity (
a.
u.)
Graphite SHER
Raman Shift (cm-1
)
Graphite BarG
D3D1 D2D4
800 1000 1200 1400 1600 1800 2000
500
1000
1500
Inte
nsi
ty (
a. u
.)
Raman Shift (cm-1)
observed spectrumand curve fit
D4
D1
D3
G
D2

Il trattamento termico non comporta
sensibili variazioni strutturali (%)
Il campione del diesel è molto più fluorescente,
1720 (chetonici) e 1550 (insaturi isolati)
Diesel piu’ ordinato del benzina
Anche piu’ ossidato
Campioni catturati su filtro:
Insaturazioni isolate

AG Schlögl, Fritz Haber Institut, Berlin

Rezioni con O3
ΔE=-40 Kcal/mol

- O2- O2 - O2
B
A
OO
O
O
O
O
O
O OO
POD-EPAD
b: concertedasynchronous TS
a: concertedsynchronous TS
OO
O
ISCsinglet triplet
O3 +
O OO
TCD -OCD
TCD- EPO
POD-OCD
PO-EPAD
R-TCD
POD-EPO
PO-POD
PO-TCD
R-PO
R
OCD EPO
EPADPOD
TCDPO
non-concerted
PAH
- O2
Legend
R: reactantsPO: primary ozonideTCD: trioxyl cyclohexadienyl diradicalPOD: peroxyl oxyl diradicalEPAD: epoxide peroxyl allyl diradicalOCD: oxyl cyclohexadienyl diradicalEPO: epoxide
non-concertedprocesses
con certed
O
O OO
EPAD-EPO
ACRONYMS in dashed boxes: not found
PO -EPO
3

Studio della cinetica di adsorbimento
• SS + O3 → SSO + O2 ; exp = 3.3 x 10-3
• E= -23 kcal/mol; E‡ = 13.1 kcal/mol
• theor = (kBT/h) q‡/qR exp(-E‡/ kBT)/ = 1.2 x 10-13
• SS + OSS + O33 →→ SS SS------OO33 →→ SSO + O SSO + O22
• E= -2.8 kcal/mol (-0.3+2.5vdw), senza barrieraE= -2.8 kcal/mol (-0.3+2.5vdw), senza barriera
• = (k= (kBBT/h) (qT/h) (qpp/q/qRR)) (1/(1/)) = = 44..11 x 10 x 10-3-3

• Misure normalmente effettuate nella scienza delle superfici e della catalisi possono fornire importanti informazioni sulla natura chimica e la reattivita’ del particolato
• La simulazione su scala atomistica permette di connettere le informazioni sperimentali ottenute con tecniche diverse
• In questa fase del progetto abbiamo verificato la possibilita’ di introdurre delle informazioni su scala atomica nei modelli macroscopici su scala geografica