Ronéo P2 n° 3 T2 - ampcfusion.com©o-3-P2.pdf · Description des hépatocytes iv. Voies biliaires...
Transcript of Ronéo P2 n° 3 T2 - ampcfusion.com©o-3-P2.pdf · Description des hépatocytes iv. Voies biliaires...

1
Ronéo P2 n° 3 T2
Semaine du 16/01 au 20/01/17

2

3
Sommaire de la ronéo n° 3 du 2e trimestre
Semaine du 16 au 20 janvier
Errata ................................................................................................................................................................................. 4
UE 6
SD Histologie .................................................................................................................................................................................... 5
Cours 4 : Histologie des glandes digestives : foie et voies biliaires, pancréas et voies excréto-
pancréatiques ................................................................................................................................................................................ 5
SD Sémiologie ............................................................................................................................................................................... 25
Cours 5 : Sémiologie radiologique du foie et des voies biliaires ............................................................................ 25
Cours 6 : Sémiologie et explorations du foie et des voies biliaires ....................................................................... 43
Cours 7 : Sémiologie radiologique de l’étage sous-mésocolique ........................................................................... 55
SD Anatomie pathologique .................................................................................................................................................... 77
Cours 3 : Evolution morphologique d’une hépatite virale chronique .................................................................. 77
SD Anatomie .................................................................................................................................................................................. 89
Cours 5 : Foie et voies biliaires ............................................................................................................................................ 89
Cours 6 : Rectum, canal anal .............................................................................................................................................. 103
SD Pharmacologie.................................................................................................................................................................... 117
Cours 2 : Antisécrétoires et antiacides, médicaments de la motilité digestive ............................................. 117
SD Biochimie .............................................................................................................................................................................. 131
Cours 1 : Principes biochimiques des ictères .............................................................................................................. 131

4
ERRATA ET PRECISIONS
Ronéo 2 SD Anapath 2 Précision du prof :
p.133 : “Concernant l’instabilité génétique sporadique, il faut noter que dans le cadre sporadique cette instabilité est secondaire à la méthylation du promoteur de MLH1 contrairement au syndrome de Lynch qui est lié à des mutations de MLH1, MSH2, MSH6 ou PMS2.”

5
Plan :
I. Les glandes salivaires principales A. La portion sécrétrice i. Points communs ii. Différences B. La portion excrétrice
i. Points communs ii. Particularités
II. Le pancréas A. Le pancréas exocrine
i. Portion sécrétrice ii. Portion excrétrice
B. Le pancréas endocrine i. Composante insulaire ii. Composante extra-insulaire
III. Le foie et les voies biliaires
A. Introduction i. Vascularisation hépatique ii. Embryologie iii. Macroanatomie
B. Microanatomie i. Espaces portes ii. Parenchyme iii. Description des hépatocytes iv. Voies biliaires extra hépatiques
UE6 – SD Histologie – n°4
16/01/17 Pr. Patrick BARBET
RT : Lauriane Deker
RL : Vanessa Bernard
Histologie des glandes digestives : foie et voies biliaires, pancréas et voies excréto-pancréatiques

6
Ce cours traite des glandes anatomiquement individualisées annexées au tube digestif :
- les glandes salivaires principales annexées à la cavité buccale : exocrines, paires et
symétriques, avec une organisation soit séreuse, soit muqueuse :
o 2 glandes sous-maxillaires
o 2 glandes sublinguales
o glande parotide
- dans l’abdomen :
o le pancréas
o le foie
I. Les glandes salivaires principales
A. La portion sécrétrice
i. Points communs Ce sont des glandes exocrines, anatomiquement individualisées. Il y a d’ailleurs la présence d’un canal
excréteur qui va aller se jeter dans la cavité buccale. Ce sont des glandes lobulées, c’est-à-dire entourées
d’une petite capsule de tissu conjonctif vascularisé. Cette capsule envoie des fibres en profondeur qui
forment des lobules glandulaires.
A l’intérieur des lobules on retrouve le composant épithélial à l’origine de la sécrétion : le parenchyme
glandulaire.
Remarque : Le mot parenchyme peut signifier « tissu d’une glande »
ou pour les puristes « composante épithéliale d’une glande ».
Dans les lobules des glandes salivaires, en plus de la structure
conjonctive, on trouve des zones claires, qui correspondent à des
adipocytes.
ii. Différences On peut, en microscopie optique, distinguer les formations épithéliales de nature séreuse, et les
formations épithéliales de type muqueux. Ces deux composantes peuvent se retrouver au sein d’une
seule et même glande – on parlera de glande mixte (= séro-muqueuse) - le cas échéant, on parlera de
glande pure.
Glande parotide

7
La glande parotide est une glande exocrine encapsulée SEREUSE
PURE ; c’est la seule glande anatomiquement individualisée séreuse
pure de l’organisme. Elle comporte de nombreux acini séreux (pas
toujours aussi caractéristiques que ceux vus en première année) qui
sont arrondis, avec une lumière mal visible, virtuelle et bordés par une
seule couche de cellules au noyau relativement arrondi. Elle sécrète
des enzymes de la phase salivaire de la digestion, au premier rang
duquel l’amylase salivaire. Une membrane basale sépare les acini
séreux de la trame conjonctive à fonction de nutrition.
Remarques : La parotide comporte également des éléments lymphoïdes. Elle est en rapport anatomique avec
le nerf facial.
Glande sublinguale
Dans l’espèce humaine, la glande sublinguale est une glande MIXTE à prédominance MUQUEUSE.
Glande sous maxillaire
Dans l’espèce humaine, la glande sous maxillaire est une glande MIXTE à prédominance SEREUSE, dont
les acini sont caractérisés par une polarité apico-basale.
B. La portion excrétrice
i. Points communs Les canaux excréteurs annexés à ces unités sécrétrices, confluent pour donner des canaux de plus en plus
volumineux, qui eux-mêmes donneront le canal excréteur principal, macroscopiquement visible des
différentes glandes s’abouchant dans la cavité buccale (par exemple pour la parotide, il s’agit du canal de
Stenon). Les canaux excréteurs comportent donc deux parties : une portion intra-lobulaire, et une
portion extra-lobulaire.
Leur fonction principale est de récolter les produits de
sécrétion fabriqués dans les unités sécrétrices et de les
transporter vers la cavité buccale. Les canaux excréteurs
des glandes salivaires principales présentent des
particularités qui leur sont propres.
• Au niveau de la portion intra-lobulaire des canaux, l’épithélium en
contact avec la lumière du tube est prismatique simple, avec des limites
cellulaires bien visibles. Le cytoplasme des cellules épithéliales est
fortement éosinophile, et contient un renforcement éosinophile à sa
partie basale sous forme de stries linéaires bien visibles. Ainsi, les
canaux excréteurs des glandes salivaires principales sont également
nommés « canaux striés ». Cette caractéristique est spécifique aux

8
glandes salivaires principales.
Ces stries éosinophiles correspondent à des mitochondries fournissant de l’énergie et permettant donc
le transport actif de part et d’autre de l’épithélium, et donc des échanges entre l’épithélium et le contenu
de sa lumière. Ainsi, des échanges d’eau et d’électrolytes ont lieu au niveau des canaux, permettant le
rééquilibrage du produit de sécrétion. Les canaux excréteurs ne représentent donc pas un système inerte
de conduit.
• A mesure que les canaux excréteurs s’anastomosent, l’épithélium se
stratifie. Au niveau de la portion extra-lobulaire (ou inter-lobulaire) des
canaux, l’épithélium devient stratifié dans les canaux les plus volumineux.
Cette caractéristique n’est pas partagée par le pancréas, où quelle que soit la
taille des canaux, l’épithélium est simple.
ii. Particularités
Les glandes salivaires principales dérivent de la partie interne de l’appareil pharyngien. On y trouve donc
d’autres composantes.
Eléments sébacés
On peut retrouver les cellules sébacées annexées au système des canaux. Elles se forment par
bourgeonnement de l’épithélium en formant un sac alvéolaire. Elles sont constituées d’une couche de
cellules périphériques basales et d’une couche de cellules qui se chargent en produit de sécrétion. Les
cellules sébacées se caractérisent par une évolution holocrine ; le sébum est donc excrété dans la lumière
des canaux excréteurs (cf. figure ci-dessous). En pathologie, ces cellules peuvent donner des tumeurs
sébacées au niveau des glandes salivaires principales.
Cellules myoépithéliales

9
Les cellules myoépithéliales sont des cellules fusiformes situées près de l’épithélium de revêtement
proprement dit. Elles expriment des marqueurs épithéliaux comme la cytokératine. Elles ont également
une composante musculaire car elles expriment des protéines musculaires comme la myosine, l’actine ou
la calponine.
Remarque : Ces cellules pourraient avoir une fonction contractile mais cela est très discuté.
Elles sont présentes après la portion excrétrice, à la partie originelle des canaux excréteurs, et peuvent
donner lieu à des tumeurs qui sont parmi les plus fréquentes de la parotide ou des glandes salivaires : les
tumeurs mixtes ou adénomes pléiomorphes.
Oncocytes
Les oncocytes se regroupent en masses compactes, ils sont riches en
mitochondries et ont un aspect épithélial avec un cytoplasme fortement
éosinophile. On peut également trouver ces glandes au niveau de la thyroïde.
En pathologie, elles peuvent donner des oncocytomes, plus rares que les
tumeurs mixtes.
Toutes ces cellules peuvent donc donner naissance à des tumeurs d’aspect assez variables : (de la gauche vers la droite sur le schéma)
- carcinome (tumeur épithéliale) à cellule acineuse
- cellules myoépithéliales => adénomes pléimorphes, etc
- partie striée => oncocytome
- partie stratifiée terminale => tumeurs épithéliales

10
II. Le pancréas
Le pancréas est une portion charnue, qui barre
transversalement l’abdomen, en passant par 4 cadres jusqu’à la
loge splénique. Cette glande est d’origine entoblastique en ce qui
concerne ses composants épithéliaux. Mais sa trame
conjonctive quant à elle, se développe à partir de la
splanchnopleure.
Sa structure est extrêmement variable notamment au niveau des
canaux excréteurs.
Le pancréas est une glande salivaire abdominale, anatomiquement individualisée, lobulée
macroscopiquement, avec deux composantes :
- Essentiellement une composante exocrine (amylase pancréatique) avec des canaux excréteurs
intra et extra lobulaires
- Mais aussi une composante endocrine, avec les îlots de Langerhans (régulations métaboliques)
Histologiquement on observe :
- Une bordure épithéliale prismatique TOUJOURS simple (il n’y a pas de canaux striés !)
- Les lobules cunéiformes (à angles aigus). Ces derniers sont spécifiques de cette glande.
A. Le pancréas exocrine
i. Portion sécrétrice
La portion sécrétrice du pancréas exocrine est lobulée. On parle de lobulation cunéiforme : en effet, les
lobules pancréatiques ont une forme particulière, avec des angles aigus.
Les cellules sécrétrices des lobules sont regroupées en acini séreux totalement purs, avec des limites
cellulaires mal visibles, une polarité baso-apicale avec une basophilie basale (ergastoplasme) et une
acidophilie apicale (grains de zymogènes de stockage des sécrétions). A la différence des glandes
salivaires principales, il n’y a pas, dans les lobules du pancréas, d’infiltration graisseuse (à faible
grossissement).

11
ii. Portion excrétrice
A proximité des lobules, des canaux excréteurs naissent et s’anastomosent jusqu’à former le canal
pancréatique principal (de Wirsung), qui se jette en D2, et le canal pancréatique accessoire (de
Santorini). Le revêtement épithélial de ces canaux est prismatique simple.
Attention : L’épithélium des canaux excréteurs du pancréas n’est jamais stratifié !
An centre des acini, près de la lumière, on distingue des cellules centro-acineuses, claires, à fonction
d’excrétion.
B. Le pancréas endocrine
i. Composante insulaire
A côté de la composante exocrine, sont visibles, même à faible
grossissement, des amas de cellules épithéliales, de taille variables et
d’architecture trabéculaire : les îlots de Langerhans.
Ils représentent la composante endocrine du pancréas. Ils sont mis en
évidence par des techniques d’immunomarquage spécifiques des
différents peptides produits par ces cellules (insuline, glucagon,
somatostatine, PP).
Comme l’épithélium des canaux excréteurs du pancréas exocrine, les îlots
de Langerhans sont d’origine entoblastique. Les cellules des îlots de
Langerhans, sans canaux excréteurs, sont séparées par une trame
conjonctive fortement vascularisée : chaque cellule endocrine est en
contact avec un capillaire sanguin.
Dans les îlots de Langerhans, les cellules basophiles sont majoritaires,
surtout localisées en position centrale, et les cellules acidophiles sont
minoritaires et surtout périphériques.
Les cellules de ces îlots sont hormono-sécrétantes et élaborent l’insuline, le glucagon, la somatostatine
ainsi qu’un polypeptide pancréatique (PP).

12
Chacune de ces hormones est synthétisée par une population de cellule distincte :
Cellules Alpha (A)
- Acidophiles
- Périphériques
- Fonction : synthèse et excrétion de GLUCAGON (l’une des hormones hyperglycémiantes du corps
humain)
Cellules Beta (B) (majoritaires)
- Basophiles
- Centrales
- Fonction : synthèse et excrétion d’INSULINE (la seule hormone hypoglycémiante du corps
humain)
Cellules Delta (D) (ou cellules à somatostatine)
- Localisées entre les cellules Alpha et les cellules Beta
- Fonction : synthèse et excrétion de SOMATOSTATINE, dont le rôle n’est pas central mais qui
régule localement l’activité des cellules Alpha et Beta (régulation paracrine)
Cellules PP
- Très rares, sauf dans la face postérieure de la tête du pancréas (petit pancréas de Winslow) où les
îlots de Langerhans sont très riches en cellules PP => on parle de « lobe PP ».
- Fonction : synthèse du POLYPEPTIDE PANCREATIQUE (PP).
A proximité des îlots de Langerhans, on trouve des
formations de cellules nerveuses ganglionnaires. Ces
complexes neuro-insulaires ne s’articulent jamais avec les
noyaux des neurones des cellules endocrines : il n’y a jamais
de synapse neuro-glandulaire dans le pancréas (à la
différence de la médullosurrénale par exemple). La
régulation nerveuse se fait indirectement, par exemple par la
régulation du système vasculaire.

13
ii. Composante extra-insulaire Le pancréas endocrine comporte également une partie extra-
insulaire, avec des cellules endocrines dispersées dans le
parenchyme et qui peuvent être à l’origine de pathologies.
A noter aussi que la
lipomatose pancréatique est un exemple de pathologie du pancréas,
caractérisée par des infiltrations adipeuses qui ne sont, en principe,
pas caractéristiques du pancréas.
III. Foie et voies biliaires
A. Introduction
i. Vascularisation hepatique
Le foie comporte 4 circulations :
Circulation systémique (artere hepatique + veine sus-hepatique)
Circulation porte (le foie recoit la veine porte naissant derriere l’isthme du pancreas, et donne la
veine sus-hepatique)
Circulation biliaire (secretion biliaire exocrine)
Circulation lymphatique (l’essentiel de la lymphe provient du foie)
ii. Embryologie La composante épithéliale du foie provient du
diverticule hépatique (entoblaste, partie caudale de
l’intestin antérieur). L’ébauche hépatique se développe de
manière précoce dans le territoire du mésogastre
antérieur. Les hépatocytes s’organisent peu à peu en
travées, sur un réseau vasculaire complexe.

14
Cette coupe transversale à J48 montre que le foie occupe déjà une place importante dans l’abdomen ( la
quasi totalité).
Cette grande taille est due à une activité importante d’hématopoïèse au cours de la vie fœtale. Cette
activité disparaît avant la naissance, vers 32 SA.
Les voies de retour sanguins préférentielles depuis le placenta jusqu’au cœur vont s’organiser dans le
foie. Le ductus venosus va « court-circuiter » le foie.
iii. Macroanatomie Le foie est segmenté en 8 segments. (Remarque : les lobes sont numérotés dans le sens des aiguilles d’une
montre, comme les arrondissements parisiens !)
B. Microanatomie Le foie présente à sa surface une capsule, la capsule de Glisson, conjonctive qui n’envoie pas de fibre en
profondeur.
L’architecture conjonctive du foie est liée à la vascularisation qui va former un ensemble de systèmes
entourés de tissu conjonctif : les espaces portes.

15
Le tissu hépatique, d’aspect homogène/monotone à la base, présente en réalité :
- Une composante épithéliale, surtout : des travées d’hépatocytes, constituant le parenchyme
hépatique
- Une composante conjonctive comportant des vaisseaux : les espaces portes
i. Espaces portes
Au sein du tissu hépatique, on distingue des espaces portes, formations de tissu conjonctif constituées :
- d’une artère (branche de l’artère hépatique)
- d’une veine (branche terminale de la veine porte)
- d’un canal biliaire (canal excréteur, une rangée de cellules épithéliales bordant une lumière)
Les espaces portes se disposent généralement en hexagone, au milieu duquel se trouve une veine centro-
lobulaire dont la fonction est de ramener le sang hépatique vers la veine sus-hépatique.
ii. Parenchyme
Les hépatocytes, principales cellules du foie, sont organisées en travées, séparées par des vaisseaux
sanguins, au sein d’une trame conjonctive particulière (il n’y a pas de basale) extrêmement riche en fibres
de réticuline.
a) Unités Fonctionnelles Les hépatocytes s’organisent selon une architecture particulière. Plusieurs systématisations sont
possibles :
Lobule de Kiernan (Lobule hépatique)
Le lobule de Kiernan est l’unité fonctionnelle du foie telle qu’on l’a décrite en première année.Il s’agit
d’un hexagone, qui n’est pas délimité par une trame conjonctive avec :
- au sommet, les espaces portes (artère hépatique, canal biliaire et veine porte).
C’est l’afférence veineuse.
- au milieu, une veine centro-lobulaire, réseau de drainage du sang du lobule vers
la veine sus-hépatique. C’est l’efférence veineuse.

16
Il y a deux sens de circulation :
- le sang circule de manière centripète : o le sang de la veine porte et de l’artère hépatique se mêle
o il passe dans les capillaires sigmoïdes, tendus de la périphérie vers le centre
o pour atteindre la veine centro-lobulaire puis la VCI
- la bile circule de manière centrifuge :
o elle est synthétisée dans les travées d’hépatocytes
o rejoint les canaux biliaires des espaces portes
o pour pouvoir rejoindre le canal hépatique et in fine se jeter dans D2
Lobule biliaire de C. Sabourin Le lobule biliaire de C. Sabourin a une forme de triangle :
- aux sommets, trois veines centro-lobulaires
- au centre, un espace porte

17
Il y a deux sens de circulation :
- le sang circule de manière centrifuge:
o le sang de la veine porte et de l’artère hépatique se mêlent au niveau de l’espace porte
o il passe dans les capillaires sigmoïdes, tendus de l’espace porte vers les veines centro-lobulaires
o pour atteindre la veine centro-lobulaire puis la VCI
- la bile circule de manière centripète:
o elle est synthétisée dans les travées d’hépatocytes
o rejoint les canaux biliaires des espaces portes au centre du lobule
o pour pouvoir rejoindre le canal hépatique et in fine se jeter dans D2
Acinus hépatique de Rappaport
L’acinus de Rappaport a une forme de losange, dont deux
sommets sont des espaces portes (afférence du sang), et deux
sommets des veines centro-lobulaires (efférentes) vers lesquelles
le sang est drainé.
Le sang arrive dans la région centrale et est drainé vers la
périphérie.

18
On peut diviser le losange en trois zones d’activités fonctionnelles différentes :
- la zone 1, où le sang est le plus riche en dioxygène et en
facteurs métaboliques
- la zone 2, où c’est moins riche
- la zone 3, où c’est encore moins riche, près des veines centro
-lobulaires
L’architecture fonctionnelle du foie est donc très élaborée, et ces représentations sont juste des
représentations intellectuelles d’une seule et même chose : le parenchyme hépatique. On peut tout
simplement retenir que l’unité élémentaire du foie est l’hépatocyte et son organisation en travées.
Aujourd’hui, pour faire plus simple, on considère surtout l’unité microcirculatoire hépatique :
Unité microcirculatoire hépatique Il s’agit d’une formation à l’interface entre l’acinus hépatique de Rappaport et le lobule biliaire de
Sabourin. Elle comporte d’un côté un espace porte et de l’autre une veine centrolobulaire. Comme
précédemment, le sang hépatique est drainé vers la veine centrolobulaire, tandis que la bile est drainée
vers l’espace porte.
Ce ne sont que des conceptualisations d’une structure commune avec une afférence vasculaire dans les
espaces portes et une efférence au niveau des veines centro-lobulaires.

19
b) Description des hépatocytes Les hépatocytes, principales cellules du foie (ne se trouvent pas dans les espaces porte mais au centre
des unités microcirculatoires hépatiques), sont des cellules :
- épithéliales
- essentiellement basophiles
- aux limites cellulaires bien visibles et jointives les unes des
autres
- aux noyaux arrondis, vésiculeux, irréguliers, mononuclées mais
possédant parfois 2 ou 3 noyaux, présentant des inclusions de
glycogène
- de tailles irrégulières
- au cours du vieillissement, caractérisées par une anisocytose et des
dépôts de lipofuscine
Les hépatocytes sont entourés d’une trame conjonctive extrêmement fine,
avec des capillaires sinusoïdes discontinus et pas de membrane
basale.
L’hépatocyte présente trois territoires fonctionnels :
Un territoire basolatéral (70% de la surface des
hépatocytes) : faces latérales en contact avec les capillaires
sanguins sinusoïdes (discontinus)
Dans le territoire basolatéral on trouve de nombreuses
microvillosités qui permettent une multiplication par 6 de la surface
d’échange entre l’hépatocyte et l’espace de Disse.
Entre les hépatocytes et les capillaires sinusoïdes on trouve l’espace
de Disse (tissu conjonctif très particulier peu visible, quasi virtuel) :
o Ne possède pas de membrane basale
o Contient quelques fibres de réticuline (imprégnation
argentique au MO) on parle de trame « grillagée »
o Contient des cellules étoilées ou cellules d’ITO riches en :
- lipides
- vitamine A +++ (on les appelle aussi vitamin A storing cell)
- desmine (une protéine musculaire)

20
Au-delà de l’espace de Disse, on trouve des capillaires
sinusoïdes discontinus, présentant des fenêtres (fentes, trous) de
l’endothélium au travers desquelles on peut voir les
microvillosités des hépatocytes. Il n’y a presque rien entre les
hépatocytes et le sang : les échanges sont donc facilités.
Dans le revêtement endothélial des sinusoïdes, on peut voir des
cellules plus volumineuses avec quelques grains de phagocytose dans
le cytoplasme : les cellules de Kuppfer.
Les cellules de Kuppfer sont des cellules à activité phagocytaire du fer
dans certaines conditions. Un marquage par la réaction de Perls
montre en effet, en cas d’hémosidérose, quelques dépôts de fer
dans les cellules de Kuppfer.
Un territoire canaliculaire (15%)
Il y a un réseau de canalicules biliaires creusé individuellement dans les
hépatocytes.
Cet espace est bien délimité par des jonctions de différents types.
C’est un espace extracellulaire ou la bile va être excrétée selon un mode
exocrine.
La bile va être drainée le long du réseau dans l’épaisseur des
travées hépatiques vers les espaces portes.

21
Un territoire latéral (15%)
Ce territoire présente de nombreux complexes de jonctions qui
séparent les territoires latéraux et canaliculaires et des gap junctions
(jonctions communicantes) qui permettent les échanges entre les
cellules.
Ce schéma résume la structure des travées d’hépatocytes :
Remarque : il est inexact, en effet il aurait fallu laisser des trous entre les cellules endothéliales car les
capillaires sont sinusoïdes
Y sont illustrées la circulation artério-veineuse (avec les cellules endothéliales et les cellules de Kuppfer)
et la circulation biliaire (avec les canalicules biliaires). Dans les capillaires sinusoïdes voyagent des
hématies (déformables).
Pour passer à travers les capillaires, les cellules vont se
déformer. Elles vont ainsi transmettre de l’énergie sous
forme d’ «endomassage vasculaire » ce qui va être à
l’origine de flux liquidiens. Cela va notamment
permettre la circulation de la lymphe à l’intérieur du
parenchyme hépatique.

22
iii. Les espaces portes
Les espaces portes sont des formations conjonctives contenant les éléments de la vascularisation
hépatique :
- une branche artérielle : l’artère hépatique
- une banche veineuse : la veine porte
- un canal biliaire : les canalicules se drainent dans les canaux biliaires
- la circulation lymphatique : les vaisseaux lymphatiques
Le canal biliaire est toujours entouré d’une rangée de cellules hépatiques.
Les hépatocytes vivent environ 300 jours. Plusieurs théories ont été émises sur leur renouvellement.
Certains disent que c’est à partir des canaux biliaires et du système de transition avec les canaux biliaires,
que les hépatocytes sont remplacés au niveau des travées : c’est la « streaming theory ».
Il y a une bordure d’hépatocytes autour de chaque espace porte qui ne forme pas des travées
d’hépatocytes mais qui forme la lame bordante des espaces portes. La lame bordante est une
séparation fonctionnelle : d’un côté il y a les espaces portes et de l’autre côté on est dans le lobule
hépatique. Lors d’une hépatite, l’inflammation peut soit rester confinée à l’intérieure de l’espace porte,
soit dépasser la lame bordante, ce qui traduit un autre stade d’évolution de la pathologie, c’est dans ce
cas une barrière.
iv. Voies biliaires extra-hépatiques
La vésicule biliaire possède une paroi en trois
couches :
- muqueuse :
Celle-ci présente des franges, en surface on observe
un épithélium prismatique simple dont la partie
superficielle présente de petites vacuoles.
- musculeuse lisse
- adventice conjonctive
La fonction principale de la vésicule biliaire étant la sécrétion de la bile on observe des vacuoles d’eau qui
permettent de concentrer la bile.

23
FICHE RECAPITULATIVE
Les glandes salivaires principales (2 glandes sous-maxillaires + 2 glandes sublinguales+
glande parotide) La portion sécrétrice
Points communs : Ce sont des glandes : Exocrines, anatomiquement individualisées avec un canal excréteur. Elles sont lobulées. Et dans les lobules on a du parenchyme mais aussi des adipocytes.
Différences
Parotide Sublinguale Sous maxillaire
-SEREUSE PURE -Acini séreux arrondis ++ -Sécrète enzymes de la phase salivaire de la digestion (amylase salivaire)
-Glande MIXTE à prédominance MUQUEUSE
-Glande MIXTE à prédominance SEREUSE -Acini caractérisés par une polarité apico-basale
La portion excrétrice Points communs : Les canaux excréteurs annexés à ces unités donnent des canaux de plus en plus volumineux, qui eux-mêmes donneront le canal excréteur principal. Canaux excréteurs = 2 parties : 1 portion intra-lobulaire & 1 portion extra-lobulaire Principale fonction des canaux = récolter les produits de sécrétion et les transporter cavité buccale Particularités : les canaux sont striés éosinophiles sur la partie intra lobulaire et l’épithélium est stratifié au niveau extralobulaire.
Particularités : Dans les glandes salivaires principales on trouve d’autres composantes : Cellules sébacées/Cellules myoépithéliales / Oncocytes. Toutes ces cellules peuvent donner naissance à des tumeurs d’aspect assez variables.
Le pancréas (glande salivaire abdominale, anatomiquement individualisée, lobulée macroscopiquement, avec deux composantes : exocrine et endocrine) Pancréas exocrine (amylase
pancréatique) avec des canaux excréteurs intra et extra lobulaires
Pancréas endocrine aves les îlots de Langerhans
-Portion sécrétrice : Lobulation cunéiforme
-Portion excrétrice : canaux excréteurs s’anastomosent jusqu’à former le canal pancréatique principal de Wirsung
-L’épithélium des canaux excréteurs de
pancréas n’est jamais stratifié !
Composante insulaire : amas de cellules épithéliales de tailles variables, d’architecture trabéculaire : Les îlots de Langerhans
4 populations cellulaires principales: -Cellules Alpha (A) (15 à 20%) périphériques -Cellules Beta (B) (80%) centrales -Cellules intermédiaires Delta (D) (5%) -Cellules PP (très rares)
Composante extra-insulaire : Cellules

24
endocrines dispersées dans le parenchyme et qui peuvent être à l’origine de pathologies
Foie et voies biliaires
Vascularisation hépatique : circulation systémique + circulation porte + circulation biliaire +
circulation lymphatique
Microanatomie Espaces portes : une artère + une veine + un canal biliaire Parenchyme : Les hépatocytes, principales cellules du foie, sont organisées en travées, séparées par des vaisseaux sanguins, au sein d’une trame conjonctive particulière (il n’y a pas de basale) extrêmement riche en fibres de réticuline.
Unité microcirculatoire hépatique
Les hépatocytes sont des cellules :
- Epithéliales
- Essentiellement basophiles
- Aux limites cellulaires bien visibles et jointives les unes des autres
- Aux noyaux arrondis, vésiculeux, nucléoles, visibles ++, mononuclées mais parfois 2 ou 3
noyaux, présentant des inclusions de glycogène (marquage au PAS)
- De tailles irrégulières
- Vieillissement : anisocytose + anisocaryose physiologique + dépôts de lipofuscine
- Entourées d’une trame conjonctive extrêmement fine, avec des capillaires sinusoïdes discontinus et pas de membrane basale
3 territoires fonctionnels : territoire basolatéral (70% de la surface des hépatocytes-
microvillosités ++ & entre hépatocytes et capillaires : espace de Disse. Dans le revêtement endothélial des sinusoides : les cellules de Kuppfer) + territoire canaliculaire (15%) + territoire latéral (15%)
Les espaces portes : Formations conjonctives contenant les éléments de la vascularisation hépatique. Ils sont entourés par une lame bordante : travée d’hépatocytes. Voies biliaires extra hépatiques : Cholédoque, canal cystique, vésicule : ont une structure de tube avec une lumière et une paroi de type digestif, mais en trois couches : muqueuse / musculeuse lisse / adventice. La vésicule biliaire a une fonction de concentration de la bile, elle absorbe l’eau afin de concentrer la bile.

25
Plan :
I. Indications et modalités d’imagerie A. Indications B. Modalités d’imagerie
i. Echographie ii. Scanner TDM iii. IRM iv. Opacifications directes
C... Segmentation du foie
II. Sémiologie radiologique des voies biliaires A.. Echographie
i. Voies biliaires intra-hépatiques ii. Voie biliaire principale iii. Vésicule biliaire
B.. Scanner C. IRM D. Opacifications directes
III. Sémiologie radiologique du foie A. Echographiehie B. .Pathologies hépatiques
i. Cirrhose ii. Lésions et tumeurs
Abréviations : IV : intra veineuse
PA : phase artérielle
PP : phase portale
PT : phase tardive
UE6 – SD Sémiologie – n°5 17/01/17
Pr. Paul LEGMANN [email protected]
RT : Fanny Delaigue
RL : Alizée Verdon
Sémiologie radiologique du foie et des voies
biliaires

26
I. Indications et modalités d’imagerie
A. Indications
Examen systématique (« check up »), bilan d’un cancer déjà connu (bilan d’extension du cancer)
Syndrome douloureux abdominal Masse, Ictère, fièvre persistante Altération de l’état général (amaigrissement) Altération du bilan biologique hépatique et/ou pancréatique
B. Modalités d’imagerie
i. Echographie
1er
examen généralement
non invasif
être à jeun depuis 12h
permet l’exploration de :
o la vésicule biliaire
o les voies biliaires
o le parenchyme hépatique o les vaisseaux (doppler couleur : étude de la vitesse des globules rouges dans les
structures vasculaires)
étude pancréatique, splénique : recherche d’adénopathie, de masse
étude de la cavité abdominale, recherche d’épanchement dans le péritoine (intra péritonéal)
Coupe sur le foie gauche au niveau du dôme hépatique
Estomac échogène

27
ii. Scanner : TDM à rayon X mode hélicoïdal
C’est une acquisition volumique et continue, on demande au patient de faire une apnée de quelques secondes.
On étudie :
Les parenchymes (foie, pancréas)
Les vaisseaux (produit de contraste iodé : artère hépatique, veine porte, parenchyme, voies biliaires => Méthode invasive)
Le tube digestif (plus visible qu’à l’échographie)
La cavité abdominale
Le pelvis, rétro péritoine
Les liquides sont hypodenses (gris foncé) alors que les calculs sont hyperdenses. Les
foies et la rate sont isodenses : ils ont un même niveau de gris.

28
iii. IRM : imagerie à résonance magnétique Cette technique permet d’étudier des tissus riches en protons H. Il ne s’agit plus de rayons X comme le
scanner.
On aligne les ions H+ dans un champ magnétique et on envoie par des bobines de gradient des ondes
de radiofréquence qui vont modifier l’agencement géométrique des ions H+ et on va mesurer leur
retour à la phase d’équilibre et de stabilité. C’est une fois les ions H+ revenus à la phase de stabilité que
le signal est déclenché.
L’IRM permet d’étudier :
- Le foie - La vésicule biliaire - Les vaisseaux (par injection de gadolinium)

29
Pondération T1 Pondération T2
Liquide hypointense : noir Liquide hyperintense : blanc
On peut aussi faire une IRM avec une IV : on n’utilise pas de l’iode mais du chélate de
gadolinium, très peu allergisant.
Le scanner se fonde sur l’utilisation d’une échelle de gris pour distinguer les différentes
structures. L’IRM utilise les contrastes et est ainsi plus précise que le scanner.
Les séquences de Biliwirsungo-IRM accentuent le signal des liquides NON-circulants,
réduisant ainsi les autres signaux.
iv. Opacifications directes : injection de produit de contraste
On injecte du produit de contraste directement dans les voies biliaires : - Par voie rétrograde : par le duodénum et le canal cholédoque - Par voie directe : à travers le foie (transhépatique)

30
C. Segmentation du foie, la segmentation de Couinaud
Le foie se découpe en 8 segments qui se regroupent au niveau de 4 secteurs :
⋆ Secteur latéral gauche (SLG): seg. 2 et 3
⋆ Secteur paramédian gauche (SPMG) : seg. 4a et 4b ⋆ Secteur paramédian droit (SPMD) : seg. 5 et 8 ⋆ Secteur postérieur et latéral droit (SLD): seg. 6 et 7
Un secteur donne deux segments. Le segment 1 se trouve en arrière, au contact de la VCI.
Les veines portes sont intra-segmentaires : chaque branche de division va irriguer un secteur. Les veines hépatiques sont extra-segmentaires : - La V hépatique gauche sépare le SLG et le SPMG - La V médiane sépare le SPMG et le SPMD - La V hépatique droite sépare le SPMD et le SLD
Les voies biliaires suivent également cette distribution intra-segmentaire.
II. Sémiologie radiologique des voies biliaires
L’imagerie permet de : _ Détecter une pathologie
_ Préciser son siège :
Voies biliaires intra-hépatiques
Confluent biliaire supérieur : hile hépatique
Voies biliaires extra-hépatiques
A. Echographie
L’échographie est la procédure initiale pour évaluer les voies biliaires et la vésicule car : - Elle permet l’exploration de toute la cavité abdominale. - Elle est non invasive, non irradiante et peut se faire au lit du patient. - Elle n’est pas chère. - Le diagnostic de la lithiase vésiculaire est très sensible et très spécifique (Voie
biliaire principale < vésicule biliaire). - On peut la coupler au Doppler pour étudier les vaisseaux sanguins adjacents.
Les seuls inconvénients sont qu’elle est opérateur dépendant et que le patient doit être à jeun depuis 12h.

31
Anomalie Lésion
Foie Diffuse ou localisée
Unique ou multiple
Hypo échogène (noir)
Hyper échogène (blanc) Mixte Anéchogène (sans écho)
Hétérogène
Homogène
Voies biliaires
Visibles ? Dilatation, obstacle à l’évacuation du produit en aval :
sténose. Ou obstacle dans la lumière du canal correspondant à
un calcul, une tumeur qui amène une dilatation au-dessus.
On parle d’obstacle endo ou exoluminal.
i. Les voies biliaires intra-hépatiques
Normales Anomalies Aspects pathologiques Voies biliaires
intra hépatiques
Fines
Non visibles
Calibre (dilatation ?)
Contenu
paroi
Dilatation
Sténose
Irrégularités Contenu
échogène

32
ii. Les voies biliaires extra-hépatiques sous le confluent biliaire (canal hépatique commun et canal cholédoque)
Rappel :
Les deux portions de la voie biliaire principale (a,b) se
rejoignent au niveau du confluent biliaire supérieur (c)
et donnent le canal hépatique commun (d). La vésicule
biliaire se jette par le canal cystique (f) dans le canal
hépatique commun pour ensuite former le canal
cholédoque (h).
Normale Pathologiq
ue Voie biliaire principale Fine et visible
Diamètre ≤ 6mm
Augmentation physiologique
Diamètre > 8mm
Pour repérer la voie biliaire principale, d’arrière en avant on a : - Veine cave - Veine porte - Voie biliaire principale

33
i. La vésicule biliaire
Exploration échographique
Examen en décubitus dorsal
Vésicule orthotopique, rebord costal inférieur
Décubitus latéral gauche, inspiration profonde bloquée
Coupes intercostales latérales antérieures ou postérieures
Patient assis
Normal
e Anomalie
s Vésicule biliaire Piriforme, ovalaire, allongée
Taille : 5-8cm
Epaisseur pariétale ≤ 3 mm
- Si épaisseur pariétale > 3 mm cholécystite
- Si lithiase (calcul) + épaississement pariétal
cholécystite aiguë lithiasique (signe de Murphy : douleur au passage de la sonde)
Calcul : formation hyperéchogène avec cône d’ombre
acoustique postérieur (les échos ont été arrêtés par
une structure dense, calcifiée)
B- Scanner
Il permet de détecter des anomalies comme les calculs (sur les images ci-dessous, on descend le long des canaux biliaires) :
Voies biliaires intra-hépatiques dilatées
Voie biliaire principale très dilatée
Calcul en distal
Le calcul sur le troisième scanner est responsable de la dilatation des voies biliaires extra et intra hépatiques.
Il permet également de détecter des cancers comme celui de la tête du pancréas.

34
En effet, la tumeur va comprimer les voies biliaires extra-hépatiques entrainant une dilatation des voies biliaires situées au-dessus de la sténose. C’est donc une sténose exoluminale extrinsèque.
C- IRM
On peut appliquer une bili-IRM (ou cholangio-IRM), fortement pondérée en T2 : tout ce qui est liquidien est en hypersignal. On privilégie ainsi les voies biliaires qui sont en signal hyperintense alors que la lacune (qui représente l’obstacle) est en signal hypointense.
Normal Voie biliaires intraH dilatées
Sténose ss-hilaire Cholédocholithiase
L’IRM permet de détecter de petits calculs qui ne seraient pas visibles à l’échographie ou au scanner.
D- Opacifications directes
Conclusion : Imagerie dans l ’exploration des voies biliaires :
1) Échographique : 1er examen : vésicule et voies biliaires
2) TDM : étude de la cavité abdominale
Pathologie bilio-pancréatique : lithiase, adénopathie, cancer du pancréas.
3) Complément par cholangio-IRM : Visualiser lumière des voies biliaires, pathologie endoluminale, lithiase, tumeur
III. Sémiologie radiologique du foie

35
Caractéristique de la pathologie
Exemple
Diffuse Stéatose (infiltration de graisse) Fibrose (cirrhose à cause de l’alcool ou virus B-C)
Focale Tumeur (maligne ou bénigne)
A. Pathologies hépatiques
i. Cirrhose
- Hépatomégalie - Splénomégalie - Ascite - Dérivations veineuses : la veine porte est bloquée par l’augmentation de taille du foie, des voies
dérivatives se mettent donc en place pour compenser. On parle de « shunt porto-systémique ». - Foie hyperéchogène - Etude de l’hypertension portale - Recherche de nodules - Risque : développement du carcinome hépatocellulaire (CHC)
Lésions et tumeurs
- Lésions bénignes :
Echographie Scanner IRM
Kystes Fréquent
- Anéchogène avec un renfort postérieur (accélération des échos à la sortie du kyste)
- Paroi fine
- Hypodense (liquide) - Sans imprégnation de
contraste (avasculaire)
- Kyste biliaire lésion arrondie
- Homogène T1 hypo-intense T2 hyper-intense Après IV aucun remplissage

36
Angiomes + fréquente
- Hyperéchogène, homogène
- <3cm, capsulaire - Localisation à
propos d’une structure veineuse
- De préférence dans foie droit
- Opacification de la périphérie vers le centre en aspect de motte (des petits nodules apparaissent), remplissage centripète dit globulaire
- Lésion hyperdense à 3mn de l’injection
T1 : hypointense T2 : hyper-intense - Remplissage
centripète discontinu
(avec injection de gadolinium) voir si angiome atypique, risque de malignité
Abcès
- Tumeur hépatique bénigne
Echographie TDM IRM
Hyperplasie nodulaire focale (HNF)
Lésion bien limitée sans capsule
Homogène
Iso intense en T1 et T2
même signal que le foie
Hyper vascularisation au temps artériel
Cicatrice centrale : Pondération T2 : Hypo-intense sans injection Hyper-intense en phase tardive
Adénome Lésion encapsulée
Pas de cicatrice centrale
Hétérogène
Transformation maligne
Fortement hypervasculaire
Hypervascularisation à la phase artérielle : pas de cicatrice
Phase portale ; iso-dense
- Tumeur maligne primitive
Tumeur sur cirrhose : Hépatocarcinome se développe suite à des remaniements architecturaux et développement de nodules sur cirrhose. Des nodules de régénération bénins sont susceptibles d’évoluer vers des nodules dysplasiques ou des carcinomes hépatocellulaires.
Echographie TDM IRM

37
Carcinome hépatocellulaire
Avant injection : Hypo ou isodense
Après injection : Phase artérielle hyperdense
Phase portale : hypo ou isodense
Phase tardive : hypodense
Lavage : « wash-in »/« wash-out »
Hétérogène T2 :
modérément hyper intense
T1 : hypo intense
Capsule apparaità la phase tardive
- Tumeur maligne secondaire : lésions les plus fréquentes du foie :
La métastase provient d’une lésion primitive cancéreuse (recto-colon, seins, poumons, pancréas, estomac).
Echographie TDM IRM
Métastase Très fréquente
Modérément hypo-iso-échogène avec un halo hypoéchogène circonférentiel
Hétérogène
Hypodense
Couronne hyperdense
T1 :
hypointense après IV
Couronne hypervasculaire
T2 :
hyperintense
hétérogène
Halo hyperintense
B. Pathologies hépatiques en imagerie
Echographie TD
M IRM Kyste

38
Angiome Angiome
HNF
HNF
Cicatrice centrale
Adénome
CHC
HyperV phase
isodense portale artérielle
PA
PP Couronne
hypoéchogène PA
PT

39
Métastase
couronne hypervasculaire
halo hyperintense
Mot du RT : Pour ce cours il faut absolument savoir la segmentation du foie. A noter aussi : calcul = lithiase et lésion bénigne = tumeur bénigne. Une femme chez le chirurgien esthétique : - J'aimerais avoir de plus gros seins. Combien cela me coûterait-il ? L'homme de l'art : - Cela coûterait environ 50 000 frs. La femme : - Je ne peux pas me le permettre... N'y a-t-il pas une alternative à la chirurgie ? Le docteur essayant d'être aimable : - Vous pourriez essayer de vous frotter les seins avec du papier toilette... La femme : - Du papier toilette ??? Comment cela pourrait-il me rendre les seins plus gros ? Le docteur : - Regardez ce que cela a réussi à faire à votre postérieur...

40
FICHE RECAPITULATIVE
Indications et modalités en imagerie :
Indications : Examen systématique, bilan d’un cancer connu, syndrome douloureux abdominal, masse, ictère, fièvre persistante, altération de l’état général, du bilan biologique hépatique et/ou pancréatique.
Modalités :
Echographie : 1er
examen, non invasif ; à jeun ; exploration de la vésicule et des voies biliaires, du parenchyme hépatique, des vaisseaux ; étude pancréatique, splénique, de la cavité abdominale.
Scanner : Parenchymes, vaisseaux, tube digestif, cavité abdominale, pelvis, rétro péritoine.
IRM : Foie, vésicule biliaire, vaisseaux. Utilisation des contrastes, méthode plus précise que le scanner.
Segmentation du foie :
8 segments au niveau de 4 secteurs : SLG (2 et 3), SPMG (4a et 4b), SPMD (5 et 8), SLD (6 et 7). Segment 1 en arrière au contact de la VCI
Veines portes intra-segmentaires (une branche pour un secteur), veines hépatiques extra-segmentaires.
Sémiologie radiologique des voies biliaires :
Echographie :
Voies biliaires intra-hépatiques :
Normales Anomalies Aspects pathologiques
Voies biliaires intra hépatiques
Fines
Non visibles
Calibre (dilatation ?)
Contenu paroi
Dilatation
Sténose
Irrégularités
Contenu échogène
Voies biliaires extra-hépatiques :
Normale Pathologique
Voie biliaire principale Fine et visible
Diamètre ≤ 6mm
Augmentation physiologique
Diamètre > 8mm

41
Vésicule biliaire :
Normale Anomalies
Vésicule biliaire
Piriforme, ovalaire, allongée
Taille : 5-8cm
Epaisseur ≤ 3 mm
- Si épaisseur > 3 mm cholécystite
- Si lithiase (calcul) + épaississement pariétal cholécystite aiguë lithiasique (signe de Murphy : douleur au passage de la sonde)
- Scanner :
Voies biliaires intra- hépatiques dilatées
VoB principale très dilatée Calcul en distal
- IRM :
Utile pour les petits calculs non visibles à l’échographie ou au scanner.
Sémiologie radiologique du foie :
Cirrhose : Hépatomégalie, splénomégalie, ascite, dérivations veineuses, foie hyperéchogène.
Lésions et tumeurs : - Lésions bénignes : Kystes (fréquent), angiome (+ fréquents), abcès - Tumeurs hépatiques bénignes : Hyperplasie nodulaire focale (HNF), adénome - Tumeur maligne primitive : tumeur sur cirrhose = carcinome hépatocellulaire - Tumeur maligne secondaire (lésions les plus fréquentes) : métastase
Normal Voie biliaires intraH dilatées
Sténose ss-hilaire Cholédocholithiase

42

43
UE6 – SD – Sémiologie - n° 6
19/01/2017
Pr Philipe Sogni
RT : Maxence Delaporte
RL : Léa Vieilledent
Sémiologie et explorations du foie et des voies biliaires
Plan :
Introduction
I. Les grands syndromes de la pathologie hépatique A. Cholestase B. Cytolyse C. Insuffisance hépato-cellulaire D. Hypertension portale
II. Ascite
III. Ictère
IV. Sémiologie biliaire
A. Lithiase Biliaire B. Colique hépatique C. Cholécystite aigüe D. Migration lithiasique
Abréviations : Aspartate AminoTransférase (ASAT) Alanine AminoTransférase (ALAT) Taux de Prothrombine (TP) Hypertension Portale (HP)

44
Introduction
En hépatologie, la démarche diagnostique est simple et repose sur peu d’examens sémiologiques et peu
d’examens biologiques : un minimum de moyens pour un maximum de résultats. L’essentiel est
d’effectuer un interrogatoire complet et un examen clinique ciblé, (Cf stages de sémio) complétés par un bilan biologique hépatique standard :
- Taux de Prothrombine (TP)
- Albuminémie
- Transaminases (ALAT, ASAT)
- GammaGT
- Phosphatases alcalines
- Bilirubine (Totale et conjuguée)
- NFS plaquettes
L'imagerie est aussi utilisée (écho, scanner, IRM, etc..). On utilise en priorité l’échographie qui est simple
et facile à obtenir en urgence, mais qui est opérateur dépendant.
I. Les grands syndromes de la pathologie hépatique
A. Cholestase
Définition : diminution de la sécrétion biliaire.
Il existe 2 types de cholestase :
- Extra-hépatique : due en général à l’obstruction des voies biliaires extra-hépatiques.
- Intra-hépatique : due à une atteinte/défaut de la sécrétion de bile par les hépatocytes ou due à
l’obstruction des voies biliaires intra-hépatiques.
Le bilan biologique hépatique montre :
- Augmentation des phosphatases alcalines (rapport ALAT/Phosphatases Alcalines < 2).
- Augmentation des GammaGT.
- Augmentation ou non du taux de bilirubine totale (=bilirubine conjuguée +bilirubine non
conjuguée) avec une augmentation ou non du taux de bilirubine conjuguée.
A l’échographie, on peut remarquer une dilatation des voies biliaires en cas d’obstruction mais pas
nécessairement.
Remarque : On retrouve une augmentation isolée des phosphatases alcalines dans diverses situations
physiologiques et pathologiques telles que les pathologies osseuses (maladie de Paget, tumeurs osseuses),
mais aussi lors de la croissance osseuse physiologique des adolescents, ainsi que la grossesse chez la femme
(via le placenta). Les GammaGT sont habituellement normales dans ces situations.
Les conséquences d’une cholestase sont en général :
- Une diminution voire une abolition de la sécrétion biliaire.
- Un ictère par accumulation de bile pouvant être constant ou intermittent selon la fréquence de
l’obstruction des canaux biliaires. L’ictère apparait d’abord au niveau des conjonctives, puis au
niveau de la peau.
- Un défaut d’acides biliaires au niveau du tube digestif à l’origine d’une malabsorption des
graisses et des vitamines liposolubles : A, D, E, K et de diarrhées.

45
- Un prurit (dépôts de bilirubine au niveau des nocicepteurs cutanés)
B. Cytolyse
Définition : Augmentation des transaminases ALAT et ASAT avec le rapport ALAT / Ph Alc > 5.
Remarque : On peut retrouver une augmentation des transaminases d'origine non hépato-biliaire. Elle peut
être d'origine musculaire après un effort physique notamment (concerne les muscles striés et le myocarde
principalement) avec une prédominance des ASAT. Le reste du bilan hépatique est normal.
Macro-ASAT : ASAT augmentent, le reste est normal.
Démarche diagnostique :
- Déterminer l’origine hépatique de la cytolyse.
- Déterminer le caractère aiguë (<6 mois) ou chronique (>6 mois) de l’affection.
- Y a-t-il une insuffisance hépato cellulaire ? (signe de gravité)
- Rechercher les étiologies possibles : nombreuses mais principalement virus, toxiques et
médicaments (plus rarement maladies auto-immunes ou maladies rares).
C. Insuffisance Hépato-Cellulaire (la partie la plus importante du cours)
Définition : défaut/insuffisance de fonctionnement du foie, notamment au niveau de ses fonctions de
synthèse, de transformation, de détoxification (épuration) et de ses fonctions biliaires.
Aiguë ou chronique, l’IHC conduit à une baisse du taux de Prothrombine et du facteur V.
Une IHC fulminante est définie par un TP<50% accompagné d’une encéphalopathie hépatique et dont le
délai d’apparition est inférieur à 15 jours.
Une IHC sub-fulminante apparait après un délai supérieur à 15 jours.
Remarque : Le taux de Prothrombine (TP) est un reflet de l’hémostase et donc de la fonction hépatocytaire.
Lorsque le taux de prothrombine est inférieur à 50% de la norme on parle d’IHC sévère.
Signes Cliniques : (à savoir+++)
Signes majeurs :
Encéphalopathie (astérixis)
Angiomes stellaires
Diminution du Taux de Prothrombine
Diminution du facteur V
Diminution de l’albuminémie (par défaut de synthèse)
Signes non spécifiques
Asthénie
Ictère
Foetor hépaticus (odeur spécifique des patients atteints d'IHC)
Syndrome hémorragique (par diminution de la coagulation)
Sepsis (infections car patients souvent immunodéprimés)

46
Erythrose palmaire
Hippocratisme digital
Aménorrhée chez la femme / Hypogonadisme chez l’homme
Hypoglycémies
Dans l’IHC Aiguë, on retrouve les signes qui arrivent rapidement : encéphalopathie et baisse du TP et du
facteur V.
Dans l’IHC Chronique on aura les mêmes signes : encéphalopathie, baisse
du TP et du facteur V et ceux arrivant plus lentement : angiomes stellaires et hypo-albuminémie.
L’encéphalopathie hépatique évolue en 3 stades :
- Stade 1 : inversion du rythme nycthéméral, le patient dort le jour
et est réveillé la nuit (il ne faut pas lui prescrire de psychotropes, du fait de l’hépatotoxicité). Et
astérixis ou flapping : (bras et mains tendues devant soit, doigts écartés, yeux fermés pendant 30
secondes) mouvement en battement d’aile en deux temps, perte du tonus rapide des muscles
extenseurs de la main et correction lente.
- Stade 2 : confusion.
- Stade 3 : troubles de la vigilance voire coma.
Angiome stellaire :
On les retrouve au niveau de la face et de la partie supérieure du tronc et du dos.
Artériole centrale d’où irradient des petits vaisseaux en forme d’étoile.
Disparait à l’appui puis se remplit à partir du centre (vitropression), parfois pulsatile. Ils sont liés à des troubles endocriniens.
On considère que le patient doit présenter au moins 5 angiomes
stellaires pour que ce soit un signe clinique d’IHC.
Remarque : la grossesse peut entrainer l’apparition d’angiomes stellaires.
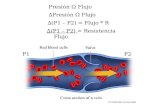
Prothrombine et coagulation :
La thromboplastine tissulaire, après une
cascade de réactions avec les facteurs VII, X et V,
permet la conversion de la prothrombine
(facteur II) en thrombine, responsable de la
conversion du fibrinogène (facteur I) en fibrine,
protéine insoluble qui conduit à la formation d'un caillot.
Lors d'un déficit en vitamine K, on observe une
baisse des facteurs dépendants de la
vitamine K (facteurs II, VII et X), ce qui
provoque une chute du taux de thrombine qui
entraine une chute du taux de fibrine et donc un défaut de coagulation.
Le facteur V ou proaccélérine est indépendant de la vitamine K.

47
Lors d'une IHC, on observe une baisse de tous les facteurs (y compris le facteur V) ce qui conduit à un
défaut de coagulation.
On différencie donc un déficit en vitamine K, notamment lors d’une cholestase où il y a malabsorption des
vitamines liposolubles dont la vitamine K, d'une IHC en regardant le taux de facteur V. Lors d'un déficit en vitamine K, celui-ci reste à un niveau normal, tandis que lors d'une IHC, celui-ci est abaissé.
D. Hypertension portale
Définition : Augmentation de la pression Porte d’au moins 15 mmHg.
Cette mesure est difficile à réaliser, on utilise donc le
gradient de pression hépatique : la différence entre
la veine Porte et les veines hépatiques. On parle
d’hypertension portale s’il y a une augmentation de plus de 5mmHg de ce gradient.
Il existe 3 types anatomiques (3 causes) d’HTP :
- Infra-hépatique : En amont du capillaire
sinusoïde, la veine porte est bloquée
(gradient normal).
- Intra-hépatique (souvent dû à une
cirrhose) : le gradient augmente. - Supra-hépatique : qui peut être dû à une
thrombose des veines sus-hépatiques. Le
gradient est normal. Présente lors d’une
insuffisance cardiaque droite.
Signes cliniques :
- L'ascite (=liquide dans la cavité péritonéale).
- L’œdème des membres inférieurs.
- Une splénomégalie (car la veine splénique se gorge de sang) qui induit de l'hypersplénisme
(=hyperactivité de la rate), responsable des anomalies du bilan biologique : séquestration des
plaquettes et des leucocytes au sein de la rate et donc diminution du nombre de plaquettes
(=thrombopénie) et de leucocytes (=leucopénie) dans le sang.
- Une circulation veineuse collatérale porto-cave : shunt visible à l’œil nu, paramédian,
ombilico xyphoïdienne, ascendante (en appuyant, le sang doit être bloqué et en relâchant
réapparaitre en se dirigeant vers la tête).
La cirrhose provoque le développement d’une fibrose (foie dur) et ainsi une augmentation des
résistances vasculaires intra-hépatiques et une augmentation de la tension portale.
L'organisme réagit dans le but de diminuer l'HTP en créant des voies de dérivations sanguines, appelées
shunts porto-systémiques : les toxiques ne passent plus par le foie, mais vont directement dans la veine
cave.

48
Par exemple, les varices œsophagiennes qui sont liées à la réouverture de veines embryonnaires suite
à la redistribution vasculaire. Elles sont caractéristiques de l’HTP et gonflent selon les lois physiques de Laplace.
L'organisme réagit aussi en produisant des médiateurs comme le monoxyde d'azote NO, ce qui induit une
vasodilatation artérielle, et par baroreflexe (Cf T1) une augmentation du débit cardiaque ainsi
qu'une hypervolémie relative. C'est le syndrome hyperkinétique. L'hypervolémie entraîne une augmentation du flux et donc augmente le phénomène d’HTP.
Il y a ensuite activation neuro-hormonale en réponse à cette augmentation de pression et sécrétion d’endothéline, de catécholamines, arginine-vasopressine.
En moyenne l’HTP tend à augmenter chez le cirrhotique.
Le diagnostic clinique de cirrhose se fait à la palpation : le bord inférieur du foie est dur voire tranchant.
Selon l'étiologie on retrouve une cytolyse, une cholestase ou les deux. Il est possible d’avoir un bilan
hépatique normal (pas de TP bas et de bilirubine haute).
II. Ascite
Définition : accumulation de liquide dans la cavité péritonéale.
Signes cliniques : matité déclive des flancs à la
percussion, signe du flot. Confirmation du diagnostic à
l’échographie (épanchement).
Les diagnostics différentiels de l’ascite sont : la
grossesse, le globe vésical, les kystes ovariens, une
masse abdominale.
Le diagnostic d’ascite est difficile lorsque l’épanchement est de faible volume.
Il existe 2 types d’ascite :
- Ascite transsudative : faible taux de protéines (< 30g /l). On les retrouve majoritairement en cas
de cirrhose non compliquée.
- Ascite exsudative : taux élevé de protéine (>30g/l) avec des étiologies variées : cancer (avec
extension péritonéale), infection BK, trouble cardiaque, inflammatoire (réaction à la pancréatite).
La ponction d’ascite se fait stérilement, au lit du patient en pleine matité, toujours en fosse iliaque
gauche (car le colon est plus mobile à gauche) sur la ligne virtuelle entre l’ombilic et l’épine iliaque antérosupérieure à la jonction 2/3-1/3.
On récupère le liquide pour confirmer le diagnostic d’ascite.
Souvent les patients atteints d’ascite présentent une hernie ombilicale « en tête de méduse », un
syndrome de Cruveilhier-Baumgarten et on peut remarquer un réseau veineux ascendant bleuté péri-
ombilical : c’est la circulation collatérale porto-cave. A distinguer de la circulation des flancs (thrombose de la veine cave).

49
III. Ictère
Définition : coloration jaune de la peau et des muqueuses en raison d'une accumulation de bilirubine (conjuguée ou non conjuguée).
La bilirubine est un pigment qui est issu de la dégradation des globules rouges. Lors de l'hémolyse, la bilirubine est relarguée dans le sang sous forme libre = forme indirecte, donc sous forme non conjuguée.
Lorsque la bilirubine libre passe dans le foie, elle subit une réaction de glucurono-conjugaison avec la
glucuronyltransférase : c'est la forme conjuguée de la bilirubine, qui lui permet ensuite d'être sécrétée puis excrétée dans la bile au niveau du tube digestif.
Il existe deux types d’ictère :
- Ictère à bilirubine non-conjuguée : Dû à une hémolyse trop importante (thalassémies) ou à une
anomalie de la conjugaison. Les signes cliniques et biologiques sont un ictère, des urines de
couleur normale, des selles de couleur normale et une hyperbilirubinémie à prédominance
non-conjuguée. Chez le nouveau-né il y a un risque de passage de la barrière hémato-
encéphalique à l’origine de complications neurologique.
- Ictère à bilirubine conjuguée : Trouble de la sécrétion et de l’excrétion. Les signes cliniques et
biologiques sont un ictère, des urines foncées, des selles décolorées et une hyperbilirubinémie
à prédominance conjuguée. Il y a un défaut de sécrétion de la bile (= cholestase) on retrouve
donc : malabsorption des lipides, des diarrhées chroniques (stéatorrhée) et une malabsorption
des vitamines liposolubles (A, D, E, K).
IV. Sémiologie Biliaire
A. Lithiase Biliaire
Définition : Formation des calculs biliaires.
C’est une pathologie fréquente : elle touche 20% de la population. Dans 80% des cas elle est asymptomatique. 20% des patients présentent des complications à 20 ans.
On distingue plusieurs types de calculs :
- Les calculs cholestéroliques (en grande majorité : 80%) : par stagnation de la bile.
- Les calculs pigmentaires parmi lesquels on retrouve les calculs noirs liés à l’hémolyse chronique
et les calculs bruns liés à une infection ou une malformation.
La formation de calculs biliaires a lieu le plus souvent dans la vésicule biliaire.
Plusieurs facteurs influencent la formation de calculs :
- Age, prédisposition familiale, sexe (F>H), ethnie.
- Alimentation, obésité, dyslipidémie (fibrates).
- Grossesse, contraceptifs, oestrogénothérapie (les œstrogènes réduisent la mobilité vésiculaire)
- Malabsorption des acides biliaires. Différentes complications sont possibles :
- La colique hépatique.
- La cholécystite aigüe : due à une obstruction du canal cystique.
- La migration lithiasique.

50
B. Colique hépatique
Définition : douleur aiguë d’origine biliaire, liée à la présence d’un calcul vésiculaire.
Signes cliniques : Douleur localisée dans l’hypochondre
droit, irradiant en hémi-ceinture et vers l’omoplate droite. Le
plus souvent en situation postprandiale, la douleur est
marquée par un début brutal et une durée plutôt longue
(plusieurs heures). Et une inhibition de l’inspiration
profonde par contraction des muscles de manière localisée
(signe de Murphy).
La colique hépatique ne s’accompagne PAS de fière, de
syndrome septique ou d’ictère. La présence de ces signes permet d’éliminer le diagnostic de colique hépatique.
Signes Biologiques : Bilan hépatique sub-normal, lipasémie normale.
Signes visibles à l’échographie :
- Lithiase vésiculaire (typique dans 80% des cas : images hyper-échogènes, arrondies, mobiles,
déclives, avec cône d’ombre postérieur).
- Signe de Murphy échographique (au passage de la sonde).
- Paroi vésiculaire normale.
A l’échographie (Cf image) on a une image hyper-échogène, mobile, avec un cône d’ombre postérieur.
(Absence d’épaississement de la paroi vésiculaire)
C. Cholécystite aiguë
Définition : inflammation de la vésicule biliaire, le plus souvent suite à un calcul dans le canal cystique. Elle s'accompagne d'une douleur (la même que pour la colique hépatique) et de fièvre.
On retrouve des signes cliniques et biologiques de sepsis.
Signes à l’échographie :
- Lithiase vésiculaire.
- Épaississement de la paroi
(dédoublement) (> 3 mm).
- Vésicule sous tension, signe de Murphy.
- Pas de dilatation des voies biliaires
intra-hépatiques et extra-hépatiques.

51
D. Migration lithiasique
Définition : Lithiase de la voie biliaire principale après migration du calcul.
La migration lithiasique donne suite à plusieurs situations :
- Asymptomatique (majorité des cas).
- Ictère obstructif (bloc des voies biliaires).
- Angiocholite.
- Pancréatite aiguë biliaire. Signes Cliniques : Triade DOULEUR FIEVRE (due à l’inflammation) ICTERE
Attention ! Apparition de chaque symptôme dans cet ordre !!!
Colique hépatique Cholécystite aigue Migration lithiasique
Douleur +++ ++ +
Fièvre NON OUI OUI
Ictère NON NON OUI
Echographie Calculs vésiculaires +Paroi vésiculaire +Dilatation VB principale
En conclusion, la démarche diagnostique dans le cas de pathologies hépatique se traduit par :
- L’analyse des symptômes (Colique hépatique ; Cholécystite aiguë ; Angiocholite).
- L’examen physique (Ictère ; Signes d’insuffisance hépato-cellulaire ; Ascite et signes physiques
d’hypertension portale).
- La biologie sanguine (Bilan hépatique : transaminases (ALAT, ASAT), gammaGT, phosphatases
alcalines, bilirubine totale et conjuguée, NFS, plaquettes, TP (facteur V), électrophorèse des
protides (albumine).
- L’imagerie : Echographie-Doppler ; Fibroscopie oeso-gastroduodénale.

52
FICHE RECAPITULATIVE
En hépatologie la pose du diagnostic se base sur un interrogatoire complet, un examen ciblé. L’échographie est l’examen d’imagerie qui sera le plus pratiqué.
Bilan hépatique standard : Transaminases ALAT et ASAT, GammaGT, Phosphatases alcalines, Bilirubine, Taux de prothrombine, Albuminurie, NFS Plaquettes.
Les grands syndromes de la pathologie hépatique :
Cholestase : diminution de la sécrétion biliaire. - Extra hépatique (obstruction voies biliaires extra hépatiques) ou Intra hépatique (défaut
sécrétion ou obstruction voies biliaires intra hépatiques) - Bilan biologique : augmentation des phosphatases alcalines et des gammaGT - Quand obstruction des voies biliaires : visible sur échographie - Conséquences : ictère (accumulation bilirubine) + Défaut d’acides biliaires ( diarrhée+
malabsorption lipides et vit. Liposolubles) + Prurit
Cytolyse : augmentation des transaminases ALAT et ASAT ALAT/Ph Alc>5 - Attention pas toujours d’origine hépato-biliaire : origine musculaire (prédominance
ASAT) - Démarche diagnostic : Origine hépatique+ Aigue/Chronique+ IHC ? + Etiologies possibles
(= virus, toxique, médicament)
Insuffisance Hépato-Cellulaire (IHC) : défaut de fonctionnement des hépatocytes (synthèse, détoxification, fonctions biliaires)
- Aigue ou chronique - Bilan biologique : baisse du taux de Prothrombine(TP) et du facteur V - IHC sévère si TP<50% norme / IHC fulminante si TP<50% norme + encéphalopathie
hépatique + apparition en 15 jours - Signes cliniques majeurs : encéphalopathie (3 stades : inversion rythme nycthéméral +
astéréxisconfusioncoma) + angiomes stellaires(>5)+ diminution TP+ diminution du facteur V( indépendant de la vitamine K)+ diminution albuminurie +/- signes non spécifiques (asthénie, ictère, sepsis …)
- IHC aigue : encéphalopathie + baisse TP et facteur V / quand chronique en + angiomes stellaires + hypo albuminémie
Hypertension portale (HP) : augmentation de la pression porte > 15mmHg ou augmentation de plus de 5 mmHg du gradient de pression hépatique
- 3 types anatomiques de HP : Bloc pré-hépatique (dans le tronc porte) /Intra hépatique
augmentation du gradient / Post hépatique (thrombose veines hépatiques)
- Signes cliniques : Ascite+ Œdème des membres inférieurs+ Splénomégalie
Hypersplénisme ( Thrombopénie+ Leucopénie) +Varices œsophagiennes +
Circulation veineuse collatérale
- Cirrhose (diagnostic par palpation = bord du foie dure et tranchant): augmentation
résistances vasculaires intra hépatiques augmentation tension portale (car
fibrose+++). L’organisme cherche à diminuer l’HTP via shunts porto-systémiques +
Production de NO( Vasodilatation artérielle) + Baroréflexe augmente débit cardiaque
+ Hypervolémie relative = Syndrome hyperkinétique

53
Ascite : Accumulation de liquide dans la cavité péritonéale
- Signes cliniques : matité déclive des flancs à la percussion + signe de flot +/- circulation collatérale porto cave et hernie ombilicale
- Diagnostics différentiels : grossesse + globe vésical+ kystes ovariens+ masse abdominale - 2 types d’ascite : transsudative (taux prot<20g/L, quand cirrhose) ou exsudative (taux
prot> 20 g/L, quand cancer, infection BK, trouble cardiaque, inflammation) - Ponction d’ascite : au lit du patient en pleine matité, fosse iliaque gauche, jonction 2/3 –
1/3 ligne entre ombilic et épine iliaque antéro sup
Ictère : Coloration jaune de la peau et de muqueuses (accumulation bilirubine)
- Bilirubine : pigment issu de l’hémolyse, relargué sous forme libre (indirecte= non conjuguée), dans le foie subit glucurono-conjugaison pour être éliminé dans la bile dans le tube digestif (forme conjuguée)
- 2 types d’ictères : à bilirubine non conjuguée : ictère + urines de couleur normale + selles
de couleur normale + hyperbilirubinémie à prédominance non conjuguée à bilirubine conjuguée : urines foncées + selles décolorées +
hyperbilirubinémie à prédominance conjuguée + défaut de sécrétion biliaire ( malabsorption lipides, vitamines liposolubles + diarrhée chronique)
Sémiologie biliaire :
Lithiase biliaire : formation de calculs biliaires le plus souvent dans la vésicule biliaire (20% de la population, dans 80% des cas asymptomatique)
- 2 types de calculs : cholestéroliques ou pigmentaires - Facteurs influençant la formation de calculs : âge, prédisposition familiales, sexe (F>H),
ethnie, alimentation grasse, obésité, dyslipidémie, grossesse, contraceptifs, oestrogénothérapie, malabsorption des acides biliaires
- Calculs peuvent se trouver à différents niveaux : dans vésicule biliaire (si se bloque colique hépatique) / Dans canal cystique (cholécystite) / Dans canal cholédoque(angiocholite)
Cholique Hépatique : douleur aigue d’origine biliaire localisée dans l’hypochondre droit, irradiant en hémi ceinture ou vers la pointe de l’omoplate droite. Début brutal et durée longue
- Signes cliniques : douleur + défense dans hypochondre droit + signe de Murphy PAS de fièvre ni ictère ni syndrome septique
- Signes biologiques : bilan hépatique et lipasémie normaux - Signes visibles à l’échographie : lithiase vésiculaire hyperéchogène, arrondie, mobile,
déclive avec cône d’ombre postérieur PAS de dilatation voies biliaires + paroi vésiculaire normale
Cholécystite aigue : inflammation de la vésicule quand calcul dans le canal cystique = Douleur + Fièvre Signes cliniques et biologiques de sepsis
- Signes à l’échographie : lithiase vésiculaire+ épaississement paroi (> 3mm) + vésicule sous tension+ PAS dilatation voies biliaires
Migration lithiasique : lithiase de la voie biliaire principale après migration du calcul - Complications : ictère obstructif / angiocholyte +++/ pancréatite aiguë biliaire - Signes cliniques : DOULEUR BILIAIRE FIEVRE ICTERE - Signes biologiques : Hyperleucocytose+ Cholestase+ Cytolyse + Lipasémie normale - Signes à l’échographie : dilatation de la voie biliaire principale

54

55
UE6 – SD – Sémiologie – cours n°7
20/01/2017
Pr Charles-André Cuenod
RT : Manon Delville
RL : Damien Jeune
Sémiologie radiologique de l'étage sous-mésocolique
Plan :
I. Rappels anatomiques
A. Vascularisation par le meso B. Les segments du co lon C. Anses digestives D. Les mesos E. Le grand omentum/epiploon
II. Technique d'imagerie A. Rayons X B. Echographie C. Scanner D. IRM E. Arteriographie
III. Aspect normal en imagerie
A. Intestin gre le B. Appendice C. Co lon D. Rectum E. Vaisseaux
IV. Sémiologie élémentaire
A. Lumiere B. Paroi

56
C. Meso D. Vaisseaux E. Espace interperitoneal F. Autres organes
Mot du RT : Ce cours est long et pas si facile que ca mais le prof a precise que la plupart des techniques
d'imagerie seraient revues en ED, pas de panique si vous n'avez pas tout bien assimile :).

57
I. Rappel anatomique
Le mésocôlon transverse situé dans l'abdomen est une structure qui le relie le côlon transverse au rétro péritoine. A mi-distance dans l'abdomen, il le sépare en deux étages :
Un étage sus mésocôlique au-dessus du mésocôlon transverse. Contient essentiellement des organes
pleins : foie, rate, pancréas mais aussi l'estomac, D1 et une partie de D2.
Un étage sous mésocôlique en dessous du mésocôlon transverse (celui qui va être détaillé dans ce
cours). Contient plutôt un tube.
Ces étages sont illustrés par les séquences ci-dessous
A. Vascularisation par le meso :
Sur l’illustration cicontre, le co lon transverse et son
meso ont ete reclines vers le haut pour bien mettre en
evidence le mesoco lon transverse.
B. Les segments du co lon
Le co lon comporte differentes portions, qui citees
dans le sens de progressions des matieres fecales, sont :

58
1= La valvule iléo-cæcale ou valvule de Bauhin : jonction entre l’intestin gre le et le co lon.
2= Le cæcum : sorte de reservoir faisant suite a la valvule
3= L’appendice vermiculaire : il est appendu au cæcum
4= Le côlon droit ou co lon ascendant
5= L’angle colique droite ( = angle hepatique pour les anglosaxons car situe juste en dessous du foie)
6= Le côlon transverse
7= L’angle colique gauche
8= Le côlon gauche ou co lon descendant
Le côlon sigmoïde ou pelvien
Le rectum avec le canal anal
→ L’étage sous méso-colique contient :
• Le gre le :
Duodenum mais uniquement D2, D3 et D4
Jejunum
Ileon
=> Valvule ileocæcale
• Le co lon :
Cæcum et appendice
Co lon droit
Co lon transverse
Co lon gauche
Co lon sigmoï de
• Le rectum haut
/!\ Les rectums moyens et bas sont sousperitoneaux, dans le petit bassin. Le canal anal est egalement
sousperitoneal et appartient au perinee. /!\
Mot du RT : Le prof a precise qu'il fallait savoir reconnaï tre et situer les structures precedentes sur des
images anatomiques comme sur des images radiologiques !

59
C. Anses digestives
Les anses digestives presentent une lumiere (dans laquelle passe le bol alimentaire) bordee d'une
paroi organisee en differentes couches, depuis l’interieur vers l’exterieur :
une muqueuse
une sousmuqueuse
une musculeuse
La classification des cancers va se baser sur les differents niveaux d'atteinte de ces couches.
Le tube digestif est relie au retroperitoine par la membrane peritoneale qui va recouvrir la musculeuse.
Cette membrane va former en arriere une structure graisseuse qui contient des vaisseaux, il s'agit du
méso. Il contient des vaisseaux permettant d'irriguer le tube (arteres, veines et lymphatiques) ainsi que
quelques ganglions.
Il faut imaginer que la membrane
se continue et se referme sur elle-
même si bien que la cavité
péritonéale est une cavité close.
Chez l'homme il n'y a aucune communication entre la cavite peritoneale et l'exterieur, il n'y a pas d'organe
peritoneal pur. Alors que chez la femme, les ovaires sont intra peritoneaux, il y a une communication entre
l'exterieur et le peritoine (cancer de l'ovaire : les cellules tumorales vont directement ensemencer le
peritoine=> carcinose). En scanner on pourra voir un « ga teau peritoneal »
Petite anecdote : le meso serait depuis une semaine le 79e organe a part entiere chez l'espece humaine ;)
D. Les mesos :
Le peritoine va changer de nom selon la structure qu'il recouvre : péritoine viscéral lorsqu'il
recouvre un viscere et péritoine pariétal quand il recouvre une paroi. Le meso est une lame porte
vaisseaux, il correspond aux deux feuillets de peritoine accoles
l'un contre l'autre. Les mesos contiennent plus ou moins de
graisse selon le morphotype.
Cicontre le chirurgien a sorti une anse d'intestin gre le et donc
du mesentere, on distingue bien les vaisseaux et la graisse. Le
mesentere permet en particulier le mouvement pour le
peristaltisme. Les replis tres importants du mesentere sont
appeles la fraise de veau (col a la renaissance).

60
Chaque meso prend le nom de l’organe dont il depend :
le meso du gre le → le mésentère (derivant de meso enteron =IG)
le meso du cæcum → le mésocæcum (caecum =organe libre du co lon)
le meso de l’appendice → le mésoappendice
le meso du co lon transverse → le mésocôlon transverse et le grand epiploon
le meso du co lon sigmoï de → le mésosigmoïde
le meso de la partie haute du rectum → le mésorectum
Le co lon droit et le co lon gauche ont la particularite de ne pas e tre mobiles physiologiquement, ils sont
accoles au retroperitoine et il n'y a donc pas de meso individualise en tant que tel. En revanche, le
jejunum, l'ileon, le cæcum, l’appendice, le co lon transverse et le sigmoï de sont mobiles, libre et l’on peut
voir leur meso.
E. Le grand omentum/épiploon
Il est constitué par l’accolement du prolongement de deux mésos, appendus d’une part à la partie
inférieure côlon transverse et d’autre part à la partie inférieure de l’estomac :
Le mésocôlon transverse au lieu de se réfléchir autour du côlon
transverse, se prolonge caudalement. Le méso de l’estomac se
développe lui aussi caudalement. Ces 4 feuillets de péritoines (2
pour chaque méso) se rejoignent et forment un tablier, encore
appelé tablier de sapeur. C’est le grand omentum ou grand
épiploon, celui-ci comporte beaucoup graisse et de nombreux
vaisseaux.
=> Rôle : On peut le comparer à une « serpillère ». Lorsque du
liquide est en excès dans la cavité péritonéale, le grand épiploon va nettoyer la cavité et aspirer le liquide superflu.

61
II. Techniques d'imagerie
Rayons X Echographie Scanner IRM Artériographie
Grêle Transit du grêle ++ +/-injection
+/-micropaque
Entéroscanner
EntéroIRM +
Côlon Lavements
barytés ou
hydrosolubles
+ +/-injection
+/-lavements
Coloscanner
Coloscopie
virtuelle
+/- +/-
Appendice - +++ +/- injection
+/- lavement
+/- voire - -
Rectum Lavements Echo-
endoscopie
+/- +++ -
A. Rayons X
Pour le gre le, on utilisait une technique appelee transit du grêle, on faisait boire un produit de
contraste au patient. Cette technique a ete abandonnee au profit du scanner et surtout de l’IRM. Pour le
co lon, on introduisait un lavement baryté ou hydrosoluble (produits de contraste) par voie basse afin de
mouler le colon (realisee par les radiologues). Cette technique a ete abandonnee au profit de la
coloscopie, effectuee par les gastroenterologues. L’appendice n’est pas visible avec les rayons classiques
et pour le rectum, on utilisait des lavements. Aujourd’hui cette technique a ete totalement abandonnee.
B. E chographie
L’echographie est tres utilisee pour visualiser l’appendice. Lors d’une suspicion d’appendicite,
l’echographie est l’examen minimum (voire un scanner) avant toute operation chirurgicale, surtout chez
les jeunes pour eviter l'irradiation. Cependant, elle est operateur dependant.
C. Scanner
La majorite des examens radiologiques sont fait avec le scanner. Cependant, l’un des inconvenients
majeurs du scanner est qu’il est tres irradiant.
L’observation du gre le avec un scanner classique peut se faire avec ou sans injection, avec ou sans
lavement. L'injection rehausse les parois du tube digestif pour e tre mieux visible. L’entéroscanner est
un examen dedie a l’analyse du gre le. On distend volontairement l’intestin gre le avec beaucoup de liquide
(1 a 2L) qui peut e tre de l’eau pure, du PEG (polyethylene glycol), du micropaque (baryte) ou du mannitol.

62
Concernant le scanner du co lon, celuici peut e tre effectue avec ou sans injection (c'est toujours mieux
avec ;) ). Quand on veut se focaliser sur le colon, on va le distendre d 'une facon ou d'une autre et selon la
maniere de faire, le nom va changer :
Scanner avec lavement : en urgence, le scanner est realise avec un lavement aux hydrosolubles
Coloscanner a l'eau : pour rechercher des grosses masses, grosses stenoses ( ex :un gros cancer du co lon,
chez un patient a ge ne pouvant pas supporter une coloscopie classique) on fait un scanner abdominal
avec un lavement a l'eau
Coloscopie virtuelle : a pour but de remplacer la coloscopie classique. Me me preparation que la
coloscopie reelle mais au lieu d'introduire un coloscope dans le patient, on va distendre le co lon avec de
l'air ambiant ou du CO2 (+++). On fait alors le scanner et des reconstitutions 3D virtuelles.
D. IRM
Pour l'intestin gre le : L'entéroIRM est exactement la me me chose que l'entero scanner (cf C) : On
fait boire au patient de l'eau, du PEG, ou du mannitol pour distendre les anses gre les : environ 1,5L a boire
dans un certain timing (1 verre toutes les 5 min).
On fait beaucoup plus d'enteroIRM que d'entero scanner pour les pathologies chroniques pour diminuer
l'irradiation (surtout quand la maladie se declare jeune), on reserve le scanner a l'urgence.
Pour le co lon et l'appendice, l'IRM n'est vraiment pas une technique de choix ! Mais pour l'analyse du
rectum, c'est LA technique de choix !
E. Arteriographie
Est beaucoup moins utilisee qu'elle n'a ete, elle ne sert aujourd’hui plus au diagnostic mais a un
but therapeutique. Utilisee en cas de saignement digestif pour boucher les vaisseaux qui saignent.
III. Aspect normal
A. Aspect de l'intestin gre le
Le gre le presente une paroi fine : < 3 mm (en general).
Cette paroi ne doit pas e tre ni epaissie, ni virtuelle et doit se
rehausser apres injection. Il existe des plis ou des valvules
conniventes sur le jejunum et elles disparaissent sur l’ileon (paroi
lisse et reguliere). Le jejunum commence a l’angle de Treitz situe
a gauche du rachis (sinon defaut d’accolement du mesentere).
=> En entéroscanner : On peut tracer virtuellement une oblique
en bas et vers la gauche, separant l’abdomen en deux : le jéjunum
est essentiellement en haut et a gauche et l’iléon en bas et a
droite. Les plis ou valvules conniventes du jejunum sont
clairement visibles, et en radiographie classique, on parlait
d’aspect en feuilles de fougere. Les anses de l’ileon sont elles
totalement lisses.

63
Ce scanner reformate revele apres injection un rehaussement normal des parois du tube digestif dont
l’epaisseur est bien reguliere. L’opacification est ici faite avec de l’eau, du PEG ou du mannitol : la lumiere
apparaï t hypodense (noire) et a la paroi hyperdense (blanche) ⟶contraste négatif. On obtient un
contraste inverse en utilisant de la gastrografine diluee : la lumiere apparaï t hyperdense et a la paroi
hypodense ⟶ contraste positif.
/!\ Attention au pseudo-épaississement pariétal : Parfois, au niveau du jéjunum, la paroi peut
donner l’impression d’être très épaisse (signe pathologique)
→ piège : si par hasard, la coupe axiale passe dans la valvule cela donnera une impression
d’épaississement, il faut donc regarder les coupes sus- et sous-jacentes pour vérifier s’il s’agit d’un épaississement complet ou d’un pseudo- épaississement.
=> Le mésentère :
La quantite de graisse mesenterique « normale » est tres variable selon les morphotypes et
notamment selon le sexe :
les hommes : accumulation de graisse dans le mesentere
les femmes : accumulation de graisse en souscutanee. Cette graisse est « meilleure » que celle intra
abdominale
=> En IRM :
Avantages par rapport au scanner :
- non irradiant
- signal blanc ou noir : pondération T2 = eau en blanc et paroi noire et en pondération T1 , l'eau est noire
et les parois sont en hypersignal si on injecte un produit de contraste (blanches)

64
B. Aspect de l’appendice
C’est une petite structure vermiculaire physiologiquement creuses et borgne, au niveau du bas fond cæcal,
environ 11,5cm en dessous de la jonction ileocæcale (= valvule de Bohin). Sa paroi est fine, homogene,
lumiere bien visible.
Le fait que l'appendice soit borgne permet de differencier l'appendice distendu de l'intestin gre le. On
remarque le petit meso de l’appendice avec un petit peu de graisse autour. Sa position habituelle est au
point de Mac Burney cependant, cette position est variable. Les variations de position les plus classiques
sont l’appendice retrocæcale et sous hepatique.

65
C. Aspect du côlon
Le long du co lon il y 3 bandelettes (= taenias) : 1 anterieure et 2 posterieures, les haustrations
se repartissent alors comme une forme de trefle :
Une entre la bandelette ventrale et la bandelette dorsomediale
Une entre la bandelette ventrale et la dorsolaterale
Une entre les deux bandelettes dorsales
Plis et haustrations : /!\ Les hautrastions ne correspondent pas aux plis : confusion frequente. Les
haustrations sont les bosselures entre les plis semi lunaires.
=> coloscopie virtuelle : (cf II C) Elle necessite une preparation equivalente a la coloscopie. Le
patient doit boire un produit la veille de maniere a nettoyer le co lon de toute matiere. Une fois le
patient dans le scanner, on introduit de l’air, ou mieux du CO2, dans le co lon afin de le gonfler. Deux
acquisitions sont effectuees : une sur le dos et une sur le ventre. Chaque acquisition dure 17s. Ces
deux acquisitions permettent d'avoir la totalite du co lon.
A partir de la difference de contraste entre l’air et la paroi, un logiciel reconstruit une image virtuelle tres precise du co lon. Cette reconstitution permet de visualiser l’interieur du co lon, et comme avec une camera, on peut cheminer dans le co lon afin de rechercher un eventuel

66
polype (lesion de petite taille). En coloscopie reelle, lorsque le gastroenterologue repere un polype, il le reseque afin de traiter le patient et peut en faire la biopsie afin de verifier la presence d’une eventuelle metaplasie ou une cancerisation debutante. En coloscopie virtuelle, on indique la taille (risque de degenerescence ↑ avec la taille) et la localisation du polype.
Via une coloscopie réelle, on ne trouve de polype dans une population normale que dans 20% des cas. Ainsi les 80% des coloscopies sont normales.
D. Aspect du rectum
Le rectum est en 3 parties :
le haut rectum dans la cavite peritoneale
le moyen rectum dont une partie est dans le haut rectum
le bas rectum sous peritoneal
La cavite peritoneale s'arre te au niveau du cul de sac de Douglas
(accumulation de liquides).
En coupe sagittale, on voit clairement la totalité du rectum et ses différentes portions.
E. Vaisseaux
L'arteriographie est aujourd'hui completement remplacee par l'imagerie en coupe (produit de
contraste par voie IV) ce qui va permettre des reconstructions en 3D. Trois vaisseaux arteriels
alimentent le tube digestif. Ils sont originaires de l’aorte abdominale et sont medians :

67
le tronc cœliaque (susmesocolique) arque vers le haut. Il va donner 3 branches : l'artère
splénique qui va vers la gauche, l'artère hépatique commune qui va vers la droite et l'artère
gastrique gauche qui est plus petite. L'artere hepatique commune se separe elle me me en deux
branches : l'artère hépatique propre (A HP) qui va aller directement au foie et l'artère gastro
duodénale (A GD) qui va aller vers le duodenum et l'estomac.
l'artere mesenterique superieure arquee vers le bas avec la pince aorto mésentérique dans
laquelle passe le duodenum et la veine renale gauche
l’artère mésentérique inférieure
IV. Sémiologie élémentaire
Grille de lecture en 6 points pour lire une image, avec du centre vers l’exterieur (revu en ED) :
lumiere digestive
paroi
mesos
vaisseaux
cavité péritonéale
autres organes
Pour chaque image on va regarder la morphologie et le signal (en IRM, l’atténuation en scanner,
l'échogénicité en échographie).

68
A. La lumiere digestive
=> Morphologie :
Diametre : normal (gre le : <2cm diametre)
Dilatation : diametre augmente (gre le > 2cm diametre)
Stenose : diametre diminue
Image de soustraction : lacune dans la lumiere
Image d’addition : la lumiere s'etend ou elle ne devrait pas s'etendre (=diverticule)
Fistule ou perforation : paroi rompue, communication vers l’exterieur.
=> Signal : contenu anormal ou defaut de remplissage
=> Exemples :

69
Il est possible que le contenu de la lumiere soit anormal. Ici, on voit dans la lumiere de l'appendice
un element hyperechogene avec un co ne d'ombre. En scanner, il apparaï t de densite equivalente a
la vertebre en arriere ⇒ element calcique. Ces images, en echo comme en scanner, sont
pathognomoniques : c'est une stercolithe appendiculaire.
B. La paroi
=> Morphologie :
Épaisseur normale (on tolère 5mm, mais normalement, <3mm)

70
Épaississement : Circonférentiel, Asymétrique/Excentré,
Irrégulier (cancer)/régulier
Amincissement
Nodule : épaississement focal
=> Signal : On peut avoir un hypo (noir)/hyper signal (blanc)
Disparition des couches
Aspect en cocarde : les couches sont trop bien visibles
Si c'est hyper dense c'est qu'il y a trop de produit de contraste
dans la paroi ou qu'il y a du sang. Si c'est hypo dense, c'est au
contraire que la paroi est ischémique. Si on a des bulles de gaz
dans la paroi, on appelle ça une pneumathose.
=> Exemples :

71
C. Le méso
=> Morphologie :
Normale
Ganglions hypertrophiques
Masse mésentérique
Graisse hypertrophique
=> Signal
Infiltration de la graisse
Oedème
=> Exemples :

72
D. Les vaisseaux

73
=> Morphologie
Sténose
=> Signal
Thrombose
=> Exemple :
E. La cavité péritonéale
épanchement (air = pneumopéritoine, liquide= ascite)
collection, abcès
adhérence
=> Exemples :
F. Autres organes
Il est important de les regarder les autres organes : foie, rate, reins, pancréas…

74
FICHE RECAPITULATIVE
Le péritoine
sereux pour les visceres
parietal pour la paroi
meso s’il se reflechit sur luime me.
Il permet l’innervation et la vascularisation des organes qu’il entoure.
C’est une cavite close. Les ovaires sont les seuls organes intra peritoneal, si cancer => ensemence
la cavite peritoneale.
–le meso du gre le → le mesentere (derivant de meso enteron =IG) – le meso du cæcum → le mesocæcum (caecum =organe libre du co lon) –le meso de l’appendice → le mesoappendice
–le meso du co lon transverse → le mesoco lon transverse et le grand epiploon
–le meso du co lon sigmoï de → le mesosigmoï de
–le meso de la partie haute du rectum → le mesorectum
Grand épiploon = fusion du prolongement du mesocolon transverse avec celui de l’estomac
=> ro le de serpillere de la cavite abdominale, reabsorbe tous les liquides .
Gre le : jejunum =>paroi plisse en feuilles de fougeres, valvules conniventes.
Ileon : => paroi lisse
Appendice : tube borgne 1,5 cm en dessous de la valvule ileocaecale
Colon : haustrations (sac tri folie) entre les plis semi lunaire se repartissent en trefle separe par
des bandelettes => ventrales , dorso laterale et dorso mediale
Rectum :3 partie => Haut rectum, Moyen rectum,Bas rectum ( le HR et une partie du MR sont
peritoneaux)
Vaisseau : Tronc cœliaque => A splenique, A gastrique gauche et A hepatique commune qui se
divise pour donner A hepatique propre et A gastro duodenale
A mesenterique superieur et A mesenterique inferieur
Plusieurs techniques d’imagerie pour explorer les differents organes :
Grille de lecture d’une image en 6 points :
1/ La lumière 2/ La paroi 3/ Le méso 4/ Les vaisseaux 5/ La cavité péritonéal 6/ Autres
organes
Pour chaque point il faut étudier la morphologie et le signal/atténuation/échogénicité.

75
Rayons X Echographie Scanner IRM Artériographie
Grêle Transit du grêle ++ +/-injection
+/-micropaque
Entéroscanner
EntéroIRM +
Côlon Lavements
barytés ou
hydrosolubles
+ +/-injection
+/-lavements
Coloscanner
Coloscopie
virtuelle
+/- +/-
Appendice - +++ +/- injection
+/- lavement
+/- voire - -
Rectum Lavements Echo-
endoscopie
+/- +++ -

76

77
UE6 – Anatomopathologie –
Cours n°3
Du 20/01/2017
B. TERRIS – [email protected]
RT : Eloïse DELIRY
RL : Maxime VIGNAC
Evolution morphologique d’une hépatite virale
chronique
Plan :
I. Présentation de l’hépatite A. Généralités
B. L’hépatite chronique virale B C. L’hépatite chronique virale C D. Mode de découverte des hépatites chroniques virales E. Mécanismes des lésions hépatiques
II. Les méthodes diagnostiques
A. Biopsie transpariétale
i. Dégré d’activité ii. Degré de fibrose
B. Fibrotest C. Fibroscan
III. Phénomènes de réparation et de cicatrisation
A. La fibrose B. De la fibrose à la cirrhose

78
I. Présentation de l’hépatite
A. Généralités
Pour les cliniciens, l’hépatite chronique est un état inflammatoire de longue durée au niveau
hépatique (+ de 6 mois). L’évolution de ces hépatites chronique dépend :
- De l’étiologie
- De facteurs intrinsèques au patient
- De l’état des lésions au moment du diagnostic.
Pour les pathologistes, l’hépatite chronique se définie de manière morphologique : elle prend la
forme de lésions nécrotico inflammatoire de sévérité variée. Cette notion exclut les
pathologies liées à l’alcool et les pathologies biliaires.
On s’intéresse ici aux infections virales qui sont les étiologies les plus fréquentes des hépatites
chroniques. Il existe un grand nombre de virus à tropisme hépatique qui diffèrent :
- par la nature de leur matériel génétique (ARN ou ADN)
- par leur mode de transmission
- par les signes cliniques et la sévérité de l’atteinte hépatique qu’ils induisent.
Les seuls qui peuvent induire une hépatite chronique sont les virus B, C et delta. Le virus delta
nécessite une infection au virus B préexistante car il constitue une surinfection au virus B. Les
autres virus de A à G n’induisent quant à eux pas d’hépatite chronique mais sont responsable
d’hépatite aigue.
Les coinfections ne sont pas rares car les modes de transmission sont assez semblables entre
le virus de l’hépatite C (HCV), celui de l’hépatite B (HBV) et le virus du Sida (HIV). Le HIV favorise
le développement et la sévérité des hépatites chroniques.
D’autres virus sont à tropisme hépatique accessoire, c’est-à-dire qu’il y a une atteinte plus
générale, incluant une atteinte hépatique . C’est le cas par exemple de la mononucléose (EBV).
B. Hépatite chronique virale B
Le virus de l’hépatite B est un virus à ADN.
L’hépatite aiguë B peut survenir au niveau périnatal, dans ce cas, 50% à 90% des nourrissons
vont évoluer vers une hépatite chronique. Tandis que lors d’une contamination à l’âge adulte,
seulement 5 à 10% vont évoluer vers une hépatite chronique. Les autres guérissent.
Ceci explique la forte incidence endémique de l’hépatite virale B dans les pays asiatiques et en
Afrique du fait de l’absence de politique vaccinale dans certains pays et du fait de la contamination
qui a lieu au moment de l’accouchement. Ainsi une infection périnatale du virus de l’hépatite B
entraine l’infection d’une grande partie de la population et ainsi perdure dans le temps.

79
L’hépatite chronique B entraine une cirrhose (30% des cas) puis à terme un carcinome
hépatocellulaire (CHC).
C. L’hépatite chronique virale C
Le virus de l’hépatite C est un virus à ARN (Flavivirus).
Il existe environ 600 000 porteurs du virus de l’hépatite C en France. L’hépatite C est
principalement liée à une transmission sanguine. Aujourd’hui on assiste à une régression de
l’incidence des nouveaux cas de l’hépatite C pour amener dans 20-30 ans à une disparition de
l’hépatite chronique virale C.
L’hépatite chronique virale C mène aussi à une cirrhose puis à un CHC.
D. Mode de découverte des hépatites chroniques virales
La découverte d’une hépatite chronique virale est souvent fortuite car la maladie est longtemps asymptotique. On observe ainsi lors d’une prise de sang une augmentation des transaminases qui mène à la réalisation d’un bilan hépatique. Elle peut aussi se faire au cours du suivi de l’évolution d’une hépatite aiguë par l’observation de l’altération de l’état général. Mais souvent, on la découvre au stade tardif qu’est la cirrhose.
E. Mécanismes des lésions hépatiques
On décrit 2 causes de lésions hépatiques :
- Soit le virus va induire une cytotoxicité directe au niveau des cellules hépatiques
- Soit les lymphocytes T vont reconnaitre des épitopes à la surface des hépatocytes infectés
et vont détruire ces hépatocytes par une réaction immunitaire à médiation cellulaire
+++.

80
II. Les méthodes diagnostiques
A. Biopsie transpariétale
Elle a lieu lorsqu’on a fait le diagnostic d’hépatite virale, pour juger de la sévérité des lésions
histologiques.
Pour réaliser cette biopsie, on recherche par percussion la matité correspondant au foie dans
l’hypochondre droit. On ponctionne alors grâce à une aiguille pour prélever une « carotte
biopsique ».
Ainsi on peut évaluer la sévérité des lésions en s’appuyant sur le score Metavir qui combine deux
scores :
un score d’activité ( pour apprécier l’inflammation et les nécroses hépatocytaires )
de A0 -> A3
un score de fibrose de F0 -> F4
Cette biopsie et sa lecture grâce au score Metavir permet :
d’aider à la décision thérapeutique
d’apprécier le degré de fibrose et d’inflammation pour surveiller la maladie
de rechercher des causes associés de l’hépatite lorsque le bilan n’est pas complètement
caractéristique d’une hépatite virale = rechercher une hépatopathie associée.
Le fragment prélevé lors de la biopsie transpariétale représente 1/50 000ème du foie. Cependant
cet échantillon est représentatif car la répartition des lésions d’une hépatite chronique virale est
homogène sur l’ensemble du foie. Donc à partir de 2 cm, l’échantillon est exploitable.
i. Degré d’activité
Le foie est constitué d’espaces portes et de veines centrolobulaires. Les espaces portes,
structures terminales, contiennent la triade portale constituée d’un canal biliaire, d’une artère
et d’une veinule porte. Le sang arrive au niveau de l’espace porte et irrigue les sinusoïdes (espaces
entre travées les hépatocytaires et où ont lieu les échanges métaboliques) puis le sang revient au
niveau des veines centrolobulaires -> veines sus hépatiques -> veine cave inférieure.
Espace porte
Lobule
Veine centrolobulaire

81
Lors d’une hépatite chronique, on va avoir la survenue d’inflammation portale et lobulaire
avec des nécroses périportales ou hépatocytaires. Sur le plan morphologique on observe :
Un amas de lymphocytes de
petites tailles (les points noirs)
qui réalisent une sorte de
nodule lymphoïde caractéris-
tique d’une hépatite chronique.
Cet infiltrat lymphoïde ne reste
pas en place et a tendance à
infiltrer les 1ères couches
hépatocytaires au contact de
l’espace porte : la lame
bordante. Les lymphocytes
pénètrent à l’intérieur de ces
travées hépatocytaires
périportales et vont être à
l’origine de la destruction des
hépatocytes infectés.
Cette activité périportale se
retrouve au niveau lobulaire
avec des foyers nécrotico-
inflammatoires.
Les lymphocytes sont au
contact des hépatocytes
infectés et les détruisent par
l’immunité a médiation
cellulaire.
Dans le cas du virus de l’hépatite B, on a la présence d’enveloppe virale dans le cytoplasme des
hépatocytes infectés. On les révèle grâce à des anticorps anti-HBS ou anticorps anti-HBC
(anticorps anti capside) lors d’une prise de sang pour connaître l’état de l’infection.

82
ii. Degré de fibrose
On a des scores de F1 à F4 qui traduisent le degré d’avancement de l’hépatite chronique. Plus il y
a de destruction d’hépatocyte dans le temps, plus cette destruction va entrainer une fibrose qui
va devenir progressivement mutilante.
La fibrose s’étend à partir des espaces portes puis à l’intérieur des lobules avec des ponts fibreux
(septa) qui relient les espaces portes entre eux. Les ponts vont ensuite relier les espaces portes à
la veine centrolobulaire. A terme ces ponts entrainent une modification de l’architecture
hépatique qui va aboutir à une nodulation au niveau du foie.
Cette fibrose annulaire délimite un nodule de régénération (indiqué par la flèche), nodule qui
essaye de préserver une fonction hépatique. Cet état hépatique traduit l’existence d’une cirrhose.
Une cirrhose se traduit par un aspect avec des nodules de régénération entourés par de la fibrose.
C’est la résultante de l’hépatite virale chronique à terme et de toutes autres agressions du foie.
Le foie cirrhotique est un état prénéoplasique qui prépare la venue d’une tumeur maligne du
foie : le carcinome hépatocellulaire.
Fibrose -> cirrhose -> carcinome hépatocellulaire

83
La biopsie est un examen invasif qui a un coût et une mortalité. On met donc en place des tests
non invasifs pour apprécier l’état de fibrose.
B. Fibrotest
But : évaluation de l’index de fibrose.
On fait une prise de sang et on dose 5 marqueurs
indirects de fibrose (Alpha 2 macroglobuline,
Haptoglobuline, Apolipoprotéine A1, bilirubine totale,
GGT) et les transaminases (ALAT).
En fonction de l’âge et du sexe on va obtenir un
score du fibrotest qu’on fait correspondre à un score
de fibrose via le tableau ci- contre.
C. FibroScan
But : analyse de l’élasticité hépatique car plus le foie est dur plus la fibrose est importante.
L’élasticité est la capacité d’un milieu à se déformer sous l’exercice d’une contrainte mécanique.
Plus un milieu est dur, plus son élasticité augmente, de la même manière qu’une pression. Dans
notre cas, la fibrose rend le foie dur. Donc plus le foie est fibrosé, plus son élasticité sera
élevée.
On pratique l’élasticité impulsionnelle : on engendre une vibration à la surface de la peau et ces
vibrations se propagent jusqu’au foie, puis on enregistre la vitesse de retour de ces vibrations.
Plus ces vibrations se déplacent rapidement, plus le foie est dur. On en déduit une valeur de
l’élasticité en KPa.
Cet examen est régulièrement utilisé et il est fiable et sensible.
III. Phénomènes de réparation et de cicatrisation
Les processus d’inflammation et de réparation reflètent la capacité remarquable du corps à se
« restaurer ».
Lors d’une agression aiguë se met en place le processus inflammatoire au niveau du site lésé pour effectuer une restitution ad integrum du tissu lésé.
Cette restitution ne laisse aucune séquelle lorsque la lésion est minime, mais laisse une cicatrice fibreuse résiduelle qui peut aboutir à une restauration de la fonction de l’organe ou au contraire entrainer une dysfonction : exemple de L’Infarctus du myocarde étendu, la fonction cardiaque est altérée en fonction de l’étendu de l’atteinte des fibres musculaires qui sont remplacées par un tissu fibreux non fonctionnel, ce qui entraîne une insuffisance cardiaque.

84
Lors d’une agression chronique, on observe une destruction progressive du parenchyme
(hépatocytes infectés) avec progressivement l’apparition d’une fibrose qui entraîne un
dysfonctionnement de l’organe.
La fibrose à un rôle dans la cicatrisation et la régénération mais entraîne un dysfonctionnement
de l’organe.
Matrice extracellulaire (rappel) :
La matrice extracellulaire (MEC) correspond à la substance intercellulaire. Elle joue un rôle
important, notamment de soutien et de cohésion intercellulaire, mais aussi de nutrition (via la
circulation des métabolites), d’épuration et d’information (les cellules communiquent de manière
paracrine entre elles).
Toute altération de cette MEC peut avoir un retentissement important au niveau de l’organe et
peut engendrer des foyers lésionnels multiples au sein de l’organisme.
Elle est composée de protéines fibrillaires et de substance fondamentale :
Les protéines fibrillaires : fibres de collagènes +++, fibres élastiques et fibres
réticuliniques.
La Substance fondamentale : composée de glycoprotéines, de protéoglycanes,
d’acide hyaluronique et de protéines matricellulaires (SPARC, thrombospondine
2, ostéopontine)
A. Fibrose
La fibrogénèse est un processus dynamique caractérisé par la transcription de gènes de la MEC. Elle intervient lors d’une inflammation pour limiter l’inflammation et limiter la perte de substance éventuelle. C’est un mécanisme de cicatrisation physiologique et non spécifique. Dans le foie normal, la fibrogénèse intervient au ralenti et au quotidien pour maintenir un pool constant de tissu fibreux et un équilibre entre la destruction et la production de la MEC. La fibrose est quant à elle un phénomène pathologique, secondaire à une fibrogénèse prolongée, due à la persistance d’un agent agresseur (virus…). Elle correspond à un dépôt anarchique de molécules de la MEC néosynthétisées lors de la fibrogénèse, déstabilisant la balance entre synthèse et dégradation. A long terme, dans le foie, la fibrose peut mener à une cirrhose.

85
La fibrogénèse correspond à la production des substances de la MEC (étape gènes ->
protéines) grâce à l’activation des cellules étoilées du foie situées dans l’espace de Disse
(=espace entre les cellules endothéliales de l’espace sinusoïde et les travées hépatocytaires).
Les cellules étoilées du foie sont présentes sous deux phénotypes : Etat normale = quiescent sous forme de lipocytes car cytoplasme riche en graisse Activées : elles prennent l’aspect de myofibroblastes qui produisent de la MEC.
B. De la fibrose à la cirrhose

86
La fibrose est un tournant dans l’évolution de la maladie chronique du foie avec une augmentation
quantitative et qualitative de la MEC : on passe d’une MEC lâche de type membrane basale à
une MEC dense de type collagène fibrillaire et qui va être résistante à la dégradation
enzymatique.
Il n’y a donc plus de balance entre destruction et formation. Cette MEC ne sera plus dégradée et
se déposera au fur et à mesure du temps et sera à l’origine de la fibrose qui va s’étendre grâce au
pont fibreux = fibrose extensive qui au fur et à mesure du temps va aboutir à la cirrhose.
La cirrhose est le stade ultime = fibrose annulaire associée à des nodules de régénération.
Si on s’y prend tôt, la cirrhose n’est pas totalement irréversible car on peut avoir sous traitement
une régression partielle de la fibrose après éradication de l’agent infectieux lors d’une hépatite
virale ou de même après sevrage pour une hépatite d’origine alcoolique.
IV. Conclusion
Les hépatites chroniques virales correspondent à :
Une agression tissulaire chronique qui résulte d’un infiltrat inflammatoire portale et
lobulaire avec des nécroses hepatocytaires liées à une réaction immune à médiation
cellulaire.
Des lésions morphologiques variées qui peuvent être quantifiées par le score
METAVIR de A0F0 à A3F4.
La Fibrose (-> cirrhose) correspond à :
Un mécanisme séquentiel précédé par une phase prolongée de fibrogénèse, nécessaire
au processus de cicatrisation. On a un déséquilibre entre synthèse et dégradation de la
MEC.
Un état cicatriciel modifiant l’architecture et altérant la fonction des organes.
La cirrhose est habituellement irréversible. Mais en s’y prenant tôt, on peut arriver à une
régression partielle de cette fibrose ou cirrhose chez l’individu.

87
FICHE RECAPITULATIVE
- Hépatite chronique : état inflammatoire longue durée (>6mois) avec lésions nécrotico-
inflammatoires.
- Virus à tropisme hépatique de A à G (mais seuls les virus B,C et Delta provoquent une
hépatite chronique)
- HBV (ADN) conduit à une hépatite chronique dans 50-90% des cas en périnatal
(transmission mère-enfant à la grossesse) et 5-10% des cas adultes. Sinon on observe
une guérison spontanée.
- HCV (ARN) a une prévalence de 600 000 cas en France mais a une incidence en forte
baisse.
- L’hépatite chronique est un facteur contributif des carcinomes hépatocellulaires.
- Les lésions induites de ces hépatites sont la cytotoxicité directe et la réaction
immunitaire à médiation cellulaire.
- Par biopsie transpariétale, on peut facilement caractériser les lésions histologiques.
- On détermine alors le score METAVIR par :
o L’Activité de A0 à A3 qui caractérise l’inflammation et la nécrose
o La Fibrose de F0 à F4
-
- Il existe également des tests diagnostiques non invasifs :
o Le Fibrotest : - utilise des index de fibrose qui sont dosés par prise de sang
- 5 marqueurs + transaminases
- score de [0;1] (avec F0 en 0 et F4 en 1)
o Le Fibroscan : fait une mesure d’élastométrie (en kPa) par mesure de vibration
car plus le foie est dur, plus il y a de fibrose.
- On distingue l’inflammation portale (nécrose périportale) de l’inflammation lobulaire
(nécrose lobulaire).
- La fibrose est mutilante en « ponts » ou « septa » ce qui se traduit par une fibrose
annulaire avec des mécanismes de régénération.
- Fibrogénèse : transcription de gènes de la Matrice Extra Cellulaire afin de limiter
l’extension de l’inflammation et combler les pertes de substance fondamentale.
- Si hépatite : activation des cellules étoilées du foie qui produisent de la MEC. Elles sont :
Soit quiescentes, qui stockent des boules de graisses : Lipocytes
Soit activées, qui synthétisent de la MEC : Cellules myofibroplastiques
- En cas de fibrose donc de cirrhose, il y a une augmentation quantitative de MEC et un
modification qualitative de cette dernière qui était lâche et qui devient réticulée, dense,
résistante à la dégradation, faisant de la fibrose annulaire accompagnée de nodules de
régénération.
- Les hépatites chroniques sont habituellement irréversibles mais une régression est
néanmoins possible lors de l’élimination précoce de l’agent responsable (ex : VHC).

88

89
UE6 – SD – Anatomie - n° 5
16/01/2017
Pr Richard Douard [email protected]
RT : DEBIAIS Mélanie
RL : TURCK Clara RD : Camille LECOULES
Foie et voies biliaires
Plan :
I. Le foie A- Le lobule hépatique B- Topographie C- Anatomie D- Segmentation hépatique E- Applications chirurgicales F- Coupes à connaitre
II. Les voies biliaires A- Anatomie B- Vascularisation C- La lithiase biliaire D- Cholécystectomie
Abréviations : VCI : Veine Cave Inférieure VC : Veine Cave AMS : Artère Mésentérique Supérieure

90
I. Le foie
A- Le lobule hépatique Le lobule hépatique est l’unité fonctionnelle du foie. Les hépatocytes sont organisés en cocarde, hexagones en périphérie desquels arrive le flux porte. Au niveau des espaces portes périphériques, on retrouve des canalicules biliaires, des artères et veines portes. Le flux porte va traverser l’hépatocyte de facon centripète et être transformé. Le produit final arrive dans la veine centrolobulaire, ces veines se rassemblent pour former les veines hépatiques, qui gagneront ensuite la VCI. NB : on parle bien ici de veines hépatiques et non sus hépatiques.
On a donc d’un côté la veine porte, l’artère porte et les voies biliaires, de l’autre la veine hépatique. La segmentation hépatique fonctionnelle (différente de la description anatomique) a été définie selon les pédicules artériels/veineux/biliaires et non selon les veines hépatiques. Cirrhose : atteinte du foie créant des nodules de régénération qui vont bloquer les espaces portes. Le flux porte arrivant difficilement au foie, il y a apparition d’une hypertension portale.
B- Topographie Le foie est situé dans l’hypochondre droit, sous la coupole diaphragmatique droite. Cette topographie est importante en traumatologie digestive : en effet, le foie fait partie des organes situés dans l’abdomen mais protégés par les côtes (en regard du thorax). On ne peut donc normalement pas palper le foie, soit en raison des côtes, soit de la contraction du muscle droit. La vésicule biliaire repose sur le rebord chondro costal, au croisement avec le bord externe du muscle droit.

91
Ici il est intéressant de noter qu’une discussion « entre amis » dégénérant par un coup de couteau au thorax peut toucher la plèvre, le poumon, de nouveau la plèvre, traverser le diaphragme puis atteindre le foie. Le foie est un organe thoraco-abdominal.
Sur une coupe sagittale paramédiane, on distingue 3 faces au foie :
- Face supérieure : moulée sur le diaphragme et la paroi abdominale - Face postérieure : le long de la VCI - Face inférieure : regardant en bas et en arrière. On y trouve le hile (ou porte) du foie. Le
hile comporte un élément portal (veineux), un élément artériel et un élément biliaire. On a d’un côté les veines hépatiques entre le foie et la VC, de l’autre les éléments artériels, biliaires et portaux.
Le carrefour hépatico-cave est la jonction entre les veines hépatiques et la VC. Il y a 2 types de veines hépatiques : les principales (grosses) et les accessoires (petites).
Ce sont les 3 veines hépatiques principales qui vont constituer le carrefour hépatico-cave, juste sous le diaphragme. Il y a très peu de place entre le diaphragme et les veines, il est donc difficile de clamper la VC en cas de plaie des veines hépatiques. On peut alors être amené à clamper la VCI en intra-thoracique, au bloc. Les veines accessoires, plus variables, sont situées le long de la VCI rétro-hépatique.
Sur une coupe parasagittale droite, on peut observer la naissance de la veine porte, qui va passer par le pédicule hépatique et se terminer dans la Pars Vasculosa, où elle se divise en 2 branches droite et gauche. On voit également sur cette coupe parasagittale le foramen épiploïque = l’entrée de la bourse omentale. On a en avant de ce dernier la veine porte et en arrière la veine cave. Sur un scanner, la VC est systématiquement en arrière de la veine porte.

92
Il faut noter que le référentiel n’est pas le même, selon si l’on parle du SYSTÈME porte ou de la VEINE porte.
Le système porte commence au niveau des branches de constitution de la veine porte et se termine dans le lobule hépatique.
La veine porte a une origine (derrière l’isthme pancréatique), un trajet et une
terminaison (bifurcation)
C- Anatomie Le foie possède une anatomie macroscopique et une anatomie fonctionnelle. Macroscopiquement, le ligament rond et le ligament falciforme séparent le foie en 2 lobes inégaux :
- Lobe gauche : représente 20 à 25% du volume hépatique - Lobe droit : particulièrement volumineux, 80% à lui seul
La vésicule biliaire et le ligament rond délimitent le lobe carré (nom dû à sa forme) à la face inférieure du foie. En arrière, on trouve un petit lobe compris entre la VC et le ligament veineux : le lobe caudé.
Les empreintes sont également importantes :
- Face inférieure du lobe G : empreinte gastrique - Face inférieure du lobe D : empreintes colique et rénale

93
L’image du haut est une vue antérieure du foie. L’image du bas est une vue inférieure, avec la VCI dorsale et la vésicule biliaire ventrale.
L’image est une vue inférieure du foie. Le foie est ici soulevé et on voit la VCI car les structures passant devant ont été sectionnées. On voit bien le hile hépatique, avec en arrière de ce dernier le lobe caudé.

94
On regarde maintenant une vue postérieure. Le foie comme tous les organes abdominaux est péritonisé mais à l’extérieur de la cavité péritonéale. Les zones en marronné sont les zones du foie recouvertes de péritoine viscéral, cela correspond à la capsule de Glisson. L’area nuda, en blanc, est la zone non péritonisée. Les ligaments triangulaires, attaches péritonéales postérieures doivent leur nom à leur forme. Celui du lobe G est fin, à l’inverse de celui du lobe D, plus large.
D-Segmentation hépatique Dans les années 50, l’anatomie interne du foie n’était pas connue. Hors on commence à s’intéresser aux hépatectomies dans le traitement des cancers du foie. Les anglo-saxons proposent une segmentation basée sur les veines hépatiques, tandis qu’un français (Pr Claude Couinaud) se base lui sur les éléments portaux, biliaires et artériels (éléments glissoniens : ils emmènent de la capsule en s’enfonçant dans le foie). C’est la 2e que nous utilisons actuellement. Des injections de latex dans les vaisseaux puis la dissolution des tissus adjacents ont permis d’obtenir une empreinte (un cast) et d’en voir la répartition interne. On décrit dans le foie 8 segments et 2 parties fonctionnelles (à ne pas confondre avec les lobes, qui sont des parties anatomiques). Le segment 1 est à part car vascularisé par les deux branches portales et drainé par des veines hépatiques accessoires. La bile produite se jette dans le confluent biliaire supérieur. On décrit deux « demis foies » :
- Le foie droit : vascularisé par la branche D de la veine porte, la branche D de l’artère hépatique et drainé par la branche D de la voie biliaire
- Le foie gauche : vascularisé par la branche G de la veine porte, drainé par la voie biliaire G
On a une limite, séparant les 2 foies fonctionnels, la fissure principale. Elle passe par la bifurcation portale et la veine hépatique moyenne y chemine. La limite va de la VCI au lit de la voie biliaire.

95
NB : Encore une fois, il ne faut pas confondre lobes (anatomiques) et foies (fonctionnels). C’est pourquoi lobectomie et hépatectomie ne sont pas synonymes. Foie Droit = 2 secteurs, 4 segments (5 à 8) La branche droite de la veine porte se divise en 2 branches. Cela forme des secteurs, séparés par la veine hépatique droite. Chaque branche porte sectorielle va se diviser en 2 autres branches, les branches segmentaires.
- Secteur antérieur (ou paramédian), entre la veine hépatique moyenne et la veine hépatique droite -> segments 5 et 8
- Secteur postérieur (ou latéral), entre la veine hépatique droite et la VC -> segments 6 et 7
Foie Gauche = segments 2 à 4 (lobe G + segment 4) La branche portale gauche se sépare en deux branches créant, séparés par la veine hépatique gauche, 2 secteurs :
- Secteur paramédian -> segment 4 - Secteur latéral -> segments 2 et 3
En réalité le segment 1 est vascularisé par les deux veines portes. On ne le voit que sur une vue inférieure et il n’appartient vraiment ni au foie D, ni au G. Chaque segment possède une voie artérielle, une voie biliaire et une branche porte. En revanche, le drainage hépatique ne suit pas cette systématisation. Les veines hépatiques ne sont pas terminales, contrairement à la circulation portale ou artérielle. Ceci dit, la circulation qui apparait dans un premier temps terminale n’empêche pas la mise en place de suppléances en cas d’arrêt de la vascularisation dans un secteur (les suppléances seraient assez développées, pas comme dans le cas du cerveau où la vascularisation est complètement terminale) Pour résumer, on parle d’une segmentation des pédicules glissoniens, chaque segment possédant une artère, une veine porte et une voie biliaire.

96
On décrit 3 scissures portes :
- Scissure porte principale = veine hépatique moyenne, du bord G de la VC au lit vésiculaire
- Scissure porte D = veine hépatique D, non visible à la surface du foie - Scissure porte G = ligament rond, où l’on trouve la veine hépatique G
E- Applications chirurgicales
Les segmentations anatomiques et fonctionnelles du foie diffèrent. C’est de là que vient la différence lobectomie / hépatectomie. Hépatectomie : retrait d’un foie fonctionnel
• Hépatectomie droite = segments 5, 6, 7, 8 • Hépatectomie gauche = segments 2, 3, 4
Lobectomie : ablation d’un lobe anatomique
• Lobectomie gauche = segments 2,3 • Lobectomie droite = segments 4, 5, 6, 7, 8
F- Coupes à connaitre Il y a 2 coupes axiales à connaitre.
Une coupe basse, où sont visibles les segments 3, 4, 5 et 6. Au niveau du pédicule. Le bord inférieur du lobe G = S3. Le lobe carré correspond à la partie inférieure du 4. Le 1 est entre veine porte et VC. Vascularisé par le hile (porte D et G).
Une coupe haute, avec les segments 2, 8 et 7. En T11, au niveau des confluents. On a les veines hépatiques moyenne et G qui forment un tronc commun (84% des cas).
Le 2 est à G de la veine hépatique G. Le 4 entre les 2 veines hépatiques. Le 8 entre les hépatiques moyenne et D et le 7 à D de la hépatique D.

97
II. Les voies biliaires
A- Anatomie L’artère se trouve sur le bord gauche du pédicule hépatique, alors que la voie biliaire est à droite. On a une anatomie modale (65% des cas) dans laquelle l’artère hépatique propre se divise en deux branches D et G. La voie biliaire est elle la réunion des voies biliaires D et G. La jonction entre les voies biliaires se situe plus haut que la bifurcation de l’artère. On parle par ailleurs de confluent biliaire supérieur pour la réunion des 2 voies biliaires, et de confluent biliaire inférieur quand le conduit cystique rejoint la voie biliaire principale pour former le conduit cholédoque.

98
Le canal cholédoque est au cours de son trajet : - Rétro duodénal - Rétro pancréatique - Intra pancréatique
Au niveau de l’ampoule pancréatique, il se joint au conduit pancréatique principal. La vésicule biliaire a une artère : l’artère cystique. Elle est issue de la branche D de l’artère hépatique ou de l’artère hépatique. On a soit l’un soit l’autre. Dans le premier cas elle est courte et en arrière du plan biliaire, dans le 2e elle est longue et en avant du plan biliaire.
B- Vascularisation La vascularisation artérielle des voies biliaires est sous la dépendance de l’artère gastroduodénale (7) et de l’artère hépatique (6).
L’artère hépatique va donner l’artère cystique et l’artère gastroduodénale Les arcades duodénopancréatiques vont donner l’artère gastroduodénale et l’AMS (8). A l’inverse de la vascularisation portale qui est terminale mais très anastomotique, la vascularisation biliaire va être anastomotique mais sous la dépendance d’uniquement 2 troncs. En cas de sténose du tronc cœliaque, on a une ischémie que supportent bien les hépatocytes mais pas les voies biliaires.
Le drainage veineux se fait dans le système porte directement. Les veines cystiques se jettent dans la veine porte accessoire (vont vers le foie sans passer par la veine porte), et les arcades parabiliaires, situées sur le bord G de la voie biliaire, qui vont vers la veine porte par les veines pancréaticoduodénales Il n’y a pas de veine cystique au niveau du pédicule, donc en cas de cholécystectomie on ne doit couper que 2 tuyaux : le conduit cystique et l’artère cystique. L’IRM est un bon examen pour observer les vaisseaux et voies biliaires. De plus on a possibilité de réaliser une opacification des voies biliaires :
- Cholangiopancratographie rétrograde endoscopique - Opacification par un drain chirurgical transcystique (drain placé en retirant la vésicule)
C- La lithiase biliaire La vésicule est drainée par le conduit cystique, comportant une valvule. La bile venant du foie entre dans la vésicule puis en ressort au moment des repas. Si la bile stagne dans la vésicule elle peut alors former des calculs de cholestérol ou de bilirubine, c’est la lithiase biliaire. Selon la taille des calculs il y a différentes conséquences :

99
- Un calcul qui tente de sortir de la vésicule sans y parvenir provoque une douleur biliaire, épigastrique ou à droite (autrefois appelée colique hépatique).
- Si la douleur persiste, la vésicule n’étant plus drainée on aboutit à une cholécystite aigue.
Il y a accumulation de bile puis infection, formant une sorte d’abcès (pas d’ictère car pas de compression des voies biliaires).
- Si le calcul migre et se coince dans les voies biliaires, bloquant l’évacuation de la bile, on a
une angiocholite. Douleur, fièvre et ictère = triade de l’angiocholite.
- Si le calcul migre et passe en mettant en tension le système pancréatique on a une pancréatite.
NB 1 : On décrit plusieurs complications à la lithiase biliaire, mais on oublie souvent que ces dernières peuvent être associées. NB 2 : un ictère non associé à d’autres symptômes (souvent dû à un cancer) est parfois appelé « ictère nu ». Il s’oppose à l’ictère de la triade de l’angiocholite. MAIS il vaut mieux préciser ictère sans douleur ni fièvre que d’utiliser ce terme.
D- Cholécystectomie Cholécystectomie : ablation de la vésicule biliaire, se faisant maintenant majoritairement par voie endoscopique. Sur une vue endoscopique, on voit de nombreux vaisseaux qu’il faut « griller » pour éviter le saignement. On voit le foie et sa capsule, et la vésicule attachée au foie par le péritoine. On appelle ce péritoine le mésocyste. Par ailleurs, on ne coupe que 2 éléments lors d’une cholécystectomie : conduit et artère cystiques (les veines se drainent directement dans le foie). Il ne faut pas aller chercher l’artère cystique à son origine si l’on ne veut pas abimer les voies biliaires, on reste au contact de la vésicule.
Mot du RT : - Il faut bien comprendre la segmentation hépatique (vous avez dit lourdeur ?) :
- lobe foie - hépatectomie lobectomie

100
FICHE RECAPITULATIVE
I. Le foie
A. Le lobule hépatique C’est l’unité fonctionnelle du foie. Les hépatocytes sont organisés en cocarde. Le flux porte arrive au niveau des espaces portes périphériques (canalicules biliaires + artère + veine porte), traverse l’hépatocytes de facon centripète et gagne la veine centrolobulaire. Les veines centrolobulaires se réunissent pour former les veines hépatiques qui gagneront la VCI.
B. Topographie Dans l’hypochondre droit, sous la coupole diaphragmatique droite. La vésicule biliaire repose sur le rebord chondro-costal au croisement avec le bord externe du
muscle droit. Face supérieure : diaphragme + paroi abdominale Face postérieure : VCI Face inférieure : hile du foie Carrefour hépatico-cave : sous le diaphragme, jonction entre les veines hépatique et la VC
C. Anatomie Macroscopique : Lobe gauche (20% volume hépatique) et lobe droit (80% volume) Vésicule biliaire et ligament rond délimite lobe carré. VC et ligament veineux délimite lobe caudé. Les empreintes :
- Face inf du lobe gauche : empreinte gastrique - Face inf du lobe droit : empreintes colique et rénale
D. Segmentation hépatique
Foie droit et foie gauche séparés par fissure principale (bifurcation portale + veine hépatique moyenne)
Foie droit : 2 secteurs séparés par veine hépatique droite, 4 segments vascularisés par veines branches porte segmentaires (division des 2 veines branches porte sectorielles) - Secteur antérieur : segments 5 et 8, entre veine hépatique droite et veine hépatique moyenne - Secteur postérieur : segments 6 et 7, entre veine hépatique droite et VC
Foie gauche : 2 secteurs séparés par veine hépatique gauche - Secteur paramédian : segment 4 - Secteur latéral : segments 2 et 3
Segment 1 ni foie gauche ni foie droit !!!
3 scissures : - Scissure porte principale = veine hépatique moyenne, du bord G de la VC au lit vésiculaire - Scissure porte D = veine hépatique D, non visible à la surface du foie - Scissure porte G = ligament rond, où l’on trouve la veine hépatique G
E. Applications chirurgicales Hépatectomie : retrait d’un foie fonctionnel ≠ Lobectomie : ablation d’un lobe anatomique

101
F. Coupes à connaître
II. Les voies biliaires
A. Anatomie
Voies biliaires D et G se réunissent pour former voie biliaire principale au-dessus de la bifurcation
de l’artère hépatique = confluent biliaire supérieur.
Canal cystique de la vésicule biliaire rejoint la voie biliaire principale pour former le canal
cholédoque (rétro duodénal, rétro pancréatique, intra pancréatique) = confluent biliaire inférieur.
Vésicule biliaire vascularisée par artère cystique.
B. Vascularisation des voies biliaires
Artérielle
- Artère hépatique artère cystique et artère gastroduodénale
- Arcades duodénopancréatiques l’artère gastroduodénale et l’AMS - Voies biliaires vascularisées part artère hépatique et artère gastroduodénale
Veineuse Les veines cystiques se jettent dans la veine porte accessoire et les arcades parabiliaires vont vers la veine porte par les veines pancréaticoduodénales
C. La lithiase biliaire
Bile stagne dans la vésicule et peut former des calculs de cholestérol et de bilirubine.
- Douleur biliaire : calcul n’arrive pas à sortir de la vésicule - Cholécystite aigue : vésicule non drainée, accumulation de bile puis infection, formant
comme un abcès. - Angiocholite : calcul bloqué dans les voies biliaires - Pancréatite : calcul migre et met en tension le système pancréatique
D. Cholécystectomie
Ablation de la vésicule en coupant seulement deux éléments : conduit et artère cystique

102

103
UE6 – SD – Anatomie - n°6
16/01/2017
Pr. Richard Douard
RT : DEHAENE Barbara
RL : TUTIN Mikaïl
Rectum, canal anal
Plan :
I. Le rectum A. Les coupes
i. Coupe frontale ii. Coupe axiale iii. Coupe sagittale chez l’homme iv. Coupe sagittale chez la femme
B. La vascularisation i. Les artères ii. Les veines
II. Le canal anal
A. Coupe frontale B. L’appareil sphinctérien C. Les éléments de la continence anale D. La physiologie de la défécation
III. Pathologies
A. Les hémorroïdes B. La fistule anale
IV. Le muscle élévateur de l’anus

104
Le rectum est la partie terminale du tube digestif. Il était enseigné comme ayant 2 parties : le rectum pelvien (qui correspond à ce que l’on appelle le rectum) et le rectum périnéal (qui correspond au canal anal).
Le rectum est situé dans le petit bassin et l’anus dans le périnée. Le muscle élévateur de l’anus les sépare.
L’anus est accessible par l’examen clinique de la marge anale. Le toucher rectal commence par
l’examen de la marge anale puis on met le doigt et on entre dans le canal anal puis on arrive dans le rectum.
I. Le rectum
Le rectum est dans le petit bassin, emballé dans une loge qui est la loge rectale.
La vascularisation se fait en trois étages ce qui est important pour la cancérologie.
A. Les coupes
i. La coupe frontale
On ne peut pas voir dans une même coupe frontale le canal anal et le rectum car ils ne sont pas dans le même axe : il y a un angle entre les deux : le cap anal.
A la partie terminale du tube digestif, il y a le colon sigmoïde en forme de boucle avec des
bandelettes. Au niveau de la charnière recto-sigmoïdienne, le tube digestif devient droit et sans bandelette : c’est le rectum.
Le rectum est constitué de deux parties : la partie supérieure est le rectum péritonisé car il est
recouvert de péritoine (tout comme la partie supérieure de l’utérus chez la femme), la partie inférieure quant à elle, est le rectum sous péritonéal.

105
Après le rectum, à la toute fin du tube digestif on retrouve le canal anal qui est la partie périnéale du
tube digestif. Le rectum et le canal anal sont séparés par le muscle élévateur de l’anus qui est
constitué de 2 faisceaux : le faisceaux pubo-rectal, antéro-postérieur et le faisceau sphinctérien, en forme d’entonnoir. L’anus n’appartient pas au rectum : il est périnéal.
Attention : Lorsque l’on parle de voie chirurgicale transrectale on parle en fait de la voie trans-rectus
abdominis qui correspond à une incision paramédiane à travers le droit de l’abdomen donc pas de
rapport avec le rectum !
ii. La coupe axiale
Cette coupe est effectuée au niveau sous péritonéal chez la femme. En avant on a la vessie, au milieu la partie basse du col utérin et en arrière le rectum dans la loge rectale.
En arrière du rectum on a le fascia présacral qui sépare en avant la loge rectale de en arrière l’espace
présacré. C’est dans ce dernier que l’on trouve les veines dites présacrées qui ont une tendance à se
rétracter dans l’os : pour arrêter le saignement c’est alors très compliqué on doit parfois les
punaiser. On y trouvera aussi l’artère sacrale médiane qui découle de l’aorte abdominale tout comme les artères iliaques primitives droites et gauches.
La voie d’exérèse du rectum est donc de passer entre le fascia présacral et la loge rectale.
En avant du rectum on aura la cloison recto vaginale. Un toucher bimanuel (toucher rectal + vaginal)
est nécessaire en cas de cancer de la face antérieure du rectum pour savoir s’il envahit la cloison recto vaginale. Cette cloison est mince.
Sur les côtés du rectum on a les lames sacro-recto-génito-pubiennes. Celles-ci partent du sacrum,
passent latéralement sur les côtés du rectum et de l’appareil génital et vont jusqu’au pubis. Ces lames
contiennent le plexus hypogastrique ou pelvien latéral qui est végétatif (sympathiques et
parasympathiques). Ces nerfs ont un intérêt pour la continence, l’appareil génital et pour la motricité du rectum. En revanche ces lames ne contiennent pas de nerfs moteurs et volontaires.

106
La loge rectale est donc limitée en avant par la cloison recto vaginale, en arrière par le fascia
présacral et latéralement par les lames sacro-recto-génito-pubiennes.
On trouve autour du rectum de la graisse que l’on appelle le « mésorectum » et qui est entourée par
un fascia : le fascia recti.
Lors d’un cancer du rectum, pour enlever la loge rectale, on va cliver le fascia recti ce qui va
permettre de tout enlever d’un coup. Cette méthode a été décrite par Heald.
Attention : Le mésorectum n’est pas un méso : il n’y a pas de péritoine c’est un terme.
iii. La vue sagittale chez l’homme
On voit le rectum péritonisé avec le cul de sac de Douglas.
Le rectum part du bord supérieur de la 3eme vertèbre sacrée et se termine au plancher pelvien. Il
fait 15 cm de longueur en courbe. On aura tout d’abord une courbure sacrale puis périnéale. On
décrit trois parties : la partie inférieure du rectum est sous-péritonéale, la partie supérieure est péritonisée et la partie moyenne affleure le cul de sac de Douglas, chacune fait environ 5cm.
Au niveau antérieur la courbure est petite, ainsi il sera dur de décrire la localisation des différentes tumeurs alors qu’au niveau postérieur, cela sera plus facile car la courbure est plus grande.
La loge rectale a 2 étages : le rectum péritonisé, le rectum sous péritonéal qui sont les 2 parties du rectum .
Le fascia prostatopéritonéal de Denonvillier sépare le rectum en arrière de la prostate en avant. Lors
d’un cancer on enlève cette cloison : les nerfs érecteurs passent juste en avant de cette cloison et peuvent alors être touchés ce qui peut affecter l’érection.
iv. La vue sagittale chez la femme

107
En principe on a la même chose que chez l’homme.
Au niveau du rectum sous péritonéal on retrouve la cloison rectovaginale qui descend jusqu’au
noyau central du périnée.
Le noyau central du périnée est une zone fibreuse, il est très solide chez l’homme. Il est situé entre
la face postérieure de la vulve et le bord antérieur de l’anus. Chez l’homme il est beaucoup plus palpable en arrière du bulbe spongieux de la verge.
B. La vascularisation
i. Les artères du rectum

108
Il y a 3 étages de vascularisation qui sont très anastomosés :
- L’artère rectale supérieure est la branche terminale de l’artère mésentérique inférieure : elle
se sépare en deux branches au niveau du sommet du rectum. C’est le vaisseau principal du
rectum.
- Les deux artères rectales moyennes sont des branches des artères iliaques internes. Elles
sont inconstantes et beaucoup plus petites et sont sous péritonéales.
- L’artère rectale inférieure est périnéale et naît de l’artère pudendale. Cette dernière
contourne l’épine ischiatique, passe dans le périnée par le canal pudendal et donne l’artère
rectale inférieure.
Ces trois artères vascularisent le rectum.
Il y a aussi une branche très accessoire qui est la sacrale médiane et qui donne des petites branches.
ii. Les veines du rectum
Le drainage veineux se fait principalement par la veine mésentérique inférieure qui se draine ensuite
dans le système porte en rejoignant la veine splénique pour former le tronc spléno mésaraïque et la
veine porte.
Les veines rectales moyennes se jettent dans les veines iliaques internes qui elles même se jettent
dans le système cave. Elles sont sous péritonéales.
Les veines rectales inférieures passent pas le canal pudendal et se jettent dans la veine pudendale. Celle-ci se jette dans les veines iliaques internes qui se jettent dans le système cave.
On retrouve aussi la veine sacrale médiane qui se jette dans la veine iliaque primitive gauche mais
qui est d’un intérêt vasculaire moyen.

109
En sous muqueux il peut se développer des anastomoses porto-cave lors de l’hypertension portale
notamment.
Au niveau superficiel on a les veines de la marge anale qui ne se drainent pas en pelvien mais en
fémoral. Les veines pudendales externes viennent de part et d’autre de la fémorale profonde. Ces veines sont pour le périnée et la marge annale
Sur le plan lymphatique c’est pareil.
Le cancer du canal anal est un cancer épidermoïde associé au papillomavirus (comme celui du col
de l’utérus). Il se draine en fémoral.
Le cancer du rectum est un adénocarcinome car c’est la paroi épithéliale du rectum qui dégénère. Il se draine vers les vaisseaux mésentériques inférieurs.
Cela n’est pas absolu (dès fois le rectum se draine dans le réseau iliaque interne) notamment le bas
rectum le long des artères rectales moyennes.
Il y aura donc des ganglions qui suivent les artères donc dans le cas d’une ablation du rectum on
enlève l’artère mésentérique inférieure et les ganglions se trouveront le long des vaisseaux iliaques internes ou des artères fémorales.
II. Le canal anal
A. La coupe frontale
On voit entre la ligne ano-rectale et la ligne pectinée des colonnes de muqueuses glandulaires. Au
sommet de ces cryptes c’est la ligne ano-rectale qui sépare le rectum du canal anal. Les valvules semi-lunaires sont au niveau de la ligne pectinée.

110
On a donc deux parties dans l’anus : une partie rouge avec une muqueuse glandulaire et une partie
sous la ligne pectinée qui est le canal anal avec une muqueuse malpighienne non kératinisée. Au niveau de la marge anale on a une muqueuse malpighienne kératinisée et des poils.
La ligne pectinée est un résidu de la membrane cloacale qui sépare l’épiblaste de l’entoblaste.
B. L’appareil sphinctérien du canal anal
On voit de part et d’autre deux sphincters :
- Le sphincter interne lisse est l’épaississement de la couche circulaire interne du rectum. Il
est végétatif.
- Le sphincter externe quant à lui est strié et donc volontaire. Il est divisé en 3 parties.
Entre les deux sphincters on a la couche longitudinale qui se transforme en ligament de Parks au
niveau de l’anus. Il fixe la muqueuse du canal anal et traverse le faisceau sous cutané du sphincter
externe : des fibres de la couche longitudinal se fixent sous la peau en traversant la partie sous
cutanée du sphincter. Cet attachement donne l’aspect ridé car il y a des plis dus au fait que le
sphincter externe soit attaché à la partie profonde de la peau par la couche longitudinale externe qui sépare les faisceaux du sphincter externe sous cutané et va permettre d’avoir l’aspect plissé.
En sous muqueux on a des plexus hémorroïdaires. Les hémorroïdes sont des plexus artério-veineux :
ce sont les artères qui saignent. Il y a des anastomoses artérielles entre les artères rectales
inférieures issues et drainées par les pudendales, et les rectales moyennes et supérieures. Il en est
de même au niveau veineux. Au-dessus du ligament de Parks on parle d’hémorroïdes internes et en
dessous d’hémorroïdes externes. Les deux sont associés et anastomosés.
Il y a 3 faisceaux au sphincter strié externe :
- Le faisceau superficiel s’attache par le ligament ano-coccygien au coccyx. Il s’attache aussi
sur le noyau central du périnée en avant.
- Le faisceau profond qui correspond au faisceau pubo-rectal du muscle élévateur de l’anus
qui est une sangle. Il maintient le tonus et l’angle entre le rectum et l’anus. Lorsque l’on fait

111
un toucher rectal on sent un angle et c’est celui-là. Le faisceau pubo-rectal passe autour du
noyau central du périnée.
- Le faisceau sous-cutané qui est perforé par les fibres issues de la couche longitudinale du
rectum et qui va fixer ce faisceau à la peau et donner les rides de l’anus.
L’ensemble va permettre une pression volontaire qui va permettre de maintenir l’occlusion de
l’anus.
C. Les éléments de la continence anale
Avec l’âge la continence anale peut être altérée : cela fait partie des éléments à prendre en compte lors du vieillissement. Un des principaux facteurs de l’incontinence est le tabac.
Il y a plusieurs facteurs de la continence :
- L’angle ano-rectal maintenu par la sangle pubo-rectale assure une continence. La pression
abdominale appuie sur le centre tendineux du périnée et sur le ligament ano-coccygien et
ouvre l’angle ano-rectal. Si le rectum est dans l’axe de l’anus il sera difficile d’avoir une
continence si les matières sont lourdes.
- Les tonus sphinctériens internes et externes permettent l’occlusion du sphincter.
- La consistance des selles. Il est physiologique que des selles liquides entrainent une
incontinence annale. Pendant une gastro on a des troubles de la continence.
Il y a trois types d’incontinence :
- Motrice : Les muscles sphinctériens ne fonctionnent plus. Par exemple les sphincters
peuvent être sectionnés par un traumatisme périnéal lors d’un accouchement car la ligne
d’explosion du périnée a effondré le sphincter.
- Neurologique : Altération ou section nerveuse qui amène les infos.
- Sensorielle : Pas d’information sur la contenance du rectum : il n’est donc pas possible
d’avoir une action adaptée.
D. Physiologie de la défécation
L’appareil sphinctérien est sous commande végétative et somatique.
Tout d’abord on a une sensibilité végétative qui est la sensibilité proprioceptive à la distension du
sphincter interne et de la partie inférieure du rectum. On a une espèce de pesanteur qui arrive au
cerveau et on sent qu’il se passe quelque chose. Ces informations proviennent du plexus
hypogastrique qui passe par les lames sacro-recto-génito-pubiennes. Le sympathique passe par le tronc latéro-vertébral tandis que le parasympathique passe par les racines sacrées.
La motricité végétative sympathique contracte le sphincter interne alors que le parasympathique
l’inhibe. Ainsi lors d’un malaise vagal ou lors d’une grosse stimulation vagale il n’est pas rare d’avoir une perte d’urine ou de matière.
Le réflexe végétatif recto-anal inhibiteur : quand les selles arrivent dans le rectum il y a une
distension de la partie inférieure avec un axe réflexe qui aboutit à la baisse du tonus du sphincter
interne. C’est-à-dire que spontanément quand les matières arrivent, le sphincter s’ouvre. Ce n’est
pas contrôlable. On voit cela aussi chez les nourrissons qui n’ont pas la maturité neurologique de contrôler cela. Lors d’une maladie de Hirschprung on a perte de ce réflexe.

112
Il y a beaucoup de récepteurs dans la partie basse du rectum et dans l’anus (au chaud, au froid…).
Ainsi quand le sphincter interne se distant on sait ce qu’il y a dans notre anus et on adopte l’attitude
adaptée. Ces informations passent par le plexus pudendal avec le nerf anal qui passe par l’extérieur
latéro-anal et dans le canal pudendal puis sort par l’échancrure ischiatique, contourne l’épine et va
dans le canal d’Alcock (=canal pudendal).
Ainsi, lors d’une chirurgie du rectum on peut traumatiser le plexus hypogastrique mais pas le
pudendal ce qui conservera la sensibilité et la motricité somatique.
Les nerfs anaux et pudendaux amènent une contraction du pubo-rectal qui va maintenir l’angle
anorectal et le tonus des faisceaux sous cutanés et superficiel pour maintenir une continence volontaire mais épuisable.
Lors d’une chirurgie du rectum on diminue la sensibilité (suppression du rectum, altération de la
partie haute du canal anal). Ainsi le patient est informé que les selles arrivent au dernier moment.
De même lors d’une anastomose colo-anale on a altéré les récepteurs et souvent il y a un certain degré d’incontinence après. Il faudra alors une rééducation par la suite.
Le syndrome de fractionnement des selles consiste en un tranchement des selles : on doit aller aux
toilettes plusieurs fois de suite. C’est le résultat de l’ablation du rectum.
III. Les pathologies
A. Les hémorroïdes
Il y a beaucoup de malades qui sont adressés comme ayant des hémorroïdes même si cela n’est pas
le cas. Par exemple : fistule anale, cancer, fissure anale, etc…
C’est une pathologie vasculaire avec un certain degré de prolapsus muqueux qui peut survenir chez des malades constipés.

113
Les hémorroïdes peuvent être internes ou externes.
En position gynécologique, on retrouve des sièges de prédilection des paquets hémorroïdaux à 3h,8h et 11h.
Cela consiste en un développement de la muqueuse qui va se prolaber. On aura alors des replis muqueux qui vont s’extérioriser à la défécation selon les grades.
Hémorroïdes selon les grades :
- 2 : joufflus
- 3 : ils sortent et rentrent avec les selles ce qui est très désagréable
- 4 : ils sont tous le temps sortis
Les hémorroïdes sont des coussinets qui servent à l’occlusion de l’anus donc quand on souhaite les
retirer on ne peut pas enlever toute la muqueuse : on enlève juste les paquets mais on doit laisser
de la muqueuse sensible entre les paquets car sinon cela provoquerait une incontinence sensorielle. Si on enlève toute la muqueuse on peut aussi avoir une sténose anale mais cela est rare aujourd’hui.
B. Les fistules anales
Au niveau de la ligne pectinée on a les glandes d’Hermann et Desfosses.
Ces glandes s’ouvrent dans le fond des cryptes mais on ne connait pas leur fonction. Elles sont
profondes en inter sphinctérien c’est-à-dire entre la couche circulaire et longitudinale et parfois elles se bouchent.
Une fois que l’abcès est constitué, il va, pour s’évacuer soit de nouveau dans la glande (c’est la
guérison) soit s’extériorisé à la surface de la peau : c’est ce que l’on appelle une fistule anale car il
met en communication par l’intérieur de la glande et par l’intermédiaire de l’abcès l’anus à l’extérieur.
Le trajet de la fistule pourra être inter sphinctérien c’est à dire entre les sphincters interne et
externe. Dans ce cas on coupe un peu de sphincter interne mais dans certains cas elle est plus loin
de la marge anale et dans ce cas on coupe le sphincter. Chez un homme le sphincter est plus solide

114
que chez la femme. Ainsi si la fistule est antérieure chez la femme cela se compliquera
d’incontinence.
Le trajet de la fistule peut aussi être transphinctérien à travers le sphincter interne et le sphincter
externe.
IV. Le muscle élévateur de l’anus
Il sépare le rectum du canal anal.
Il a deux faisceaux :
- Le faisceau pubo-rectal
- Le faisceau sphinctérien qui correspond au plancher pelvien.

115
FICHE RECAPITULATIVE
Le rectum est la partie terminale du tube digestif, on le distingue du colon sigmoïde car le rectum
est droit et sans bandelette.
Le rectum est pelvien,
Le canal anal est périnéal
/!\ Anus (dans le périnée) ≠ rectum (dans le petit bassin)
Le muscle élévateur de l’anus les sépare.
Quelques Rapports :
Sur les faces latérales du rectum on a les lames sacro-recto-génito-pubienne contenant le plexus
hypogastrique ou pelvien latéral qui est végétatif.
En arrière du rectum on a le fascia présacral qui sépare en avant la loge rectale de l’espace
présacré
Chez la femme on a le cul de sac péritonéal dit de Douglas (recto-vaginal) et 3 loges
(rénale,génitale et rectale)
Chez l’homme on a le fascia prostatopéritonéal Denonvillier (entre rectum et prostate) et 2 loges
(uro-génitale et rectale)
Le rectum comporte 2 étages :
- Péritonisé
- Sous péritonéal
Au niveau périnéal c’est le canal anal
- Périnéal= canal anal (délimité par la ligne ano-rectale)
Le rectum et le canal anal sont vascularisés par trois pédicules
Vascularisé par 3 artères :
- Artère Rectale Supérieure née de l’artère mésentérique inférieure
- Artère Rectale moyenne née de l’artère iliaque interne
- Artère Rectale inférieure née de l’artère pudendale
Drainé par 3 veines :
- Veine Rectale supérieure vers veine mésentérique inférieure (système porte)
- Veine Rectale moyenne vers veine iliaque interne (système cave)
- Veine Rectale inférieure vers veine pudendale (système cave)
Sphincters :
Un sphincter interne interne lisse (= épaississement de la couche circulaire interne du rectum) végétatif et un sphincter externe strié volontaire
Il y a 3 faisceaux au sphincter strié externe :
- Le faisceau superficiel
- Le faisceau profond (= faisceau pubo-rectal du muscle élévateur de l’anus) permettant le maintien
de l’angle entre rectum et anus
- Le faisceau sous-cutané (donne les rides de l’anus)
Physiologie de la défécation :
1) Récepteurs +++ sensibles à la distension du sphincter interne et de la partie inférieure du rectum.
Ces informations provenant du plexus hypogastrique qui passe par les lames sacro-recto-génito-pubiennes sont transmises au cerveau

116
2) Situation a : t’es en plein marathon c’est pas le moment !!! -> La motricité végétative sympathique
contracte le sphincter interne
Situation b : tu es en condition prêt à lâcher la bête -> le parasympathique inhibe la contraction
du sphincter interne
Innervation de 2 types :
-somatique, motrice : muscle élévateur de l’anus
-végétative défécation et continence des selles (une part somatique (volontaire) et végétative
(involontaire)).
Les nerfs anaux et pudendaux (somatique) amènent une contraction du pubo-rectal qui va maintenir
l’angle anorectal, le tonus des faisceaux sous-cutané et superficiel du sphincter pour maintenir une
continence volontaire maist épuisable.
Attention Chirurgie : par voie abdominale on peut léser les nerfs le plexus hypogastrique mais pas
le pudendal ce qui conservera la sensibilité et la motricité somatique. De plus, réduire la taille du
rectum e rectum implique moins de récepteurs donc on ressent le besoin plus tard
Maladie de Hirschsprung => absence de réflexe recto-anal inhibiteur =>
Ce réflexe ouvre spontanément le sphincter interne lorsque les matières arrivent. Le réflexe
rectoanal inhibiteur est normal, c’est son absence qui caractérise la maladie de hirschprung.
Malaise vagal => risque d’incontinence
Incontinence :
3 types : - motrice : problème musculaire
- neurologique : altération nerveuse
- sensorielle : 0 information
La consistance des selles joue aussi un rôle
Les Pathologies :
Les fistules Les hémorroïdes Il y a des glandes au niveau anal qui peuvent se boucher et former un abcès 2 cas :
L’abcès s’évacue de nouveau par la glande (= Tout va bien ouf)
L’abcès s’évacue par la peau (beuuurk)
Le trajet de la fistule peut être : - Inter sphinctérien (= entre sphincters
internes et externe) - Transphinctérien
Vaisseaux se dilatent et tombent formant un prolapsus muqueux
2 types : internes ou externes suivant leur position par rapport au ligament de Parks
Muscle élévateur de l’anus :
2faisceaux : -> Le faisceau pubo-rectal -> Le faisceau sphinctérien (=plancher pelvien)

117
UE6 – SD– Pharmacologie – n°2
20 janvier 2017
Laurent Chouchana
RT : Nicolas Delobel
RL : Anne-Lise Vouillot
Antisécrétoires et antiacides, médicaments de la
motilité digestive
Plan :
I. Antisécrétoires et antiacides A. Définitions d’atteintes digestives B. Rappels physiologiques C. Traitements : classes pharmaco-thérapeutiques
i. Antiacides gastriques ii. Antisécrétoires iii. Analogues des prostaglandines
II. Médicaments de la motilité digestive
A. Antiémétiques
i. Prokinétiques ii. Antagonistes 5-HT3 (setrons) iii. Antihistaminiques
B. Anti-diarrhéiques i. Ralentisseurs du transit ii. Anti-sécrétoires
C. Laxatifs i. Laxatifs de lest ii. Laxatifs lubrifiants iii. Laxatifs osmotiques iv. Laxatifs irritants ou stimulants v. Laxatifs par voie rectale

118
I. Antisécrétoires et antiacides
A. Définitions d’atteintes digestives
• La gastrite, de forme aiguë ou chronique, correspond à une inflammation de la muqueuse
gastrique. On la diagnostique grâce à l’endoscopie. Elle donne à voir, à l’échelle histologique, des
lésions inflammatoires et atrophiques de la muqueuse gastrique.
• L’ulcère gastroduodénal consiste en une perte de substance de la muqueuse et de la paroi de
l’estomac ou du duodénum. On observe une infection par l’Helicobacter pylori dans 85 % des cas
d’ulcère gastrique ainsi que dans 95 % des cas d’ulcère du duodénum.
• Le Reflux Gastro-Œsophagien (RGO) est le passage à travers le cardia d’une partie du contenu
gastrique dans l’œsophage. On le nomme couramment « aigreur » ou « brûlure ».
• L’œsophagite par reflux, inflammation de la muqueuse œsophagienne, est une conséquence
du RGO que l’on observe chez un quart des patients qui en souffrent.
• L’hernie hiatale, enfin, correspond à la protrusion par glissement, entière ou partielle, de
l’estomac dans le thorax à travers le hiatus œsophagien du diaphragme.
B. Rappels physiologiques
L’histamine, l’acétylcholine (neuromédiateurs), et la gastrine (hormone) activent la pompe à proton
de la cellule pariétale de l’estomac.
Il y a toujours un équilibre entre les mécanismes d’agression de la muqueuse (HCl, pepsine,
gastrine) et de protection (mucus, bicarbonates, cytoprotection, flux sanguin, prostaglandines E).

119
Le pH de la lumière gastrique est à 1-2.Il y a production de 2,5 L/24H de suc gastrique
digestion du bol alimentaire.
C. Traitements : classes pharmaco-thérapeutiques
Il y en a trois :
- Les topiques gastriques
- Les anti-sécrétoires (inhibiteurs de la pompe à protons (IPP) et antihistaminiques anti-H2)
- Les analogues des prostaglandines (très peu utilisés)
Le traitement du RGO et de l’œsophagite :
1) Prise en charge :
- suppression du tabac et de la prise d’AINS
- règles hygiéno-diététiques plus ou moins efficaces (surélévation de la tête du lit, amaigrissement,
suppression de la sieste postprandiale, qui favorise le reflux, réduction des repas riches en graisse
et en sucre …)
- les médicaments
2) Objectifs du traitement :
- diminuer les symptômes
- réduire la fréquence et la durée des reflux
-cicatriser l’œsophagite
-prévenir récidive et complications

120
i. Antiacides topiques : « pansements gastriques »
Mécanisme d’action :
Les antiacides forment un gel visqueux en « raft » (radeau) au-dessus du bol alimentaire au contact
de l’acidité gastrique : ils constituent donc une protection mécanique contre l’acidité, car, en cas
de reflux, c’est le gel qui est régurgité le premier, formant ainsi une barrière entre la muqueuse
œsophagienne et le liquide gastrique acide.
Effets indésirables :
Ils sont rares, et consistent principalement dans la neutralisation des médicaments associés, piégés
dans le gel, qui sont alors inefficaces.
Précautions d’emploi :
À prendre à distance des repas, et avec un intervalle de une à deux heures avec tout autre
médicament.
Le Gaviscon®, composé d’alginate et de bicarbonate de sodium, se prend en flacon ou sachets
unidoses. En plus de l’effet mécanique, il neutralise l’acidité de l’estomac. Il n’est pas prescrit pour
des prises prolongées, et l’on doit faire attention à la présence de sodium. Ses effets indésirables sont
la constipation (à cause de l’aluminium), la diarrhée (à cause du magnésium), et les interactions
médicamenteuses (inefficacité des traitements associés).
Le Diméticone (Polysilane®), est prescrit, lui, plutôt chez les nouveaux-nés. Il peut causer des
réactions allergiques. On doit faire attention à la présence de saccharose et de sorbitol.
Le Smecta® a une action uniquement mécanique, mais il est moins efficace que le Gaviscon®.

121
ii. Antisécrétoires
Les antihistaminiques anti-H2 :
Leur mise sur le marché en 1988 a révolutionné le traitement de l’ulcère gastroduodénal, mais la première molécule commercialisée, la cimétidine (Tagamet®), est peu utilisée actuellement car c’est un inhibiteur enzymatique.
Mécanisme d’action : ils opèrent une inhibition compétitive des récepteurs H2 de l’histamine situés sur les cellules pariétales, mais non un blocage complet de la pompe à protons.
Le Ranitidine (Azantac®, Raniplex®), peut être pris per os (300 mg/jour le soir), ainsi que par IV lente ou IM (50 mg, de une à quatre fois par jour), pour des patients en réanimation, par exemple. Il est indiqué pour : les ulcères gastroduodénaux (après avoir vérifié l’absence de lésion cancéreuse), l’œsophagite par reflux, le RGO, le syndrome de Zollinger-Ellison, et comme traitement préventif ou curatif des lésions causées par les AINS. Ses effets indésirables sont rares et bien tolérés :
- troubles digestifs, céphalées, éruptions - état de confusion, surtout chez le sujet âgé et l’insuffisant rénal - bradycardie sinusale - leucopénie, thrombopénie, agranulocytose (rare) - commun à tous les antisécrétoires : risque de développement de certaines bactéries
par diminution de l’acidité gastrique
Les inhibiteurs de la pompe à proton (IPP) : Leur mise sur le marché en 1996 a de nouveau opéré un grand renouvellement dans le traitement de l’ulcère gastroduodénal, au point que la première molécule, l’oméprazole (Mopral®), a longtemps été le médicament le plus vendu au monde.
Rappels physiologiques : la pompe à proton dépend des enzymes et du magnésium, pour assurer l’échange d’un proton contre un ion potassium à travers une membrane. Cela entraîne la formation d’HCl et cause l’acidité gastrique. Mécanisme d’action :

122
Ils inhibent la pompe à proton de manière irréversible quel que soit le mode de stimulation de celle-ci, après avoir été absorbés par l’intestin, distribués dans l’organisme sous forme non-ionisée, métabolisés par le foie, puis sécrétés au niveau des cellules gastriques. Ils se prennent généralement sous forme de comprimés gastro-résistants, qui n’agissent donc pas par contact direct avec la muqueuse intestinale. Une prise unique assure une inhibition de près de 24 heures, le temps de demi-vie de renouvellement des pompes à protons.
Médicaments : Oméprazole (Mopral®), Ésoméprazole (Inexium®), Lansoprazole (Langor®, Ogast®), Rabéprazole (Pariet®), sont des molécules proches et de même efficacité, le choix n’est qu’une question de marketing. Indications : ulcères gastro-duodénaux, œsophagite par reflux, RGO, syndrome de Zollinger-Ellison,
traitement préventif ou curatif des lésions causées par les AINS.
L’utilisation hors de l’AMM, du fait d’une incitation importante des laboratoires, ainsi que
l’automédication (en vente libre), sont importantes. Or ce sont des médicaments coûteux, et non
sans risque.
Les effets indésirables sont rares mais largement observés du fait de la prescription importante :
- hypersensibilité - hépatites - pneumopathies - infections à C. difficile - thrombopénies - néphropathies interstitielles - hyponatrémie - hypomagnésémie, hypocalcémies importantes => risque de fractures - anémie (moins bonne absorption du fer) - interactions médicamenteuses (car inhibition du CYP2C19) : clopidogrel, atzanavir, MTX … - effet rebond à l’arrêt du traitement
iii. Analogues des prostaglandines Le Misoprostol (Cytotec®) : 100 à 200 g quatre fois par jour (courte durée)

123
Mécanisme d’action : analogue de la PG1, il a un effet antisécrétoire et cytoprotecteur Effets indésirable : dans l’ensemble, il est mal toléré, les troubles digestifs (diarrhées) fréquents le font peu utiliser ; on observe aussi des nausées et vomissements. Contre-indication : femmes enceintes (risque de fausse-couche => utilisé en obstétrique pour l’IVG)
II. Médicaments de la motilité intestinale
A. Antiémétiques
Objectifs pédagogiques :
– Devant des vomissements, argumenter les principales hypothèses diagnostiques et justifier les
examens pertinents
– Argumenter l’attitude thérapeutique et planifier le suivi et l’évolution
Les nausées et vomissements sont des symptômes très fréquents dus à des affections diverses (étiologies nombreuses), et non des maladies.
Définitions :
Le vomissement est un rejet brutal du contenu de l’estomac par la bouche.
Les « hauts le cœur » sont des contractions synchrones et rythmiques du diaphragme, des
muscles abdominaux, et des muscles intercostaux externes, contre la glotte fermée.
La nausée est la sensation subjective, désagréable, d’une envie imminente de vomir.
Les vomissements sont possibles sans nausées et hauts le cœur, et vice versa !
Objectifs du traitement :
– Traiter les vomissements eux-mêmes
– Prévenir les perturbations hydro-électrolytiques et une éventuelle dénutrition
– Traiter si possible la cause (non abordé ici)
Mesures diététiques :
– Fragmenter les repas
– Diminuer l’apport de graisse
– Supprimer les boissons gazeuses
– Régime à adapter (liquide ou mixé)
Physiopathologie du vomissement : c’est un processus réflexe complexe contrôlé par le centre du
vomissement qui recoit des informations d’une zone spécifique du cerveau, la « CTZ » :
Chemoreceptor Trigger Zone. De nombreux récepteurs ont été identifiés : récepteurs
sérotoninergiques, dopaminergiques, histaminergiques, et récepteurs aux opiacés.

124
i. Prokinétiques
Le Domperidone (Motilium®) et le Métoclopramide (Primperan®), sont des dérivés neuroleptiques antagonistes de D2, ils stimulent l’activité motrice du tube digestif.
Leurs effets indésirables : sédatifs (pas la dompéridone car ne passe pas la barrière hémato-encéphalique) ; cardiaques (allongement du QT et risque de torsades de pointe) => contre-indiqués en pédiatrie ; neurologiques (rigidité musculaire, parkinsonisme = syndrome extrapyramidal)
ii. Antagonistes 5-HT3 (setrons)
L’Ondansetron (Zophren®), et le Granisetron (Kytril®) bloquent les récepteurs centraux et périphériques 5-HT3 à la sérotonine. Ils sont indiqués en prévention et traitement des nausées aiguës induites par les chimiothérapies
Leurs effets indésirables : céphalées, vertiges (fréquent) ; bouffées de chaleur, flush (fréquent) ; constipation (fréquent), voire occlusion intestinale (rare) ; troubles du rythme et de la conduction allongement du QT, en particulier par voie intraveineuse (rare) ; réaction au point d’injection (fréquent).
iii. Antihistaminiques
Le Diphénhydramine (Nautamine®) est indiqué pour le mal des transports. Il a des propriétés annexes atropiniques ou anticholinergiques contre-indication en cas de glaucome à angle fermé et d’adénome de prostate.

125
B. Anti-diarrhéiques
Objectifs pédagogiques : – devant une diarrhée aiguë chez l’adulte, argumenter les principales hypothèses diagnostiques et
justifier les examens complémentaires pertinents.
– argumenter l’attitude thérapeutique et planifier le suivi du patient.
Rappels physiologiques : une diarrhée aiguë est définie par l’émission de plus de trois selles par
jour, les selles dépassant 300 g par 24 heures. Son origine est infectieuse ou médicamenteuse. Elle
est souvent bénigne dans les pays occidentaux, en l’absence d’immunosuppression, mais est une
cause majeure de mortalité infantile dans les pays pauvres.
Traitement des diarrhées aiguës : – Symptomatique : réhydratation +++ => per os : solution OMS ou Coca-cola rouge (dilué au demi,
avec jus de citron pour l’apport en potassium) ; perfusion intraveineuse si déshydratation sévère.
– Eviter les laitages et précaution avec les crudités.
i. Ralentisseurs du transit
Le Loperamide (Imodium®) est un dérivé morphinique à action périphérique. Sa posologie est de 1-2 gélules de 2 mg puis 1 gélule après chaque selle non moulée (MAX 8 gélules/24 h).
Ses effets indésirables : la constipation
Contre-indication : si fièvre ou suspicion de diarrhée bactérienne (risque de stase et d’aggravation de l’infection) ; chez le nourrisson de moins de 2 ans (risque de troisième secteur par accumulation des liquides dans le tube digestif)
ii. Anti-sécrétoires Le Racécadotril (Tiorfan®) est un inhibiteur de l’enkephalinase (enzyme de l’épithélium intestinal) => prolonge la durée d’action de l’enképhaline et réduit l’hypersécrétion d’eau. Il n’a pas d’effet sur le transit intestinal.
Ses effets indésirables : céphalées, risque d’angio-œdème et d’urticaire.
C. Laxatifs
Objectifs pédagogiques :
– Devant une constipation : argumenter les principales hypothèses diagnostiques et justifier les
examens complémentaires pertinents.
– Argumenter l’attitude thérapeutique et planifier le suivi du patient.
Rappels physiologiques : la constipation n’est pas une maladie mais un symptôme.
Sa définition clinique : diminution du nombre de selles qui devient inférieur à trois par semaine.
Sa définition physiopathologique : association d’un ralentissement du transit supérieur à 72H
et d’une déshydratation excessive.

126
C’est un symptôme très fréquent qui concerne 15-20% de la population.
Traitement de la constipation :
– Le traitement de la cause (non exposé ici) => nombreuses étiologies
– Mesures hygiéno-diététiques : repas au calme à heures fixes , en mâchant bien lentement ; boire
abondamment ; manger des légumes verts, de la salade, des céréales ; pratiquer une activité
physique régulière (renforcement de la sangle abdominale)
– Traitement symptomatique après avoir éliminé une cause organique : laxatifs de lest, lubrifiants,
osmotiques, irritants, par voie rectale.
i. Laxatifs de lest
Le Mucilage pur Ispaghul (Spagulax®) est composé de fibres alimentaires, à consommer toujours
accompagnées d’eau => augmentation du volume et de l’hydratation, et progression du bol
alimentaire.
La posologie doit être très progressive en raison du risque de ballonnement
Pas de prise après le dîner => risque d’occlusion, en particulier chez le sujet âgé insuffisamment
hydraté.
Contre-indications : colopathies organiques, syndrome occlusif, syndrome abdominal de cause
indéterminée, fécalome.
ii. Laxatifs lubrifiants
Ils sont composés d’huile de paraffine ou huile de vaseline, et ont un délai d’action de 6 à 8
heures.
Ils sont à ne pas prendre le soir, et à ne pas utiliser de façon prolongée => réduction de résorption
de vitamines liposolubles : A, D, E, K.
Les enfants, personnes âgées, personnes alitées présentent un risque d’inhalation pulmonaire en
particulier en cas de RGO.
La durée maximale est de 15 jours.
iii. Laxatifs osmotiques
Le Lactulose (Duphalac®), et le Macrogol (Forlax®) sont des polymères linéaires de haut poids
moléculaire hydrophiles, qui provoquent un mouvement d’eau entrainant une augmentation de
volume.
Pas de traitement prolongé. Attention au sucre : présence de galactose.
Contre-indications : colopathies organiques, syndrome occlusif, syndrome douloureux abdominal
de cause non connue.
iv. Laxatifs irritants ou stimulants
Les Sennosides calciques (Pursennide®) stimulent la motricité colique.
Contre-indications : enfants, femmes enceintes, personnes âgées, colopathie organique, syndrome
occlusif, syndrome douloureux abdominal de cause non connue
Ils présentent un risque d’hypokaliémie.

127
Une prise prolongée entraîne une maladie des laxatifs (diarrhées, douleurs abdominales) => pas
de place dans la thérapeutique actuelle
v. Laxatifs par voie rectale
Ce sont des suppositoires à la glycérine, non adaptés à un traitement prolongé. Ils sont prescrits aux
personnes âgées, et exceptionnellement aux enfants.
Parmi tout ce qui a été vu dans ce cours, les médicaments ne sont pas au premier plan de la prise en charge de la constipation !!!

128

129

130

131
UE6 – SD – Biochimie – Cours n°1
20/01/2016
Marie-Anne Loriot
marie-anne.loriot@hegp/aphp.fr
RT : Claire Denery
RL : Hélène Watchel
Principes biochimiques des ictères
I. Métabolisme de la bilirubine
II. Méthodes de dosage
A. Sérum ou plasma
B. Autres liquides biologiques
III. Méthodes de dosage
A. Ictères pré-hépatiques
i. Description
ii. Causes d’hémolyse intravasculaire
B. Ictères hépatocellulaires
C. Ictères post-hépatiques
D. Hyperbilirubinémies héréditaires chroniques
i. Hyperbilirubinémies à prédominance non conjuguée :
déficit de conjugaison
ii. Hyperbilirubinémies à prédominance conjuguée : défaut
d’excrétion, de captation ou de stockage

132
Introduction:
Un ictère est le résultat d’une accumulation excessive de bilirubine.
La bilirubine est le produit final de dégradation du métabolisme de l'hème, l'hème étant un
composant des hémoprotéines mais en particulier dans l'hémoglobine puisqu'il est responsable
de la fixation de l'O2 (noyau tétra-pyrrolique qui fixe un atome de fer, le tout permettant la
captation de l'O2). Mais la bilirubine provient aussi de la dégradation d'autres hémoprotéines
comme la myoglobine, les cytochromes (P450...) ainsi que d'enzymes anti oxydantes comme les
catalases...
La production de bilirubine n'est pas négligeable puisqu'elle est en moyenne de 0,5 mmoles
(300mg) par jour.
Son catabolisme débute dans le Système Réticulo-endothélial, principalement dans les
macrophages de la rate, mais également dans le foie et la moelle, et se termine dans le foie. Il y
a aussi une étape d'élimination de la bilirubine dans la bile (composera ensuite les pigments
biliaires).
Le rôle de la bilirubine dans la circulation est d'être un antioxydant, ce qui est important chez
le nouveau-né, mais l'on verra aussi que l'accumulation de bilirubine libre peut être la cause de
problèmes neurologiques extrêmement graves.
La situation dans laquelle on pourra parler d'ictère, est celle d'une élévation de la
concentration de bilirubine plasmatique >70 μmol/L, entraînant alors une coloration jaune
des téguments (jaunisse en langage populaire).
I. Métabolisme de la bilirubine
Avant toute chose, l’hème a une structure aromatique ou porphyrine, constituée de quatre
noyaux pyrrols.
Au terme des 120 jours moyens de vie des globules rouges, ces derniers vont être détruits.
L'hémoglobine ainsi libérée va rentrer dans un cycle de dégradation. L'hème des globules
rouges sénescents (80%), mais aussi l’hème provenant d'autres enzymes hépatiques et d'autres
protéines (20%), va alors être prise en charge par l'enzyme Hème Oxygénase.

133
Cela va permettre l'ouverture du cycle de l'hème et aboutir à une première molécule : la
biliverdine (colorée en vert), qui sera convertie ensuite en bilirubine (colorée en jaune)
(phénomène observé au niveau d’un ecchymose: d’abord bleue puis verte puis jaune).
Il persiste deux problèmes majeurs dans le métabolisme de l'hème :
Le noyau porphyrine de l’hème est hydrophobe et doit être solubilisé pour être excrété.
Le fer qui est libéré lors de la dégradation de l'hème doit être conservé pour maintenir
le pool de réserve et servir à la nouvelle synthèse d'hème (NB : le fer ne peut pas être
directement excrété de l’organisme; il faut donc le recycler, le stocker et le réutiliser).
Le métabolisme de l'hème : deux enzymes impliquées
L'hème oxygénase : c'est une enzyme du réticulum endoplasmique qui est
responsable de l'oxydation et donc de l'ouverture du cycle tétrapyrrolique de l'hème
avec liberation de Fe3+ et de CO. Elle consome de l’O2 et du NADPH.
La biliverdine réductase : c'est une enzyme cytosolique, qui va catalyser une réaction de
réduction. Elle utilise aussi le NADPH.
Il s’agit de la seule réaction de l’organisme qui produit du CO (le CO est donc un indicateur du
catabolisme de l’hème).
NB : lorsque que l'on se fait un bleu (ecchymose), la
couleur évolue dans le temps. Au départ il est bleu,
vert puis jaune. Il s'agit de la réaction de dégradation
de l'hème.
Une fois que l'on a produit cette bilirubine, elle ne peut pas rester libre car elle est très toxique
sous cette forme, notamment pour le cerveau (neurotoxique). Elle va donc être éliminée dans
la bile, en suivant plusieurs étapes.
Présente dans la rate, la bilirubine va être libérée dans la circulation où elle sera prise en charge
par l'albumine (transporteur de la bilirubine qui permet sa captation par le foie). La bilirubine
liée à l'albumine va pouvoir ainsi être captée par les hépatocytes. Dans le foie la bilirubine
sera conjuguée. Cette bilirubine conjuguée devient alors un produit hydrosoluble,
permettant son passage dans la bile, passage permis par un transporteur (ABCC2/MRP2).
L’excrétion biliaire est l’étape limitante du métabolisme donc il faut une coordination étroite
avec la conjugaison.

134
Une fois dans la bile, la bilirubine conjuguée va dans l'intestin et est transformée (étape de
déconjugaison de la bilirubine) par les bactéries intestinales en urobilinogène incolore.
Une grande partie de l’urobilinogène
(90%) pourra être transformée en
stercobilinogène qui va être oxydé
dans la partie basale de l’instestin en
stercobiline, qui est éliminée dans les
selles (c'est un pigment brun, qui
permet la coloration foncée des selles).
L’autre partie de l'urobilinogène (10%) va rejoindre la circulation entrainant un retour vers le foie
par le système porte, puis retourne vers l’intestin via l’excrétion biliaire. C’est le cycle entéro-
hépatique. L’urobilinogène qui se retrouve dans la circulation peut aussi être captée par le rein
où elle subit des étapes d’oxydation et devient l’urobiline (permet une légère coloration des
urines). Les urines deviennent trop colorées quand il y a un excès. On peut ainsi détecter de
l’urobiline dans les urines sans que ce soit pathologique.
Conjugaison hépatique de la bilirubine :
Dans les hépatocytes, la bilirubine est rapidement prise en charge par l'enzyme UDP-
glucuronyltranférase (UGT1A1), présente dans le réticulum endoplasmique lisse qui va
ajouter 1 ou 2 groupements d'acide glucuronique aux sites propionyl de la bilirubine (2 sites
propionyl donc potentielment 2 groupements d’acide glucuronique). On obtient des conjugués
monoglucuronides ou diglucuronides (terme générique : acylglucuronides) plus solubles
dans l'eau. L'augmentation de la solubilité aqueuse du tetrapyrrole facilite son excrétion biliaire
avec les autres pigments biliaires.
II. Méthodes de dosage
Quels sont les marqueurs biochimiques utilisés et en quoi peuvent-ils être utiles pour un
diagnostic ?
Le dosage permet de savoir l’intensité de l’ictère et d’orienter le diagnostic, pour faire ensuite
d’éventuels examens complémentaires. Selon les liquides biologiques dosés, nous chercherons
différentes formes de bilirubine.
A) Sérum ou plasma
On y trouvera :

135
● bilirubine non conjuguée (dite aussi libre ou indirecte), qui
est liée à l'albumine de façon non covalente.
● bilirubine delta, qui est une forme conjuguée et liée de façon
covalente à l'albumine (bilirubine directe) présence en faible quantité dans
le plasma.
● bilirubine mono- et di-glucuroconjuguée, qui est une forme
soluble et non liée à l'albumine (bilirubine directe).
L'ensemble de ces formes correspond à la bilirubine totale (la totale est dosée avec un accélérateur
et la directe est dosée sans). L'analyse de première intention est celle de la bilirubine totale. Si l'on
cherche plus de détails, on fera une analyse de la bilirubine conjuguée (delta et mono/di-
glucuroconjuguée) appelée bilirubine directe car mesurée directement. La bilirubine non
conjuguée/indirecte sera dosée par simple soustraction, car étant insoluble, on ne peut pas la
mesurer directement.
NB : la réaction de dosage est une réaction de coloration : diazoréaction, entraînant la formation
d'azobilirubine bleue.
Valeurs normales : Bilirubine Totale < 17 μmol/L
Bilirubine conjuguée < 4 μmol/L
Bilirubine non conjuguée < 14 μmol/L
Bilirubine delta < 3 μmol/L
C'est donc la bilirubine non conjuguée que l'on trouvera majoritairement dans le plasma. Ces
valeurs sont valables pour l'adulte.
Les principales causes d'erreurs de dosage sont l'hémolyse, la lipémie (plasma avec beaucoup
d'acide gras) et aussi différentes interférences médicamenteuses.
Chez le nouveau-né il n'y a pas de bilirubine delta dans le plasma. En effet à la naissance, la
glucuroconjugaison est très peu efficace (teint un peu jaune à la naissance: ictère physiologique).
B) Autres liquides biologiques Dans les urines, on peut trouver de la bilirubine et de l'urobiline (évaluation semi-
quantitative par colorimétrie). Il est nécessaire de faire des analyses sur des urines
fraîchement émises (<1 heure) et conservées à 4°C pour éviter l'oxydation de la bilirubine.
Lorsque de la bilirubine conjuguée est trouvée dans les urines, cela est
systématiquement pathologique. Urobilinurie: 3-16 μmol/L (test peu sensible).
Le liquide amniotique est également susceptible de faire l'objet de dosage de la
bilirubine (par spectrophotométrie directe). Cet examen a généralement pour but de

136
rechercher une incompatibilité fœto-maternelle (Rhésus). Certaines causes d'erreurs
comme le méconium (premières selles de l’enfant après sa naissance), ou la présence de
sérum maternel dans la poche amniotique sont à prendre en compte dans la réalisation du
dosage.
III. Variations pathologiques
L'augmentation de la bilirubine circulante se traduit par un ictère clinique dont la gravité
dépend de la nature de la fraction de bilirubine augmentée, de l'importance de cette élévation
et de l'âge du patient (maturité de la barrière hémato-encéphalique). Ici nous classifierons les
ictères selon la pathogénie (cause et biochimie qui l'accompagne).
A. Ictères pré--hépatiques ou hémolytiques (avant la captation par le
foie)
i. Description
Son origine provient d'une destruction excessive de globules rouges circulants (hyper
hémolyse) qui entraîne une hyperproduction de bilirubine. Ici c'est la concentration de
bilirubine non conjuguée qui est augmentée, mais aussi par voie de conséquences, il y aura
un reflux de bilirubine conjuguée entraînant alors une petite élévation de sa concentration (la
concentration de bilirubine delta, elle, est normale). Ce sont les ictères potentiellement les plus
dangereux en raison de la toxicité neurologique de la bilirubine non conjuguée.
Ainsi : [bilirubine totale] plasmatique 50 à 85 μmol/L (maxi 170 μmol/L).
Une des caractéristiques cliniques notables est l'hyper-coloration des selles due à
l'augmentation de l'urobilinogène fécal. Le dosage de l'haptoglobine est également important,
car cette glycoprotéine produite par le foie représente le meilleur marqueur de la lyse intra
vasculaire des GR. En effet, elle lie l'hémoglobine circulante, et lorsque les globules rouges
sont lysés, le complexe hémoglobine/haptoglobine est éliminé du plasma. Ainsi
l'effondrement de la concentration du plasma en haptoglobine signe une destruction
massive des globules rouges circulants.
De façon logique on assiste à une très forte érythropoïèse (hyper-réticulocytose =
augmentation des réticulocytes, précurseurs des GR) traduisant un caractère régénératif. Dans
ce type d'ictères il n'y a pas de signe d'atteinte hépatocellulaire (sauf en cas de cirrhose sous-
jacente), cependant on observera toujours une splénomégalie due à une hyper captation des
globules rouges détruits.

137
ii. Causes d'hémolyse intra---vasculaire
Anémies hémolytiques chroniques constitutionnelles (patients porteurs d'une
maladie génétique +/- rare selon la population concernée).
o Maladie de Minkowski--Chauffard ou microsphérocytose héréditaire, qui est
une anomalie de la membrane des globules rouges les rendant plus fragiles (protéine
de la membrane anormale) hyperproduction de bilirubine.
o Maladies génétiques de l'hémoglobine: β--thalassémie et drépanocytose
homozygotes
o Déficits enzymatiques érythrocytaires: déficit en G6P (glucose-6-phosphate
déshydrogénase) qui permet normalement la production de NADPH (protection contre le
stress oxydant, or les GR sont exposés à de grandes quantités d’O2 donc au stress oxydant).
Ces maladies génétiques entraînent des affaiblissements de la membrane des globules
rouges, les fragilisant. Ils ont alors tendance à être détruit plus rapidement.
Anémies hémolytiques acquises d'origine :
o toxique (médicaments, toxiques industriels, métaux lourds, venins);
o infectieuse ou parasitaire (paludisme);
o par fragmentation érythrocytaire (mécanique lors des prothèses
valvulaires, traumatique après gros effort (hémoglobinurie), lors de micro
angiopathies chez l'enfant);
o immunologique (transfusion sanguine incompatible, immunisation fœto-
maternelle)
● Incompatibilité fœto‐maternelle (mécanisme immunologique) (antigène D = antigène
rhésus): mère Rh(D)--/fœtus Rh(D)+:
Quand l'antigène D est présent chez le fœtus mais absent chez la mère, on peut avoir une
immunisation de la mère contre le fœtus. Le problème n'intervient pas lors de la première
grossesse: à la première naissance, des globules rouges fœtaux vont aller dans le sang maternel et
seront reconnus comme du non soi, entraînant la production d’anticorps anti-D. Cela peut passer
inaperçu si l'on ne s'est pas rendu compte de l'incompatibilité rhésus.
Mais si à la deuxième grossesse le fœtus est lui aussi Rh+, les Anticorps produits par la mère peuvent
passer dans le sang du fœtus à travers le placenta et détruire les globules rouges de ce dernier,
entraînant une hémolyse gravissime. Ainsi, si le diagnostic n'a pas été fait, une transfusion
in--utero sera nécessaire. Risque d’atteinte neurologique grave pour le fœtus (bilirubine
neurotoxique).

138
À l'heure actuelle, les typages rhésus sont faits avant d'arriver à de telles situations, et l'on pourra
prévenir cela par injection d’Iganti---D (traitement préventif de l’alloimmunisation foeto-
maternelle).
Si la prévention n’a pas pu être faite, on peut faire un traitement curatif par exsanguino transfusion
à la naissance (pour les formes très sévères), par photothérapie (les UV vont casser les molécules
de bilirubine ce qui va permettre sa solubilisation) ou par le phénobarbital qui induit la
glucuroconjugaison en stimulant les enzymes.
● Ictères du nouveau-‐né
Certains nouveau-nés (sans nécessairement présence d'une incompatibilité fœto-
maternelle), peuvent naître un peu "jaune". L’ictère « physiologique » du nouveau-né est dû à une
activité UGT insuffisante par immaturité du foie. La photothérapie pourra être utilisée pour faire
baisser le taux de bilirubine si les valeurs de bilirubine ne sont pas trop élevées (les UV oxydent
et ouvrent le cycle de la bilirubine, permettant sa solubilisation et facilitant son élimination). On
pourra aussi utiliser le phénobarbital pour induire la gluroconjugaison.
Il faut intervenir rapidement à cause de la neurotoxicité de la bilirubine.

139
B. Ictères hépatocellulaires (atteinte primitive de la fonction
hépatique)
Dans ce cas d'ictère, c'est l'insuffisance
hépatocellulaire qui en est responsable. On a
donc une atteinte primitive de la fonction
hépatique, pouvant inclure les étapes majeures
du métabolisme hépatique de la bilirubine
(captation, conjugaison, excrétion) en
l'absence d'hyperproduction de bilirubine.
Ce type d'ictère est associé à une
augmentation simultanée des différentes
formes plasmatiques de la bilirubine
(conjuguée, non conjuguée, delta).
Cela s'accompagne généralement de signes de
cytolyse hépatique (transaminases très
élevées).
Les urines sont hyper-colorées et les selles normales ou décolorées (en fonction de la
cholestase). Ce sont de bons indicateurs.
La première cause de ces ictères sont les hépatites virales : A, B principalement en France ; le virus
de l’hépatite C donne moins d’ictères et passe donc plus inapercue (pas de forme aigue très
marquée) mais ils peuvent aussi être dus à des hépatites médicamenteuses (paracétamol++) ou
encore à différents types de cirrhoses (alcoolique, post-hépatique, biliaire primitive,
hémochromatosique [=atteinte héréditaire au niveau du métabolisme du fer qui entraîne
l'accumulation de ce dernier dans le foie provoquant des atteintes hépatocellulaires]).
Existence de formes cholestatiques: prédominance de l’atteinte de l’excrétion.
Dans l'ictère hépatocellulaire, on a une augmentation de l'urobilinogène urinaire, ainsi que la
bilirubine conjuguée urinaire (hyper-coloration des urines) et une diminution de
l’urobilinogène fécal.
C. Ictères post-hépatiques
Ces ictères ont pour origine l'obstruction des voies biliaires principales entraînant un reflux de
la bilirubine conjuguée (cholestase, ca ne s’écoule plus). Cependant la production de
bilirubine et sa conjugaison sont normales. Ce sont des ictères à bilirubine conjuguée est associé
à une augmentation de la bilirubine delta.
L'élévation de la concentration de la bilirubine totale est très marquée :
[bilirubine totale]= 500 à 700 μmol/L avec la bilirubine delta qui peut représenter
jusqu'à 30 à 50% de la bilirubine totale.

140
L'absence d'excrétion biliaire de la bilirubine empêche la formation d'urobilinogène
fécal, entraînant alors une décoloration des selles (quasi blanches).
En ce qui concerne le bilan enzymatique, la gamma-GT et les phosphatases alcalines ont une
concentration élevée.
Les signes cliniques de ces types d'ictères sont :
- ictère très sombre, téguments parfois «
vert bouteille »;
- urines foncées, presque noires,
moussantes ;
- selles blanchâtres graisseuses,
«mastic»;
- prurit, parfois féroce, dû à l'élévation
concomitante des sels biliaires dans le
sang ;
- hépatomégalie
Les causes sont :
o calculs dans les voies biliaires : lithiases.
o cancer de la tête du pancréas : La tumeur obstrue de façon mécanique les
voies biliaires.
o autres : médicaments, cholestase intra-hépatique de la grossesse (3ème
trimestre); cirrhoses biliaires primitives.

141
D. Ictères d'origine héréditaire : Hyperbilirubinémies héréditaires
chroniques
i. Hyperbilirubinémies à prédominance non conjuguée : déficit de
conjugaison
Ces maladies sont liées à une anomalie dans l'activité de glucuro-conjugaison (UGT1A1),
avec un déficit de conjugaison partiel ou total; l'existence de polymorphismes génétiques
étant responsable d'une variation de l'activité enzymatique.
● Maladie de Gilbert (15/20% de la population)
C'est un ictère bénin qui débute à 15--20 ans ou qui peut même passer inaperçu (examen
clinique normal). Cette maladie est l'expression d'un déficit modéré de l'activité UGT1A1 dû à
une anomalie moléculaire principale : insertion d'un dinucléotide TA dans une séquence répétée
en amont du gène UGT1A1 dans le promoteur (modification de l'activité transcriptionelle du
promoteur). On a alors une diminution de la quantité de UGT1A1 et donc une conjugaison moins
efficace.
[bilirubine non conjuguée] entre 20 et 50 μmol/L
Ce type de maladie est la plupart du temps découvert suite à un traitement d'une autre
maladie, où les médicaments utilisés sont éliminés normalement par UGT1A1. Il y a une
compétition de la fixation à UGT1A1 entre le médicament et la bilirubine, entraînant ainsi une
augmentation de bilirubine non conjuguée, et ses effets délétères. On a alors une majoration
de l’ictère.
C’est une maladie bénigne. Il n'y a pas de traitement à proprement parler pour cette maladie,
seulement des précautions à prendre quant aux autres médicaments qui doivent être
administrés au patient (exemple : camptothécine = Irinitécan).
● Maladie de Criggler-‐Najjar : Maladie rare, à début précoce
Type I
Maladie très sévère liée à un déficit total en activité UGT1A1, à transmission
autosomique récessive
Débute dès la naissance
[bilirubine non conjuguée] entre 350 et 500 μmol/L
photothérapie inefficace, seul traitement : transplantation hépatique
Type II
Maladie moins sévère, déficit partiel en activité UGT1A1, à transmission
autosomique récessive
Début parfois plus tardif, pronostic plus favorable que le type I.

142
[bilirubine non conjuguée] entre 150 et 300 μmol/L
traitement par le phénobarbital = inducteur de l’activité UGT
ii. Hyperbilirubinémies à prédominance conjuguée : défaut d'excrétion,
de captation ou de stockage
Ce sont des maladies rares !
2 maladies difficiles à différencier et qui touchent des transporteurs différents :
● Syndrome de Dubin‐Johnson : autosomique
récessif
C'est un ictère familial bénin dû à une mutation dans un gène codant pour un transporteur
= ABCC2 ou MRP2 (famille des "ATP Binding-protein Cassette). La mutation entraîne un défaut
de captation de la bilirubine conjuguée dans le foie, et n'est donc pas bien éliminée. C'est un
défaut d'excrétion canaliculaire.
On a une hyper-bilirubinémie mixte à prédominance conjuguée avec bilirubinurie
(bilirubine dans les urines) : [bilirubine conjuguée] entre 50 et 250 μmol/L.
Le test de la BSP (Brome Sulphone Phtaléine) peut être utilisé : colorant capté par le foie,
conjugué et excrété dans la bile, reproduisant ainsi le trajet de la bilirubine ⇒ Permet de
mettre en évidence un reflux secondaire de BSP conjuguée (mis en évidence par des
techniques echographiques).
Les coproporphyrines urinaires sont normales mais il y a une inversion du ratio isomère I/III.
De plus il y a un dépôt de type mélanine dans le foie.
● Syndrome de Rotor : autosomique récessif
Ce sont des défauts de captation et de stockage hépatiques de la bilirubine (test BSP:
diminution de la vitesse de disparition plasmatique et absence de reflux secondaire) dus à
des mutations dans des transporteurs OATP1B1/3 assurant la re-captation hépatique de
bilirubine conjuguée.
L'excrétion urinaire des protoporphyrines est augmentée, et il y a une absence de
pigmentation des hépatocytes (à la différence du syndrome du Dubin-Johnson où on a des
dépôts de mélanine). C’est donc une biopsie qui permet en général de les différencier.

143
Ce qu'il faut retenir (diapo récapitulative du professeur)
Bilirubine = produit final de dégradation dans le métabolisme de l’hème (foie, SRE);
Elimination dans la bile sous forme conjuguée (enzyme hépatique = UGT 1A1);
Produits de dégradation: urobiline (urines) et stercobiline (selles);
Exploration biochimique: bilirubine totale, non conjuguée et conjuguée;
Intégration dans le bilan d’exploration hépato-biliaire pour apprécier l’intensité de
l’ictère clinique et orienter les investigations étiologiques en différenciant les formes
conjuguées et non conjuguées;
Pathologies: ictères
1) ictères pré-hépatiques
2) ictères hépatiques
3) ictères post-hépatiques
Ictère du nouveau--né : incompatibilité fœto-maternelle
Maladies héréditaires: maladie de Gilbert (bénigne), Criggler-Najjar (grave)
Abréviations :
GR = globules rouges
Mot du RT : Le cours est identique à celui de l’année dernière ! Courage

144
Fiche récapitulative
Introduction
Bilirubine = issue de la dégradation de l’hème principalement, myoglobline, cytochromes, catalases. Catabolisme dans la rate, le foie, la moelle, la bile, se termine dans le foie. Rôle : Antioxydant. Ictère : Élévation de la concentration de bilirubine plasmatique > 70 μmol/L.
I---/ Métabolisme de la bilirubine
2 ENZYMES Hème oxygénase (RE) Biliverdine réductase
(cytosol) - Ouverture du cycle de l’hème puis dégradation de
l’hème en biliverdine puis bilirubine
- Responsable de l’oxydation et l’ouverture du cycle
tétrapyrrolique de l’hème avec libération de Fe3+ et
de CO
Réduction d’un pont méthylène
Bilirubine libre = toxique, présente dans la rate, libérée dans la circulation où elle se lie à l’albumine permettant son captage par les hépatocytes ; rendue hydrosoluble par conjugaison via UDP-‐glucuronyltranférase (UGT1A1) (REL) (ajout de 1 ou 2 groupement acide glucoronique) afin d’être excrétée via la bile et rejoindre l’intestin où elle subit diverses transformations : Bilirubine conjuguée Urobilinogène incolore stercobilinogène (oxydation dans la partie basale de l’intestin) -> stercobiline -> Selles, ou Urobilinogène (oxydation dans les urines) -> Urobiline.
- 80% urobilinogène suit cette voie - 20% empreinte la voie du cycle entéro---hépatique : Retour vers le foie par la veine porte
(produit extrêmement soluble) et excrétion rénale (détection urinaire non pathologique).
II---/ Dosage
A) Serum/Plasma
2 FORMES DE BILIRUBINE
Non conjuguée (indirecte)
Conjuguée
Liée à l’albumine (delta)
Non liée à l’albumine (directe)
Liaison non covalente
Liaison covalente /
Les 3 = Bilirubine totale. (NB : Pas de delta et UGT1A1 chez les nouveau-nés -> Conjugaison très peu efficace : Ictère du nouveau--né physiologique)

145
1ère analyse : Bilirubine totale, 2nde si besoin : Bilirubine conjuguée (delta ou directe) (indirecte non dosable)
Valeurs normales (pour un adulte)
/!\ aux artéfacts (médicaments, hémolyse, lipémie)
Bilirubine totale < 17 μmol/L
Bilirubine conjuguée < 4 μmol/L
Bilirubine non conjuguée < 14 μmol/L
Bilirubine delta < 3 μmol/L
B) Autres liquides biologiques
Urine Liquide amniotique - Bilirubine et urobiline, urines fraîches et
bien conservées
- Bilirubine conjuguée dans les urines =
pathologique systématiquement
Recherche d’incompatibilité foeto-maternelle (Rhésus sanguin)
III---/ Variations pathologiques
A) Ictères pré---hépatiques ou hémolytiques
Lyse d’un trop grand nombre de globule rouge : élévation de la bilirubine libre non conjuguée ++ ET conjuguée car le problème à lieu en amont de la conjugaison. Toxicité neurologique de la forme libre donc danger. Ainsi : [bilirubine totale] plasmatique 50 à 85 μmol/L (maxi 170 μmol/L) (on dose la forme libre)
Conséquences : Hypercoloration des selles, rapport hémoglobine/haptoglobine s’effondre (haptoglobine = présente si lyse), érythropoïèse = réponse régénérative à la trop grande perte, et dans tous les cas splénomégalie.
CAUSES
Constitutionnelles Acquises - Déficits enzymatiques (ex:
déficit en G6PD)
- Maladie de Minkowski--- Chauffard --> affaiblissement de la membrane des globules rouges qui ont alors tendance à être détruit plus rapidement
- β--thalassémie
- Drépanocytose
- Toxique (médicament, métaux, venins)
- Infectieuse (paludisme)
- Immunologique (rhésus)
- Incompatibilité fœto-maternelle : Antigène D chez le fœtus, absent chez la mère. 1ère grossesse, reconnaissance dans le sang maternelle de l’antigène D fœtal étranger. Production d’anticorps, mais aucune signification (peut passer inaperçu). Seconde grossesse : Réponse plus forte et rapide -> Traverse la barrière placentaire, attaque et destruction des globules rouges fœtaux. Traitement par photothérapie si possible (valeur bilirubine pas trop

146
homozygote
élevée), ou par phénobarbital (= induction médicamenteuse de la conjugaison)
B) Ictères hépatocellulaires
Insuffisance hépatocellulaire qui altère la capacité de traitement de la bilirubine. Augmentation de toutes ses formes. S’accompagne de cytolyse hépatique (transaminases élevées).
Causes :
- Hépatites virales (A et B majoritairement, C) - Hépatites médicamenteuses - Cirrhoses - Existence de formes cholestatiques : prédominance de l’atteinte de l’excrétion.
Conséquences : Cycle entéro-hépatique perturbé, accumulation urobilinogène urinaire hypercoloration des urines, présence de bilirubine conjuguée possible, cholestase sans obstruction biliaire.
C) Ictères post---hépatiques
Production/conjugaison normale : [Bilirubine totale] = 500 à 700 μmol.L--1
Elévation de la bilirubine delta (30--50% de la bilirubine totale). Causes :
- Obstruction des voies biliaires principales : reflux de bilirubine conjuguée (=cholestase) - Lithiases par exemple cancer de la tête du pancréas qui obstrue mécaniquement les canaux
biliaires.
Conséquences : L'absence d'excrétion biliaire de la bilirubine empêche la formation urobilinogène fécale décoloration des selles (quasi blanches). La gamma---GT et les phosphatases alcalines ont une concentration élevée. Ictère sombre (vert bouteille), prurit, urines foncées presque noires.

147
Maladies dues à un déficit de conjugaison (prédominance non conjuguée)
Problème avec UGT1A1
Maladies dues à un défaut d’excrétion, captage ou stockage (prédominance
conjuguée) Pas de problème avec UGT1A1
Maladie de Gilbert Maladie de Criggler--Najjar
Syndrome de Dubin--Johnson
Syndrome de Rotor
- Ictère bénin (débute à 15-20 ans, peut passer inaperçu, examen clinique normal)
- Expression d'un déficit modéré de l'activité UGT1A1 dû à une anomalie moléculaire
- Découverte quand traitement médicamenteux en compétition avec la bilirubine pour fixation à UGT1A1 augmentation de [bilirubine non conjuguée] (entre 20 et 50 μmol/L) et effets délétères
- Problème apparaissant car pas assez de UGT1A1 pour assurer les deux fonctions Contre- indications de certains médicaments
Autosomique récessive Type I : Déficit complet de UGT1A1. - Débute dès la
naissance. - [bilirubine non
conjuguée] entre 350 et 500 μmol/L.
- Photothérapie inefficace,
- Seul traitement : transplantation hépatique
Type II : Déficit partiel. - Début parfois plus
tardif, pronostic favorable.
- [bilirubine non conjuguée] entre 150 et 300 μmol/L.
- Traitement par le phénobarbital = inducteur de l’activité UGT.
Autosomique récessive - Ictère familial
bénin - Dû à une mutation
dans un gène codant pour un transporteur ABCC2 ou MRP2
- Entraîne défaut de captation de la bilirubine conjuguée dans le foie qui n'est donc pas bien éliminée défaut d'excrétion canaliculaire
- Hyperbilirubinémie mixte à prédominance conjuguée avec bilirubinurie
- [bilirubine conjuguée] entre 50 et 250 μmol/L
- Test de la BSP peut être utilisé : colorant capté par le foie, conjugué et excrété dans la bile, reproduisant ainsi le trajet de la bilirubine ⇒ reflux secondaire de BSP conjuguée
- Dépôt de type mélanine dans le foie
Autosomique récessive - Défauts de captation
et de stockage hépatiques de la bilirubine (test BSP: diminution de la vitesse de disparition plasmatique et absence de reflux secondaire)
- Dû à des mutations dans des transporteurs OATP1B1/3 assurant la recaptation hépatique de bilirubine conjuguée
- L'excrétion urinaire des protoporphyrines est augmentée
- Absence de pigmentation des hépatocytes (à la différence du syndrome du Dubin--Johnson).

148
Le mois de Février arrive et qui dit février dit 14 février et Saint
Valentin… Que vous soyez accompagné ou seul ne soyez pas timide et venez déclarer votre flamme à la personne de votre choix ! Avec SOLEM vous pourrez offrir une, deux, dix, cinquante roses en tout anonymat ainsi qu’un petit poème si l’envie vous prend… On se retrouve donc en février pour une splendide livraison de roses !
Vous ne l’attendiez plus mais il arrive pour de bon !
Le CALENDRIER SOLIDAIRE de toutes vos assos revient et tout le monde s’est donné beaucoup de mal pour vous présenter un Calendar digne des dieux du stade. Au retour du ski fac, faites le plein de sensualité et de romantisme, c’est tout ce qu’on aime.
UN PEU D’AMOUR