REFERAT SIROSIS HEPATIS
-
Upload
putri-nisrina -
Category
Documents
-
view
44 -
download
10
description
Transcript of REFERAT SIROSIS HEPATIS

BAB I
PENDAHULUAN
Hati adalah organ intestinal terbesar dengan berat antara 1,2 – 1,8 kg atau kurang
lebih 25% berat badan orang dewasa yang menempati sebagian besar kuadran kanan atas
abdomen dan merupakan pusat metabolisme tubuh dengan fungsi yang sangat kompleks. 1
Sirosis adalah suatu keadaan patologis yang menggambarkan stadium akhir fibrosis
hepatik yang berlangsung progresif yang ditandai dengan distorsi dari arsitektur hepar dan
pembentukan nodulus regeneratif. Gambaran ini terjadi akibat nekrosis hepatoseluler.
Jaringan penunjang retikulin kolaps disertai deposit jaringan ikat, distorsi jaringan vaskular
dan regenerasi nodularis parenkim hati. 1,2,3
Sirosis hati secara klinis dibagi menjadi sirosis hati kompensata yang berarti belum
adanya gejala klinis yang nyata dan sirosis hati dekompensata yang ditandai gejala-gejala dan
tanda klinis yang jelas. Sirosis hati kompensata merupakan kelanjutan dari proses hepatitis
kronik dan pada satu tingkat tidak terlihat perbedaannya secara klnis. Hal ini hanya dapat
dibedakan melalui pemeriksaan biopsi hati. 1,4
Prevalensi sirosis hati sulit untuk dinilai karena stadium awalnya bersifat asimtomatis.
Namun, sirosis tercatat sebagai penyakit kematian ke-14 tersering pada dewasa di dunia,
dengan angka kematian sekitar 1,04 juta jiwa per tahun. Sirosis juga menjadi indikasi utama
untuk 5.00 kasus transplantasi hepar per tahun di negara maju.2
Tujuan
1

Tujuan dari penulisan referat ini yaitu untuk mengetahui secara lebih mendalam
mengenai penyakit Sirosis Hepatis.
Manfaat
Manfaat dari penulisan referat ini; pembaca diharapkan dapat mengetahui dan
memahami secara mendalam mengenai penyakit Coronary Artery Disease.
2

BAB II
TINJAUAN PUSTAKA
1. ANATOMI HEPAR
Hepar adalah organ intestinal terbesar dengan berat antara 1,2-,1,8 kg atau
kurang lebih 25% berat badan orang dewasa yang menempati sebagian besar kuadran
kanan atas abdomen dan merupakan pusat metabolisme tubuh dengan fungsi yang
sangat kompleks5. Hepar menempati daerah hipokondrium kanan tetapi lobus kiri dari
hepar meluas sampai ke epigastrium. Hepar berbatasan dengan diafragma pada bagian
superior dan bagian inferior hepar mengikuti bentuk dari batas kosta kanan. Hepar
secara anatomis terdiri dari lobus kanan yang berukuran lebih besar dan lobus kiri
yang berukuran lebih kecil. Lobus kanan dan kiri dipisahkan oleh ligamentum
falsiforme6. Lobus kanan dibagi menjadi segmen anterior dan posterior oleh fisura
segmentalis kanan yang tidak terlihat dari luar. Lobus kiri dibagi menjadi segmen
medial dan lateral oleh ligamentum falsiformis yang terlihat dari luar7. Pada daerah
antara ligamentum falsiform dengan kandung empedu di lobus kanan dapat ditemukan
lobus kuadratus dan lobus kaudatus yang tertutup oleh vena cava inferior dan
ligamentum venosum pada permukaan posterior6. Permukaan hepar diliputi oleh
peritoneum viseralis, kecuali daerah kecil pada permukaan posterior yang melekat
langsung pada diafragma. Beberapa ligamentum yang merupakan peritoneum
membantu menyokong hepar. Di bawah peritoneum terdapat jaringan ikat padat yang
disebut sebagai kapsula Glisson, yang meliputi permukaan seluruh organ ; bagian
paling tebal kapsula ini terdapat pada porta hepatis, membentuk rangka untuk cabang
vena porta, arteri hepatika, dan saluran empedu. Porta hepatis adalah fisura pada
3

hepar tempat masuknya vena porta dan arteri hepatika serta tempat keluarnya duktus
hepatika5.
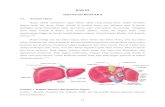
Gambar 1. Anatomi hepar
(dikutip dari kepustakaan 8)
Hepar memiliki dua sumber suplai darah, dari saluran cerna dan limpa melalui
vena porta hepatica dan dari aorta melalui arteri hepatika. Arteri hepatika keluar dari
aorta dan memberikan 80% darahnya kepada hepar, darah ini masuk ke hepar
membentuk jaringan kapiler dan setelah bertemu dengan kapiler vena akan keluar
sebagai vena hepatica. Vena hepatica mengembalikan darah dari hepar ke vena kava
inferior. Vena porta yang terbentuk dari vena lienalis dan vena mesenterika superior,
mengantarkan 20% darahnya ke hepar, darah ini mempunyai kejenuhan oksigen
hanya 70 % sebab beberapa O2 telah diambil oleh limpa dan usus. Darah yang berasal
dari vena porta bersentuhan erat dengan sel hepar dan setiap lobulus dilewati oleh
4

sebuah pembuluh sinusoid atau kapiler hepatika. Pembuluh darah halus yang berjalan
di antara lobulus hepar disebut vena interlobular7.
Vena porta membawa darah yang kaya dengan bahan makanan dari saluran
cerna, dan arteri hepatika membawa darah yang kaya oksigen dari sistem arteri. Arteri
dan vena hepatika ini bercabang menjadi pembuluh-pembuluh yang lebih kecil
membentuk kapiler di antara sel-sel hepar yang membentik lamina hepatika. Jaringan
kapiler ini kemudian mengalir ke dalam vena kecil di bagian tengah masing-masing
lobulus, yang menyuplai vena hepatika. Pembuluh-prmbuluh ini menbawa darah dari
kapiler portal dan darah yang mengalami deoksigenasi yang telah dibawa ke hepar
oleh arteri hepatika sebagai darah yang telah deoksigenasi. Selain vena porta, juga
ditemukan arteriol hepar didalam septum interlobularis. Anterior ini menyuplai darah
dari arteri ke jaringan jaringan septum diantara lobules yang berdekatan, dan banyak
arterior kecil mengalir langsung ke sinusoid hepar, paling sering pada sepertiga jarak
ke septum interlobularis7.
Gambar 2 . Pembuluh darah pada hepar
(dikutip dari kepustakaan 8)
5

Hepar terdiri atas bermacam-macam sel. Hepatosit meliputi 60% sel hepar,
sedangkan sisanya terdiri atas sel-sel epithelial sistem empedu dalam jumlah yang
bermakna dan sel-sel non parenkimal yang termasuk di dalamnya endothelium, sel
Kuppfer dan sel Stellata yang berbentuk seperti bintang5.
Hepatosit sendiri dipisahkan oleh sinusoid yang tersusun melingkari eferen
vena hepatika dan ductus hepatikus. Saat darah memasuki hepar melalui arteri
hepatica dan vena porta menuju vena sentralis maka akan didapatkan pengurangan
oksigen secara bertahap. Sebagai konsekuensinya, akan didapatkan variasi penting
kerentanan jaringan terhadap kerusakan asinus. Membran hepatosit berhadapan
langsung dengan sinusoid yang mempunyai banyak mikrofili. Mikrofili juga tampak
pada sisi lain sel yang membatasi saluran empedu dan merupakan penunjuk tempat
permulaan sekresi empedu. Permukaan lateral hepatosit memiliki sambungan
penghubungan dan desmosom yang saling bertautan dengan disebelahnya5.
Sinusoid hepar memiliki lapisan endothelial berpori yang dipisahkan dari
hepatosit oleh ruang Disse (ruang perisinusoidal). Sel-sel lain yang terdapat dalam
dinding sinusoid adalah sel fagositik Kuppfer yang merupakan bagian penting dalam
sistem retikuloendotelial dan sel Stellata (juga disebut sel Ito, liposit atau perisit) yang
memiliki aktivitas miofibriblastik yang dapat membantu pengaturan aliran darah
sinusoidal disamping sebagai faktor penting dalam perbaikan kerusakan hepar.
Peningkatan aktivitas sel-sel Stellata tampaknya menjadi faktor kunci pembentukan
fibrosis di hepar.5
6

Gambar 3 . Histologi hepar
(dikutip dari kepustakaan 9)
2. Fisiologi Hepar
Hepar adalah suatu organ besar, dapat meluas, dan organ venosa yang mampu
bekerja sebagai tempat penampungan darah yang bermakna di saat volume darah
berlebihan dan mampu menyuplai darah ekstra di saat kekurangan volume darah.
Selain itu, hepar juga merupakan suatu kumpulan besar sel reaktan kimia dengan laju
metabolisme yang tinggi, saling memberikan substrat dan energi dari satu sistem
metabolisme ke sistem yang lain, mengolah dan mensintesis berbagai zat yang
diangkut ke daerah tubuh lainnya, dan melakukan berbagai fungsi metabolisme lain.6
Fungsi metabolisme yang dilakukan oleh hepar adalah10 :
Metabolisme karbohidrat. Dalam metabolisme karbohidrat, hepar melakukan fungsi
sebagai berikut :
o Menyimpan glikogen dalam jumlah besar
o Konversi galaktosa dan fruktosa menjadi glukosa
o Glukoneogenesis
7

o Pembentukan banyak senyawa kimia dari produk antara metabolisme
karbohidrat
Hepar terutama penting untuk mempertahankan konsentrasi glukosa darah normal.
Penyimpanan glikogen memungkinkan hepar mengambil kelebihan glukosa dari
darah, menyimpannya, dan kemudian mengembalikannya kembali ke darah bila
konsentrasi glukosa darah rendah. Fungsi ini disebut fungsi penyangga glukosa hepar.
Metabolisme lemak. Beberapa fungsi spesifik hepar dalam metabolisme lemak antara
lain :
o Oksidasi asam lemak untuk menyuplai energy bagi fungsi tubuh yang lain
o Sintesis kolesterol, fosfolipid, dan sebagian besar lipoprotein
o Sintesis lemak dari protein dan karbohidrat
Hepar berperan pada sebagian besar metabolisme lemak. Kira-kira 80 persen
kolesterol yang disintesis didalam hepar diubah menjadi garam empedu yang
kemudian disekresikan kembali ke dalam empedu, sisanya diangkut dalam lipoprotein
dan dibawa oleh darah ke semua sel jaringan tubuh. Fosfolipid juga disintesis di hepar
dan ditranspor dalam lipoprotein. Keduanya digunakan oleh sel untuk membentuk
membran, struktur intrasel, dan bermacam-macam zat kimia yang penting untuk
fungsi sel.
Metabolisme protein. Fungsi hepar yang paling penting dalam metabolisme protein
adalah sebagai berikut :
o Deaminasi asam amino
o Pembentukan ureum untuk mengeluarkan ammonia dari cairan tubuh
o Pembentukan protein plasma
o Interkonversi beragam asam amino dan sintesis senyawa lain dari asam amino
8

Diantara fungsi hepar yang paling penting adalah kemampuan hepar untuk
membentuk asam amino tertentu dan juga membentuk senyawa kimia lain yang
penting dari asam amino. Untuk itu, mula-mula dibentuk asam keto yang mempunyai
komposisi kimia yang sama dengan asam amino yang akan dibentuk. Kemudian suatu
radikal amino ditransfer melalui beberapa tahap transaminasi dari asam amino yang
tersedia ke asam keto untuk menggantikan oksigen keto.
Hepar merupakan tempat penyimpanan vitamin. Hepar mempunyai kecenderungan
tertentu untuk menyimpan vitamin dan telah lama diketahui sebagai sumber vitamin
tertentu yang baik pada pengobatan pasien. Vitamin yang paling banyak disimpan
dalam hepar adalah vitamin A, tetapi sejumlah besar vitamin D dan vitamin B12 juga
disimpan secara normal
Hepar menyimpan besi dalam bentuk ferritin. Sel hepar mengandung sejumlah besar
protein yang disebut apoferritin, yang dapat bergabung dengan besi baik dalam
jumlah sedikit ataupun banyak. Oleh karena itu, bila besi banyak tersedia dalam
cairan tubuh, maka besi akan berikatan dengan apoferritin membentuk ferritin dan
disimpan dalam bentuk ini di dalam sel hepar sampai diperlukan.
Hepar memiliki aliran darah yang tinggi dan resistensi vaskuler yang rendah. Kira-kira
1050 milimeter darah mengalir dari vena porta ke sinusoid hepar setiap menit, dan tambahan
300 mililiter lagi mengalir ke sinusoid dari arteri hepatika dengan total rata-rata 1350
ml/menit. Jumlah ini sekitar 27 persen dari sisa jantung. Rata-rata tekanan di dalam vena
porta yang mengalir ke dalam hepar adalah sekitar 9 mmHg dan rata-rata tekanan di dalam
vena hepatika yang mengalir dari hepar ke vena cava normalnya hampir tepat 0 mmHg. Hal
ini menunjukkan bahwa tahanan aliran darah melalui sinusoid hepar normalnya sangat rendah
namun memiliki aliran darah yang tinggi. Namun, jika sel-sel parenkim hepar hancur, sel-sel
9

tersebut digantikan oleh jaringan fibrosa yang akhirnya akan berkontraksi di sekeliling
pembuluh darah, sehingga sangat menghambat darah porta melalui hepar. Proses penyakit ini
disebut sirosis hepatis, Sistem porta juga kadang-kadang terhambat oleh suatu gumpalan
besar yang berkembang di dalam vena porta atau cabang utamanya. Bila sistem porta tiba-
tiba tersumbat, kembalinya darah dari usus dan limpa melalui system aliran darah porta hepar
ke sirkulasi sistemik menjadi sangat terhambat, menghasilkan hipertensi portal. 10
3. Definisi Sirosis Hepatis
Sirosis didefinisikan secara histopatologi dan mempunyai bermacam-macam
penyebab, gambaran klinis dan komplikasi. Pada sirosis hepatis terdapat
perkembangan fibrosis hati sampai suatu saat ada gangguan arsitektur jaringan hati
yang ditandai dengan regenerasi nodular yang bersifat difus dan dikelilingi oleh septa-
septa fibrosis. Peubahan (distorsi) struktur tersebut dapat mengakibatkan peningkatan
aliran darah portal, disfungsi sintesis hepatosit, penurunan fungsi hati, serta
meningkatkan risiko karsinoma hepatoseluler (KHS). 2,3,4
4. Etiologi
Seluruh penyakit hati yang bersifat kronis dapat mengakibatkan sirosis hati.2,3
Etiologi dari sirosis hati disajikan dalam Tabel 1.
Tabel 1. Sebab-sebab Sirosis dan/atau Penyakit Hati Kronik
Penyakit Infeksi
BruselosisEkinokokusSkistosomiasis
10

ToksoplasmosisHepatitis virus (hepatitis B, hepatitis C, hepatitis D, sitomegalovirus)
Di negara barat yang tersering akibat alkoholik sedangkan di Indonesia
terutama akibat infeksi virus hepatitis B maupun C. Hasil penelitian di Indonesia
menyebutkan virus hepatitis B menyebabkan sirosis sebesar 40-50%, dan virus
hepatitis C 30-40%, sedangkan 10-20% penyebabnya tidak diketahui dan termasuk
kelompok virus bukan B dan C (non B-non C). Alkohol sebagai penyebab sirosis di
Indonesia mungkin frekuensinya kecil sekali karena belum ada datanya. 1
5. Epidemiologi
11
Penyakit Keturunan dan Metabolik
Defisiensi α1-antitripsinSindrom FanconiGalaktosemiaPenyakit GaucherPenyakit simpanan glikogenHemokromatosisIntoleransi fluktosa herediterTirosinemia herediterPenyakit Wilson
Obat dan Toksin
AlkoholAmiodaronArsenikObstruksi bilierPenyakit perlemakan hati non alkoholikSirosis bilier primerKolangitis sklerosis primer
Penyebab Lain atau Tidak Terbukti
Penyakit usus inflamasi kronikFibrosis kistikPintas jejunoilealSarkoidosis

Lebih dari 40% pasien sirosis asimtomatis. Pada keadaan ini sirosis ditemukan
pada waktu pemeriksaan rutin kesehatan atau pada waktu autopsy. Keseluruhan
insidensi sirosis di Amerika diperkirakan 360 per 100.000 penduduk. Penyebabnya
sebagian besar akibat penyakit hati alkoholik maupun infeksi virus kronik. Hasil
penelitian lain menyebutkan perlemakan hati akan mengakibatkan steatohepatitis non
alkoholik (NASH, prevalensi 4%) dan berakhir dengan sirosis hati dengan prevalensi
0,3 %. Prevalensi sirosis hati akibat steatohepatitis alkoholik dilaporkan 0,3% juga. Di
Indonesia data prevalensi sirosis hati belum ada, hanya laporan-laporan dari beberapa
pusat pendidikan saja. Di RS Dr. Sardjito Yogyakarta jumlah pasien sirosis hati
berkisar 4,1 % dari pasien yang dirawat di Bagian Penyakit Dalam dalam kurun waktu
1 tahun (2004) (tidak dipublikasi). Di Medan dalam kurun waktu 4 tahun dijumpai
pasien sirosis hati sebanyak 819 (4 %) pasien dari seluruh pasien di Bagian Penyakit
Dalam.2
6. Klasifikasi
Sirosis secara konvensional diklasifikasikan sebagai makronodular (besar
nodul lebih dari 3 mm) atau mikronodular (besar nodul kurang dari 3 mm) atau
campuran mikro dan makronodular. Selain itu juga diklasifikasikan berdasarkan
etiologi, fungsional namun hal ini juga kurang memuaskan.1
Sebagian besar jenis sirosis dapat diklasifikasikan secara etiologis dan
morfologis menjadi: 1) alkoholik, 2) kriptogenik dan post hepatitis (pasca nekrosis),
3) biliaris, 4) kardiak, dan 5) metabolic, keturunan, dan terkait obat.1
7. Patofisiologi
12

Sirosis hati kini dikenal sebagai proses yang dinamis dan pada kondisi tertentu
bersifat reversible. Transisi dari penyakit hati kronis menjadi sirosis melibatkan
proses yang kompleks antara reaksi inflamasi, aktivasi sel Stelata (penghasil kolagen),
angiogenesis, dan oklulsi pembuluh darah yang berdampak pada perluasan lesi
parenkim hati.2
Patogenesis utama dari proses fibrosis dan sirosis hati ialah aktivasi sel Stelata
(disebut juga sel Ito atau sel perisinusoidal). Sel Stelata normalnya bersifat “diam”
dan berperan dalam penyimpanan retinoid (vitamin A). Namun, adanya stimulus jejas
dan reaksi inflamasi akan mengaktivasi sel Stelata sehingga sel tersebut berproliferasi,
memproduksi matriks ekstraseluler (kolagen tipe I dan III, proteoglikan sulfat dan
glikoprotein), serta menjadi sel miofibroblas yang mampu berkontraksi.2
Sirosis alkoholik berperan sekitar 40% kematian karena sirosis. Riwayat
penggunaan alkohol berlebihan sering disangkal pasien. Bentuk yang berat (hepatitis,
sirosis) berkaitan dengan minum alkohol 160 g/hari selama 10-20 tahun; wanita lebih
rentan daripada pria dan berkembang lebih lanjut penyakit hati walaupun dengan
penggunaan alkohol yang lebih sedikit. Hepatitis B dan C mungkin sebagai penyerta
dalam perkembangan penyakit hati. Malnutrisi mungkin ikut berperan dalam
perkembangan sirosis.4
Sirosis alkoholik atau secara historis disebut sirosis Laennec ditandai oleh
pembentukan jaringan parut yang difus, kehilangan sel-sel hati yang uniform, dan
sedikit nodul regeneratif. Sehingga kadang-kadang disebut sirosis mikronodular.
Sirosis mikronodular dapat pula diakibatkan oleh cedera hati lainnya. Tiga lesi hati
utama akibat induksi alkohol adalah 1). Perlemakan hati alkoholik, 2). Hepatitis
alkoholik, dan 3). Sirosis alkoholik.1
13

1) Perlemakan hati alkoholik
Steatosis atau perlemakan hati alkoholik, hepatosit teregang oleh vakuola
lunak dalam sitoplasma berbentuk makrovesikel yang mendorong inti hepatosit ke
membrane sel.1
2) Hepatitis alkoholik
Fibrosis perivenular berlanjut menjadi sirosis panlobular akibat
masukan alkohol dan destruksi hepatosit yang berkepanjangan. Fibrosis yang
terjadi dapat berkontraksi di tempat cedera dan merangsang pembentukan
kolagen. Di daerah periportal dan perisentral timbul septa jaringan ikat seperti
jarring yang akhirnya menghubungkan triad portal dengan vena sentralis.
Jalinan jaringan ikat halus ini mengelilingi massa kecil sel hati yang masih ada
yang kemudian mengalami regenerasi dan membentuk nodulus. Namun
demikian kerusakan sel yang terjadi melebihi perbaikannya. Penimbunan
kolagen terus berlanjut, ukuran hati mengecil, berbenjol-benjol (nodular)
menjadi keras, terbentuk sirosis alkoholik.1
Mekanisme cedera hati alkoholik masih belum pasti. Diperkirakan
mekanismenya sebagai berikut: 1). Hipoksia sentrilobular, metabolisme
asetaldehid etanol meningkatkan konsumsi oksigen lobular, terjadi hipoksemia
relatif dan cedera sel di daerah yang jauh dari aliran darah yang teroksigenasi
(missal daerah perisentral); 2). Infiltrasi/aktivitas neutrophil, terjadi pelepasan
chemoattractants neutrofil oleh hepatosit yang memetabolisme etanol. Cedera
jaringan dapat terjadi dari neutrophil dan hepatosit yang melepaskan
intermediet oksigen reaktif, protease, dan sitokin; 3). Formasi acetaldehyde-
protein adducts berperan sebagai neoantigen, dan menghasilkan limfosit yang
14

tersensitisasi serta antibody spesifik yang menyerang hepatosit pembawa
antigen ini; 4). Pembentukan radikal bebas oleh jalur alternative dari
metabolisme etanol, disebut system yang mengoksidasi enzim mikrosomal.1
Patogenesis fibrosis alkoholik meliputi banyak sitokin, antara lain
faktor nekrosis tumor, interleukin-1, PDGF, dan TGF-beta. Asetaldehid
kemungkinan mengaktifasi sel stelata tetapi bukan suatu faktor patogenik
utama pada fibrosis alkoholik.1
3) Sirosis Hati Pasca Nekrosis
Gambaran patologi hati biasanya mengkerut, berbentuk tidak teratur,
dan terdiri dari nodulus sel hati yang dipisahkan oleh pita fibrosis yang padat
dan lebar. Gambaran mikroskopik konsisten dengan gambaran makroskopik.
Ukuran nodulus sangat bervariasi, dengan sejumlah besar jaringan ikat
memisahkan pulau parenkim regenerasi yang susunannya tidak teratur.1
Patogenesis sirosis hati menurut penelitian terakhir, memperlihatkan
adanya peranan sel stelata (stellate cell). Dalam keadaan normal sel stelata
mempunyai peran dalam keseimbangan pembentukan matriks ekstraseluler
dan proses degradasi. Pembentukan fibrosis menunjukkan perubahan proses
keseimbangan. Jika terpapar faktor tertentu yang berlangsung secara terus
menerus (missal: hepatitis virus, bahan-bahan hepatotoksik), maka sel stelata
akan menjadi sel yang membentuk kolagen. Jika proses berjalan terus maka
fibrosis akan berjalan terus di dalam sel stelata, dan jaringan hati yang normal
akan diganti oleh jaringan ikat.1
15

Sirosis hati yang disebabkan oleh etiologi lain frekuensinya sangat
kecil sehingga tidak dibicarakan disini.
8. Manifestasi Klinis
Sirosis hati merupakan kondisi histopatologis yang bersifat asimtomatis pada
stadium awal. Secara klinis, sirosis dapat dibedakan menjadi sirosis kompensata
(gejala klinis belum ada atau minimal) dan sirosis dekompensata (gejala dan tanda
klinis jelas).2
Gejala umum anoreksia, mual, muntah, diare, nyeri kuadran kanan atas
samar-samar, lelah, lemah, demam, icterus, amenorea, impotensia, infertilitas.4
1) Sirosis kompensata
Stadium awal sirosis sering tanpa gejala sehingga kadang ditemukan pada
waktu pasien melakukan pemeriksaan kesehatan rutin atau karena kelainan
penyakit lain. Sirosis kompensata hanya dapat didiagnosis melalui pemeriksaan
fungsi hati. Gejala awal sirosis (kompensata) meliputi perasaan mudah lelah dan
lemas, selera makan berkurang, perasaan perut kembung, mual, berat badan
menurun, pada laki-laki dapat timbul impotensi, testis mengecil, buah dada
membesar, hilangnya dorongan seksualitas. Tanda khas (stigmata) sirosis juga
seringkali belum tampak pada tahap ini. Sebenarnya sekitar 40% kasus sirosis
kompensata telah mengalami varises esophagus, namun belum menunjukkan
tanda-tanda perdarahan.1,2
2) Sirosis dekompensata
16

Bila sudah lanjut (sirosis dekompensata), gejala-gejala lebih menonjol
terutama bila timbul komplikasi kegagalan hati dan hipertensi porta, meliputi
hilangnya rambut badan, gangguan tidur, dan demam tak begitu tinggi. Mungkin
disertai adanya gangguan pembekuan darah, perdarahan gusi, epistaksis,
gangguan siklus haid, ikterus dengan air kemih berwarna seperti teh pekat, asites
dan edema perifer, muntah darah dan/atau melena (akibat perdarahan varises
esophagus), jaundice, ensefalopati (baik tanda dan gejala minimal hingga
perubahan mental, meliputi mudah lupa, sukar konsentrasi, bingung, agitasi,
sampai koma).1,2
Asites merupakan tanda dekompensata yang paling sering ditemukan
(sekitar 80%). Selain itu, terdapat beberapa stigmata sirosis lainnya yang dapat
diidentifikasi, antara lain:
a. Tanda gangguan endokrin:
i. Spider angioma. Gambaran seperti laba-laba di kulit, terutama
daerah leher, bahu, dan dada;
ii. Eritema palmaris pada tenar dan hipotenar;
iii. Atrofi testis. Sering disertai penurunan libido dan impotensi;
iv. Ginekomastia;
v. Alopesia pada dada dan aksila;
vi. Hiperpigmentasi kulit, diduga akibat peningkatan kadar
melanocyte-stimulating hormone (MSH);
b. Kuku Muchrche. Gambaran pita putih horizontal yang memisahkan warna
kuku normal;
c. Kontraktur Dupuytren. Penebalan fasia pada palmar (terutama sirosis
alkoholik);
17

d. Fetor hepatikum. Bau napas khas akibat penumpukan metionin (gagal
dimetabolisme), atau akibat peningkatan konsentrasi dimetisulfida akibat
pirau portosistemik yang berat;
e. Atrofi otot;
f. Petekie dan ekimosis bila terjadi trombositopenia koagulopati berat.
g. Splenomegali;
h. Pemeriksaan palpasi hati sangat bervariasi, mulai dari tidak ditemukan
pembesaran hati, lobus kiri hati yang dapat teraba lunak (khas sirosis), atau
teraba nodul dengan konsistensi keras.2
9. Temuan Klinis
Temuan klinis sirosis meliputi, spider angio maspiderangiomata (atau spider
teleangiektasis), suatu lesi vaskular yang dikelilingi beberapa venavena kecil. Tanda
ini sering ditemukan di bahu, muka, dan lengan atas. Mekanisme terjadinya tidak
diketahui, ada anggapan dikaitkan dengan peningkatan rasio estradiol/testosterone
bebas. Tanda ini juga bisa ditemukan selama hamil, malnutrisi berat, bahkan
ditemukan pula pada orang sehat, walau umumnya ukuran lesi kecil.1
Eritema palmaris, warna merah saga pada thenar dan hipothenar telapak
tangan. Hal ini juga dikaitkan dengan perubahan metabolisme hormon estrogen.
Tanda ini juga tidak spesifik pada sirosis. Ditemukan pula pada kehamilan, artritis
rheumatoid, hipertiroidisme, dan keganasan hematologi.1
Perubahan kuku-kuku Murche berupa pita putih horizontal dipisahkan dengan
warna normal kuku. Mekanismenya juga belum diketahui, diperkirakan akibat
18

hipoalbuminemia. Tanda ini juga bisa ditemukan pada kondisi hypoalbuminemia yang
lain seperti sindrom neftorik.1
Jari gada lebih sering ditemukan pada sirosis bilier. Osteoartropati hipertrofi
suatu periostitis proliferatif kronik menimbulkan nyeri.1
Kontraktur Dupuytren akibat fibrosis fasia palmaris menimbulkan kontraktur
fleksi jari-jari berkaitan dengan alkoholisme tetapi tidak secara spesifik berkaitan
dengan sirosis. Tanda ini juga bisa ditemukan pada pasien diabetes mellitus, distrofi
refleks simpatetik, dan perokok yang juga mengkonsumsi alkohol.1
Ginekomastia secara histologis berupa proliferasi benigna jaringan glandula
mammae laki-laki, kemungkinan akibat peningkatan androstenedione. Selain itu,
ditemukan juga hilangnya rambut dada dan aksila pada laki-laki, sehingga lakilaki
mengalami perubahan ke arah feminism. Kebalikannya pada perempuan menstruasi
cepat berhenti sehingga dikira fase menopause.1
Atrofi testis hipogonadisme menyebabkan impotensi dan infertile. Tanda ini
menonjol pada alkoholik sirosis dan hemokromatosis.1
Hepatomegali – ukuran hati yang sirotik bisa membesar, normal, atau
mengecil. Bilamana hati teraba, hati sirotik teraba keras dan nodular.1
Splenomegali sering ditemukan terutama pada sirosis yang penyebabnya non
alkoholik. Pembesaran ini akibat kongesti pulpa merah lien karena hipertensi porta.1
Asites, penimbunan cairan dalam rongga peritoneum akibat hipertensi porta
dan hipoalbuminemia. Caput medusa juga sebagai akibat hipertensi porta.1
19

Fetor hepatikum, bau napas yang khas pada pasien sirosis disebabkan
peningkatan konsentrasi dimetil sulfide akibat pintasan porto sistemik yang berat.1
Ikterus-pada kulit dan membrane mukosa akibat bilirubinemia. Bila
konsentrasi bilirubin kurang dari 2-3 mg/dl tidak terlihat. Warna urin gelap seperti air
teh.1
Asterixis-bilateral tetapi tidak sinkron berupa gerakan mengepak-ngepak dari
tangan, dorsofleksi tangan.1
Tanda-tanda lain yang menyertai di antaranya :
Demam yang tak tinggi akibat nekrosis hepar
Batu pada vesika felea akibat hemolysis
Pembesaran kelenjar parotis terutama pada sirosis alkoholik, hal ini akibat
sekunder infiltrasi lemak, fibrosis, dan edema.
Diabetes mellitus dialami 15 sampai 30% pasien sirosis. Hal ini akibat
resistensi insulin dan tidak adekuatnya sekresi insulin oleh sel beta pancreas.1
10. Komplikasi
Morbiditas dan mortalitas sirosis tinggi akibat komplikasinya. Secara garis
besar, komplikasi sirosis hati terjadi akibat: (1) Hipertensi portal dan kondisi
hiperdinamis, serta (2) insufisiensi hati. Selain itu, sirosis hati (bersama dengan
etiologinya) dapat menimbulkan perubahan materi genetik pada hepatosit sehingga
berpotensi menjadi karsinoma hepatoseluler (KHS). Kualitas hidup pasien sirosis
diperbaiki dengan pencegahan dan penanganan komplikasinya.1,2
20

a. Hipertensi porta dan kondisi hiperdinamik
Hipertensi porta didefinisikan sebagai peningkatan gradient tekanan vena
hepatic >5 mmHg. Hipertensi porta terjadi akibat peningkatan resistensi
terhadap aliran darah porta dan peningkatan aliran masuk ke vena porta.
Peningkatan resistensi tersebut disebabkan oleh perubahan struktur parenkim
hati (deposisi jaringan fibrosis dan regenerasi nodular), serta mekanisme
vasokontriksi pembuluh darah sinusoid hati (utamanya akibat defisiensi nitrit
oksida).2
Adanya hipertensi porta akan berdampak pada:
- Pembesaran limpa dan sekuestrasi trombosit (pada tahap lanjut dapat
menjadi hipersplenisme);
- Terjadi aliran darah balik dan terbentuk pirau (shunt) dari sistem porta
ke pembuluh darah sistemik (portosistemik). Aliran portosistemik akan
menurunkan kemampuan metabolisme hati (first-pass effect), fungsi
retikuloendotelial, dan mengakibatkan hiperamonemia. Kendati demikian,
kolateral portosistemik tetap tidak adekuat dalam mengurangi tekanan
vena porta. Sebaliknya, justru akan meningkatkan produksi NO sehingga
terjadi vasodilatasi splanikus dan peningkatan aliran darah ekstrahepatik
(sementara kadar NO intrahepatic tetap rendah).
- Aktivasi sistem renin-angiotensin-aldosteron, akibat vasodilatasi
splanknikus dan vasodilatasi sistemik. Pada tahap lanjut kondisi ini
mengakibatkan komplikasi pada jantung, paru, dan renal.2
Secara klinis, hipertensi porta dan pembentukan kolateral
portosistemik akan mengakibatkan komplikasi berikut:
21

Varises gastro-esofagus dan perdarahan varises tersebut;
Asites. Selain hipertensi porta, risiko kejadian asites juga semakin
meningkat akibat hipoalbuminemia. Asites adalah komplikasi yang
paling umum dari SH. Sekitar 60% pasien dengan SH terkompensasi
akan menjadi asites dalam jangka waktu 10 tahun sejak awal mula
perjalanan penyakit. Asites menurut jumlahnya dibagi menjadi tiga
tingkatan/grade. Grade I (minimal) ialah asites dalam jumlah sangat
kecil yang hanya dapat terdeteksi melalui USG. Grade II (moderate)
ialah asites yang terlihat sebagai distensi abdomen yang tampak
simetris. Grade III (large) ialah asites dalam jumlah besar hingga
menimbulkan distensi abdomen yang sangat nyata (EASL, 2011). 2,3
Hiponatremia. Hiponatremia umum ditemui pada pasien dengan SH
dekompensata dan berkaitan dengan terjadinya kelainan pada ekskresi
cairan sekunder terhadap hipersekresi vasopressin akibat terjadinya
disproporsi retensi air dibandingkan dengan retensi garam. Secara
umum, pada kasus SH, kadar natrium diperhitungkan sebagai
hiponatremia yang perlu diberikan terapi adalah pada konsentrasi
dibawah 130 mmol/L (Verbalis et al, 2007). Kadar natrium pada kasus
SH merupakan marker yang cukup penting untuk menentukan
prognosis. Hiponatremia pada kasus SH berkaitan dengan
meningkatnya angka morbiditas, terutama berkaitan dengan
komplikasi neurologis dan menurunnya angka survival pasca
transplantasi (Biggins et al, 2005).3
Sindrom hepatorenal, akibat vasokontriksi arterirenalis sebagai respon
terhadap vasodilatasi sistemik (mekanisme arterial underfilling);
22

Peritonitis bakterialis spontan, yaitu infeksi cairan asites akibat migrasi
bakteri lumen usus ke nodus limfe mesenterika dan lokasi ekstra-usus
lainnya. Diduga terjadi karena gangguan sistem imunitas lokal dan
sistemik.
Ensefalopati hepatikum, terjadi akibat hiperamonemia.
Komplikasi lainnya: sindrom hepatopulmonal, hipertensi
portopulmonal, dan kardiomiopati.2
Komplikasi yang sering dijumpai antara lain peritonitis bacterial spontan,
yaitu infeksi cairan asites oleh satu jenis bakteri tanpa ada bukti infeksi sekunder intra
abdominal. Biasanya pasien ini tanpa gejala, namun dapat timbul demam dan nyeri
abdomen.1
Pada sindrom hepatorenal, terjadi gangguan fungsi ginjal akut berupa oliguria,
peningkatan ureum, kreatinin tanpa adanya kelainan organik ginjal. Kerusakan hati
lanjut menyebabkan penurunan perfusi ginjal yang berakibat pada penurunan filtrasi
glomerulus.
Salah satu manifestasi hipertensi porta adalah varises esofagus. Duapuluh
sampai 40% pasien sirosis dengan varises esofagus pecah yang menimbulkan
perdarahan. Angka kematiannya sangat tinggi, sebanyak duapertiganya akan
meninggal dalam waktu satu tahun walaupun dilakukan tindakan untuk
menanggulangi varises ini dengan beberapa cara.
Ensefalopati hepatik, merupakan kelainan neuropsikiatrik akibat disfungsi
hati. Mula-mula ada gangguan tidur (insomnia dan hiperinsomnia), selanjutnya dapat
timbul gangguan kesadaran yang berlanjut sampai koma.
23

Pada sindrom hepatopulmonal terdapat hidrotoraks dan hipertensi
portopulmonal. 1
b. Insufisiensi hati
Perubahan struktur histologis hati akan diiringi oleh penurunan fungsi
hati antara lain:
- Gangguan fungsi sintesis: hypoalbuminemia dan malnutrisi, defisiensi
vitamin K dan kolagulopati (penurunan faktor koagulasi yang
membutuhkan vitamin K, yaitu faktor II, VII, IX, dan X), serta gangguan
endokrin ((kadar estrogen darah meningkat, hiperparatiroidisme);
- Gangguan fungsi eksresi: kolestasis dan ikterus, hiperamonemia dan
ensefalopati;
- Gangguan fungsi metabolisme: gangguan homeostasis glukosa (dapat
menjadi diabetes mellitus), malabsorpsi vitamin D dan kalsium.2
Timbulnya komplikasi-komplikasi seperti asites, ensefalopati, varises esofagus
menandai terjadinya pergantian dari SH fase kompensasi yang asimtomatik menjadi
SH dekompensasi.3
11. Pemeriksaan Penunjang
1) Pemeriksaan Laboratorium
Parameter hematologi: hemoglobin, leukosit, hitung trombosit, waktu
protombin (INR);
24

Biokimia serum: bilirubin, transaminase (ALT dan AST), alkalin
fosfatase, γglutamyl transpeptidase ( γ GT), albumin dan globulin,
immunoglobulin, ferritin serum dan saturasi transferrin;
Apabila ditemukan asites: kadar elektrolit (natrium, kalium, bikarbonat,
klorida), ureum dan kreatinin, serta urinalisis (urin tamping 24 jam);
Deteksi/pemantauan etiologi: penanda serologi hepatitis B dan C, profil
lipid dan glukosa, penanda autoimun, dan sebagainya.2
Gambaran Laboratoris
Adanya sirosis dicurigai bila ada kelainan pemeriksaan laboratorium pada
waktu seseorang memeriksakan kesehatan rutin, atau waktu skrining untuk evaluasi
keluhan spesifik. Tes fungsi hati meliputi aminotransferase, alkali fosfatase, gamma
glutamil transpeptidase, bilirubin, albumin, dan waktu protombin.1
Aspartat aminotransferase (AST) atau serum glutamil oksalo asetat (SGOT)
dan alanin aminotransferase (ALT) atau serum glutamil piruvat transaminase (SGPT)
meningkat tapi tak begitu tinggi. AST lebih meningkat daripada ALT, namun bila
transaminase normal tidak mengenyampingkan adanya sirosis.1
Alkali fosfatase, meningkat kurang dari 2 sampai 3 kali batas normal atas.
Konsentrasi yang tinggi bisa ditemukan pada pasien kolangitis sclerosis primer dan
sirosis bilier primer.1
Gamma-glutamil transpeptidase (GGT), konsentrasinya seperti halnya alkali
fosfatase pada penyakit hati. Konsentrasinya tinggi pada penyakit hati alkoholik
kronik, karena alkohol selain menginduksi GGT mikrosomal hepatik, juga bisa
menyebabkan bocornya GGT dari hepatosit.1
Bilirubin, konsentrasinya bisa normal pada sirosis hati kompensata, tapi bisa
meningkat pada sirosis yang lanjut.1
25

Albumin, sintesisnya terjadi di jaringan hati, konsentrasinya mneurun sesuai
dengan perburukan sirosis.1
Globulin, konsentrasinya meningkat pada sirosis. Akibat sekunder dari
pintasan, antigen bakteri dari sistem porta ke jaringan limfoid, selanjutnya
menginduksi produksi immunoglobulin.1
Waktu protombin mencerminkan derajat/tingkatan disfungsi sintetis hati,
sehingga pada sirosis memanjang.1
Natrium serum menurun terutama pada sirosis dengan asites, dikaitkan dengan
ketidakmampuan eksresi air bebas.1
Kelainan hematologi anemia, penyebabnya bisa bermacam-macam, anemia
normokrom, normositer, hipokrom mikrositer (karena kehilangan darah) atau
hipokrom makrositer (karena defisiensi folat), anemia hemolitik (sindrom Ziete).
Anemia dengan trombositopenia, leukopenia, dan neutropenia akibat splenomegali
kongestif berkaitan dengan hipertensi porta sehingga terjadi hipersplenisme
(pansitopenia).1,4
2) Biopsi hati dan pemeriksaan histopatologis, merupakan baku emas untuk
diagnosis dan klasifikasi derajat sirosis.2
3) Pemeriksaan radiologi (non-invasif), bertujuan untuk:
a. Deteksi nodul hati atau tanda hipertensi porta: USG hati, CT-scan/MRI;
b. Penilaian kekakuan jaringan hati (derajat fibrosis): transien elastografi
(Fibroscan), MR elastrografi.2
26

Pemeriksaan radiologis barium meal dapat melihat varises untuk
konfirmasi adanya hipertensi porta. Ultrasonografi (USG) sudah secara rutin
digunakan karena pemeriksaannya non invasif dan mudah digunakan, namum
sensitivitasnya kurang. Pemeriksaan hati yang bisa dinilai dengan USG
meliputi sudut hati, permukaan hati, ukuran, homogenitas, dan adanya massa.
Pada sirosis lanjut, hati mengecil dan nodular, permukaan irregular, dan ada
peningkatan eksogenitas parenkim hati. Selain itu USG juga bisa untuk
melihat asites, splenomegali, trombosis vena porta dan pelebaran vena porta,
serta skrining adanya karsinoma hati pada pasien sirosis.1
Tomografi komputerisasi, informasinya sama dengan USG, tidak rutin
digunakan karena biayanya relatif mahal.1
Magnetic Resonance Imaging, peranannya tidak jelas dalam
mendiagnosis sirosis selain biayanya mahal. 1
4) Pemeriksaan esofago-gastroduodenoskopi (EGD), baik untuk deteksi varises
esofagus.
5) Beberapa prediktor sirosis telah dikembangkan dengan menggunakan metode
indirek, antara lain:
a. Umumnya rasio AST/ALT >1. Namun, rasio sebaliknya tidak mengekslusi
kejadian sirosis.
b. Skor APRI (indeks rasia AST/trombosit). Dapat digunakan untuk etiologi
hepatitis B kronis dan hepatitis C.
Rumus APRI = AST (IU/L) / Hitung trombosit (109/L) x 100
Nilai APRI: 1,0 memiliki sensitivitas 76% dan spesifisitas 72% dalam
mendeteksi sirosis.
27

c. Skor FIB4. Dapat digunakan untuk etiologi hepatitis B kronis, hepatitis C,
dan NAFLD/NASH
Rumus FIB4 = Usia (tahun) X AST (IU/L) / Hitung trombosit (109/L x √ (ALT
(IU/L))
Pada NAFLD/NASH: Skor FIB4 <1,30 = Sirosis METAVIR F0-F1;
Skor FIB4 >2,67= Sirosis METAVIR F3-F4.
Pada hepatitis C: Skor FIB4 <1,45 = Sirosis
METAVIR F0-F1 ; Skor FIB4 >3,21 = Sirosis METAVIR F3-F4
d. Indeks Forns. Dapat digunakan untuk etiologi hepatitis B kronis dan hepatitis
C.
Indeks Forns =
7,8111 – {3,131 x 1n[ γ GT (IU/L)]}+{3,467 x 1n[usia]}-{0,14 x [kadar
kolesterol (mg/dl)]}
Keterangan: 1n, logaritma natural; γ GT, gamma-glutamyl transpeptidase.
Tabel 2. Skor METAVIR untuk Penilaian Fibrosis dan Inflamasi
Skor Fibrosis Skor Aktivitas
F0 = tidak ada fibrosis A0 = tidak ada aktivitas
F1 = Fibrosis porta tanpa septa A1 = aktivitas ringan
F2 = Fibrosis porta dengan septa A2 = Aktivitas sedang
F3 = Banyak septa, namun belum terjadi sirosis A3 = Aktivitas berat
F4 = Sirosis
Skor Indeks Forns <4,25: nilai prediksi negatif 96% untuk ekslusi
fibrosis METAVIR F2-F4.
28

Skor Indeks Forns >6,9: nilai prediksi positif 66% untuk fibrosis
METAVIR F2-F4.2
12. Diagnosis dan Penilaian Derajat Sirosis
Diagnosis klinis SH dibuat berdasarkan kriteria Soedjono dan Soebandiri
tahun 1973, yaitu bila ditemukan 5 dari 7 keadaan berikut: eritema palmaris, spider
nevi, vena kolateral atau varises esofagus, asites dengan atau tanpa edema,
splenomegali, hematemesis dan melena, rasio albumin dan globulin terbalik.3
Dasar diagnosis tergantung pada keadaan klinik. Serum: HBsAg, anti-HB, anti
HCV, anti-HDV, Fe, total iron-binding capacity, ferritin, antimitochondrial antibody
(AMA), smooth-muscle antibody (SMA), anti-liver/kidney microsomal (anti-LKM),
ANA, seruloplasmin, α1 antitripsin (dan pi typing); Doppler ultrasound abdomen, CT
atau MRI (mungkin tampak sirosis hati, splenomegali, kolateral-kolateral, thrombosis
vena). Baku emas diagnosis sirosis hati ialah biopsi hati (per kutan, transjugular, atau
terbuka) dengan pemeriksaan histopatologis. Deteksi sirosis harus dipertimbangkan
untuk setiap etiologi penyakit hati kronis. Diagnosis juga harus menyertakan: (1)
etiologi penyakit, dan (2) grading/staging histopatologis untuk menilai derajat nekro-
inflamasi dan fibrosis (misalnya dengan skor METAVIR).2,4
Secara klinis, sirosis dapat dibedakan menjadi beberapa derajat kategori
berdasarkan kriteria Child Turcotte Pugh bertujuan untuk menilai prognosis (angka
kesintasan) pasien. Adapun system skor MELD (Model for End-Stage Liver Disease),
yang digunakan untuk menentukan prognosis pada pasien yang akan menjalani
pemasangan TIPS.1
29

13. Penatalaksanaan
Etiologi sirosis mempengaruhi penanganan sirosis. Terapi ditujukan
mengurangi progresi penyakit, menghindarkan bahan-bahan yang bisa menambah
kerusakan hati, pencegahan dan penanganan komplikasi. Bilamana tidak ada koma
hepatic diberikan diet yang mengandung protein 1g/kgBB dan kalori sebanyak 2000-
3000 kkal/hari.2
Pengobatan Sirosis Kompensata :
Tatalaksana pasien sirosis yang masih kompensata ditujukan untuk
mengurangi progeresi kerusakan hati dan untuk mencegah perkembangan menjadi
sirosis dekompensata. Terapi pasien ditujukan untuk menghilangkan etiologi, di
antaranya: alkohol dan bahan-bahan lain yang toksik dan dapat mencederai hati
dihentikan penggunaannya. Pemberian asetaminofen, kolkisin, dan obat herbal bisa
menghambat kolagenik.1,2
1. Terapi medikamentosa
a. Terapi sesuai etiologi: hepatitis B kronis, hepatitis C, NASH, sirosis alkoholik,
autoimun, dan sebagainya.
Pada hepatitis autoimun bisa diberikan steroid atau imunosupresif.
Pada hemakromatosis flebotomi setiap minggu sampai konsentrasi besi
menjadi normal dan diulang sesuai kebutuhan.
Pada penyakit hati nonalkoholik; menurunkan berat badan akan mencegah
terjadinya sirosis.
30

Pada hepatitis B, interferon alfa dan lamivudine (analog nukleosida)
merupakan terapi utama. Lamivudin sebagai terapi lini pertama diberikan 100 mg
secara oral setiap hari selama satu tahun. Namun pemberian lamivudine setelah 9-12
bulan menimbulkan mutase YMDD sehingga terjadi resistensi obat. Interferon alfa
diberikan secara suntikan subkutan 3 MIU, tiga kali seminggu selama 4-6 bulan,
namun ternyata juga banyak yang kambuh.1
Pada hepatitis C kronik, kombinasi interferon dengan ribavirin merupakan
terapi standar. Interferon diberikan secara suntikan subkutan dengan dosis 5 MIU tiga
kali seminggu dan dikombinasi ribavirin 800-1000 mg/hari selama 6 bulan.1
Pada pengobatan fibrosis hati; pengobatan antifibrotik pada saat ini lebih
mengarah kepada peradangan dan tidak terhadap fibrosis. Di masa datang,
menempatkan sel stelata sebagai target pengobatan dan mediator fibrogenik akan
merupakan terapi utama. Pengobatan untuk mengurangi aktifitas dari sel stelata.
Kolkisin memilik efek anti peradangan dan mencegah pembentukan kolagen, namun
belum terbukti dalam penelitian sebagai anti fibrosis dan sirosis. Metotreksat dan
vitamin A juga dicobakan sebagai anti fibrosis. Selain itu, obat-obatan herbal juga
sedang dalam penelitian.1
b. Bila perlu, terapi defisiensi besi. Dapat diberikan tambahan zink sulfat 2x200
mg PO untuk memperbaiki nafsu makan dan keram otot.
c. Bila perlu, dapat diberikan antiprutitus: kolestiramin, antihistamin,
antihistamin, atau agen topical;
d. Suplementasi vitamin D (atau analognya) pada pasien berisiko tinggi
osteoporosis.
31

2. Terapi non-medikamentosa
a. Diet seimbang 35-4 kkal/KgBB ideal dengan protein 1,2-1,5 g/KgBB/hari;
b. Aktivitas fisik untuk mencegah inaktivitas dan atrofi otot, sesuaikan toleransi
pasien;
c. Stop konsumdi alkohol dan merokok;
d. Pembatasan obat-obatan hepatotoksik dan nefrotoksik: OAINS, isoniazid,
asam valproat, eritromisin, amoksisilin/klavulanat, golongan aminoglikosida
(bersifat nefrotoksik pada sirosis), ketokonazol, klorpromazin, dan ezetimibe.1
3. Surveilans komplikasi sirosis
a. Monitor kadar albumin, bilirubin, INR, serta penilaian fungsi kardiovaskular
dan ginjal.
b. Deteksi varises dengan esofago-gastroduodenoskopi (EGD):
Bila tidak ditemukan varises: Ulangi EGD setiap 2 tahun;
Bila ditemukan varises kecil: Ulangi EGD setiap 1 tahun;
Bila ditemukan varises besar: penyekat-β nonselektif (propanolol),
prosedur ligase varises (pada kasus intoleran).
c. Deteksi retensi cairan dan pemantauan fungsi ginjal.
d. Deteksi ensefalopati (atau ensefalopati minimal/subklinis): tes psikometri dan
neuropsikologis terhadap atensi dan fungsi psikomotrik setiap 6 bulan.
e. Deteksi karsinoma hepatoseluler: pemeriksaan α-fetoprotein dan USG hati
setiap 6 bulan.
f. Vaksinasi hepatitis B dan hepatitis A, bila perlu.1
Pengobatan Sirosis Dekompensata :
32

Terapi ditujukan untuk mengatasi kegawatdaruratan dan mengembalikan ke
kondisi kompensata.2
1. Tatalaksana spesifik sesuai komplikasi yang ditemukan. Berikut pilihan terapi
yang dapat diberikan untuk masing-masing komplikasi :
- Asites, tirah baring dan diawali diet rendah garam, konsumsi garam sebanyak 5,2
gram atau 90 mmol/hari. Diet rendah garam dikombinasi dengan obat-obatan
diuretik. Awalnya dengan pemberian spironolakton dengan dosis 100-200 mg
sekali sehari. Respon diuretik bisa dimonitor dengan penurunan berat badan 0,5
kg/hari, tanpa adanya edema kaki atau 1 kg/hari dengan adanya edema kaki.
Bilamana pemberian spironolakton tidak adekuat, bisa dikombinasi dengan
furosemid dengan dosis 20-40 mg/hari. Pemberian furosemid bisa ditambah
dosisnya bila tidak ada respons, maksimal dosisnya 160 mg/hari. Parasentesis
dilakukan bila asites sangat besar. Pengeluaran asites bisa hingga 4-6 liter dan
dilindungi dengan pemberian albumin.
- Ensefalopati hepatik, meminimalisasi faktor pencetus, pemberian laktulosa
dengan/tanpa rifakmisin membantu pasien untuk mengeluarkan amonia.
Suplementasi asam amino rantai bercabang dan diet rendah asam amino lisin,
metionin, dan triptofan. Neomisin bisa digunakan untuk mengurangi bakteri usus
penghasil amonia, diet protein dikurangi sampai 0,5 gr/kg berat badan per hari,
terutama diberikan yang kaya asam amino rantai cabang.1,2
- Hipertensi porta dan varises esofagus, sebelum berdarah dan sesudah berdarah
bisa diberikan obat penyekat beta (propanolol). Waktu perdarahan akut, bisa
diberikan preparat somatostatin atau okreotid, diteruskan dengan tindakan
skleroterapi atau ligase endoskopi. Selain itu diberikan terpai endoskopik,
pemasangan TIPS maupun prosedur bedah. 1,2
33

- Peritonitis bakterial spontan; kultur dan pemberian antibiotic spectrum luas
seperti sefotaksim intravena, amoksilin, dana tau aminoglikosida.
- Sindrom hepatorenal; mengatasi perubahan sirkulasi darah di hati, tatalaksana
untuk mengatur keseimbangan garam dan air (elektrolit) dan asam basa.
Penggunaan agen vasopressor dan albumin.
- Koagulopati dan gangguan hematologi: pertimbangkan transfuse pada kondisi
gawat darurat.
2. Pada kebanyakan kasus, dekompensasi terjadi akibat adanya faktor pencetus,
seperti sepsis, hipotensi, atau penggunaan obat-obatan tertentu. Identifikasi dan
tatalaksana faktor pencetus tersebut dapat membantu mengembalikan ke kondisi
kompensata.2
3. Pertimbangkan transplantasi hati; terapi definitif pada pasien sirosis dekompensata
atau karsinoma hepatoseluler. Namun sebelum dilakukan transplantasi ada
beberapa kriteria yang harus dipenuhi resipien dahulu. Jika tidak memungkinkan
maka dilakukan pengobatan paliatif untuk mengurangi gejala dan mengurangi
morbiditas.2,3
Transplantasi hati dikontraindikasikan pada kondisi berikut:
Aktif menggunakan obat-obatan terlarang, misalnya metadon;
AIDS. Infeksi HIV saja bukan kontraindikasi;
Keganasan ekstrahepatik;
Sepsis tidak terkendali;
Gagal organ ekstrahepatik (jantung, paru);
34

Trombosis splanikum yang meluar ke vena mesenterika superior. 1,2
14. Prognosis
Prognosis sirosis sangat bervariasi dipengaruhi sejumlah faktor, meliputi
etiologi, beratnya kerusakan hati, komplikasi, dan penyakit lain yang menyertai.1
Klasifikasi Child Pugh, juga untuk menilai prognosis pasien sirosis yang akan
menjalani operasi, variabelnya meliputi konsentrasi bilirubin, albumin, ada tidaknya
asites dan ensefalopati juga status nutrisi. Klasifikasi ini terdiri dari Child A, B, dan
C. Klasifikasi Child Pugh berkaitan dengan kelangsungan hidup. Angka
kelangsungan hidup selama satu tahun untuk pasien dengan Child A, B, dan C
berturut-turut 100, 80, dan 45%.1
Tabel 3. Klasifikasi Child Pasien Sirosis Hati dalam Terminologi Cadangan Fungsi Hati
Derajat Kerusakan Minimal Sedang Berat
Bil serum (mu.
Mold/dl)
<35 35 >50
Alb. Serum (gr/dl) >35 30-55 <30
Asites nihil Mudah dikontrol sukar
PSE/ensefalopati nihil minimal berat/koma
Nutrisi sempurna baik kurang/kurus
PT <4 4-6 >6
Keterangan:Skor 5-6 = Child A [angka kesintasan 1 tahun pertama = 100% angka kesintasan 2 tahun pertama = 85%Skor 7-9 = Child B [angka kesintasan 1 tahun pertama = 81% angka kesintasan 2 tahun pertama = 57%Skor 10-15 = Child C [angka kesintasan 1 tahun pertama = 45% angka kesintasan 2 tahun pertama = 35%
Penilaian program yang terbaru adalah Model for End Stage Liver Disease
(MELD) digunakan untuk pasien sirosis yang akan dilakukan transplantasi hati.
Tabel 4. Skor Model of End-Stage Liver Disease (MELD)
35

Rumus {,957 X 1n[kreatinin (mg/dL)] + 1,12 X 1n[INR(mg/dL)] + 0,643} X 10
Keterangan: 1n, logaritma natural; INR, international normalized ratio
Interpretasi Prediksi mortalitas dalam 3 bulan sebagai berikut:
Skor MELD ≥40: mortalitas 71,3%
Skor MELD 30-39: mortalitas 52,6%
Skor MELD 20-29: mortalitas 19,6%
Skor MELD 10-19: mortalitas 6,0%
Skor MELD ≤9: mortalitas 1,9%
Umumnya, mortalitas hanya terjadi setelah pasien mengalami fase
dekompensasi. Untuk sirosis kompeten saja, angka kesintasan selam 10 tahun
diperkirakan sekitar 90%, namun terjadinya dekompensata dalam 10 tahun tersebut
meningkat 50%. Sementara itu, angka kejadian KHS dilaporkan konstan 3% per tahun
dan berkorelasi dengan prognosis yang buruk pada setiap stadium KHS. 2
Tabel 5. Prognosis Sirosis Hati Berdasarkan Kondisi Klinis
Stadium Kompensasi Mortalitas 1 Tahun
Stadium 1 Terkompensasi, tanpa varises esofagus 1% per tahun
Stadium 2 Kompensasi, dengan varises esofagus 3-4 %
Stadium 3 Dekompensasi dengan asites 20%
Stadium 4 Dekompensasi dengan perdarahan gastrointestinal 57%
Stadium 5 Infeksi dan gagal ginjal 67%
BAB III
KESIMPULAN
36

Sirosis merupakan stadium akhir fibrotik hati akibat penyakit hati kronik
difus yang ditandai dengan adanya perubahan arsitektur hati yang membentuk jaringan
ikat dan gambaran nodul.
Penyakit ini dapat disebabkan berbagai etiologi. Infeksi virus hepaittis B dan C
merupakan penyebab yang s e r i ng d i I ndones i a , s edangkan a lkoho l
me rupakan penyebab terbanyak di daerah Barat. Seiring meningkatnya
obesitas, diabetes mellitus,penyakit jantung koroner, maka non alkoholik
steatohepatitis juga menjadi etiologi sirosis yang penting.
Pengobatan penyakit ini didasarkan pada etiologi dan gejala klinis yang tampak
serta ada tidaknya komplikasi yang timbul. Prognosis penyakit ini baik jika diobati pada
stadium dini (kompensata), namun jika telah lanjut, akan sulit untuk bertahan hinggalebih
dari 5 tahun, karena sirosis bersifat irreversibel. Terapi pasien sirosis dapat diberikan
mulai dari medikamentosa hingga transplantasi hepar.
Umumnya menegakkan diagnosis diperlukan pemeriksaan klinis dan pemeriksaan laboratorium
terhadap sirosis hepatis tersebut. Namun penemuan sirosis hati yang masih terkompensasi
mempunyai prognosa yang baik. Oleh karena itu ketepatan diagnosa dan penanganan yang tepat
sangat dibutuhkan dalam penatalaksanaan sirosis hati.
DAFTAR PUSTAKA
37

1. Nurdjanah S. Sirosis Hati diambil dari Buku Ajar Ilmu Penyakit Dalam Jilid I Edisi 5.
Aru W sudoyo dkk. 2009. Jakarta : FK UI. Halaman : 668-673.
2. Mansjoer, Arif. 2014. Kapita Selekta Kedokteran Edisi Keempat. Jakarta : FK UI. Halaman :
693 – 697.
3. W, Emiliana. Sirosis Hepatis Child Pugh Class C Dengan Komplikasi Asites Grade III dan
Hiponatremia. Medula. 2013. Volume 1 Nomor 5.
4. Fauci, dkk. 2009. Harrison Manual Kedokteran Jilid Dua. Halaman : 264-272.
5. Amiruddin Rifai. Fisiologi dan Biokimia Hati. Dalam : Sudoyo AW et.al, eds. Buku
Ajar Ilmu Penyakit Dalam. Edisi 4. Jakarta : Pusat Penerbitan ilmu Penyakit Dalam
Fakultas Kedokteran UI; 2006. Halaman: 6 - 415.
6. Faiz O, Moffat D. The liver, gall-bladder, biliary tree. In : Anatomy at a glance. USA:
Blackwell Publishing Company; 2002. Page : 5 – 44.
7. Lindseth, Glenda N. Gangguan Hati, Kandung Empedu, dan
Pankreas. Dalam : Sylvia A.Price et.al, eds. Patofisiologi. Edisi 6.
Jakarta : Penerbit Buku Kedokteran EGC ; 2006. Hal.472-5.
8. Netter FH. Surface and bed of liver. In : Atlas of Human Anatomy. 4 th Edition. USA :
Saunders Elsevier; 2006. Page : 287.
9. Douglas Eder. Histology. In : Laboratory Atlas of Anatomy and Physiology. 4 th
Edition. USA : McGraw-Hill Science; 2001. Page : 35
10. Hall & Guyton. Fisiologi Kedokteran. Edisi 11. Jakarta : Penerbit Buku
Kedokteran EGC; 2004. hal. 902-6.
38

39