Modulo 13 La glicolisi - moodle2.units.it · 8. fosfoglicerato mutasi: 3-fosfoglicerato...
Transcript of Modulo 13 La glicolisi - moodle2.units.it · 8. fosfoglicerato mutasi: 3-fosfoglicerato...

Modulo 13 La glicolisi
1

La glicolisi: via metabolica centrale del catabolismo del glucosio
2
} Via metabolica antica avviene interamente nel citoplasma delle cellule.
} Converte il glucosio in piruvato, producendo ATP e NADH. Il piruvato prodotto dalla glicolisi può avere diversi destini.
} Funzione: fornire energia e precursori per le biosintesi.
} Il processo è anaerobico. Può rappresentare la parte iniziale di un processo ossidativo successivo.
} Consiste di 10 reazioni sequenziali, suddivise in:
} Fase preparatoria: il glucosio è convertito in due molecole di trioso-P (fase di investimento - 2ATP)
} Fase di recupero energetico: vengono prodotte 2 molecole di piruvato + 4 ATP

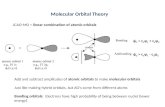
Conversione del glucosio a Fruttosio-6-P
3
Il Glucosio-6P non può più essere trasportato fuori dalla cellula.
1) La esochinasi conversione il glucosio a a glucosio-6- fosfato (Il fegato contiene anche una esochinasi diversa chiamata glucochinasi) .
H O
OH
H
OHH
OH
CH2OH
H
OH
H H O
OH
H
OHH
OH
CH2OPO32−
H
OH
H
23
4
5
6
1 1
6
5
4
3 2
ATP ADP
Mg2+
glucose glucose-6-phosphate Hexokinase
Glucosio Glucosio-6-fosfato Esochinasi
ΔG°’= -16,7 kJ mol-1
Glucosio + ATP Glucosio-6-P + ADP
La reazione richiede Mg2+ che si coordina con i due O carichi del gruppo P terminale dell’ATP .
2) Isomerizzazione del G-6-P a F-6-P
H O
OH
H
OHH
OH
CH2OPO32−
H
OH
H
1
6
5
4
3 2
CH2OPO32−
OH
CH2OH
HOH H
H HOO
6
5
4 3
2
1
glucose-6-phosphate fructose-6-phosphate Phosphoglucose Isomerase
Glucosio-6-fosfato Fosfoglucosio isomerasi
fruttosio-6-fosfato Converte un aldoso in chetoso.
ΔG°’= -1,7 kJ mol-1

Fosforilazione del F-6-P a fruttosio-1,6-BP
4
CH2OPO32−
OH
CH2OH
HOH H
H HOO
6
5
4 3
2
1 CH2OPO32−
OH
CH2OPO32−
HOH H
H HOO
6
5
4 3
2
1ATP ADP
Mg2+
fructose-6-phosphate fructose-1,6-bisphosphate
Phosphofructokinase
fruttosio-6-fosfato fruttosio-1,6-bisfosfato
Fosfofruttochinasi
ΔG°’= -14,2 kJ mol-1
3. Fosfofruttochinasi 1 (PFK-1): fruttosio-6-P + ATP fruttosio-1,6-bisfosfato + ADP La fosfofruttochinasi è un enzima allosterico (tetramero di 340 kDa), sottoposto a regolazione che condiziona tutto il flusso della via metabolica.

Scissione del fruttosio-1,6-BP in gliceraldeide 3P
5
4. Aldolasi (fruttosio-1,6-bisfosfato aldolasi) fruttosio-1,6-bisfosfato diidrossiacetone-P + gliceraldeide-3-P
gliceraldeide-3-fosfato
fruttosio-1,6-bisfosfato
Diidrossiacetone -3-fosfato
4. Aldolasi
6 5
4
3
2
1 C H 2 O P O 3 2 -
C
C
C
C
C H 2 O P O 3 2 -
O
H O H
H O H
H O H
3 2
1
C H 2 O P O 3 2 -
C
C H 2 O H
O
C
C
C H 2 O P O 3 2 -
H O
H O H +
1
2 3
La reazione è una scissione aldolica, f a c i lmente rever s i b i l e i n una condensazione aldolica (reazione inversa).
gliceraldeide-3-fosfato
Diidrossiacetone -3-fosfato
3
2
1
C H 2 O P O 3 2 -
C
C H 2 O H
O
C
C
C H 2 O P O 3 2 -
H O
H O H
1
2
3
5. Trioso fosfato isomerasi (TPI) Diidrossiacetone-3-P gliceraldeide-3-P
ΔG°’= 7,5 kJ mol-1
La rimozione della gliceraldeide-3-P spinge la conversione del diidrossiacetone-3-P verso l’isomero aldeidico,
ΔG°’= 23,8 kJ mol-1

Ossidazione della gliceraldeide-3-P a acido 1,3 bisfosfoglicerico
6
gliceraldeide-3-P + NAD+ + Pi 1,3-bisfosfoglicerato + NADH + H+
La reazione esoergonica dell’ossidazione di una aldeide ad acido carbossilico viene conservata e porta alla formazione di gruppo acilfosfato (anidride mista) con un elevato potenziale di trasferimento del gruppo fosforico. L’acil fosfato ha una energia libera di idrolisi elevata ΔG°’= -49,3 kJ /mol.
C
C
CH2OPO32−
H O
H OH
C
C
CH2OPO32−
O OPO32−
H OH+ Pi
+ H+
NAD+ NADH 1
2
3
2
3
1
glyceraldehyde- 1,3-bisphospho- 3-phosphate glycerate
Glyceraldehyde-3-phosphate Dehydrogenase
gliceraldeide-3-fosfato
1,3-bisfosfoglicerato
6. G3PDH
ΔG°’= 6,5 kJ mol-1
6. Gliceraldeide-3-fosfato deidrogenasi (GAPDH): unica tappa ossidativa della glicolisi, in cui NAD+ è ridotto a NADH + (+H+)

La reazione catalizzata dalla gliceraldeide-3P deidrogenasi (GADPH)
7
In realtà l’ossidazione non avviene in modo diretto: le due reazioni sono accoppiate attraverso un intermedio tioestere: ha una energia libera più elevata dell’acido carbossilico libero
ossidazione +
C C C H 2 O P O 3 2 -
H O H O H
2 3 1
NAD+ + H2O
C C C H 2 O P O 3 2 -
O O - H O H 2
3 1
NADH + H+ +
C C C H 2 O P O 3 2 -
O O - H O H 2
3 1
P i C C C H 2 O P O 3 2 -
O O P O 3 2 - H O H 1
2 3
+
gliceraldeide-3-P
1,3-bisfosfoglicerato
3-fosfoglicerato
3-fosfoglicerato
La reazione potrebbe essere considerata come la somma di due reazioni consecutive non accoppiate : i) l’ossidazione dell’aldeide ad acido carbossilico, mediata da NAD+, ii) unione dell’ortofosfato all’acido carbossilico per dare acil-fosfato.
Caso ipotetico
Caso effettivo

Meccanismo catalitico della GAPDH
8
Struttura della GAPDH : il sito attivo include una His ed una Cys adiacenti ad una molecola di NAD+
L’energ i a r i l a sc i a t a dal l ’oss idaz ione del c a r b o n i o v i e n e conservata in elevato p o t e n z i a l e d i t r a s f e r i m e n t o d e l gruppo fosforico.

Trasferimento del gruppo P all’ADP ed isomerizzazione del 3-fosfoglicerato
9
Il potenziale di trasferimento del 1,3 bisfosfoglicerato è superiore a quello dell’ATP. Esempio di fosforilazione a livello di substrato.
8. fosfoglicerato mutasi: 3-fosfoglicerato 2-fosfoglicerato
C
C
CH2OPO32−
O OPO32−
H OH
C
C
CH2OPO32−
O O−
H OH
ADP ATP1
22
3 3
1
Mg2+
1,3-bisphospho- 3-phosphoglycerate glycerate
Phosphoglycerate Kinase
1,3-bisfosfoglicerato
3-fosfoglicerato
C
C
CH2OH
O O−
H OPO32−
2
3
1C
C
CH2OPO32−
O O−
H OH2
3
1
3-phosphoglycerate 2-phosphoglycerate
Phosphoglycerate Mutase
3-fosfoglicerato 2-fosfoglicerato
Reazione di riordinamento molecolare. Il fosfato viene spostato dall’ossidrile sul C3 all’ossidrile in C2.
ΔG°’= -18,5 kJ mol-1
7. fosfoglicerato chinasi: 1,3-bisfosfoglicerato + ADP 3-fosfoglicerato + ATP
Mg2+

Formazione del fosfoenolpiruvato e trasferimento del gruppo fosforico all’ADP
10
9. Enolasi:
2-fosfoglicerato fosfoenolpiruvato + H2O
La deidratazione introduce un doppio legame (enolo). Il fosfoenolpiruvato (PEP), un enol-P, ha un ΔG di idrolisi del gruppo P > di quello dell’ATP. Perché: il P mantiene la molecola nella sua forma enolica instabile.
10. Piruvato chinasi: fosfoenolpiruvato + ADP piruvato + ATP
La rimozione del Pi dal PEP da parte dell’ADP dà origine ad un enolo instabile che spontaneamente si converte nella forma chetonica, cioè nel piruvato.
ΔG°’= -31,4 kJ mol-1
fosfoenolpiruvato enolpiruvato piruvato
2-fosfoglicerato fosfoenolpiruvato
C
C
C H 2
O O -
H O P O 3 2 -
2
3
1 C
C
C H 2
O O -
O P O 3 2 -
2
3
1
+ H 2 O
Enolasi
C
C
C H 3
O O -
O 2 3
1 A D P A T P C
C
C H 2
O O -
O P O 3 2 -
2 3
1 C
C
C H 2
O O -
O H 2 3
1
Piruvato chinasi
ΔG°’= + 7,5 kJ mol-1
HO
K+, Mg2+

Bilancio della glicolisi
11
In totale durante le dieci tappe, il bilancio per quanto riguarda i legami fosforici è stato:
• 2 ATP spesi
• 4 ATP prodotti (2 da ogni trioso formato dal glucosio)
• Produzione netta 2 legami ~P di ATP per molecola di glucosio
Il bilancio complessivo della glicolisi è: 1 glucosio + 2 NAD+ + 2 ADP + 2 Pi à 2 piruvato + 2 NADH + 2 ATP + 2 H20
Se la glicolisi si fermasse a questo punto non potrebbe procedere a lungo: il bilancio redox è venuto meno (deplezione di NAD+).
http://themedicalbiochemistrypage.org/glycolysis.php

Utilizzo metabolico di altri monosaccaridi/disaccaridi
12

I possibili destini metabolici del piruvato
13
Il destino del piruvato dipende dalle condizioni fisiologiche, dai tessuti e gli organismi in cui viene prodotto.
Lieviti, altri microrganismi
Glicolisi
Muscoli in anaerobiosi
Fermentazioni Ossidazione Completa
glucosio
piruvato
lattato
Etanolo
Microrganismi lattici
respirazione

Il lattato è l’accettore terminale degli elettroni nella fermentazione lattica
14
In esercizio il muscolo scheletrico lavora anaerobicamente quando la disponibilità di ossigeno diventa insufficiente ed il metabolismo aerobico non può fornire l’energia richiesta. La glicolisi è, in condizioni anaerobie, la maggior fonte di ATP
ΔG°’= -25,1 kJ mol-1
Il piruvato è convertito a lattato, in questo modo viene rigenerato NAD+ necessario per la continuazione della glicolisi
glucosio + 2 ADP + 2 Pi à 2 lattato + 2 ATP + 2H2O
Piruvato Lattato
Lattico deidrogenasi
C
C
C H 3
O -
O
O C
H C
C H 3
O -
O H
O N A D H + H + N A D +

La fermentazione alcolica
15
Diversi organismi anaerobi (lieviti) trasformano il piruvato ad etanolo, secreto come prodotto di scarto. L’alcol deidrogenasi rigenera il NAD+, necessario per continuare la glicolisi.
Piruvato Acetaldeide Etanolo
Alcol deidrogenasi
Piruvato decarbossilasi
3
C
C
C H
O -
O
O
C
C H 3
O H C
C H 3
O H H
H
N A D H + H + N A D + C O 2
glucosio + 2 ADP + 2 Pi + 2H+ à 2 etanolo + 2CO2 + 2H2O +2ATP

La regolazione della glicolisi
16
Sono tre enzimi regolatori il cui controllo determina il flusso metabolico (la velocità di reazione) lungo la via glicolitica. Essi catalizzano reazioni virtualmente irreversibili, cioè reazioni che sono lontane dall’equilibrio (ΔG <<=0) I. la fosfofruttochinasi: principale punto di controllo, inibito da ATP II. la esochinasi, inibita allostericamente dal suo prodotto il glucosio-6-
fosfato. III. piruvato chinasi: enzima allosterico inibito da ATP (elevata energia),
alanina (elevato livello precursori) , attivato invece dal F-1,6-BP
Il controllo avviene a due livelli:
Controllo locale: dipendenza delle reazioni catalizzate da enzimi da parte delle concentrazioni di substrati ed intermedi presenti nella cellula. Controllo globale: controllo esercitato da ormoni, che agiscono a distanza tramite secondi messaggeri e regolano le vie metaboliche a beneficio dell’intero organismo.

La fosfofruttochinasi è modulata allostericamente
Fosfofruttochinasi: il principale punto di controllo della glicolisi nei mammiferi e determina il flusso lungo questa via. È il rapporto ATP/ADP a svolgere un ruolo primario.
17
L’ATP si lega ad un sito regolatorio promuovendo un cambiamento c o n f o r m a z i o n a l e l ’ i n i b i z i o n e dell’enzima (curva spostata a destra).
L’enzima (omotetramero) v i e n e i n i b i t o allostericamente dall’ATP, mentre AMP ed ADP ne antagonizzano l’effetto. La glicolisi è inibita quando la carica energetica è elevata.

Schema di controllo della glicolisi nei muscoli
18

Variazioni di energia libera delle reazioni dellaglicolisi (calcolate da stime di concentrazioni di substrati)
0.8FOSFOGLICERATO MUTASI-3.3ENOLASI
-16.7PIRUVATO CHINASI
-1.8FOSFOGLICERATO CHINASI-1.7GLICERALDEIDE-3P DEIDROGENASI+2.5TRIOSO FOSFATO ISOMERASI-1.3ALDOLASI
-22.2FOSFOFRUTTOCHINASI-2.5FOSFOGLUCOISOMERASI
-33.5ESOCHINASIΔG (kJmol-1)ENZIMA

20
La gluconeogenesi non è l’inverso della glicolisi: produzione di glucosio da fonti non glucidiche

La gluconeogenesi non è l’inverso della glicolisi
21
Gluconeogenesi: sintesi del glucosio da precursori non glucidici (lattato, amminoacidi, glicerolo) convertiti in piruvato o in intermedi che entrano nella via successivamente.
Organi interessati: fegato in primis, poi rene ed intestino per rifornire altri organi (cervello).
Funzione: mantenere alti i livelli di glucosio durante il digiuno. La gluconeogenesi non è l’inverso della glicolisi: tre reazioni scavalcano le reazioni virtualmente irreversibili
della glicolisi: 1. La conversione del piruvato in PEP (piruvato carbossilasi +
PEP carbossichinasi) 2. La defosforilazione del F 1,6 BP (fruttosio 1,6 bifosfatasi 1 ) 3. La defosforilazione del G6P (glucosio 6 fosfatasi)
Complessivamente è un processo dispendioso: 2 Piruvato + 4 ATP + 2 GTP + 2 NADH + 6 H2O → Glucosio + 4 ADP + 2 GDP + 6 Pi + 2 NAD+

Gluconeogenesi – conversione del piruvato in PEP
22
1. P i r u v a t o c a r b o s s i l a s i e n z i m a (mitocondriale) che utilizza la biotina come donatore di CO2 per convertire il piruvato in ossalacetato (OA)
2. PEP carbossichinasi, enzima che decarbossila l ’OA per formare PEP. Il donatore di P è il GTP
Le decarbossilazioni spesso favoriscono reazioni altrimenti endoergoniche. La carbossilazione/decarbossilazione è un sistema di “attivazione” del piruvato.
Piruvato + ATP + GTP + HCO3- → PEP + ADP + GDP + Pi + CO2
ΔG°’= 0,9 kJ /mol

Glicolisi e gluconeogenesi sono regolate reciprocamente
23
Glicolisi e gluconeogenesi sono fortemente esoergoniche, non c’e’ nessun impedimento di ordine termodinamico a che entrambe possano svolgersi allo stesso tempo: devono essere regolate reciprocamente. Principali punti di controllo: conversione del F 6-P a F 1,6-P e del PEP a piruvato
Se carica energetica è bassa ATP↓ : glicolisi J gluconeogenesi L
Se carica energetica è alta ATP ↑ : glicolisi L gluconeogenesi J
Se precursori abbondanti: citrato, alanina ↑ glicolisi L gluconeogenesi J
Presenza di F-2,6-BP ↑ glicolisi J gluconeogenesi L
Glicolisi: ΔG °’ complessivo per produrre piruvato da glucosio: ΔG °’ = -84 kJ mol-1
Gluconeogenesi: ΔG °’ per produrre glucosio da piruvatoΔG °’ = -38 kJ mol-1

La regolazione epatica della glicolisi e gluconeogenesi
24
Il fegato ha funzioni aggiuntive ed uniche: 1) mantiene costanti i livelli ematici di glucosio sintetizzando glucosio, degradando glicogeno, e rilasciando glucosio. 2) Utilizza glucosio per produrre NADPH (potere riducente ). I meccanismi di regolazione della glicolisi sono più complessi nel fegato.
Il più importante regolatore della glicolisi nel fegato: fruttosio 2,6 bisfosfato (F-2,6-BP). Quando il g lucosio è abbondante v iene prodotto F-2 ,6-BP, att ivatore allosterico della PFK (stimolazione anterograda).
Attività della PFK-1 Attività della FBPasi-1

Controllo della sintesi e degradazione del 2,6-bisfosfato
25
Nel fegato il principale regolatore delle glicolisi e della gluconeogenesi è il Fruttosio 2,6 bisfosfato prodotto da un enzima bifunzionale: PFK2. La sua regolazione è controllata da ormoni.
Insulina e glucagone controllano in maniera opposta l’enzima bifunzionale PFK-2/ FBPasi-2 che produce o degrada il fruttosio 2,6 bisfosfato.
Glucagone: segnala al fegato di produrre e rilasciare glucosio stimolando l’attività della FBPasi-2 per fosforilazione e quindi della gluconeogenesi (rifornimento di glucosio).
PFK2 = fosfofruttochinasi 2 FBPasi2 = fruttosio bisfosfatasi 2
L’insulina attiva una fosfoproteina fosfatasi che inibisce la FBPasi2 e attiva la PFK2

Regolazione diRegolazione di GlicolisiGlicolisi e e GluconeogenesiGluconeogenesiREGOLAZIONE GENICA

Il metabolismo del glicogeno: la degradazione
27
La demolizione del glicogeno nel muscolo scheletrico e nel fegato è catalizzata dalla g l icogeno fosfori las i che catalizza una reazione di fosforolisi
Glucosio 1-P ↔ Glucosio 6-P (glicolisi) (fosfoglucomutasi)
Il glucosio G-1P rilasciato è poi convertito in intermedio della glicolisi G-6P

L’azione dell’enzima deramificante rende il glicogeno una catena lineare
28
Enzima deramificante: Oligo α(1→6) α(1→4)glucantransferasi

La glicogeno fosforilasi è regolata sia allostericamente che ormonalmente
29
Con elevati livelli di G in sangue: nel fegato: glucochinasi (esochinasi IV) con KM di 50 volte quella della esochinasi , non inibito dal glucosio 6 P. Ruolo nella sintesi del glicogeno.
Nel fegato il glucagone attiva la glicogeno fosforilasi per effetto di una fosforilazione AMPc/PKA dipendente della fosforilasi b chinasi (vedi regolaz enzimatica) Nel muscolo scheletrico l’adrenalina ha un effetto simile mentre Ca2+ e AMP sono attivatori allosterici.

L’ossidazione del glucosio attraverso la via del pentosio fosfato
30
Glucos io-6-P : precursore d i composti necessari alla cellula: via de l pentos io fos fato (o del fosfogluconato). Presente in tutte le cellule, nel citoplasma. Funzioni: 1) Via ossidativa per produrre
NAPDH (donatore di e- nelle biosintesi riduttive).
2) Via per produrre ribosio 5-fosfato (per sintesi di nucleotidi e quindi, DNA, RNA; NADH, FADH2 e coenzima A.
La via è versatile: il flusso può essere modificato per far prevalere uno dei due obiettivi.
Attivo soprattutto nel tessuto adiposo e nella ghiandola mammaria e negli eritrociti

Ciclo dei Pentoso Fosfati
Avviene nel citoplasma
Glucosio-6P DH
NADPH Acidi grassi liberi
6 fosfogluconato lattonasi
Fase ossidativa
6- fosfoglucono lattone
6- fosfoglucono lattone

Fase ossidativa 6-fosfo gluconato DH

Le reazioni ossidative della via del pentosio fosfato
33
Due fasi : 1) Fase ossidativa: produce pentosio P e NADPH
con 4 reazioni (2 deidrogenasi e due isomerasi).
Glucosio-6-P + 2 NADP+ + H20 → D-ribosio-5-P + 2 NADPH + 2H+
2) Fase NON ossidativa: ricicla i pentosi fosfato in glucosio-6 P, oppure gli utilizza per sintetizzare nucleotidi.
Bilancio della fase ossidativa:

Fase NON ossidativa: ricicla i pentosi fosfato in glucosio -6 P
34
Reazioni (reversibili) che convertono i pentosi (C5) in esosi (C6) e consentono alla via metabolica di proseguire. Da 6 pentosi si producono 5 molecole di G6-P

Vie che richiedono NADPH Sintesi Biosintesi degli acidi grassi Biosintesi del colesterolo Biosintesi di neurotrasmettitori Biosintesi di nucleotidi Detossificazione Riduzione del glutatione ossidato Citocromo P540 monoossigenasi

4
RAPPRESENTAZIONE SCHEMATICA DEL METABOLISMO DEL GLUCOSIORAPPRESENTAZIONE SCHEMATICA DEL METABOLISMO DEL GLUCOSIO

37
Lezione 2 - Biochimica Applicata
Farmacia AA 2011/12 6
DIGESTIONE DELL’AMIDO
AMIDO
DESTRINE
Amilasi salivare
(ptialina)
Amilasi pancreatica
MALTOSIO
GLUCOSIO
Vena porta
Enzimi parete
intestinale
DIGESTIONE DEI DISACCARIDI DISACCARIDI
MONOSACCARIDI
Enzimi parete intestinale
Vena porta
Digestione dei carboidrati
bocca
stomaco
distretto substrato enzima prodotto
amilopectina
glicogeno
ptialina
(solo a1-4 interni no
a1-6, a1-4 terminale
amilosio
maltosio
maltotriosio
destrine a-limite
inattivazione da HCl
pancreas
fegato
intestino
amilosio
amilopectina
glicogeno
a-amilasi
stessi legami della
ptialina ma più
potente
amilosio
maltosio
maltotriosio
destrine a-limite
duodeno
digiuno
Lattosio
Saccarosio
Destrine
lattasi
saccarasi
a destrinasi a1 6
galattosio+glucosio
fruttosio+glucosio
tenue a-limite
malto-oligosaccaridi
a-destrinasi a1-6
Glucoamilasi a1-4
terminali
glucosio
glucosio
glucosio