LARİNGOSKOPİ VE ENTÜBASYONA BAĞLI OLARAK GELİŞEN ...
Transcript of LARİNGOSKOPİ VE ENTÜBASYONA BAĞLI OLARAK GELİŞEN ...

T.C.
SAĞLIK BAKANLIĞI
Haseki Eğitim ve Araştırma Hastanesi
I. Anesteziyoloji ve Reanimasyon Kliniği
Şef Dr. Gülşen BİCAN
LARİNGOSKOPİ VE ENTÜBASYONA BAĞLI OLARAK
GELİŞEN HEMODİNAMİK CEVAPLARIN ÖNLENMESİNDE
DEXMEDOTİMİDİNE VE REMİFENTANİLİN
ETKİNLİĞİNİN KARŞILAŞTIRILMASI
(Uzmanlık Tezi)
Dr. Rahime AYDINLI
(Tez Danışmanları)
Uz. Dr. Feray GÜLER Uz. Dr. Sinan UZMAN
İSTANBUL-2009

ÖNSÖZ
Bilgi ve becerilerini benden esirgemeyen, varlığını ve sıcaklığını her zaman yanımda hissetti
ğim, destekleyici tavırlarıyla mesleki anlamda gelişmemi sağlayan sevgili hocam, klinik
şefimiz Sn. Dr. Gülşen Bican’a ;
Aynı ortamı paylaşmaktan onur ve mutluluk duyduğum tüm uzman ve asistan
arkadaşlarıma ;
Anlayış ve destekleri için ameliyathane ve yoğunbakım ünitesinde birlikte çalıştığımız
anestezi teknisyenlerine, hemşire ve personel arkadaşlarıma ;
Her zaman her koşulda yanımda olan danışmanlarım Uzm. Dr. Feray Güler ve Uzm. Dr.
Sinan Uzman’ a ;
Doktor olma onur ve gururunu yaşamama olanak sağlayan canımdan çok sevdiğim,
varlıkları ile bana güç veren sevgili annem ve babama, biricik kardeşim Burcu Aydınlı’ ya ve
canım ablam Funda Demetgül ’e en derin saygı ve sevgilerimi sunarım.
teşekkür ederim.
Dr. Rahime AYDINLI
i

İÇİNDEKİLER
Giriş ………………………………………………………………………… 1
Genel Bilgiler………………………………………………………………. 3
Materyal ve Metod……………………………………..………………….. 37
Bulgular, tablo, şekil ve grafikler ………………………………………… 39
Tartışma…………………………………………………………………… 51
Sonuç……………………………………………………………………… 59
Özet…………………………....................................................................... 60
Summary………………………………………………………………….. 61
Kaynaklar…………………………………………..……………………... 62
ii

iii
KISALTMALAR
LTE : Laringoskopi ve trakeal entübasyon.
LTI : Laryngoscopy and tracheal intubation.
sn : saniye
dak : dakika
SAB : sistolik arter basıncı
DAB : diastolik arter basıncı
OAB : ortalama arter basıncı
KAH : kalp atım hızı
ICP : intrakranyal basınç
s : saat
µg : mikrogram
kg : kilogram
SSS : sempatik sinir sistemi
NE : Norepinefrin
EPI : epinefrin
L : Litre
ml : mililitre
NIKB : noninvaziv kan basıncı

GİRİŞ
Laringoskopi ve trakeal entübasyonun (LTE) refleks dolaşımsal cevaplara yol açtığı uzun
yıllardan beri bilinmektedir(1). LTE; hipertansiyon, taşikardi, plazma katekolamin
konsantrasyonları ve intrakranyal basınçta artış, EKG değişiklikleri ve aritmilere yol açan
güçlü bir uyarandır (2-9). Hemodinamik değişiklerin sebebi olan sempatik ve sempatoadrenal
aktivitedeki artışın, LTE sırasında üst hava yollarının stimülasyonu ile ortaya çıktığı ve glottik
bölgedeki basının derecesiyle doğru orantılı olduğu bildirilmiştir(4,10,11).
Bu stres cevaplar, her ne kadar geçici olup sağlıklı bireylerde herhangi bir probleme yol
açmaksızın kısa sürede ortadan kalksa da, dikkatli bir hemodinamik kontrolün gerektiği
preeklamtik/eklamptik gebeler, koroner arter hastalığı, sistemik hipertansiyon, aortik veya
intrakraniyal anevrizması olan hastalarda ciddi komplikasyonların ortaya çıkışına, mortalite
ve morbiditede artışa yol açabilir(12-16). Hemodinamik cevapların önlenmesi veya azaltılması
için; alfentanil(5,14), fentanil(17), sufentanil(18) gibi opioid ajanlar, esmolol(19), nitrogliserin gibi
vazodilatörler(20), kalsiyum kanal blokerleri(21), magnezyum sülfat(22) kullanımını içeren
birçok farmakolojik manevra önerilmiştir.
Remifentanil, hızlı başlangıçlı ve çok kısa etki süresine sahip, esterazlarla metabolize olunan
potent bir μ-opioid reseptör agonistidir(23). Entübasyondan önce 1 μg.kg-1 dozda tek bolus doz
olarak uygulandığında hemodinamik cevapların azaltılmasında etkili olduğu bildirilmiştir(24).
Deksmedetomidin, yüksek derecede selektif bir α2 adrenoseptör agonistidir. Solunum
depresyonuna yol açmayan, sedatif, analjezik, anksiyolitik ve sempatolitik etkilere sahiptir.
En önemli yan etkisi hipotansiyon ve bradikardidir(25,26). Deksmedetomidinin anestezi
indüksiyonundan önce 1 μg.kg-1 tek bolus doz olarak uygulanmasının LTE sırasında oluşan
hemodinamik cevapları azalttığı gösterilmiştir(27).
Çalışmamızda, propofol ve rocuronyum ile yapılan anestezi indüksiyonundan önce; tek bolus
doz olarak 60 saniye içerisinde verilen 1 μg.kg-1 remifentanil ile, 5 dakika içerisinde verilen
1

1μg.kg-1 deksmedetomidinin laringoskopi ve trakeal entübasyon sırasında oluşan
hemodinamik cevapların azaltılmasındaki etkinliklerini karşılaştırmayı amaçladık.
2

GENEL BİLGİLER
A. LARİNGOSKOPİ ve TRAKEAL ENTÜBASYON
İnsanda uygulanan ilk trakeal entübasyona tarihi kaynaklarda İbn-i Sina’nın eserlerinde
rastlıyoruz. Bundan yaklaşık 900 yıl sonra bugünkü manada endotrakeal entübasyon, William
MacEwen tarafından 1880 yılında gerçekleştirilmiştir. MacEwen laringoskopi
uygulamaksızın parmaklarının yardımıyla trakea içerisine metal bir tüp yerleştirerek
kloroform anestezisi uygulamış ve dil tabanından bir tümör eksize etmiştir. Endotrakeal
tekniğin gelişimi baş, boyun ve ağız içi cerrahisi sırasındaki güvenli anestezi ihtiyacıyla ivme
kazanmıştır. Endotrakeal entübasyonun gelişiminde Magill ve Rowbotham’ın çabalarını göz
ardı etmek mümkün değildir. Trakea içine geniş kauçuk bir tüp yerleştirerek hastanın sadece
inhalasyonuna değil ekshalasyonuna da imkan sağlayan yarı-kapalı anestezi sistemleri
oluşturmuşlardır. 1912’de Elsberg’in Jacson’ın tasarladığı aleti endotrakeal anestezide
kullanması, o zaman kadar anestezistler tarafından ihmal edilen laringoskopiyi modern
endotrakeal anesteziye kazandırarak entübasyonların artık kör olarak değil doğrudan larenksin
görülerek yapılmasına imkan sağlamıştır(28).
Laringoskopik entübasyon güçlüğü varlığında ventilasyon ve oksijenasyonun
sağlanmasındaki yetersizlik bir anestezistin yaşayabileceği en büyük felaketlerden birisidir.
Bu yüzden havayolu kontrolünü sağlamak bir anestezistin belki de en temel becerisi ve
sorumluluğudur. Son birkaç dekaddır anestezistler, preoperatif havayolu değerlendirilmesinin
kritik önemi üzerinde daha dikkatle durmaktadırlar(29,30).
Havayolu anatomisinin bilinmesi başarılı bir trakeal entübasyonun ilk adımıdır(31).
1. Üst Hava Yolları Anatomisi
Burun ve ağız boşlukları ile, farenks, larenks, trakea’nın üst kısmından meydana gelen üst
hava yolları, solunum sisteminin göğüs boşluğu dışında kalan kısmını oluşturur. Başlıca
fonksiyonları; havanın alt solunum yollarına iletilmesi ve ısıtılıp nemlendirilmesi,
3

trakeaobronşial ağaca yabancı cisimlerinin girişinin önlenmesiyle konuşma ve koku
duyusunun alınmasında rol oynaması olarak sayılabilir. Üst hava yollarının iki girişi vardır.
Birinci giriş olan burun; nazofarenks (pars nasalis) ile, ikincisi olan ağız ise orofarenks (pars
oralis) ile devam eder. Bu giriş yerleri önde damak ile birbirlerinden ayrılırken arkada
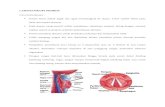
farenkste birleşirler(30,32,33).(Şekil-1)
Burun: Solunum sistemine havanın girişi ve çıkışı normal soluma sırasında burun yoluyla
olur. Burnun solunumdaki en önemli fonksiyonu havanın ısıtılıp nemlendirilmesidir. Ayrıca
koku duyusunun alındığı ve konuşma sırasında rezonansın oluştuğu bölgedir. Burun
deliklerinden nazofarenkse uzanan ve septumla ayrılmış iki boşluktan meydana gelir. Üst
solunum yollarında enfeksiyon veya polip gibi bir nedenle obstrüksiyon gelişmedikçe, burun
temel soluma yoludur. Sessiz bir solunum sırasında nazal pasajdaki direnç, hava yollarındaki
toplam direncin 2/3’ünü oluşturur(33,34).
Farenks: Hem solunum hem de sindirim sisteminin ortak olan üst kısmını meydana getirir.
Kafatabanı hizasında burnun arka kısmından başlayarak krikoid kıkırdağa kadar uzanarak
ösafagus ile devam eder. U şeklinde fibromüsküler bir yapıdır. Burun ve ağız boşuklarının
arkasında servikal vertebranın önünde yer alır. Farenks; nazofarenks, orofarenks ve
laringofarenks olmak üzere 3 kısımda incelenir ve önde sırası ile burun ve ağız boşlukları ile
larenkse serbestçe açılır. Nazofarenks burnun arkasında ve yumuşak damağın üzerinde yer
alır. Nazofarenks orofarenksten önde yumuşak damakla, arkada hayali bir düzlemle ayrılır.
Farengeal tonsil veya adenoid olarak adlandırılan lenfoid yapılar nazofarenksin arka
duvarında lokalizedir ve büyüdüklerinde hava akımına engel oluştururlar. Ayrıca östaki
borusu da nazofarenksin lateral duvarına açılır. Önde ağız boşluğuna açılan orofarenks
yumuşak damakla hyoid kemik hizasındaki dil kökü arasında uzanır. Göze çarpan en önemli
yapılar yan duvarlarındaki tonsillalardır. Genioglossus kasının tonusunda azalmayla dilin
geriye düşmesi orofarengeal obstrüksiyonun başlıca sebebidir. Bu kas dili öne doğru hareket
4

ettirerek farengeal bir dilatör olarak rol oynar. Laringofarenks (hipofarenks), farenksin en alt
kısmıdır. Önde larenkse arkada ise ösafagusa açılır. Epiglotun tepesinden, C6 hizasındaki
krikoidin alt kenarına kadar uzanır. Dil kökünde epiglot fonksiyonel olarak orofarenksi
laringofarenksten ayırır. Epiglot yutma sırasında glottisin üzerini örterek aspirasyonu
önler(30,32,33,34,35). (Şekil-1)
Şekil-1 Üst hava yollarının anatomisi
Larinks, dil tabanıyla trakea arasında yer alan ses kutusudur. Fonasyon organı olarak ve mide
içeriğinden alt hava yollarını koruyan bir kapak olarak görev yapar. 3. ve 6. servikal
vertebralar hizasında uzanır. Ligaman ve kaslar aracılığıyla birbirine bağlanan kıkırdak bir
iskeletten meydana gelir. Yapısında 3 tanesi çift 3 tanesi tek olmak üzere toplam 9 adet
kıkırdak bulunur. Tek olanlar tiroid, krikoid ve epiglot; çift olanlar ise aretenoid, kornikulat
ve kuneiform kıkırdaklardır(30,32,34). (Şekil-2)
5

Şekil-2 Larinksin anatomik yapısı
Adem elması olarak da adlandırılan tiroid kıkırdak larenksin en büyük kıkırdağıdır. İnferior
olarak birleşen iki laminadan meydana gelir. Üst kenarında V-şeklinde olan tiroid çentik
bulunur. Üst kısmı tirohyoid membranla hyoid kıkırdağa bağlanır. Epiglot geniş kaşık
şeklinde fibrökartilagenöz bir yapıdır. Yutkunma sırasında larenks girişini örterek aspirasyonu
önler. Epiglot ve dil tabanı mukoza kıvrımlarıyla birbirine bağlanarak vallekula adı verilen
küçük bir boşluk oluşturur. Bu alan laringoskop bleydinin kavsinin yerleşmesini sağlayan bir
bölge oluşturur. (Şekil-3) Krikoid kıkırdak yüzük şeklindedir ve tiroid kıkırdağın altındadır.
Larenksin arka duvarının büyük kısmını krikoid kıkırdak oluşturur. Alt kenarıyla ilk trakeal
kıkırdağa bağlanır. Aritenoid kıkırdaklar 3 yüzeyli bir piramid şeklindedir. Krikoid kıkırdağın
arka kısmının üst yüzeyine oturur. Aritenoid kıkırdakların apeksi arka ve içe doğru bir eğim
oluştur ve kornikulat kıkırdaklarla eklem yapan yassı bir yüzey oluşturur. Kuneiform ve
kornikulat kıkırdaklar areitenoidlerle yakın birliktelik gösteren küçük yardımcı
kıkırdaklardır(32,33,34).
6

Şekil-3 Laringoskopi sırasında blade ucunun vallakulaya yerleşimi.
Larengeal boşluk epiglottan krikoid kıkırdağın alt sınırına kadar uzanır. Larinks’in girişi
epiglot tarafından oluşturulur. Epiglot, her iki yanda ariepiglottik kıvrımlarla aretenoid
kıkırdakların üst ucuna bağlanır. Larengeal boşluğun içinde fibröz dokudan oluşan dar bir
bant olan vestibüler kıvrım yer alır. Vestibüler kıvrımlar, aritenoidlerin anterolateral
yüzeyinden, epiglota bağlanan tiroidal çentiğe uzanır. Vestibüler kıvrımlar yalancı vokal
kordlar olarak adlandırılır ve gerçek vokal kordlardan larengeal sinüs veya ventrikülle
ayrılırlar. Gerçek vokal kordlar, soluk beyaz renkte ligamentöz yapılardır. Önde tiroidal
çentiğe arkada ise aritenoidlere bağlanırlar. Vokal kordlar arasındaki üçgen şeklindeki aralık
(trianguler fissure) glottik girişi oluşturur. Bu, erişkinde larengeal girişin en dar segmentidir.
10 yaşın altındaki çocuklarda ise en dar segment, krikoid halka düzeyinde kordların hemen
altındadır(34). (Şekil-4)
7

Epiglot
Vokal kordlar
Glottik giriş
Şekil-4 Larinks girişinin anatomik yapısı
Trakea, 6. servikal vertebra hizasında, tiroid kıkırdak düzeyinde başlar, tübüler bir yapıdadır.
Arka kısmı düzleşmiştir ve 10-15 cm boyunca 16-20 adet atnalı şeklindeki kıkırdak halka
tarafından, 5. torasik vertebra düzeyinde, sağ ve sol ana bronşa ayrıldığı bifurkasyona kadar
desteklenir. Enine kesit alanı glottisten fazladır (150-300 mm2). Trakeada mekanik ve
kimyasal stimülüslere duyarlı birkaç tip reseptör bulunur. Trakeanın arka yüzündeki kaslar
içinde yavaş adaptasyon gösteren gerilim reseptörleri bulunur. Bunlar solunumun hızı ve
derinliğini düzenlerler. Ayrıca vagal efferent aktiviteyi azaltarak, üst havayolları ve
bronşlarda dilatasyon da oluştururlar. Diğer reseptörler, hızlı adaptasyon gösteren irritan
reseptörlerdir. Trakeanın tüm çevresi boyunca uzanırlar. Öksürük ve bronkokonstrüksiyona
yol açarlar(34).
Üst hava yollarının duysal innervasyonu, kranial sinirlerden sağlanır. Burun mukozası, önde
trigeminal sinirin oftalmik parçası (V1 anterior etmoidal sinir), arkada ise maksiller parçası
8

(V2 sfenopalatin sinirler) ile innerve olur. Palatin sinirler sert ve yumuşak damağın üst ve alt
yüzlerine trigeminal (5. kranyal sinir) sinirden duysal lifler sağlarlar. Lingual sinir (
trigeminal sinirin mandibular kısmının bir dalı [ V3 ] ) ve glossofarengeal sinir (9. kranial
sinir) sırasıyla dilin 2/3 ön ve 1/3 arka kısmının genel duyusunu sağlar. Fasiyal sinirin (7.
kranial sinir ) dalları ve glossofarengeal sinir sırasıyla dilin bu kısımlarının tad alma duyusunu
sağlarlar. Glossofarengeal sinir ayrıca farenks tavanı, tonsiller ve yumuşak damağın alt
yüzünü de innerve eder. Vagal sinir ( 10. kranial sinir ), epiglotun altındaki havayollarının
duyusunu sağlar. Vagusun süperior larengeal dalı, eksternal larengeal (motor) ve internal
larengeal (duysal) sinir olarak ayrılır. İnternal dal, larenksin epiglot ve vokal kordlar
arasındaki kısmının duysal innervasyonunu sağlar. Vagusun diğer bir dalı olan rekürren
larengeal sinir larenksin vokal kordlar altındaki kısmının ve trakeanın innervasyonunu sağlar.
Larenks kasları, rekürren larengeal sinir tarafından innerve edilir. Bunun tek istisnası, süperior
larengeal sinirin bir dalı olan eksternal larengeal sinir (motor) tarafından innerve edilen
krikotiroid kastır. Posterior krikoaretenoid vokal kordlarda abduksüyon yaparken, lateral
krikoaretenoid kaslar vokal kordların temel adduktorlarıdır(30). (Şekil-5)
Şekil-5 Üst hava yollarının innervasyonu
9

Larenksin kanlanmasını sağlayan arterler tiroid arterin dallarından köken alır. Krikotiroid
arter, eksternal karotid arterin ilk dalı olan süperior tiroid arterden çıkar, üst krikotiroid
membranın üzerinden geçer ve krikoid kartilaj ve tiroid kartilaj arasında uzanır. Süperior
tiroid arter, krikotiroid membranın lateral kenarı boyunca seyreder. Krikotirotomi
planlanırken, krikotiroid ve tiroid arterin anatomisi göz önünde bulundurulmalıdır, ancak bu
durum nadiren uygulamayı etkiler. Orta hatta krikoid ve tiroid kıkırdakların ortasında
kalınması en iyisidir.(6)
2. Laringoskopi ve Trakeal Entübasyon Girişimi
Trakeaya tüp yerleştirilmesi, genel anestezi uygulamasının rutin bir parçası haline gelmiştir.
Bununla beraber entübasyon, tamamiyle risksiz bir girişim değildir. Genel anestezi alan tüm
hastalar entübasyon gerektirmese de, havayolu açıklığının sağlanması ve korunması için
sıklıkla trakeal tüp yerleştirilir. Endotrakeal entübasyonun; havayolunun açık tutulması,
havayolu ve solunumun kontrolünü sağlaması, solunum eforunun azalması, aspirasyonun
önlenmesi, anestezistin ve diğer aygıtların sahadan uzaklaşması ile cerrahi rahatlık sağlaması,
resüsitasyon kolaylığı sağlaması ve ölü boşluk hacminde azalma gibi avantajları vardır.
Ancak bunun yanında özel beceri gerektirmesi ve ses kısıklığı, vokal kord paralizisi, trakeal
rüptür, enfeksiyon gibi komplikasyonlara neden olabilmesi gibi sakıncalar taşır(30,37).
a) Entübasyonun endikasyonları:
i. Anestezi uygulaması sırasında endikasyonlar: (37)
Anestezi uygulamasında endikasyon sınırları merkezlere göre değişmektedir. Bazı
anestezistler hemen her hastayı entübe ederken, bazıları daha sınırlı şekilde davranmaktadır.
Entübasyonun amacının havayolu açıklığı ve güvenliğini sağlamak ya da solunumu kontrol
veya asiste edebilmek olduğu dikkate alınırsa, aşağıdaki noktalar endikasyonu belirlemede
yardımcı olacaktır:
10

1) Baş-boyun ameliyatları: Havayolunun cerrahi ekiple paylaşılması ve
anestezistin havayoluna uzak kalması entübasyon gerektirir.
2) Kas gevşetici verilmesi ve yapay solunum uygulanması gereken durumlar.
3) Havayolunun kontrolünü güçleştiren pozisyonlarda yapılacak girişimler.
Yüzükoyun, yan ve oturur pozisyonlarda havayolunun ve ventilasyonun
kontrolü garanti edilemez. Aşırı baş aşağı ve litotomi pozisyonunda
diyaframın yukarı itilmesi ile ventilasyon güçlüğü ve aspirasyon riski
olabilir.
4) Torasik ve abdominal girişimler. İntratorasik girişimlerde gelişen
pnömotoraks başlıbaşına entübasyon gerektiren bir durumdur. Abdominal
girişimlerde de kas gevşemesi ve solunum kontrolü gerekir.
5) Refleks laringospazm gelişebilecek, sistoskopi, hemoroidektomi gibi
girişimler.
6) Özellikle yenidoğan grubu olmak üzere pediatrik hastalar.
7) Mide içeriği, kan, mukus ve sekresyon aspirasyonu riski olan hastalar.
8) Hipotermik ve hipotansif yöntemlerin uyulandığı girişimler.
9) Genel durumu düşkün hastalar.
10) Maske ile ventilasyonda anatomik nedenle veya girişimin uzunluğu
nedeniyle güçlük olabilecek hastalar.
11) Havayoluna dışarıdan bası yapan oluşumlar, vokal kord paralizisi, bu
bölgedeki oluşumlar.
ii. Anestezi uygulaması dışında endikasyonlar: (37)
1) İlaç zehirlenmeleri, sinir-kas hastalıkları, kardiak arrest veya kafa travmalı,
bilinci kapalı hastalarda havayolunu açık tutmak, aspirasyondan korumak.
11

2) Havayolu obstrüksiyonuna neden olan durumlar (yabancı cisim, tümör,
enfeksiyon, laringospazm, iki taraflı vokal kord paralizisi ).
3) Trakeo-bronşial temizlik (sinir-kas hastalıkları, yelken göğüs, larenks
travması, pnömoni, solunum yetmezliği).
4) Yapay solunum gereken durumlar (çeşitli nedenlerden kaynaklanan
solunum yetmezlikleri).
b) Entübasyonda kullanılan araç ve gereçler: (37)
Entübasyon işlemine başlamadan önce gerekli malzemelerin hazır ve çalışır durumda
olduğunun kontrolü şarttır. Bu amaçla bulundurulması gereken malzemeler şunlardır:
endotrakeal tüpler, tüp balonu şişirilmesi için enjektör, tüp stilesi, laringoskop, aspiratör,
maske ve ventilasyon için anestezi cihazı veya ambu, oksijen kaynağı, anestezik ve acil
ilaçlar.
c) Entübasyona hazırlık ve orotrakeal entübasyon tekniği:
Entübasyon işlemi yapılmadan önce hasta ve klinik durum, entübasyon yolu ve güç
entübasyon ihtimali yönünden değerlendirilmelidir. Aksine bir endikasyon yoksa entübasyon
işleminin rutin şekli genel anestezi altında ve tercihen kas gevşemesi sağlandıktan sonra oral
yolla ve laringoskopi ile glottisin görülerek, tüpün trakea içine yerleştirilmesidir. Entübasyon
sırasında anestezi refleks süpresyon sağlamaya yetecek derinlikte ve kas gevşemesi tam
olmalıdır. Bu amaçla erişkinde genellikle hızlı etkili intravenöz indüksiyon ajanı ve bir kas
gevşetici kombinasyonu, küçük çocuk ve bebeklerde ise tek başına veya bir kas gevşetici ile
birlikte inhalasyon anesteziği kullanılır. Çocuklarda ayrıca rektal ve intramusküler
indüksiyonda sık olarak kullanılır. Entübasyon anesteziyle fakat kas gevşetici kullanmaksızın
gerçekleştirilecekse, laringospazm gibi istenmeyen refleksleri önlemeye yetecek anestezi
derinliğine ulaşılmalıdır.(34,37)
12

İndüksiyon öncesinde, yüze sıkı oturan bir maskeyle 5 dakika boyunca hastanın %100 oksijen
solumasıyla preoksijenasyon uygulanması, ciddi kardiyopulmoner hastalığı olmayan ve
normal oksijen tüketimine sahip bireylerde apne sonrası 10 dakikaya kadar ulaşabilen bir
oksijen rezervi oluştur. Preoksijenasyon, diğer bir deyişle denitrojenasyon, akciğerlerdeki
nitrojenin (FRC’nin % 69’dan fazlasını oluşturur) oksijenle yer değiştirerek apnenin
başlaması sonrası alveo-kapiller kana difüzyon için yedek bir oksijen deposu sağlar.
Preoksijenasyon; 5 dakika süreyle % 100 oksijen solutulması, 30 sn.’lik süre boyunca peşpeşe
% 100 O2 ile 4 vital kapasite solutulması veya modifiye vital kapasite tekniği (hastaya 60 sn.
süreyle 8 derin soluk alması söylenir) gibi çeşitli şekillerde uygulanabilir.(38)
Yeterli anestezi ve gevşeme sağlandığında, herhangi bir kontrendikasyon yoksa hastanın başı
klasik sniffing pozisyona getirilir. Boyun hafif fleksiyonda, baş da ekstansiyondadır. Böylece
ağız-farenks-larenks hattının düzleşmesi sağlanır. Bunu sağlamak için başın altına 8-10 cm
yüksekliğinde küçük bir yastık ya da katlanmış çarşaf konulması yeterlidir(34,37). (şekil-3)
Laringoskop sol elle tutulurken, sağ elin parmakları kullanılarak ağız açılır. Laringoskopun
bleydi hastanın ağzına sağ taraftan sokulur. Bu sırada dişlerin hasar görmemesine özen
gösterilir. Bleydin kenarı ile dil, sola ve yukarıya doğru farenks tavanına doğru itilir. Epiglot
göründükten sonra eğri bleydin ucu genellikle vallekula içine itilirken düz bleydin ucu
epiglotu da içine alacak şekilde ilerletilir. Vokal kordları açığa çıkarmak için laringoskopun
sapı bleydle birlikte yukarı doğru kaldırılır ve hastanın mandibulası ile dik açı yapacak şekilde
hastadan uzaklaştırılır. Dişlerle bleyd arasına dudakların sıkışmasından ve dişler üzerine
kuvvet uygulanmasından kaçınılır. Trakeal tüp sağ elle tutulur ve ucu vokal kordlar arasından
geçirilir. Endotrakeal tüpün balonu trakeanın üst kısmında yerleşmeli ancak larenksin
aşağısında olmalıdır. Laringosgop, yine dişlerin zarar görmemesine dikkat edilerek çekilir.
Trakea mukozasına yansıyan basıncı azaltmak için tüpün balonu pozitif basınçlı ventilasyon
sırasında trakeayı kapatarak kaçağı önleyecek en düşük hava volümü ile şişirilir.(30,34)
13

Entübasyondan sonra, göğüs ve epigastrium hemen oskülte edilir ve tüpün intratrakeal olarak
yerleştiğinden emin olmak için kapnografik trase izlenir. Eğer tüpün özofagusta veya trakeada
olduğuna dair bir şüphe varsa, tüpün çekilmesi ve hastanın maske ile ventile edilmesi daha
güvenlidir. Diğer durumda yani tüp trakeada ise, tüpün pozisyonunu emniyet altına almak için
tüp flasterle yapıştırılır ya da bağlanır. Kapnografta sürekli olarak CO2 ye rastlanması tüpün
trakeada yerleştiğini doğrulamanın en iyi yolu olsa da, bu bulgu endobronşial entübasyon
şüphesini yok etmez. Endobronşial entübasyonun en erken belirtisi tepe inspiratuar basınç
artışıdır. Tüpün ucunun ve balonunun yerleşiminin uygun olduğu, bir elle pilot balon
sıkıştırılırken diğer elle sternal çentikte tüpün balonunun palpe edilmesi ile doğrulanabilir.
Kaf krikoid kartilaj düzeyinin üzerinde hissedilmemelidir. Çünkü tüp balonunun uzun süreli
larenks içi yerleşimi postoperatif ses kısıklığına neden olabilir ve kazayla ekstübasyon riskini
artırır. Tüpün pozisyonu akciğer grafisi ile de belirlenebilir ancak yoğun bakım dışında buna
nadiren ihtiyaç duyulur.(30,37)
3. Laringoskopi ve Trakeal entübasyona Hemodinamik Cevaplar
Laringoskopi ve trakeal entübasyona karşı gelişen cevaplar hipertansiyon, taşikardi ve
disritmileri kapsar. Çocuklarda bradikardi görülebilirse de esas neden olarak hipoksemi daima
göz önünde bulundurulmalıdır. Anestezinin derinleştirilmesi bu etkileri azaltmakta veya
tamamen ortadan kaldırmaktadır. Ancak endotrakeal entübasyon için, cerrahi insizyon için
gerekene göre % 30 daha fazla MAC değerine ihtiyaç duyulması nedeniyle göreceli olarak
daha derin bir anestezi düzeyi oluşturulmalıdır. Derin anestezinin bazı hastalarda tolere
edilememesi yüzünden havayolu girişiminin oluşturduğu cevapları bloke eden ilaçlar veya
antihipertansifler kullanılabilir. Laringoskopi ve entübasyon sırasında veya hemen sonrasında
ortaya çıkan disritmiler yeterli ventilasyonun sağlanması ve yeterli anestezi derinliğine
ulaşılmasıyla kaybolur(34,37).
14

Laringoskopi ve trakeal entübasyona karşı gelişen bu cevaplar sağlıklı bireylerde genellikle
iyi tolere edilir. Ancak koroner yetmezliği olan veya sınırlı myokardial rezerve sahip
hastalarda laringoskopi ve entübasyonu takiben myokardial iskemi veya yetmezlik gelişebilir.
İntrakranyal vasküler anomali veya torasik aort travması gibi riskli vasküler lezyonu olan
hastalarda da ciddi sekeller ortaya çıkabilir(34).
Laringoskopi ve trakeal entübasyon sonrası sempatik ve sempatoadrenal sistemin her ikisinde
de meydana gelen refleks aktivite artışına bağlı olarak plazma adrenalin ve noradrenalin
düzeylerinde ciddi artışlar görülür ancak 5 dakika içerisinde azalarak indüksiyon öncesi
değerlere döner. Kalp hızında yaklaşık 20 atım/dak, sistolik basınçta 50, diastolik basınçta 30
mm Hg dolaylarında artış olup, bu değişiklikler laringoskopi ile başlamakta, 1-2 dakika içinde
maksimuma ulaşmakta ve 5 dakika sonra da laringoskopi öncesi değerlere inmektedir(21,37).
Entübasyonun farklı dönemleri, farklı derecelerde kardiyovasküler cevaplara neden olur.
Orotrakeal entübasyon sırasında havayolu stimülasyonu iki farklı dönemde meydana
gelmektedir. İlki vokal kordların görüş alanına alınmasını sağlayan direk laringoskopi,
ikincisi ise tüpün vokal kordların arasından geçirilerek trakeaya ilerletildiği dönemdir. Bu
dönemlerin oluşan hemodinamik cevaplara katkısı hakkında farklı sonuçları olan çalışmalar
mevcuttur. Laringoskopi tek başına, laringoskopiyle birlikte entübasyon uygulanmasına eş
düzeyde pressor ve sempatoadrenal cevaba yol açmaktadır. Bu trakeal entübasyona
sempatoadrenal cevabın başlıca nedeninin supraglottik bölgenin uyarılmasından
kaynaklandığını desteklemektedir. Supraglottik bölgenin uyarılması, laringoskopiyle dokuya
bası uygulanmasıyla olmaktadır. Dil kökünde oluşan stimülüsün şiddetiyle katekolamin artışı
arasında doğru orantılı bir ilişki vardır. Ayrıca endotrakeal entübasyonun gerçekleştirilmesi
için gereken süre, OAB’daki artışla korelasyon gösterir. Kordların arasından tüpün
geçirilmesi ve infraglottik bölgede trakeal tüp balonunun şişirilmesi ise pek az ek
stimülasyona yol açar(4). Bir başka çalışmada ise trakeanın doğrudan stimülasyonunun
15

hemodinamik değişikliklerin majör nedeni olduğu ve tek başına laringoskopi uygulanmasına
nazaran daha büyük kan basıncı artışlarına yol açtığı gösterilmiştir(39).
Laringoskopi sırasında dil köküne uygulanan kuvvetin derecesiyle, oluşan hemodinamik ve
katekolamin cevabı arasında yakın bir ilişki olduğu gösterilmiştir. Laringoskopi sırasında
propioreseptörlerin stimülasyonuyla sistemik kan basıncı, kalp hızı ve katekolamin
konsantrasyonlarında artış meydana gelmektedir. Laringoskopiyi takiben entübasyon da
uygulanması hemodinamik ve epinefrin cevabını artıran ek reseptörlerin ortaya çıkmasını
sağladığı gibi bazen de kalbin vagal inhibisyonuna yol açar(40) .
Laringoskopi ve trakeal entübasyona bağlı olarak ortaya çıkan kardiyovasküler cevapların
önlenmesi için çok çeşitli anestezi teknikleri ve ilaçları mevcuttur. Bu amaçla herhangi bir
ilaç veya metodu kullanıp kullanmayacağımıza veya bunlardan hangisini seçeceğimize karar
verirken, cerrahinin tipi ve süresi, uygulanacak anestezi metodu, ilacın veriliş yolu, hastanın
tıbbi durumu ve kişisel tercihi de içeren birçok faktörü göz önünde bulundururuz.
Kullanacağımız ilacın ideal olarak hızlı etki başlangıcı ve amacına uygun etki süresine sahip,
güvenilir, hazırlama ve kullanım kolaylığı olan bir ilaç olmasını bekleriz(12).
Larengeal mask kullanımı direkt laringoskopiye göre daha az hemodinamik cevaba neden
olur. Hemodinamik cevapların ortadan kaldırılması veya azaltılması için, anestezinin
derinleştirilmesi, topikal anestezi (direkt veya transtrakeal sprey, lidokain inhalasyon veya
gargarası), işlemden birkaç dakika önce intravenöz lidokain verilmesi, vazodilatörler, α ve β
adrenerjik blokerler, prekürarizasyon ve narkotik ilaçlar verilmesi gibi önlemler alınabilir.
Fentanilin 3–4 μg/kg dozlarda etkili olduğu gösterilmiştir. Alfentanil daha hızlı etki
başlangıcına sahiptir. Remifentanil de benzer etkinliğe sahiptir. Her ne kadar bazı çalışmalar
lidokainin etkinliğine kuşkuyla bakılmasına yol açsa da, narkotiklere ek olarak i.v. lidokain de
kullanılabilir. Lidokainle topikal anestezi uygulanması hemodinamik cevapları önlemede en
az etkili metoddur. Transtrakeal anestezi cevapları önlese de kendisi ayrıca uyarıcı bir etkiye
16

sahiptir. Glossofarengeal ve süperior larengeal sinir blokları da istenmeyen hemodinamik
cevapları önlemede etkili olabilir. Entübasyona cevap olarak kan basıncı ve kalp hızında artışı
azaltan çeşitli antihipertansif ajanlar kullanılmıştır. Bunlar esmolol gibi β blokerler; diltiazem,
nicardipine, verapamil gibi Ca++ kanal blokerleri; klonidin gibi α blokerler; ayrıca sodyum
nitropurussid, nitrogliserin, hidralazin, kaptoprili içerir. Son yıllarda deksmedetomidin
hemodinamik cevapların önlenmesinde dikkati çeken bir ajan haline gelmiştir(27,34,37).
B. RESEPTÖR FİZYOLOJİSİ
Bazı ilaçlar gözlemlenen etkilerini hedef hücrelerde hormonları, nöromedyatörleri ve diğer
endojen etkin maddeleri tanıyan özel yerleri etkileyerek oluştururlar. Etkin endojen maddeleri
ya da onlara yapıca benzeyen ilaç moleküllerini yüksek afinite ile bağlayıp hücresel etkinin
başlamasına aracılık eden bu moleküllere reseptör adı verilir. Protein yapısındaki bu
reseptörler endojen maddeler için çok seçici olmakla birlikte bu selektiviteleri ilaç molekülleri
karşısında sınırlı olabilir; aynı reseptör birçok madde ile etkileşebilir(41).
Reseptör molekülleri hücrenin değişik yerlerinde bulunabilir. Örneğin katekolaminlerin ve
peptid yapılı etkin maddelerin reseptörleri hücre membranında yerleşmişken, steroid
hormonların reseptörleri sitoplazmada, tiroid hormonları ve retinoik asit reseptörleri hücre
çekirdeğinde bulunur. Reseptörlerin ana işlevi biyolojik kompartmanlar arasında iletişim
sağlamaktır. Bunlar arasında en dikkate değer olanı hücre dışından hücre içine doğru olan
bilgi iletimidir. Burada bilgi iletiminden kasıt, hücre içine giremeyen bazı kimyasal
habercilerin ( nöromedyatör, hormon, otokodid v.b.) hücre dışındaki varlığının
konsantrasyonunun hücre içindeki metabolik şebekeye bildirilmesidir. Kabaca bu olay,
kimyasal bir sinyal olan hücre dışındaki maddenin reseptör molekülüne bağlanarak hücre
içine doğru yayılan bir dizi biyokimyasal reaksiyonu başlatmasıyla gerçekleşir. Başlayan bu
reaksiyon hücre tarafından integre edilir ve belirli bir biyolojik yanıta (kasılma, salgılama
gibi) dönüştürülür. Reseptörler uyarıldıklarında sinyalin hücre içinde yayılmasını sağlayacak
17

olan yani başka bir deyişle hücre dışı sinyali hücre içi sinyale dönüştüren ikincil ulak (second
messenger) denen kimyasal maddeler ortaya çıkar(41).
Reseptörler sterospesifik bağlanma bölgeleri içeren özelleşmiş proteinlerdir. Reseptör
kendisine özel ligantı seçici olarak bağlama yeteneğine sahiptir. Reseptör ve ligantı arasındaki
bu etkileşim hücresel mesaja dönüştürülebilen bir moleküler sinyal oluşturarak hücre
fonksiyonunda değişiklik meydana getirir. En azından 4 reseptör üst ailesi tanımlanmıştır:
1. Ligand-gated iyon kanal reseptörleri; iyon kanalının bir kısmını transmitter bağlayan bölge
oluşturur. 2. G-proteiniyle eşleşmiş reseptör; ikinci habercisi GTP’dir. 3. Ligand-regulated
tirozin kinaz. 4. Nuklear reseptörler; DNA transkripsiyonunda değişiklik yaparlar(42). (Şekil 6)
Şekil 6. Reseptör Tipleri
18

Reseptörlere bağlanan ve bir etki oluşturan droglar agonist olarak isimlendirilir. Aynı
reseptöre bağlanan agonistler arasında potentlik açısından farklılık olması reseptöre olan
afinitedeki farklılığı yansıtır. Hücresel fonsiyonda herhangi bir değişikliğe yol açmaksızın
bağlanan bileşiklere antagonist adı verilir. Agonistlerin reseptörlere bağlanması antagonistler
tarafından inhibe edilir. Kompetitif antagonistler reseptörlere geri-dönüşümlü olarak bağlanır
ve bu bloke edici etkilerini ancak yüksek konsantrasyonda agonistin varlığında ortadan
kaldırmak mümkündür(43).
1. Opioid reseptör fizyolojisi
Son iki dekaddır yapılan yoğun çalışmalar sonucu 3 tip opioid reseptör varlığı belirlenmiştir.
Bunlar μ, δ ve κ reseptörleridir. μ reseptörleri de yüksek afiniteli μ1 ve düşük afiniteli μ2
reseptörleri olarak iki alt sınıfa ayrılmıştır. δ ve κ reseptörlerinin de subtipleri belirlenmiştir.
μ-opioid agonist droglarla oluşan supraspinal analjezi μ1, spinal analjezi, solunum depresyonu
ve gastrointestinal fonksiyonlar üzerindeki etkileri ise μ2 reseptörleri aracılığıyla olmaktadır.
Opioid reseptörler S.S.S.’de geniş bir alana dağılmıştır. Nosisepsiyonun regülasyonu ve
sensorimotor integrasyonun sağlandığı S.S.S.’nin bu bölgelerinde μ reseptörleri yoğun olarak
bulunmaktadır. Opioid droglar bir veya birden fazla opioid reseptör tipine bağlanarak analjezi
oluşturur ve endojen opioidlerin etkilerini taklit ederler.
Opioidlerin etkileri primer olarak inhibitördür. K + ve Ca 2+ iyon kanallarının
regülasyonundaki değişiklikler sonucu meydana gelirler. μ ve δ reseptörlerinin aktivasyonu
K+ kanallarının açılmasıyla K+ akışında artışa neden olur. Halbuki κ reseptör agonistleri N-
tip Ca2+ kanallarında kapanmaya neden olarak Ca2+ akışını azaltır. Her iki olay da hücrelerin
hiperpolarizasyonu ve Ca2+ akışınıda sekonder bir azalmanın takip ettiği postsinaptik nöron
eksitabilitesinde azalmayla sonuçlanır. Substans P gibi nörotransmitterlerin opioid aracılı
inhibisyonu muhtemelen hücre içi serbest kalsiyumundaki değişikliklerle düzenlenir.
19

Opioid reseptörlerin aktivasyonu iyon kanallarında değişikliğe doğrudan değil, dolaylı olarak
G proteinleri aracılığıyla yol açar. G proteinlerinin opioidlerle aktivasyonu adenil siklaz
aktivitesini azaltır ve böylece hücre içi cAMP konsantrasyonu düşer. Her ne kadar opioidlerin
cAMP’de oluşturduğu değişiklikler nörotransmitter salınımının modülasyonundan sorumlu
olsa da K+ ve Ca2+ kanallarındaki etkileri G protein ve iyon kanallarıyla doğrudan birleşmesi
veya cAMP’den başka bir ikinci haberci aracılığıyla olabilir(44).
Tablo 1. Opioid Reseptörlerinin Sınıflandırılması
Reseptör Klinik etki Agonistler
Mu Supraspinal analjezi μ1 Morfin
Solunum depresyonu μ2 Met‐enkefalin Fiziksel bağımlılık β‐endorfin Kas rijiditesi Fentanil
Kappa Sedasyon Morfin Spinal analjezi Nalbufin Butorfanol Dinorfin
Oksikodon
Delta Analjezi Leu‐enkefalin Davranışsal β‐endorfin Epileptojenik ketamin?
2. α-2 reseptör fizyolojisi
α2 adrenoseptörler adrenerjik nöroeffektör bağlantılarda, hem presinaptik hem de postsinaptik
olarak yerleşmiştir ve genellikle inhibitörlerdir. Bunun tek istisnası α2 adrenoseptör
stimülasyonunun vasokonstrüksiyonla sonuçlandığı vasküler düz kaslardır. Postsinaptik
membran hemen hemen eşit sayıda α1 ve α2 reseptör içerir. α2 adrenoreseptörlerin 4 subtipe
ayrılması mümkündür. Arteriyal ve venöz vazokonstrüksiyon, trombosit agregasyonu,
20

bağırsak motilitesinin inhibisyonu, büyüme hormonu salınımının stimülasyonu ve ADH’nın
salgılanmasının inhibisyonu postsinaptik α2 reseptöre bağlı etkilerden bazılarıdır(44,45).
Adrenerjik yollarda olduğu kadar kolinerjik yollarda da α2 reseptörler bulunabilir.
Parasempatik aktivitenin modülasyonunda önemlidirler. Günümüzde yapılan çalışmalar
göstermektedir ki, parasempatik yollardaki α2 reseptörlerin uyarılması; baroreseptör refleksin
(duyarlılığında artışa), vagal aracılı kalp hızı (bradikardi), bronkokonstrüksiyon ve
salivasyon( kuru ağız)’un düzenlenmesinde rol oynamaktadır. Santral sinir sistemindeki
postsinaptik α2 reseptörlerin fonksiyonel rolü henüz tam olarak ortaya konmasa da, sedasyon,
anksiyolizis, analjezi ve hipnoz muhtemelen bu yolla meydana gelmektedir(45).
Presinaptik α2 reseptörlerin stimülasyonu sinaptik aralığa norepinefrin salınımını inhibe eden
(-) feed back mekanizma olarak görev yapar. Santral etkileri başlıca sempatik outflowda
azalmayla birlikte olan parasempatik outflowdaki artıştır (örneğin, artmış baroreseptör
aktivitesi). Bu, sistemik vasküler resistansta azalma, azalmış kardiak output, myokardın
kasılma gücünde azalma ve kalp hızında yavaşlamayla sonuçlanır. Periferik presinaptik α2
etkiler benzerdir ve postganglionik nöronlarda norepinefrin salınımı inhibe edilir. Dolayısıyla
postsinaptik α2 reseptörlerin uyarılması tıpkı α1 reseptörlerde olduğu gibi vasokonstrüksiyona
yol açar(45).
NE α1 ve α2 reseptörlerinin her ikisine de etki eder. Böylece sadece düz kaslarda
vasokonstrüksiyonu aktive etmekle kalmaz ( postsinaptik α1 ve α2 reseptörler ) presinaptik α2
reseptörleri de uyarır ve kendi salınımını inhibe eder. Presinaptik α2 reseptörlerin selektif
stimülasyonu periferik vasküler dirençte faydalı bir düşüş sağlayacaktır. Ne yazık ki bilinen
tüm presinaptik α2 agonistler postsinaptik α2 reseptörleri de uyararak vasokonstrüksiyona yol
açar. Presinaptik α2 reseptörlerin blokajı NE’nin normal salınımını bozar ve
vasokonstrüksiyona yol açar. Vasodilatasyon postsinaptik α1 ve α2 reseptörlerin birlikte bloke
edilmesiyle oluşur(45).
21

Beyin ve spinal kordaki presinaptik α2 reseptörler NE’nin presinaptik salınımını inhibe
ederler. Her ne kadar beyin adrenerjik ve dopaminerjik reseptörlere sahip olsa da dolaşan
katekolaminler kan-beyin bariyerini geçemez. Beyindeki katekolaminler beynin kendisinde
sentez edilir. Bazı etkiler serebral postsinaptik α2 reseptörlere bağlıdır. Bunlar insülin ve ADH
salınımıyla barsak motilitesinin inhibisyonu ve büyüme hormonunun salgılanmasının
uyarılmasıdır. Klonidin gibi ilaçların santral nöroaksiyel injeksiyonu analjezi, sedasyon ve
kardiyovasküler depresyon oluşturur. Nonselektif α agonistlerin lokal anesteziklere
eklenmesiyle epidural ve intratekal anestezideki uzama bu mekanizmayla ek analjezi
oluşturur. Böbreklerde tubuler α2 reseptörler sodyum ve su atılımını güçlendirirler(45).
C. DEKSMEDETOMİDİN
Adrenerjik reseptörler, çeşitli aminlere verdikleri cevaplar temel alınarak Ahlquist tarafından
ilk olarak α ve β olmak üzere ayrılmışlardır. α2-adrenerjik agonistler, analjezi ve sempatolizis
oluşturdukları ölçüde aynı zamanda sedasyon, aksiyolitik ve hipnotik etki de sağlarlar. α2
adrenoreseptör agonisti 1960’ların başında sentez edilmiş ve nasal dekonjestan olarak
kullanılmıştı. Ancak klonidin olarak bilinen bu ilaçla 24 saatten uzun süren sedasyon ve
kardiyovasküler depresyon gibi beklenmeyen etkilerle karşılaşılmıştı. Daha sonra klonidin
1966 da antihipertansif olarak test edilmeye başlandı. İlk olarak anestezide α2 agonistlerin
kullanılabileceğini düşündürten etken, klonidin tedavisi alan hastalarda anestezi sırasındaki
gözlemlerdir. Klonidin kullanımıyla halotanın MAC değerinde düşüş olduğu belirlenmiştir.
Deksmedetomidin α2 adrenoreseptörler için yüksek seçiciliği olan sedatif ve analjezik
özelliklere sahip bir α2 agonisttir. Deksmedetomidine, α2 reseptörler üzerinde, α1’e göre 1600
kat daha fazla bir seçiciliğe sahiptir. Bu antihipertansif olarak kullanılan klonidine göre 7-8
kat daha fazladır. (45,46,47,48)
Deksmedetomidinin yarı ömrü yaklaşık 1,5 saattir ve klonidine göre daha kısadır. Daha hızlı
etki başlangıcına sahiptir ( 5 dakikadan kısa). Peak etkiye ulaşma süresi 15 dakikadır.
22

İntravenöz olarak verilir ve anestezide birkaç kullanım amacı vardır. Mükemmel bir sedasyon
sağlar, kan basıncı ve kalp hızını azaltır, plazma katekolamin düzeylerinde belirgin bir düşüş
sağlar. Solunum depresyonu etkisi zayıftır. Deksmedetomidin premedikasyon amacıyla
kullanıldığında anksiyolitik ve sedatif olarak etkin olduğu gösterilmiştir(45).
Fizikokimyasal özellikleri:
Medetomidine yüksek oranda selektif bir α2 adrenerjik agonisttir. Deksmedetomidine,
medetomidinin spesifik steroizomeridir ve parenteral kullanıma uygun olarak formüle
edilmiştir (Şekil 7).(46)
Şekil-7 Deksmedetomidinin kimyasal yapısı
Kimyasal adı, (+)-4-(S)-[1-(2,3-dimethylphenyl) ethyl]-1H-imidazole monohydrochloride,
kimyasal formülü C13H16N2 HCl, molekül ağırlığı ise 236.7’dir.(49)
Metabolizma ve farmakokinetik:
Deksmedetomidine hızla dağılıma uğrar ve karaciğerde büyük oranda metabolize olarak hem
idrar hem de feçesle atılır. % 41 oranında konjugasyona, % 21 oranında N-metilasyona veya
konjugasyonu takiben hidroksilasyona uğrar. Deksmedetomidine % 94 oranında proteinlere
bağlanır ve tam kanla plazma arasındaki konsantrasyon oranı 0.66’dır. Deksmedetomidine
kardiyovasküler parametreler üzerinde belirgin etkilere sahiptir ve bu özelliği nedeniyle kendi
farmakokinetik özelliklerini değiştirebilir. Yüksek dozlarda muhtemelen ilacın dağılım
volümünde azalmaya yol açan belirgin bir vazokonstrüksiyona neden olur. Böylece nonlinear
23

bir farmakokinetik gösteren bir doğası vardır. Bu nedenle yalnızca 0.5–1.0 ng/mL gibi dar bir
terapötik aralıkta olacak şekilde verilmesi uygundur. Farmakokinetik parametrelerinin bu doz
aralığında tarif edilmesi tercih edilir. Bu doz aralığında Dyck ve arkadaşları, gönüllülerde
deksmedetomidinin farmakokinetiğini incelemiş, farmakokinetik özelliklerinin tarif edilmesi
için üç kompartmanlı modelin en iyisi olduğunu göstermişlerdir. Bu farmakokinetik
parametreler yaş, ağırlık ve böbrek yetmezliğiyle değişmiyor gözükmektedir.
Deksmedetomidinin eliminasyon yarı ömrü 2–3 saattir, fakat infüzyon süresine bağlı olarak,
10 dakikalık infüzyon sonrası 4 dakikadan, 8 saatlik infüzyon sonrası 250 dakikaya kadar
değişir. Deksmedetomidinle postoperatif sedasyon uygulanan hastalar, gönüllülerde görülene
benzer farmakokinetik gösterirler.(46)
Farmakoloji:
a.Santral sinir sistemine etkileri:
α2-agonistler, locus ceruleustaki α2-reseptörlere etki ederek sedatif-hipnotik etkilerini gösterir.
Analjezik etkileri ise locus ceruleus ve spinal korddaki α2-reseptörler aracılığıyla ortaya çıkar.
Deksmedotimidinle oluşan sedasyonun kalitesinin, GABA sistemi aracılığıyla oluşan diğer
sedatiflerle oluşandan farklı oluşu ilginç bir gözlemdir. α2-agonistlerin sahip olduğu sedatif
etki, endojen uyku düzenleyici yollar üzerinde oynadığı rol aracılığıyladır. Locus ceruleusun
ventrolateral preoptik nukleusa projeksiyon aktivitesinde azalma oluşturur. Bu etki
tuberomamiller nukleusta GABAerjik etkiyi ve galanin salınımını artırır ve bunun sonucu
olarak kortikal ve subkortikal projeksiyonlarda histamin salınımında azalmaya öncülük eder.
α2 agonistler L ve P tipi kalsiyum kanallarından iyon konduktansını inhibe ederken, voltaj-
kapılı kalsiyumla aktive edilen potasyum kanallarında ise iletimi kolaylaştırıyor
gözükmektedir. α2 agonistlerin sahip oldukları bir avantaj α2 adrenerjik antagonistlerle
(atipamezole) etkilerinin kolaylıkla geri çevrilebilir olmasıdır. Uzun süreli uygulamayla α2
agonistlere tolerans gelişebilir.(28)
24

Hem düşük hem de yüksek konsantrasyonlarda, deksmedetomidine, global CBF’yi % 30
oranında düşürmektedir. Bu düşüş infüzyonun kesilmesinden sonra da en azından 30 dakika
daha devam eder. Deksmedetomidinle konvüzyon bildirilmemiştir. Doza bağımlı olarak diğer
hipofizer hormonlarda olmasa da büyüme hormonu sekresyonunda artışa yol açar. Yine doza
bağımlı olarak hafıza kaybına neden olur.(28)
b.Solunum sistemi üzerine etkileri:
Gönüllülerde, dexmedotimidine ciddi sedasyon oluşturan konsantrasyonlarda, dakika
ventilasyonunu azaltmakta, ancak artan CO2’ye solunumsal cevabı değiştirmemektedir.
Ventilasyonda görülen değişiklikler, doğal uykuda gözlenen değişikliklerle benzerlik
göstermektedir. Ebert ve arkadaşları, spontan soluyan volenterlerde 15 ng/mL’nin üzerinden
konsantrasyon sağlayacak şekilde dexmedotimidine infüzyonu uyguladığında arteriyal
oksijenasyon veya pH’da herhangi bir değişiklik olmadığını göstermiştir. Çok daha yüksek
konsantrasyonlarda, PaCO2 % 20 oranında artmaktadır. Solunum hızı, artan konsantrasyonla
birlikte 14’ten 25’e çıkar. Deksmedetomidine ve propofol eş sedasyon düzeyi oluşturacak
şekilde ( BIS index 85) titre edilip verildiğinde, her ikisinde de solunum hızında bir değişiklik
olmaz. Deksmedetomidinin 1-2 μg/kg’lık dozu PaCO2’de hafif bir artışa yol açar (45 mm Hg)
ve karbondiokside cevap eğrisinde sağa kayma depresyon oluşturur. Solunumdaki değişme
başlıca tidal volümün değişmesiyledir. Solunum frekansındaki değişiklik çok küçüktür.
Deksmedetomidine, alfentanille kombine edildiğinde daha fazla solunum depresyonuna yol
açmadan analjeziyi artırır.(28)
c.Kardiyovasküler sistem üzerine etkileri:
α2-agonistlerin kardiyovasküler sisteme başlıca etkileri, kalp hızı ve sistemik vasküler
dirençte azalma; dolaylı olarak myokardial kontraktilite, kardiak output ve sistemik kan
basıncında azalmadır. Deksmedetomidinin bolus dozunun hemodinamik etkileri bifaziktir. 2
μg/kg i.v. injeksiyonu takiben 5 dakika sonra, kan basıncında %22 artış meydana gelirken
25

kalp hızında % 27’lik bir düşüş görülür. Başlangıçta kan basıncında görülen artış muhtemelen
periferik α2 reseptörler üzerindeki etkisi nedeniyledir. Kalp hızı 15 dakika içinde bazal
değerlere dönerken kan basıncı 1 saat boyunca tedrici olarak bazal değerin %15 altına iner.
Deksmedetomidine ciddi bradikardiye ( <40 atım dk-1), nadiren de sinüs arrestine yol açabilir.
Bu episod sıklıkla spontan olarak geri döner veya antikolinerjiklerle kolaylıkla tedavi edilir.
Deksmedetomidinin iskemik myokard üzerinde yararlı etkileri olacağı düşünülmektedir.
Ayrıca serum laktat düzeylerini azaltır.(28)
d.Diğer etkileri:
Deksmedetomidinin sık görüken yan etkisi, tükürük üretiminde azalmaya bağlı olarak gelişen
ağız kuruluğudur.(28)
Kullanımı:
Deksmedetomidine, anestezi indüksiyonunda endike değildir. Rolü büyük ölçüde, 24 saatten
kısa süreli postoperatif sedasyonla sınırlandırılmıştır. Hipnotik ve opioid ihtiyacının
azaltılmasında anesteziye yardımcıdır.(28)
Bir premedikasyon ajanı olarak 0.33–0.67 μg/kg dozlarda i.v. olarak cerrahiden 15 dakika
önce verildiğinde kardiyovasküler yan etkilerin en aza indirilmesinde etkilidir. Bu doz
aralığında tiyopental ihtiyacını %30, volatil anestezik ihtiyacını ise %25 oranında azaltır.
Deksmedetomidine, 2 μg/kg fentanil ile karşılaştırıldığında endotrakeal entübasyona
hemodinamik cevapların azaltılmasında daha etkilidir. Deksmedetomidinin cerrahiden 45–90
dakika önce fentanil ile birlikte veya tek başına 2.5 μg/kg dozda i.m. olarak verildiğinde
anksiyolitik etkisine ek olarak, entübasyona cevabını, volatil anestezik ihtiyacını ve
postoperatif titremeyi azaltmakta ancak bradikardi riskini artırmaktadır.(28)
Postoperatif dönemde mekanik ventilasyon uygulanan hastalarda sedasyon için
deksmedetomidinin propofole göre daha avantajlı olduğu gösterilmiştir. Yoğun bakım
hastalarında sedasyon için deksmedetomidine ile sedasyon uygulandığında weaning sırasında
26

daha stabil bir hemodinami sağlanmaktadır. Deksmedetomidinin 2.5-6 μg/kg/s’lik yükleme
dozu sonrası, yeterli sedasyonun devamı için 0.1-1 μg/kg/s dozda infüzyona ihtiyaç duyulur.
Deksmedetomidinin 10 dakika süreyle 170 ng/kg/dak yükleme dozunu takiben 10 ng/kg/dak
infüzyonla uygulandığında anestezik ve opioid ihtiyacını azaltmaktadır.(28)
Sahip olduğu şu özellikler deksmedotimidinin anestezist için yararlı bir ilaç olmasını sağlar:
• Potent analjezi
• Sedasyon ve anksiyolizis
• Antisialog
• Hemodinamik stabilite sağlar
• Homeostatik refleksler bozulmadan kalır
• Opioid rijiditesini azaltır (hayvanlarda).
Deksmedotimidinin 2 mL’lik vialleri kullanıma için sunulmuştur ( 100 μg/mL) ve infuzyonla
kullanım için 48 mL % 0.9 NaCl ile dilüe edilmelidir. Yükleme dozu 10 dakika içerisinde
infüzyonla 1 μg/kg olarak verilir. Yükleme dozu bolus olarak verilmemelidir. Yükleme
dozunun infüzyonu sırasında geçici ve paradoksal bir hipertansiyon görülebilir. Kalp hızında
azalma görülebilir. Kan basıncında görülen bu artış vasküler düz kaslardaki α2 reseptörlerin
başlangıçtaki stimülasyonuna bağlanabilir. Santral α2 agonizmanın, periferik etkilerine baskın
gelmesiyle kan basıncında çoğunlukla düşme görülür(45).
D. REMİFENTANİL
Remifentanil; fentanil, alfentanil ve sufentanil gibi 4-anilidopiperidin yapısında, bir metil
ester yan zincire sahip, potent ve naloksanla geri çevrilebilen selektif bir μ reseptör
agonistidir. Kimyasal yapısı: 3-[4-Metoksikarbonil–4-[(L-oksopropil)-Fenilamino]-L-
Piperidin) propanoik asit metil esterin hidroklorid tuzudur. Moleküler formülü
C20H28N2O5HCI’dir (Şekil 8). Moleküler ağırlığı 412,9 Dalton’dur. İlk kez 1990’da
tanımlanmış ve klinik kullanıma 1996’da girmesiyle çok kısa etkili opioid ihtiyacına cevap
27

vermiştir. Nonspesifik doku ve plazma esterazları tarafından hızla ve tamamiyle hidrolize
edilmesi remifentanile diğer opioidlerden farklı bir farmakokinetik profil kazandırmaktadır ve
etkisinin sonlanması redistrübisyondan ziyade tamamiyle metabolik klirensine bağlıdır.
(50,51,52).
Şekil 8. Remifentanilin kimyasal yapısı
3-([4-Metoksikarbonil–4-[(L-oksopropil)-Fenilamino ]-L-Piperidin ) propanoik asit
Fizikokimyasal özellikleri: Remifentanil hidroklorid, liyofilize beyaz bir tozdur. Günümüzde
kullanılan formülasyonu glisin içerir. 1, 2 ve 5 mg’lık vialler halindedir. Uygulamadan önce
mL’sinde 25 veya 50 μ içeren solüsyon şeklinde sulandırılarak kullanılmalıdır. Hazırlanan bu
solüsyonun pH’sı ± 3,0 ve pKa değeri 7,07’dir. Spontan yıkıma uğrar. Ancak pH, 4’ün
altındaysa 24 saat stabil kalır. Liposolübüldür pH 7,4’de octanol/su partisyon katsayısı
17,9’dur (Partisyon katsayısı 13.14 olan alfentanile bu özelliği benzer). Remifentanil % 92
oranında proteine bağlanır. Opiod bağlayıcı çalışmalar, remifentanilin μ opioid reseptörlerine
karşı güçlü bir afiniteye sahip olduğunu gösterirken, delta ve kappa reseptörlerine olan
afinitenin daha az olduğunu ortaya çıkarmıştır. Diğer nonopioid reseptörlere önemli ölçüde
bağlanmaz. Remifentanil naloksanla tamamiyle antagonize edilir. Esterazlar alkol ve asit
28

komponentlere parçalayan enzimlerdir. Remifentanilin majör metaboliti karboksilik asit
metaboliti olan remifentanil asittir (RA). RA benzer şekilde μ, delta ve kapa reseptörlerine
bağlanır ancak binde birlerle ifade edilen çok daha düşük afiniteye sahiptirler. Sağlıklı
bireylerde RA’nın yaklaşık % 88’i idrarla atılır ve renal fonksiyonları normal olanlarda 2-30
μg/kg bolus doz sonrası terminal yarılanma-ömrü 88-137 dakikadır. Böbrek fonksiyonlarının
bozulmasıyla RA’nın klirensi azalır ve yarılanma-ömrü 14-32 saate uzar.(52,53).
Farmakokinetik: Remifentanil diğer piperidin derivelerine çok benzer bir konfigürasyona
sahiptir, fakat kan ve diğer dokularda bulunan nonspesifik esterazlarla metabolize edilmeye
duyarlı bir ester yan bağ içerir. İn vitro olarak kanda ve in vivo olarak köpeklerde yapılan
çalışmalarda hızlı ester hidrolizisiyle terminal eliminasyon yarı-ömrünün 3.8-8.3 dakika
olduğu gösterilmiştir. İn vitro testler plazma kolinesterazının inhibisyonu veya
fonksiyonundaki değişikliklerin yıkılımını değiştirmediğini ortaya çıkarmıştır(53).
Remifentanil hızlı etki başlangıcı, küçük dağılım hacmi, hızlı redistrübisyona sahiptir. 8.8-40
dakika olan eliminasyon yarı ömrü (t 1/2β), 60-120 dakikalık eliminsayon yarı ömrüne sahip
alfentanile göre çok daha kısadır. Remifentanilin hızlı etki başlangıcının plazma ile etkide
bulunduğu kompartman arasındaki dengelenme yarı ömrünün kısa olmasına bağlıdır ( t ½ ke0
1,0-1,5 dakika). Hızlı yeniden dağılımıyla birlikte bu kısa t ½ ke0, remifentanilin peak etkisinin
bolustan 1.5 dakika sonra ortaya çıkmasıyla sonuçlanır. Etkisinin böyle hızlı başlayıp hızlı
kaybolması, dolayısıyla doz uygulandıktan sonra etki görülene dek çok az beklenmesi,
remifentanilin klinikte dozu çok kolay titre edilebilen bir opioid olduğu anlamına gelir.
Remifentanilin santral dağılım hacmi 0.1-0.2 L/kg, steady state dağılım hacmi VDSS ise 0.3-
0.4 L/kg ve klirensi ise 40-60 ml.dak.-1.kg-1’dir. Context-sensitive yarılanma ömrü 3-4
dakikadır ve infüzyon süresinden etkilenmez. Context-sensitive yarılanma ömrü, infüzyonun
kesilmesi sonrası kan veya plazma konsantrasyonunun % 50 düşüşü için geçen süre olarak
tarif edilir. İnfüzyon süresinden etkilenmeksizin, konsantrasyonun % 80 azalması için geçen
29

süre 15 dakikadan kısadır. Esteraza dayalı metabolizma nedeniyle remifentanilin etkisinde
çok hızlı bir azalma meydana gelir. Hatta, günümüzde kullanılan diğer opioidlerin göreceli
olarak birkaç katı dozunda olacak şekilde anestezi uygulaması sırasında verilmesinden sonra
bile, remifentanille geç solunum depresyonu ortaya çıkışını, bu hızlı metabolizma
önlemektedir. Benzer şekilde analjezik etkisi de hızla sonlanmaktadır, dolayısıyla analjezi
uygulaması gerektiğinde, klinisyen ilacı kesmeden önce hastanın ağrısını nasıl gidereceğini
planlamış olmalıdır(51,52,53).
Remifentanilin esteraza dayalı metabolizması, sahip olduğu farmakokinetik özelliklerini end-
organ yetersizliğinden bağımsız kılar. Karaciğer ve böbrek yetersizliği olan hastalarda
remifentanilin farmakokinetik özelliklerinin değişmediği bildirilmiştir. Karaciğer yetersizliği
olan hastalar opioidlere daha duyarlı gibi görülmektedir ve dakika ventilasyonunda %50
süpresyon için daha düşük konsantrasyonlar gerekmektedir. Dolayısıyla karaciğer yetmezliği
olanlarda istenilen etkinin elde edilmesi için daha düşük dozlara ihtiyaç duyulmakta ancak
opioid etkisinin ortadan kaybolması ise değişmeden aynı hızda kalmaktadır. Böbrek
yetersizliği bulunan hastalarda duyarlılık artışı gözlemlenmemiştir, dolayısıyla bu hastalarda
remifentanil dozlaması aynıdır ve etkinin kaybolması da aynı hızdadır. Akciğerlerin
remifentanil metabolizmasında önemli bir yeri olmadığı düşünülmüştür. Remifentanilin
başlıca metaboliti böbreklerden atıldığından, böbrek yetmezliğinde birikme görülür. Ancak,
bu metabolitin potentliği çok zayıf olduğundan, 24 saatlik infüzyonlar sonrasında bile, klinik
açıdan önemli konsantrasyonlara erişmez. 2-12 yaş arasındaki pediatrik hasta grubunda
remifentanilin farmakokinetik özellikleri erişkinlerde bildirilene çok benzemektedir.
Yaşlılarda ilacın etkisinin başlaması daha yavaştır ve bütün μ reseptör agonistlerine olduğu
gibi remifentanile de daha çok duyarlıdır. Yaşlılarda dağılım hacmi daha küçüktür ve klirens
hafifçe uzamıştır. Bütün bu farklılıkların net sonucu yaşla birlikte dozun azaltılmasıdır.
30

Altmışbeş yaşın üzerindeki hastalarda, başlangıçtaki yükleme dozunun %50 azaltılması ve
sonrasında da hastanın ihtiyacına göre titre edilmesi önerilmektedir(53).
Piperidin sınıfindaki diğer opioidler gibi remifentanil de plasentadan kolayca geçer. Ancak,
diğer opioidlerin aksine fetüste de hızla metabolize olmaya devam eder. İ.v. 0.1 μg.kg-1
remifentanil ile epidural 100 μ fentanil karşılaştırıldığında Apgar skorları arasında bir fark
olmadığı gösterilmiştir. 39 gebenin 2’sinde doğum sonrasında hafif solunum depresyonu
bildirilmiştir. Ancak gebelerde remifentanilin kullanımı için daha fazla çalışmaya ihtiyaç
vardır. Remifentanilin günümüzde hazırlanan formülasyonunda glisin bulunduğundan
epidural ve spinal yolla uygulanmaz. Remifentanille insanlardaki çalışmalar sadece i.v.
uygulamayla gerçekleştirilmiştir(53).
Farmakodinami: Bütün μ reseptör agonistleri temelde benzer etkilere sahiptir(50).
a.Analjezi: Doza bağlı analjezik etkiler oluşturur. İnsanlarda yapılan laboratuar
çalışmalarında i.v. bolus dozların analjezik etkilerinin ( 0.625-2 μg/kg ) hedef plazma
konsantrasyonları belirlenerek ( 0.75-3 ng/mL) uygulanan bilgisayar kontrollü infüzyonlar
kadar iyi olduğu tespit edilmiştir. Bolus doz sonrası tepe analjezik etkiye 1-3 dakika içinde
ulaşılmakta ve yaklaşık 10 dakika sürmektedir. Gönüllülerde yapılan çalışmalarda MEAC
değerinin yaklaşık 0.75 ng/mL ve analjezik EC50’ nin ise 3 ng/mL olduğu belirlenmiştir. Her
iki çalışmada da remifentanilin alfentanile göre 40 kat daha potent olduğu görülmüştür. (50).
b.Volatil anesteziklerin MAC değerlerine etkileri: Remifentanilin volatil ajanların MAC
değerlerine etkileri diğer μ-opioid agonistlerine benzer şekilde dik doz-konsantrasyon ve
konsantrasyon-etki eğrilerine sahip olmasıyla karakterizedir. Köpeklerde yapılan bir
çalışmada remifentanil infüzyonunun doza bağımlı olarak sevfloranın MAC’nı % 65 azalttığı
görülmüştür. İnsanlarda remifentanilin bilgisayar destekli sürekli infüzyonla 0-32 ng.ml-1
hedef kan konsantrasyonuna ulaşacak şekilde uygulanmasıyla isofloranın MAC değerinin
doza-bağımlı olarak logaritmik şekilde düştüğü ve bunun yaştan etkilendiği bildirilmiştir.
31

Remifentanilin tam kandaki konsantrasyonu 1.3 ng.ml-1’e ulaştığında isofloranın MAC’ı % 50
azalmaktadır. İsofloranın MAC’ındaki düşüşün tavan düzeyi, 8-12 ng.ml-1 remifentanil
düzeylerine ulaşıldığında görülen % 85’lik bir azalmadır. (50)
Etki başlangıcının hızlı ve etki süresinin kısa olması remifentanili anestezi indüksiyonu için
uygun bir ilaç haline getirmektedir. Remifentanilin 2-20 μg.kg-1 doz aralığında tek başına
kullanımı bilinç kaybı oluşturulması için yeterli değildir. Remifentanilin, hastaların %
50’sinde bilimç kaybı oluşturulması gereken medyan dozu 12 μg.kg-1’dir ve 5 μg.kg-1’ın
altındaki dozlarda hiçbir hastada bilinç kaybı oluşmaz. Ayrıca bu dozlarda diğer opioidlerde
olduğu gibi kas rijiditesi ve amaçsız hareketler görülmesi nadir değildir. Hatta en düşük
remifentanil dozlarında dahi hastaların % 40’ında orta dereceli kas rijiditesi görülür. Yüksek
dozlarda ise ciddi kas rijiditesi oranı % 60’tır. Bu etki remifentanilin indüksiyonda tek başına
kullanımını sınırlar. (50).
Remifentanille yapılan ilk klinik çalışmalar, % 66 azot protoksit varlığında 0.05 μg.kg-1
remifentanil infüzyonunun hastaların % 50’sinde, trakeal entübasyon ve cilt insizyonuna
motor ve hemodinamik yanıtları önlediğini göstermiştir. Daha sonraki cerrahi uyaranlara karşı
cevapların önlenmesi için daha yüksek (0.6 μg.kg-1.dak-1) remifentanil dozlarına ihtiyaç
vardır. (50).
Remifentanille birlikte propofolün total intravenöz anestezide birlikte kullanımı gittikçe
artmaktadır. Bu kombinasyon, koroner arter bypass grefti, majör torasik, abdominal ve
ortopedik girişimlerle birlikte ambulatuar cerrahi girişimleri içeren geniş bir yelpazede
kullanılmaktadır. (50).
c.Diğer santral sinir sistemi etkileri: EEG’de klasik μ-opioid agonist etkileri oluşturur;
konsantrasyona bağlı EEG’de yavaşlama, maksimal etkinin % 50’si değişiklik oluşturan
konsantrasyonu (EC50) 15-20 ng.ml-1’dir. Etki başlangıcı alfentanile benzer ancak etki süresi
çok daha kısadır. İsofloran ve N2O anestezisi uygulanan kontrole ventilasyon altındaki
32

hastalarda kraniotomi sırasında ilk burr hole sonrasında remifentanil (0.5 veya 1 μg.kg-1)
bolus olarak verildiğinde intrakraniyal basıncın etkilenmediği ve ortalama arter basıncında
orta dereceli doza bağımlı bir düşüş olduğu görülmüştür. Opioid infüzyonuna entübasyon
öncesinde başlanıp, entübasyon sonrasında hemodinamik stabilite sağlayacak şekilde titre
edildiğinde intrakraniyal basınç ve serebral perfüzyon basıncının remifentanil ve fentanille
benzer olduğu tespit edilmiştir. Yüksek dozlarda remifentanil uygulanması (5 μg.kg-1’ı
takiben 3 μg.kg-1.dak.-1) serebral kan akım hızında ciddi düşüşlere yol açarken orta dozlarda
(2 μg.kg-1’ı takiben 1 μg.kg-1.dak.-1) bu görülmez. (50).
Bazı kraniyal ve nöroşirürjik girişimlerde uyarılmış motor cevapların ( motor evoked
potentials; MEPs ) monitörizasyonu önemlidir. Genel anestezide kullanılan opioidler, sedatif-
hipnotik droglar ve inhalasyon anesteziklerinin MEPs’i suprese ettikleri bilinmektedir.
Remifentanil diğer opioidler ve propofole göre MEPs’yi daha az baskılamaktadır. 9 ng.mL-1
hedef plazma konsantrasyonunda amplitüdü % 50 azaltır, fakat MEPs’in kalite ve
kullanılabilirliği 15 ng.mL-1 hedef konsantrasyonda dahi korunur ki bu düzey cerrahi
anestezinin sınırları içerisindedir. (50).
d.Solunum depresyonu: Remifentanil doza bağımlı solunum depresyonu oluşturur. Bu
solunum depresyonu end-tidal CO2 (ETCO2)’deki artış ve oksijen satürasyonundaki düşüşle
ölçülür. Peak solunum depresyonu etkisi remifentanilden 5 dakika sonra meydana gelir.
Solunum depresyonunun süresi 1.5 μg.kg-1 remifentanil dozundan sonra 10 dakika, 2 μg.kg-1
remifentanil dozundan sonra ise 20 dakikadır. Sürekli opioid infüzyonu sırasında 4
remifentanilin 0.0025, 0.050, 0.075 dozlarda uygulanması CO2’ye solunum cevabını sırasıyla
% 30, 45 ve 60 oranında azaltmaktadır. Remifentanilin oluşturduğu solunum depresyonunun
geri dönüşü hızlıdır bütün bu infüzyon hızlarında remifentanil kesildikten sonra ortalama 8
dakika içinde ( 5-15 ) bazal dakika ventilasyon düzeyine ulaşılmaktadır. (50).
33

e.Hemodinamik etkileri: 1 μg.kg-1 den büyük remifentanil bolus dozlarında başlıca etki
sistolik kan basıncında (5-20 torr) ve kalp hızında ( 15-25 atım.dak.-1) artıştır. İsofloran
anestezisi uygulanan hastalarda remifentanil (5 μg.kg-1’ın üstünde) sistolik kan basıncı ve
kalp hızında doza bağımlı düşüş oluşturur. Remifenatil infüzyonunda hipotansiyon sıklığı %
12 iken bradikardi daha az görülmektedir ( % 2 ). Koroner arter hastalığı olanlarda
hemodinamik değişiklikler daha büyüktür. Propofolle birlikte yüksek doz (2 μg.kg-1.dak-1)
remifentanil uygulanan hastalarda ortalama arter basıncında % 30, kardiak indekste ise %
25’lik bir düşme meydana gelmiştir. Myokard kan akımı ve oksijen tüketimi ise yaklaşık
olarak sırasıyla % 30 ve 40 azalmıştır. Remifentanilin kardiak cerrahi uygulanan hastalarda
hızlı enjeksiyonu takiben infüzyonla uygulanması ciddi bradikardi ve hipotansiyona yol
açabilir. Yükleme dozunun 60 saniye ve üstünde bir sürede uygulanması bu yan etkilerin
görülme sıklığını azaltır. (50).
f.Gastrointestinal etkiler: Diğer μ agonistleri gibi remifentanil de bulantı ve kusmaya yol
açabilir. Yüksek infüzyon hızlarında ( 1-8 μ.kg-1.dak.-1 ) % 70 oranında bulantı görülür. Diğer
opioidlere benzer şekilde remifentanil mide boşalma süresini ve safra drenajını uzatır. Biliyer
etkileri morfin ve meperidinin yol açtığı drenaj gecikmesinden daha hızlı ortadan kalkar. (50).
g.Diğer yan etkileri: Postoperatif titreme, ağız kuruluğu, kaşıntı, flushing, terlemeye yol
açabilir. (50).
Dozaj ve uygulama: Çok kısa etki süresine sahip olması nedeniyle, devamlı infüzyon için en
uygun seçenektir. Remifentanil anestezinin indüksiyonunda tek başına kullanım için uygun
değildir. 2 μg.kg-1’in üzerindeki bolus dozlarda arteriyal basınçta % 20-30’luk düşüşe yol
açar. Yüksek doz infüzyon uygulanan kardiak hastalardaki hemodinamik değişiklikler,
remifentanille birlikte propofol alanlarınkine eşittir. Potent bir inhalasyon ajanıyla kombine
edildiğinde, 60 saniye içinde 1 μg.kg-1 yükleme dozunda kullanılması hemodinamik
stabiliteyle birlikte yeterli entübasyon şartları sağlar. Anestezi indüksiyonu ve laringoskopide
34

remifentanilin en yaygın olarak bildirilen kullanım şekli; remifentanilin 0.5-1 μg.kg-1 dozda
60 saniye içerisinde verilmesine ilave olarak 1-2 mg.kg-1 propofol verilmesini takiben 0.25-
0.5 μg.kg-1.dak.-1 hızda remifentanil infüzyonudur. Premedikasyonda 1-2 mg midazolam da
bu rejimde olabilir. Benzer bir uygulamanın önerildiği pediatrik hastalarda, premedikasyonda
oral midazolam 0.5 mg/kg kullanılmaktadır. Yaşlılarda dozun azaltılması gerekmektedir. 60
saniyede verilen 0.05 μg.kg-1 remifentanille birlikte propofol titre edilerek 10 mg’lık artan
dozlarda biliç kaybı oluşana kadar verilir. Takiben 0.1 μg.kg-1.dak.-1 hızla remifentanil
infüzyonu yapılır. Anestezi indüksiyonunda hedef kontrollü infüzyon kullanılacaksa başlangıç
5-7 ng/mL remifentanil hedefi ile birlikte 0.5-1 MAC inhalasyon anesteziği veya 2 ng/mL ile
propofolün hedef kontrollü infüzyonla verilmesi önerilir(50).
% 70 N2O ve O2 ile birlikte 0.6 μg.kg-1.dak.-1 remifentanil kombinasyonu genellikle
anestezinin idamesinde yeterlidir. Ancak geniş bir infüzyon aralığı ( 0.025-2 μg.kg-1.dak.-1 )
bildirilmiştir. Pediatrik hastalarda da N2O ile birlikte benzer infüzyon hızları önerilmektedir.
Remifentanil; sevofloran ( % 1-2 ), desfloran ( % 3-3.6 ) veya isofloranla ( % 0.2-0.8 ) birlikte
kullanıldığında daha düşük infüzyon hızlarına ihtiyaç duyulur ( 0.2-0.25 μg.kg-1.dak.-1 ).
TIVA’da remifentanil ve propofol için infüzyon hızları sırasıyla 0.25-0.5 μg.kg-1.dak.-1 ve 75-
100 μg.kg-1.dak.-1’dır. N2O ilave edilirse remifentanil infüzyon hızı 0.125 μg.kg-1.dak.-1’e
kadar düşürülürken, propofol 50-75 μg.kg-1.dak.-1 hızda kullanılabilir. Yaşlı veya kardiak
hastalığı olanlarda propofol dozunun yaklaşık % 25 oranında azaltılması önerilir. Pediatrik
hastalarda bildirilen infüzyon hızları erişkinler için bildirilene eştir. Kardiak cerrahide yüksek
doz opioid infüzyonu için remifentanil 1-3 μg.kg-1.dak.-1 kullanılır ve hipotermide doz
ayarlanmalıdır. Bu yüksek doz infüzyona düşük dozda propofol ( 50 μg.kg-1.dak.-1) infüzyonu
eklenmesi cilt insizyonu, sternotomi ve aortik kanülasyona cevapları baskılar(50).
Remifentanilin en önemli dezavantajı, çok kısa etki süresine bağlı olarak anesteziden uyanma
sonrasında hastanın ağrı duymasıdır. Bu yüzden eğer orta-ciddi postoperatif ağrı olacağı
35

tahmin ediliyorsa 0.05-0.15 μg.kg-1.dak.-1 hızda remifentanil infüzyonuna devam edilmesi
tüm hastalarda yeterli analjezi sağlayacaktır(50).
Lokal veya rejyonal anesteziye yardımcı olarak kullanıldığında çok daha düşük infüzyon
hızlarında kullanılması ( 0.05-0.1 μg.kg-1.dak.-1) yeterli sedasyon ve analjezi sağlayacaktır.
Sedasyon ve analjezi için gereken remifentanil dozu midazolam veya propofolle kombine
edildiğinde % 50 azalır. 1-2 mg midazolam premedikasyon için verildiğinde 0.01-0.07 μg.kg-
1.dak.-1 remifentanil lokal ve rejyonal anestezi altında gerçekleştirilecek girişimler için yeterli
sedasyon ve analjeziyi sağlar(50).
36

MATERYAL ve METOD
Hastane etik komitesinin izni ve hastaların yazılı ve sözlü onayları alındıktan sonra,
endotrakeal entübasyon gerektiren çeşitli elektif cerrahi girişim planlanan, 18–60 yaşları
arasında ASA I-II 60 hasta çalışmaya alındı. Bazal kalp atım hızı (KAH) 60 < atım dk-1 ve
sistolik arter basıncı (SAB) < 100 mmHg olanlar, kardiyovasküler sisteme veya adrenerjik
cevaplara etkili ilaç tedavisi alan, sedatif veya opioid ilaç kullanım anamnezi olanlar, kardiak,
pulmoner, renal veya hepatik hastalık anamnezi olanlar, gebelik ve laktasyon dönemindeki
hastalarla, ideal vücut ağırlığından % 30’dan fazla sapma gösteren hastalar, güç entübasyon
ihtimali olanlar ( Mallampati sınıf ≥ 3 ), gastroösafajiyal reflü riski olan hastalar ile
remifentanil ve deksmedetomidine karşı bilinen aşırı duyarlılığı olanlar çalışma dışı bırakıldı.
Hastalar randomize olarak geliş sıralarına göre her biri 20 hasta içeren 3 gruba ayrıldı.
Çalışma çift kör ve plasebo kontrollü olarak gerçekleştirildi. Hastalara premedikasyon
uygulanmadı. Hastalara operasyon odasına alındıktan sonra, Dräger Infinity Delta ile,
noninvaziv kan basıncı (NİKB), elektrokardiogram (EKG) ve periferik oksijen satürasyonu
(SpO2) monitörizasyonu uygulandı. 5-10 dakikalık bir stabilizasyon dönemini takiben,
hastanın kalp atım hızı (KAH), sistolik, diastolik ve ortalama arter basınçları (SAB, DAB,
OAB) ölçülüp, bazal değerler olarak kaydedildi.
Daha sonra hastalara el sırtından 20-gauge intravenöz kateter ile damar yolu açılarak; Grup
D’deki hastalara deksmedetomidin toplam 1 μg.kg-1 50 mL’lik enjektörde serum fizyolojik
içinde dilüe edilerek, Grup R ve Grup P’deki hastalara ise serum fizyolojik 50 mL’lik
enjektörle 5 dakika içinde verildi. İnfüzyon tamamlanır tamamlanmaz Grup R’deki hastalara
remifentanil 1 μg.kg-1, 10 mL’lik enjektörde serum fizyolojikle sulandırılarak; Grup D ve
Grup P’deki hastalara ise 10 mL serum fizyolojik 60 saniye içerisinde bolus olarak verildi.
İlaçları hazırlayan ve uygulayan kişilerin ayrı olmasıyla çalışmanın çift kör olması sağlandı.
Böylece infüzyon süresi boyunca hastalar preoksijenize edildi. Çalışma ilaçlarının verilmesini
37

takiben 2 mg.kg-1 propofol 30 saniye içinde verilerek anestezi indüksiyonu sağlandı. Daha
sonra kas gevşemesi için 0.6 mg.kg-1 rokuronyum verildi ve % 100 O2 ile maske ventilasyon
uygulanarak 2. dakikada standart Macintoch laringoskopla endotrakeal entübasyon
gerçekleştirildi. Tüm endotrakeal entübasyonlar aynı ve deneyimli bir anestezist tarafından,
15 saniyeden kısa sürede ve tek seferde gerçekleştirilmiştir. Anestezinin idamesinde
sevofloran end-tidal konsantrasyonu % 1,5 – 2 olacak şekilde % 40-60 oranında O2+N2O
içinde kullanıldı.
Sistolik, diastolik ve ortalama arter basıncı (SAB, DAB, OAB) ile kalp atım hızını (KAH)
içeren hemodinamik parametreler; çalışma ilaçlarının verilmesi tamamlandıktan sonra,
entübasyondan önce, entübasyondan hemen sonra ve entübasyondan sonra 1, 3 ve 5.
dakikalarda olmak üzere ölçülüp bir yardımcı tarafından kaydedildi. Kayıtları tutan yardımcı
da hangi ilacın uygulandığını bilmiyordu.
Bradikardi ( KAH < 50 atım.dk-1), hipotansiyon ( sistolik arter basıncının bazal değerin %
20’sinden fazla düşüşü veya < 90 mm Hg ) , hipertansiyon ( sistolik kan basıncının bazal
değerin % 20’sinden fazla artışı veya > 160 mm Hg ) gibi yan etkiler de kaydedildi.
Olgularda eğer bradikardi gelişirse 0.5 mg atropin uygulanması, hipotansiyon gelişirse
intravenöz kristalloid verilerek tedavi edilmesi ve infüzyonun kesilmesi düşünüldü.
Verilerin değerlendirilmesinde SPSS 10,0 hazır istatistik paket programı kullanıldı. Gruplar
arasındaki cinsiyet, ASA ve mallampati farklılıklarının değerlendirilmesinde ki-kare; yaş,
vücut ağırlığı, hemodinamik değişkenlerin karşılaştırılmasında tek yönlü varyans analizi
(ANOVA) Tukey ile birlikte kullanıldı. Hemodinamik parametrelerin grup içinde
değerlendirilmesinde tekrarlı ölçümler varyans analizi dunnett testi ile birlikte kullanıldı.
Veriler ortalama ± s.s olarak gösterildi ve p < 0.05 istatistiksel olarak anlamlı kabul edildi.
38

BULGULAR
Tablo 1. Demografik veriler, ASA fizyolojik skor ve mallampati sınıflaması
Değişken Grup R (n=20) Grup D (n=20) Grup K (n=20)
Yaş 28,05±10,45 32,2±12,24 38,25± 9,99 *
Ağırlık 65,65±12,39 63,6±13,16 77,8±14,89 *
Cinsiyet (E/K) 10/10 8/12 9/11 ASA (ı / II) 19/1 19/1 14/6 *
Mallampati (1/2) 17/3 18/2 17/3
Veriler ortalama ±s.s, nicel veriler sayı olarak verilmiştir. * p<0.05
Grup K’daki hastaların yaş ve ağırlık ortalamaları Grup R ve Grup D’ye göre anlamlı ölçüde
daha yüksek ve ASA II fizyolojik skoruna sahip hasta sayısı da anlamlı ölçüde daha fazlaydı.
( p < 0.05) Gruplar arasında cinsiyet ve mallampati sınıflaması açısından fark yoktu. ( p >
0.05) ( Tablo 1; Grafik I, II, III, IV.)
.
Grafik I. Grupların yaş ve ağırlık değerleri
39

Grafik II. Grupların cinsiyet dağılımı
Grafik III. Grupların ASA fizyolojik skorları
40

Grafik IV. Grupların mallampati sınıflaması
Elde edilen hemodinamik veriler (SAB, DAB, OAB ve KAH) gruplar arasında ve grup içinde
karşılaştırıldı.
Gruplar arası karşılaştırmalarda;
Plasebo uygulanan kontrol grubundaki hastaların sistolik arter basınçları 1. dönemde,
remifentanil ve deksmedotimidin grubuna göre istatistiksel olarak anlamlı derecede daha
yüksekti. ( p < 0.05 ) 2. dönemde ise gruplar arasında sistolik arter basınçları bakımından
istatistiksel olarak anlamlı bir fark gözlenmedi. ( p > 0.05 ) ( Tablo 2. ; Grafik V. )
Entübasyon öncesi dönemde; sistolik arter basınçları, remifentanil grubunda plasebo grubuna
göre anlamlı ölçüde daha düşük iken (p < 0.01 ), deksmedetomidin grubundaki hastalarda
anlamlı bir düşüş görülmedi ( p > 0.05 ) ( Tablo 2. ; Grafik V. ).
Entübasyondan hemen sonraki dönemde; remifentanil plasebo ve deksmedotimidin uygulanan
hastaların sistolik arter basınçları, remifentanil ve deksmedetomidin grubunda kontrol
grubuna göre anlamlı ölçüde daha düşüktü. (sırasıyla p < 0.001 ve p < 0.01 ) ( Tablo 2. ;
Grafik V )
41

Entübasyondan sonraki 1. ve 3. dakikada remifentanil grubunda SAB değerleri anlamlı ölçüde
daha düşüktü (sırasıyla p < 0.001 ve ve p < 0.05 ). ( Tablo 2. ; Grafik V . ) Entübasyondan 5
dakika sonra sistolik arter basıncı değerleri, Grup R ve Grup D’de kontrol grubuna göre
istatistiksel olarak anlamlı derecede daha düşüktü (Sırasıyla p < 0.01 ve p< 0.05) (Tablo 2;
Grafik V. ).
Tablo 2. Grupların ölçüm zamanlarına göre sistolik arter basınçları.
Dönem Grup R Grup D Grup K
1 130,85±10,29 129±12,99 141,4±17,38*
2 127,05±13,53 129,6±18,52 138,75±19,46 3 92,15±10,99 ¶ 110,95±19,87 122,65±19,49
4 116,15±14,31 † 138,15±22,83 ¶ 158,3±24,13
5 113±12,52 † 129,8±19,97 135,8±24,94
6 110,65±16,72 * 118,6±16,71 124,3±14,72
7 107,25±12,65 ¶ 108,95±15,63 * 122,95±17,96
1.Bazal 2. Çalışma ilacı veya plasebo verildikten sonra 3. Entübasyondan önce 4. Entübasyondan hemen sonra 5. Entübasyondan 1 dk. sonra 6. Entübasyondan 3 dk. sonra 7. Entübasyondan 5 dk. sonra. Değerler mmHg olarak; veriler ise ortalama ± s.s olarak verilmiştir. * p < 0.05, ¶ p < 0.01, † p < 0.001.
Grup içi karşılaştırmalarda;
Remifentanil grubunda, sistolik arter basınçlarında, 2. dönem dışındaki tüm dönemlerde bazal
değerlere göre anlamlı ölçüde düşüş meydana geldi. ( p < 0.001) Bu düşüş entübasyon öncesi
dönemde en belirgin olarak gözlemlendi. (Grafik VI.)
Entübasyon öncesi döneme göre, entübasyondan sonraki dönemlerde sistolik arter
basınçlarında oluşan yükselme istatistiksel olarak anlamlıydı ( p < 0.001 ) ancak hiçbir
dönemde kontrol değerinin üzerine çıkmadı. (Grafik VI.)
.
42

Grafik V. Grupların sistolik arter basınçları (Gruplar arası karşılaştırma) 1.Bazal 2. Çalışma ilacı veya plasebo verildikten sonra 3. Entübasyondan önce 4. Entübasyondan hemen sonra 5.
Entübasyondan 1 dk. sonra 6. Entübasyondan 3 dk. sonra 7. Entübasyondan 5 dk. sonra
Deksmedotimidin uygulanan hastalarda, sistolik arter basıncında, entübasyon öncesi
dönemde, entübasyondan sonra kontrol değerlerine dönen; ancak 6. ve 7. dönemlerde devam
eden istatistiksel olarak anlamlı bir düşüş görüldü. ( p < 0.05, p < 0.001) Entübasyon sonrası
SKB’daki artış anlamlıydı. ( p < 0.05) (Grafik VI.).
Kontrol grubunda ise, sistolik arter basıncında bazal değere göre entübasyon öncesinde düşüş
meydana geldiği görüldü. Entübasyondan hemen sonra bazal değere göre anlamlı bir
yükselme gözlenmiştir. Entübasyondan 1 dakika sonra bazal değerlere dönen sistolik arter
basınçlarının, entübasyondan 3 ve 5 dakika sonra bazal değerlere göre daha düşük olduğu
gözlendi. (sırasıyla p < 0.001 ve p < 0.01) (Grafik VI.).
DAB değerleri, remifentanil grubunda deksmedotimidin ve kontrol grubuna göre, 3, 4 ve 5.
dönemlerde anlamlı ölçüde daha düşüktü. ( p < 0.001 ve p < 0.05 ) (Tablo 3. ve Grafik
VII.).Diğer dönemlerde ise gruplar arasında diastolik arter basınçları arasında anlamlı bir
fark yoktu. (p > 0.05)
43

Grafik VI. Grupların sistolik arter basınçları (Grup içi karşılaştırma) 1.Bazal 2. Çalışma ilacı veya plasebo verildikten sonra 3. Entübasyondan önce 4. Entübasyondan hemen sonra 5.
Entübasyondan 1 dk. sonra 6. Entübasyondan 3 dk. sonra 7. Entübasyondan 5 dk. sonra.
Tablo 3. Grupların ölçüm zamanlarına göre diastolik arter basınçları
Dönem Grup R Grup D Grup K
1 80,5±9,25 81±13,35 81,4±12,02 2 76,75±10,31 79,25±15,89 80,05±11,59
3 49,15±8,4 † 69±13,25 75,5±15,64
4 74,15±12,06 † 94,9±17,18 105±16,24
5 71,5±9,33 * 83,35±20,56 81,55±12,54
6 68,65±11,18 75,1±15,53 75,9±12,06 7 64,9±10,9 66,95±18,49 73,5±15,01
1.Bazal 2. Çalışma ilacı veya plasebo verildikten sonra 3. Entübasyondan önce 4. Entübasyondan hemen sonra 5.Entübasyondan 1 dk. sonra 6. Entübasyondan 3 dk. sonra 7. Entübasyondan 5 dk. sonra. Değerler mmHg olarak; veriler ise ortalama ± s.s olarak verilmiştir. * p < 0.05 ; † p < 0.001.
44

Grafik VII. Grupların diastolik arter basınçları (Gruplar arası karşılaştırma)
Grup içi karşılaştırmalarda;
DKB, remifentanil grubunda bazal değerlere göre entübasyon öncesi dönem ile 5, 6 ve 7.
dönemlerde anlamlı derecede düşüş gösterdi. (p < 0.001, p < 0.01) Bu düşüş en belirgin
olarak entübasyon öncesi dönemdeydi. Entübasyon sonrası dönemlerde entübasyon öncesine
göre diastolik arter basıncı anlamlı ölçüde artmış olsa da, kontrol değerlerinin altında
seyrettiği görüldü. (Grafik VIII.)
Deksmedotimidin grubunda; entübasyon öncesi dönem ve entübasyondan sonra 5. dakikada
diastolik arter basıncında bazal değere göre anlamlı derecede düşme görülürken,
entübasyondan hemen sonra ise anlamlı bir artış saptandı. ( p<0.001) (Grafik VIII.).
Kontrol grubunda ise; diastolik arter basıncı entübasyondan hemen sonra anlamlı ölçüde
artmıştı. (p < 0.001) Diastolik arter basıncında görülen bu yükselmenin, daha sonraki
dönemlerde kontrol değerlerine döndüğü görüldü. (Grafik VIII.)
45

Grafik VIII. Grupların diastolik arter basınçları (Grup içi karşılaştırma) 1.Bazal 2. Çalışma ilacı veya plasebo verildikten sonra 3. Entübasyondan önce 4. Entübasyondan hemen sonra 5.
Entübasyondan 1 dk. sonra 6. Entübasyondan 3 dk. sonra 7. Entübasyondan 5 dk. sonra.
Tablo 4. Grupların ölçüm zamanlarına göre ortalama arter basınçları
Dönem Grup R Grup D Grup K
1 99,05±8,38 100,35±12,95 106,6±11,34 2 94,55±12,18 102,1±17,14 103,45±13,8
3 64,4±7,49 † 86,25±15,71 94,05±17,31
4 89,8±11,51 † 114,4±19,67 * 127,9±19,52
5 87,2±10,8 ¶ 107,2±21,03 103,2±17,49
6 84,9±13,39 93,5±15,75 94,25±12,69
7 80,75±11,96 * 83,5±16,98 93,4±13,03
1.Bazal 2. Çalışma ilacı veya plasebo verildikten sonra 3. Entübasyondan önce 4. Entübasyondan hemen sonra 5. Entübasyondan 1 dk. sonra 6. Entübasyondan 3 dk. sonra 7. Entübasyondan 5 dk. sonra. Değerler mmHg olarak; veriler ise ortalama ± s.s olarak verilmiştir. * p < 0.05 , ¶ p < 0.01, † p < 0.001.
Ortalama arter basıncı; remifentanil grubunda entübasyon öncesi dönmede deksmedotimidin
ve kontrol grubuna göre anlamlı ölçüde daha düşüktü (p < 0.001). Entübasyondan hemen
sonra ortalama arter basıncı Grup R ve Grup D’de kontrol grubuna göre anlamlı ölçüde daha
düşüktü (sırasıyla; p < 0.001 ve p < 0.05). Entübasyondan sonraki 1. ve 5. dakikalarda
46

ortalama arter basıncı değerleri remifentanil grubundaki hastalarda diğer 2 gruba göre anlamlı
ölçüde daha düşüktü (sırasıyla; p < 0.01 ve p < 0.05). (Tablo 4. Grafik IX.)
Grafik IX. Grupların ortalama arter basınçları (Gruplar arası karşılaştırma)
Grup içi karşılaştırmalarda;
Remifentanil grubunda, ortalama arter basıncının, 2. dönem hariç tüm dönemlerde bazal
değere göre anlamlı ölçüde düştüğü görüldü (p < 0.001 ve p < 0.01)( Grafik X.). Bu düşüş
entübasyon öncesinde diğer dönemlere göre daha fazlaydı.
Deksmedotimidin grubunda ise, entübasyon öncesi, entübasyon sonrası 5.dakikada, ortalama
arter basıncı bazal değere göre anlamlı derecede düşmüştü (p < 0.001).
Entübasyondan hemen sonra ise ortalama arter basıncında görülen artış istatistiksel olarak
anlamlı derecedeydi (p < 0.001) (Grafik X.).
47

Grafik X. Grupların ortalama arter basınçları (Grup içi karşılaştırma)
1.Bazal 2. Çalışma ilacı veya plasebo verildikten sonra 3. Entübasyondan önce 4. Entübasyondan hemen sonra 5.
Entübasyondan 1 dk. sonra 6. Entübasyondan 3 dk. sonra 7. Entübasyondan 5 dk. sonra.
Kontrol grubunda; ortalama arter basıncı, entübasyon öncesi ve entübasyondan sonraki 3 ve
5.dakikalarda bazal değere göre anlamlı derecede düşmüşken (p < 0.01), entübasyondan
hemen sonraki dönemde ise anlamlı bir artış vardı (p < 0.001) (Grafik X.)
Tablo 5. Grupların ölçüm zamanlarına göre kalp atım hızları.
Dönem Grup R Grup D Grup K
1 83,1±16,46 82,55±13,38 83±15,52
2 85,6±20,91 69,9±12,62* 82,35±15,2
3 71,8±12,96* 71,8±16,4* 84,05±14,24
4 88,8±19,75 93,1±19,25 92,35±14,74 5 87,55±14,26 84,5±14,33 85,9±13,99 6 83,3±12,7 82,6±15,36 86,75±14,4 7 80,35±12,94 77,25±10,68 81,6±12,39
1.Bazal 2. Çalışma ilacı veya plasebo verildikten sonra 3. Entübasyondan önce 4. Entübasyondan hemen sonra 5.
Entübasyondan 1 dk. sonra 6. Entübasyondan 3 dk. sonra 7. Entübasyondan 5 dk. sonra. Değerler mmHg olarak;
veriler ise ortalama ± s.s olarak verilmiştir. * p < 0.05.
48

Kalp atım hızı; deksmedotimidin grubunda, 2. dönemde remifentanil ve kontrol grubuna göre
anlamlı ölçüde daha düşüktü (p < 0.05). Entübasyondan hemen sonraki dönemde ise
remifentanil ve deksmedotimidin grubundaki hastaların kalp atım hızları kontrol
grubundakilere göre anlamlı ölçüde daha düşüktü (p < 0.05). Gruplar arasında diğer
dönemlerde kalp atım hızları bakımından istatistiksel olarak anlamlı bir farklılık olmadığı
saptandı (p > 0.05) (Tablo 5. Grafik XI).
Grafik XI. Grupların kalp atım hızları (Gruplar arası karşılaştırma)
Grup içi karşılaştırmalarda;
Kalp atım hızının, remifentanil grubunda, sadece entübasyon öncesi dönemde bazal değere
göre anlamlı ölçüde azaldığı (p < 0.001), diğer dönemlerde ise anlamlı bir değişiklik olmadığı
gözlemlendi (p > 0.05), (Grafik XII.) .
Deksmedotimidin grubunda ise, 2 ve 3. dönemlerde kalp atım hızında meydana gelen düşme
(sırasıyla; p < 0.001 ve p < 0.001 ) ve entübasyondan hemen sonra görülen artış istatistiksel
olarak anlamlıydı (p < 0.01), (Grafik XII.).
49

Kontrol grubunda, kalp atım hızı entübasyondan hemen sonra anlamlı ölçüde artarak diğer
dönemlerde bazal değerlere yakın seyretmiştir (p < 0.05), (Grafik XII.).
Grafik XII. Kalp atım hızları (Grup içi karşılaştırma) 1.Bazal 2. Çalışma ilacı veya plasebo verildikten sonra 3. Entübasyondan önce 4. Entübasyondan hemen sonra 5.
Entübasyondan 1 dk. sonra 6. Entübasyondan 3 dk. sonra 7. Entübasyondan 5 dk. sonra.
50

TARTIŞMA
Anestezi indüksiyonuyla birlikte laringoskopi ve trakeal entübasyon anestezinin hemodinamik
değişikliklere en fazla yol açtığı dönemdir. LTE sempatik sinir aktivitesinde önemli artışlara
yol açarak plazma katekolamin düzeylerinde yükselmeyle birlikte hipertansiyon ve taşikardi
cevabının ortaya çıkmasına neden olur. Ancak bu cevaplar kısa süreli ve geçicidir(1-5,54,55).
Oluşan hemodinamik değişikliklerin derecesi indüksiyonda kullanılan anesteziklerin
kardiyovasküler sistem üzerindeki etkilerine de bağlıdır(54-57).
Plasebo olarak SF uygulanan kontrol grubundaki hastalarımızda, propofol ile anestezi
indüksiyonu sonrasında, SAB, DAB, OKB’ında sırasıyla % 13.2, % 6.7 ve % 11.7 oranında
bir düşüş meydana gelirken, KAH’da sadece % 1’lik bir artış gözlendi. Entübasyondan 1
dakika sonra ise SAB, DAB, OAB ve KAH değerlerinde sırasıyla % 12, 29, 19 ve 11
oranında olan önemli artışlar olduğunu gördük.
Miller ve ark.’nın(55) yaptıkları bir çalışmada, anestezi indüksiyonunda thiopental ve süksinil
kolin kullanmış, kontrol grubundaki hastalarda indüksiyon sonrasında SAB’da önemli bir
değişiklik olmaksızın ( % 4 artış ) KAH’de % 40’a varan ciddi artışlar olduğunu bildirmiştir.
Bu çalışmada entübasyondan sonraki 1. dakikada KAH’nin daha da artışına ilave olarak
SAB’de ortalama 52 mmHg’lik ( yaklaşık % 40 ) bir artış olduğunu gözlemledik.
Anestezi indüksiyonunda tiyopental ve süksinilkolinin kullanıldığı bir başka çalışmada ise
benzer sonuçlar elde edilmişti. İndüksiyon sonrasında arteriyal basınçlarda belirgin bir
değişiklik olmaksızın KAH’de artış görülmekte, entübasyon sonrasında ise KAH’de daha da
artışla birlikte SAB ve DAB’da ciddi artışlar meydana gelmiştir (24).
Anestezi indüksiyonunda propofol kullanılması etomidat ve tiyopentala göre arteriyal kan
basınçlarında daha fazla düşüşe yol açmakta ve baroreseptör refleks mekanizmaları
bozmaktadır. Oluşan hipotansiyona nazaran kalp hızında sadece küçük artışlar olduğu
bildirilmiştir(56,57). Kim ve ark.’ları(58) yaptıkları bir çalışmada 2 mg.kg-1 propofol ile anestezi
51

indüksiyonu sonrasında OAB’da yaklaşık olarak % 18 oranında bir düşme meydana gelirken,
KAH’da bir değişiklik olmadığını göstermişlerdir. Yapılan bir başka çalışmada ise 2.5 mg.kg-
1 propofol ile anestezi indüksiyonu sonrasında SAB’ında 27 mmHg’lik yani yaklaşık % 20
oranında ( 132 ± 4.3’ten 105 ± 4 mmHg’ye ) ve DAB’de ise 7 mmHg’lik yani yaklaşık % 10
oranında ( 66 ± 2’den 59 ± 2 mmHg’ye ) düşme olduğu gösterilmiştir(57).
Propofole bağlı hipotansiyonun en önemli nedeni sistemik vasküler rezistanstaki düşüş bir
başka deyişle afterloaddaki azalmadır(57,59). Biz de çalışmamızda bu çalışmalara benzer
sonuçlar elde ettik. Plasebo olarak SF uyguladığımız grupta OAB’da propofol ile indüksiyon
sonrası % 11.7 oranında bir düşüş meydana gelirken, KAH’da bir değişiklik gözlemlemedik.
Propofolün sempatik nöronal aktiviteyi inhibe ettiği ve barorefleks duyarlılığında azalmaya
yol açtığı bilinmektedir(57,60). İndüksiyon sonrası, kan basıncı düşüşüne rağmen kalp hızında
belirgin bir değişiklik olmaması bizim bu bilgiyi destekleyen bir bulgumuz olarak göze
çarpmaktadır. Entübasyon sonrası meydana gelen değişiklikleri ve postindüksiyon
hemodinamik durumun etkilerini değerlendiren çalışmalara ihtiyaç olduğu düşüncesindeyiz.
Tüm gruplarda indüksiyondan sonra SAB, DAB ve OAB’de, remifentanil grubunda en büyük
oranda olmak üzere düşüş meydana gelmişti. Remifentanil uygulanan hastalarda entübasyon
öncesinde SAB, DAB ve OAB’deki düşüş oranlarının sırasıyla % 29, 38.9 ve 34.9 olduğunu
gördük. Bu değerler plasebo grubuna göre anlamlı ölçüde daha düşüktü. Deksmedetomidin
grubunda ise SAB, DAB ve OAB’daki düşüş oranları % 13.9, 14.9 ve 14 idi, plasebo grubuna
göre anlamlı bir farklılık olmadığını gözlemledik. KAH’de ise indüksiyon sonrasında kontrol
grubunda anlamlı bir değişiklik gözlenmezken, hem remifentanil hem de deksmedetomidin
uygulanan hastalarda KAH sırasıyla % 13.5 ve 13 oranında azaldığını tespit ettik.
Propofolle anestezi indüksiyonu öncesinde 1 μg.kg-1 dozda remifentanil uygulanmasının tek
başına propofole göre daha belirgin bir hipotansiyon oluşturduğunu ancak deksmedotimidinin
52

buna bir katkısı olmadığını gördük. Ayrıca propofolle birlikte remifentanil ve
deksmedetomidin kullanımının KAH’de daha fazla düşüşe yol açtığını gözlemledik.
Thompson ve ark.’nın(61 ) yaptığı bir çalışmada propofolle anestezi indüksiyonu öncesi 1
μg.kg-1 bolus sonrası 0.5 μg.kg-1 hızda infüzyonla uygulanan remifentanilin, entübasyondan 1
dakika önce OAB ve KAH düşüşe yol açtığını göstermiştir ( Yaklaşık olarak OAB 95
mmHg’den, 50 mmHg’ye; KAH ise 85 atım.dak.-1’den 65 atım.dak.-1’ya ). Endotrakeal
entübasyon sonrasında, remifentanil uygulanan grupta OAB’da 8.1 mmHg artış gözlenirken
kontrol grubunda bu artış 42 mmHg düzeyinde kalmıştır. Entübasyon sonrasında remifentanil
grubunun OAB değerleri 8.1 mmHg’lık artışa rağmen indüksiyon öncesi değerlerinin altında
seyretmişti. KAH entübasyon sonrasında kontrol grubunda önemli ölçüde artış gösterirken
remifentanil grubunda artış olmadığı sonucu elde edilmişti. Ancak bu çalışmada remifentanil
grubundaki 10 hastanın 5’inde tedavi gerektiren bradikardi (KAH < 45 ) veya hipotansiyon
( SAB < 80 mmHg) geliştiği bildirilmektedir.
Bizim çalışmamızda OAB ve KAH’daki düşüş Thompson’un elde ettiği sonuçlara göre daha
azdı ve hiçbir hastamızda tedavi gerektirecek bradikardi ve hipotansiyona rastlanmamıştır.
Bunun, bizim çalışmamızda remifentanilin injeksiyon süresinin daha uzun olmasına (30
saniye karşı 60 saniye) bağlı olabileceğini düşündük. Bizden farklı olarak indüksiyon sonrası
entübasyona kadar maske ventilasyonda oksijenle birlikte % 66 azaot protoksit ve % 1
isofloran kullanımı ve bolus doz sonrasında remifentanil infüzyonuna devam edilmesi de buna
katkıda bulunmuştu. Hastaların yarısında gelişen bradikardiden kısmen vekuronyum ve
propofol kullanımı da sorumlu olabilir.
Bolus dozda uygulandıktan sonra infüzyonuna devam edildiğinde remifentanilin hipotansiyon
ve bradikardiye yol açtığı bildirilmiştir. Schüttler ve ark.’nın yaptığı, remifentanilin yine 1
μg.kg-1 bolus sonrası 0.5 μg.kg-1.dak.-1 hızda infüzyonla uygulandığı çokmerkezli bir
çalışmada indüksiyon öncesinde atropin veya glikopirolat uygulanmasına ve ve sıvı
53

yüklenmesine rağmen hastaların % 53’ünde ciddi hipotansiyon dönemlerine ve % 4 hastada
ise ciddi bradikardiye rastlandığını bildirmiştir(62).
Hall ve ark.’nın(63) remifentanilin farklı dozlarının LTE’ye bağlı hemodinamik cevaplar
üzerine etkilerini değerlendirmiş; remifentanili 0.5 veya 1 μg.kg-1 bolus olarak 30 saniye
içinde uyguladıktan sonra 0.25 veya 0.5 μg.kg-1.dak.-1 hızda infüzyonuna devam ettiğinde 5
hastada hipotansiyon 1 hastada ise bradikardi geliştiğini görmüştür. Hall indüksiyon
öncesinde hastala 200 μg glikopirolat uygulamış, glikopirolat uygulamadığı bir grubu da
kontrol grubu olarak almıştı. Remifentanil rejiminin 0.5 μg.kg-1 bolus ve 0.25 μg.kg-1.dak.-1
hızda infüzyon olduğu kontrol grubundaki hastalardaki KAH daha ortalama 69 atım.dak.-1
iken glikopirolat uygulanan diğer iki grubun her ikisinde de 81 atım.dak.-1 di. Hall’un
çalışmasında hipotansiyon ve bradikardinin daha az görülmesinin nedeni glikopirolat
uygulanmasıyla birlikte, indüksiyonda azot protoksit ve rokuronyum kullanımı ve propofolün
titre edilerek verilmesi olarak açıklanmıştır.
Kweon ve ark.’nın(64) yaptıkları bir çalışmada sevofloranla anestezi indüksiyonunun OAB’de
önemli ölçüde düşüşe yol açtığını, remifentanil uygulanmasıyla da bu düşüşün daha da
derinleştiğini göstermiştir. Bu çalışmada plasebo ve 0.5 μg.kg-1 dozda remifentanil uygulanan
hastalarda entübasyon sonrasında KAH ve OAB’da önemli artış olduğunu ancak, 1 μg.kg-1
dozda remifentanil uygulanan hastalarda ise KAH ve OAB’nin değişmediğini bildirmiştir.
Ayrıca plasebo grubunda 2 ( 20 hastadan ) ve 0.5 μg.kg-1 remifentanil uygulanan 20 hastanın
1 tanesinde tedavi gerektirmeksizin ortadan kalkan ektopik atımlara rastladığını rapor etmiştir.
Çalışmamızda 1 μg.kg-1 uygulanmasıyla OAB’de % 30 KAH’da ise % 25’den fazla bir düşüş
olduğunu gördük. (OAB yaklaşık olarak 90 mmHg’den, 60 mmHg’ye; KAH ise yaklaşık
olarak 75 atım.dak.-1’den, 55 atım.dak.-1’e). KAH’da ise Kweon’un vardığı önemli
sonuçlardan birisi de özellikle laringoskopi ve entübasyon sırasında olmak üzere QTc
süresinin uzadığı ve remifentanilin 1 μg.kg-1 dozda uygulandığında QTc süresindeki bu
54

uzamayı önlediğiydi. Ancak 0.5 μg.kg-1 remifentanil hem entübasyona bağlı hemodinamik
cevapları önlemede hem de QTc’deki uzamayı önlemede yetersiz kalmıştır. ( 30 saniye içinde
verildiğinde )
Choi ve ark.(65) yaptıkları bir çalışmada remifentanilin 0.5-1 μg.kg-1 dozlarının her ne kadar
LTE’ye karşı oluşan hemodinamik cevapları zayıflattığını bildirse de, entübasyon sonrasında
OAB ve KAH değerlerinde artış olduğu gözlemlenmiştir.
Remifentanilin 2-4 μg.kg-1 tek bolus dozlarının propofolle anestezi indüksiyonu yapıldığında
kas gevşetici uygulanmaksızın yeterli entübasyon şartları ve hemodinamik kontrol sağladığı
bildirilmiştir. Stevens ve ark. indüksiyon öncesinde prehidrasyon yaptığı hastaları 4 gruba
ayırarak 90 saniye içinde 1, 2, 3 ve 4 μg.kg-1 dozda remifentanil uygulamış, 2 mg.kg-1
propofol ile anestezi indüksiyonunu takiben 90 saniye sonra kas gevşetici kullanmaksızın
LTE uygulayarak entübasyon şartları ve hemodinamik değişiklikleri incelemiştir. Stevens
indüksiyon sonrasında tüm gruplarda indüksiyon sonrasında önemli ölçüde düştüğünü ve 2, 3,
4 μg.kg-1 dozda uygulanan gruplarda tüm çalışma boyunca bazal değerlerin altında
seyrettiğini bildirmektedir. KAH ise yüksek dozlarda remifentanil uygulandığında tüm
dönemlerde indüksiyon öncesi değerlerin altında seyretmektedir. Bizim çalışmamızda da
olduğu gibi hiçbir hastada kas rijiditesine rastlanmamıştır(66).
Remifentanilin 30 saniye içerisinde verilen 1 μg.kg-1 tek bolus dozlarının laringoskopi ve
trakeal entübasyona bağlı pressör cevapları önlediği ancak 0.5 μg.kg-1’lık tek bolus dozların
yeterli olmadığı bildirilmiştir. Özellikle hızlı indüksiyon ve endotrakeal entübasyonun
gerektiği ve kısa süreli ve uzamış opioid etkisinin istenmediği operasyonlarda süksinilkolinle
birlikte tek bolus dozlarının yeterli hemodinamik kontrol sağladığı bildirilmiştir. Bu
çalışmada SAB, DAB ve KAH değerlerinde entübasyondan 1 dakika sonra bazale göre
sırasıyla % 17, 15 ve 11 oranında bir artış meydana gelmiştir(24).
55

Song ve ark.’ları(67) da yaptıkları çalışmada 1 μg.kg-1 remifentanilin bolus olarak
uygulanmasının entübasyon sonrası dönemde kan basıncında düşüşe yol açmaksızın trakeal
entübasyona akut hemodinamik cevapları etkili şekilde kontrol ettiğini bildirmişlerdir.
Çalışmamızda entübasyondan sonra 1. dakikada SAB, DAB ve OAB’de remifentanil
grubunda yaklaşık olarak sırasıyla % 10, 7 ve 10 oranında düşüş olduğunu gördük. KAH’deki
artış ise minimaldir ( % 6 ). Kullandığımız doz ve şekilde remifentanilin ciddi hipotansiyon ve
bradikardiye yol açmadan LTE’ye bağlı hemodinamik cevapları etkili bir şekilde kontrol
ettiğini gördük.
Deksmedetomidini, propofol ve rokuronyum ile anestezi indüksiyon öncesinde 1 μg.kg-1
dozda 5 dakika içerisinde bolus olarak uyguladığımızda, LTE’ye bağlı cevapları önlemede
yetersiz olduğunu gördük. Sadece OAB değerleri, kontrol grubuna göre anlamlı ölçüde daha
düşük olsa da indüksiyon öncesine göre % 14 oranında ciddi bir artış gözlemledik.
Çalışmamızda ayrıca deksmedetomidin bolus olarak uygulandıktan sonra SAB, DAB ve
OAB’da % 1 oranında minimal bir düşüş meydana gelirken KAH’da ciddi bir düşüş olduğunu
gördük.
Özkese ve ark.’nın(68) yaptıkları bir çalışmada deksmedetomidinin 1 μg.kg-1 yükleme dozunun
10 dakika içinde verilmesini takiben 0.2 μg.kg-1.s-1 hızda infüzyonla uygulandığında
laringoskopi ve entübasyon sonrasında hemodinamik stabilite sağladığını bildirmişlerdir.
Entübasyondan sonraki 1. dakikada OAB ve KAH’de indüksiyon öncesine göre herhangi bir
değişiklik meydana gelmediğini gözlemlemiştir. Yükleme dozu sonrasında OAB’de yaklaşık
% 20 oranında bir azalma meydana gelirken KAH’daki düşüş yaklaşık % 5 civarındaydı.
Deksmedetomidin grubundaki hastaların 4 (20 hastada), kontrol grubundaki hastaların ise
2’sinde (20 hastada) atropine ihtiyaç gösteren bradikardi meydana gelmişti.
Çalışmamızın sonuçları Özköse ve ark.’nın(68) elde ettiği sonuçlara göre farklılık
göstermektedir. Bunun deksmedetomidinin verilme sürelerindeki farklılığa ve anestezi
56

indüksiyonunda ilave olarak kullanılan 2 μg.kg-1 fentanile bağlı olabileceğini düşünüyoruz.
Deksmedetomidin doza bağımlı olarak bifazik kan basıncı cevabına yol açabilir. Yüksek
dozlarla başlangıçta 5-10 dakikada sonlanan geçici bir kan basıncı artışı ve refleks
bradikardiyi takiben kan basıncı düşüşüne yol açar(69). Deksmedetomidinin verilmesini
takiben KAH değerlerinde belirgin düşüş olması ve OAB’de değişiklik olmaması da bunu
destekliyor gözükmektedir. Ayrıca entübasyondan sonraki 5. dakikadaki hemodinamik
parametrelerin remifentanil grubu ile benzer olmasının deksmedetomidinin geç başlayan
etkisinin bir delili olduğunu düşünüyoruz.
Anestezi indüksiyonundan 10 dakika önce deksmedetomidinin 0.5 μg.kg-1 dozda 1 dakika
içerisinde verilen tek bolus dozunun entübasyona bağlı hemodinamik cevapları zayıflattığı
gösterilmiştir(70).
0.6 μg.kg-1 tek bolus dozunun da 1 dakika içerisinde verildikten sonra kan basıncı ve kalp
hızında hafif bir düşmeye neden olduğu, laringoskopi ve entübasyona bağlı gelişen
hemodinamik cevapları azalttığı ancak tamamiyle de ortadan kaldırmadığı bildirilmiştir.
Deksmedetomidin verilmeden önce glikopirolat uygulanmış olması ile bradikardi oluşumu
engellenebilmektedir(71).
Lawrence ve ark.(72) yaptıkları bir çalışmada deksmedetomidini 2 μg.kg-1 dozda 5 dakika
içinde uygulamışlar, laringoskopi ve trakeal entübasyonun SAB’de bir değişikliğe yol
açmadığını, DAB’de ortalama 1 mmHg’lik ve KAH’de ise 13 atım.dak.-1 artışa yol açtığını
bulmuşlardır. Ayrıca deksmedetomidin uygulanan hastalarda plazma noradrenalin
düzeylerinin önemli ölçüde düştüğü gösterilmiştir. Deksmedetomidin uygulanan hastaların
(25 hasta), 5’inde tedavi gerektiren hipotansiyon ve 6’sında ise atropin gerektiren bradikardi
meydan gelmiş, geç dönemde postanestezik bakım odasında ise hastaların 14’ünde bradikardi
gelişmiştir.
57

SONUÇ
Sonuç olarak, anestezi indüksiyonu öncesinde 1 dakika içerisinde uygulanan 1μg.kg-1 dozda
remifentanilin LTE’ye bağlı hemodinamik cevapların önlenmesinde etkili olduğunu gördük.
1μg.kg-1 deksmedetomidinin 5 dakika içerisinde bolus olarak uygulanmasının LTE’ye bağlı
hemodinamik cevapların önlemede yetersiz olduğu ve bunun da uygulama süresine bağlı
olduğu kanaatine vardık.
58

ÖZET
Amaç: Bu çalışmanın amacı tek bolus doz remifentanil ile deksmedetomidinin laringoskopi
ve trakeal entübasyona bağlı olarak oluşan hemodinamik cevaplar üzerine olan etkilerini
karşılaştırmaktı.
Metod: Bu prospekktif çit-kör çalışmaya 60 ASA I-II hasta alındı. Hastalar rastlantısal olarak
3 gruba ayrılarak bir gruptaki hastalara 60 saniye içinde remifentanil 1 μg.kg-1 (Grup R), bir
gruptaki hastalara deksmedetomidine 1 μg.kg-1 5 dakika içinde (Grup D) ve bir gruptaki
hastalara da normal salin (kontrol) anestezi indüksiyonundan önce bolus olarak verildi.
Propofol 2 mg.kg-1 ve rokuronyum 0.6 mg.kg-1 ile anestezi indüksiyonu yapılarak 2 dakika
sonra hastalar entübe edildi. Arteriyal basınçlar ve kalp hızı non-invaziv olarak hasta
operasyon odasına alındığında (bazal), çalışma ilacı tamanlandıktan sonra, entübasyondan
hemen önce ve sonra, entübasyondan 1, 3 ve 5 dakika sonra ölçüldü.
Sonuçlar: Arteriyal basınçlar ve kalp hızı Grup R’de entübasyondan hemen ve 1 dakika sonra
diğer gruplara göre önemli ölçüde düşüktü (p < 0.01 and p < 0.001).
Tartışma: Remifentanilin 1 μg.kg-1 (60 saniye içinde) tek bolus dozu LTE’ye bağlı
hemodinamik cevapların kontrolünde etkilidir. Fakat deksmedetomidine 1 μg.kg-1 (5 dakika
içinde) ile arteriyel basınçlar ve kalp hızı yeterli şekilde kontrol edilemedi.
59

SUMMARY
Objectives: The aim of this study to compare the effecs of single bolus remifentanil and
dexmedetomidine on hemodynamic responses related to laryngoscopy and tracheal intubation.
Methods: In this prospective, double-blind study 60 ASA I-II patients scheduled for various
elective surgery were enrolled. Patients were randomly allocated into one of three groups to
receive either a bolus dose of remifentanil 1 μg.kg-1 over 60 seconds ( Group R), 1 μg.kg-1
deksmedetomidine over five minutes (Group D) or normal saline (control), given
intravenously before induction of anaesthesia. Anaesthesia was induced with 2 mg.kg-1
propofol and rocuronium 0.6 mg.kg-1 and the patients were intubated after two minutes.
Arterial pressures and heart rate were measured non-invasively at the patient was taken into
the operating room (basaline), after completion of study drugs, immediately before and after
intubation and 1, 3 and 5 minutes later intubation.
Results: Arterial pressures and heart rate were significantly low in the Group R compare to
other groups immediately after and 1 minute later intubation (p < 0.01 and p < 0.001).
Conclusions: Single bolus of remifentanil 1 μg.kg-1 (over 60 seconds) was effective to
control of hemodynamic changes related to LTI. But arterial pressures and heart rate were not
adequately controlled with dexmedetomidine 1 μg.kg-1 (over five minutes) .
60

KAYNAKLAR
1. King BD, Harris LC Jr, Greifenstein FE, Elder JD Jr, Dripps RD. Reflex circulatory responses to direct
laryngoscopy and tracheal intubation performed during general anesthesia. Anesthesiology. 1951 ; 12(5) :
556-66.
2. Prys-Roberts C, Greene LT, Meloche R, Foëx P. Studies of anaesthesia in relation to hypertension. II:
Hemodynamic consequences of induction and endotracheal intubation. 1971. Br J Anaesth. 1998 ; 80(1) :
106-22.
3. Derbyshire DR, Chmielewski A, Fell D, Vater M, Achola K, Smith G. Plasma catecholamine responses to
tracheal intubation. Br J Anaesth. 1983 Sep;55(9):855-60.
4. Shribman AJ, Smith G, Achola KJ. Cardiovascular and catecholamine responses to laryngoscopy with and
without tracheal intubation. Br J Anaesth 1987;59(3): 295-9.
5. Crawford DC, Fell D, Achola KJ, Smith G. Effects of alfentanil on the pressor and catecholamine responses
to tracheal intubation. Br J Anaesth. 1987 ; 59(6) : 707-12.
6. Ko SH, Kim DC, Han YJ, Song HS. Small-dose fentanyl: optimal time of injection for blunting the
circulatory responses to tracheal intubation. Anesth Analg. 1998 ; 86(3) : 658-61.
7. Durrani M, Barwise JA, Johnson RF, Kambam JR, Janicki PK. Intravenous chloroprocaine attenuates
hemodynamic changes associated with direct laryngoscopy and tracheal intubation. Anesth Analg. 2000 ;
90(5) : 1208-12.
8. Samaha T, Ravussin P, Claquin C, Ecoffey C. Prevention of increase of blood pressure and intracranial
pressure during endotracheal intubation in neurosurgery: esmolol versus lidocaine. Ann Fr Anesth Reanim.
1996;15(1):36-40.
9. Hung O. Understanding hemodynamic responses to tracheal intubation. Can J Anaesth. 2001 ; 48(8) : 723-6.
10. Hassan HG, el-Sharkawy TY, Renck H, Mansour G, Fouda A. Hemodynamic and catecholamine responses
to laryngoscopy with vs. without endotracheal intubation. Acta Anaesthesiol Scand. 1991 ; 35(5) : 442-7.
11. Takahashi S, Mizutani T, Miyabe M, Toyooka H. Hemodynamic responses to tracheal intubation with
laryngoscope versus lightwand intubating device (Trachlight) in adults with normal airway. Anesth Analg.
2002 Aug;95(2):480-4.
12. Kovac AL. Controlling the hemodynamic response to laryngoscopy and endotracheal intubation. J Clin
Anesth 1996;8(1):63-79.
13. Lawes EG, Downing JW, Duncan PW, Bland B, Lavies N, Gane GA. Fentanyl-droperidol supplementation
of rapid sequence induction in the presence of severe pregnancyinduced and pregnancy-aggravated
hypertension. Br J Anaesth 1987; 59: 1381-91.
14. Maguire AM, Kumar N, Parker JL, Rowbotham DJ, Thompson JP. Comparison of effects of remifentanil
and alfentanil on cardiovascular response to tracheal intubation in hypertensive patients. Br J Anaesth. 2001;
86(1) : 90-3.
61

15. Matot I, Sichel JY, Yofe V, Gozal Y. The effect of clonidine premedication on hemodynamic responses to
microlaryngoscopy and rigid bronchoscopy. Anesth Analg. 2000;91(4) : 828-33.
16. Thomson IR. The haemodynamic response to intubation: a perspective. Can J Anaesth 1989;36(4):367-9.
17. Adachi YU, Satomoto M, Higuchi H, Watanabe K. Fentanyl attenuates the hemodynamic response to
endotracheal intubation more than the response to laryngoscopy. Anesth Analg. 2002 ; 95(1) : 233-7.
18. Safavi M, Honarmand A. Attenuation of cardiovascular responses to laryngoscopy and tracheal intubation--
intravenous sufentanil vs pethidine. Middle East J Anesthesiol. 2008;19(6):1349-59.
19. Menigaux C, Guignard B, Adam F, Sessler DI, Joly V, Chauvin M. Esmolol prevents movement and
attenuates the BIS response to orotracheal intubation. Br J Anaesth. 2002;89(6):857-62.
20. Firoozbakhsh F, Mohammadi FH, Safari S, Khashayar P. The effect of intravenous nitroglycerine on blood
pressure during intubation. Middle East J Anesthesiol. 2008;19(4):859-67.
21. Mikawa K, Nishina K, Maekawa N, Obara H. Comparison of nicardipine, diltiazem and verapamil for
controlling the cardiovascular responses to tracheal intubation. Br J Anaesth. 1996 ; 76(2) : 221-6.
22. Puri GD, Marudhachalam KS, Chari P, Suri RK. The effect of magnesium sulphate on hemodynamics and its
efficacy in attenuating the response to endotracheal intubation in patients with coronary artery disease.
Anesth Analg. 1998 ; 87(4) : 808-11.
23. Wilhelm W, Kreuer S. The place for short-acting opioids: special emphasis on remifentanil. Crit Care.
2008;12 Suppl 3:S5. Review.
24. O'Hare R, McAtamney D, Mirakhur RK, Hughes D, Carabine U. Bolus dose remifentanil for control of
haemodynamic response to tracheal intubation during rapid sequence induction of anaesthesia. Br J Anaesth.
1999 ; 82(2) : 283-5.
25. Gertler R, Brown HC, Mitchell DH, Silvius EN. Dexmedetomidine: a novel sedative-analgesic agent. Proc
(Bayl Univ Med Cent). 2001 ; 14(1) : 13-21.
26. Carollo DS, Nossaman BD, Ramadhyani U. Dexmedetomidine: a review of clinical applications. Curr Opin
Anaesthesiol. 2008 ; 21(4) : 457-61.
27. Yildiz M, Tavlan A, Tuncer S, Reisli R, Yosunkaya A, Otelcioglu S. Effect of dexmedetomidine on
haemodynamic responses to laryngoscopy and intubation : perioperative haemodynamics and anaesthetic
requirements. Drugs R D. 2006;7(1):43-52.
28. Endotracheal anesthesia: I. Basic considerations. In VJ Collins, ed. Principles of Anesthesiology, general and
regional anesthesia. 3rd ed. Philadelphia: Lea & Febiger; 1993, 460-517.
29. Orlando R. Hung, Ian Morris Dynamic anatomy of upper airway: an essential pradigm Can J Anesth 2000;
47(4): 295–298.
30. Airway management. In: Morgan GE, Mikhail MS, Murray MJ, editors. Clinical Anesthesiology 4th ed.
International Edition: Lange Medical Books; 2006,91-116.
31. Matsumoto T, de Carvalho WB. Tracheal intubation. J Pediatr (Rio J). 2007 ; 83(2 Suppl): S83-90.
62

32. The anatomy and physiology of the respiratory system. In: Jardins TD, ed. Cardiopulmonary Anatomy and
Ptysiology: essentials for respiratory care 4th ed. Albany: Delmar/Thomson Learning; 2002, 1-62.
33. The Respiratory System. In: Scanlon VC, Sanders T, editors. Essentisals of Anatomy and Physiology 5th
ed. Philadelphia: F.A. Davis Company; 2007, 341-366.
34. Gal TJ. Airway management. In: Miller RD, ed. Miller’s Anesthesia 6th ed. Philadelphia: Elsevier Churchhill
Livingstone; 2005; 1617-1652.
35. Picard J. Anatomy. In: Calder I, Pearce A, editors. Core Topics In Airway Management 1st ed. New York:
Cambridge University Press;2005, 1-9.
36. Rosenblatt WH. Airway management. In: Barash PG, Cullen BF, Stoelting RK, editors. Clinical Anesthesia
4th ed. Philadelphia: Lippincott Williams & Wilkins; 2001; 595-638.
37. Endotrakeal entübasyon. İçinde: Kayhan Z, editor. Klinik Anestezi 3. baskı. İstanbul: Logos Yayıncılık;
2004;243-273.
38. Rosenblatt WH. Airway management. In: Barash PG, Cullen BF, Stoelting RK, editors. Clinical Anesthesia
4th ed. Philadelphia: Lippincott Williams & Wilkins; 2001; 595-638.
39. Takahashi S, Mizutani T, Miyabe M, Toyooka H. Hemodynamic responses to tracheal intubation with
laryngoscope versus lightwand intubating device (Trachlight) in adults with normal airway. Anesth Analg.
2002 Aug;95(2):480-4.
40. Hassan HG, el-Sharkawy TY, Renck H, Mansour G, Fouda A. Hemodynamic and catecholamine responses
to laryngoscopy with vs. without endotracheal intubation. Acta Anaesthesiol Scand. 1991 Jul;35(5):442-7.
41. Onaran O, Kayaalp SO. Reseptörler ve ilaç-reseptör ilişkisi. İçinde: Kayaalp SO, editor. Rasyonel Tedavi
Yönünden Tıbbi Famakoloji 11. baskı. Ankara: Hacettepe-Taş Kitapçılık Ltd Şti ; 2005; 78-85.
42. Youngs EJ, Shafer SL. Basic pharmacokinetic and pharmacodynamic principles. In:White PF, editor.
Textbook of Intravenous Anesthesia 1st ed. Baltimore: Williams&Wilkins; 1997;10-26.
43. Hudson RJ, Henthorn TK. Basic principles of pharmacology. In: Barash PG, Cullen BF, Stoelting RK,
editors. Clinical Anesthesia 4th ed. Philadelphia: Lippincott Williams & Wilkins; 2001; 247-274.
44. Bovill JG. Mechanisms of intravenous anesthesia. In:White PF, editor. Textbook of Intravenous Anesthesia
1st ed. Baltimore: Williams&Wilkins; 1997;26-46.
45. Lawson NW, Johnson JO. Autonomic nervous system: Physiology and pharmacology. In: Barash PG, Cullen
BF, Stoelting RK, editors. Clinical Anesthesia 4th ed. Philadelphia: Lippincott Williams & Wilkins; 2001;
275-333.
46. Reves JG, Glass PSA, Lubarsky DA, McEvoy MD. Intravenous nonopioid anesthetics. In: Miller RD, ed.
Miller’s Anesthesia 6th ed. Philadelphia: Elsevier Churchhill Livingstone; 2005; 317-378.
47. Gertler R, Brown HC, Mitchell DH, Silvius EN. Dexmedetomidine: a novel sedative-analgesic agent. BUMC
proceedings 2001;14:13–21.
63

48. Carollo DS, Nossaman BD, Ramadhyani U. Dexmedetomidine: a review of clinical applications. Cur
Opinion Anest 2008;21:457-461.
49. Bhana N, Goa KL, McClellan KJ. Dexmedetomidine. Drugs 2000;59:263–268.
50. Coda BA. Opioids. In: Barash PG, Cullen BF, Stoelting RK, editors. Clinical Anesthesia 4th ed.
Philadelphia: Lippincott Williams & Wilkins; 2001;353-383.
51. Egan TD. Remifentanil pharmacokinetics and pharmacodynamics. A preliminary appraisal. Clin
Pharmacokinet. 1995 Aug;29(2):80-94.
52. Wilhelm W, Kreuer S. The place for short-acting opioids: special emphasis on remifentanil. Critical Care
2008, 12(Suppl 3):S5.
53. Glass PS, Gan TJ, Howell S. A review of the pharmacokinetics and pharmacodynamics of remifentanil.
Anesth Analg. 1999 Oct;89(4 Suppl):S7-14. Review.
54. Russell WJ, Morris RG, Frewin DB, Drew SE. Changes in plasma catecholamine concentrations during
endotracheal intubation. Br J Anaesth. 1981 Aug;53(8):837-9.
55. Miller DR, Martineau RJ, O'Brien H, Hull KA, Oliveras L, Hindmarsh T, Greenway D. Effects of alfentanil
on the hemodynamic and catecholamine response to tracheal intubation. Anesth Analg. 1993
May;76(5):1040-6.
56. Harris CE, Murray AM, Anderson JM, Grounds RM, Morgan M. Effects of thiopentone, etomidate and
propofol on the haemodynamic response to tracheal intubation. Anaesthesia. 1988;43 Suppl:32-6.
57. Ebert TJ, Muzi M, Berens R, Goff D, Kampine JP. Sympathetic responses to induction of anesthesia in
humans with propofol or etomidate. Anesthesiology 1992; 76: 725-733.
58. Kim JT, Shim JK, Kim SH, Ryu HG, Yoon SZ, Jeon YS, Bahk JH, Kim CS. Remifentanil vs. lignocaine for
attenuating the haemodynamic response during rapid sequence induction using propofol: double-blind
randomised clinical trial. Anaesth Intensive Care. 2007;35(1):20-3.
59. Claeys MA, Gepts E, Camu F. Haemodynamic changes during anaesthesia induced and maintained with
propofol. Br J Anaesth. 1988 Jan;60(1):3-9.
60. Sellgren J, Ejnell H, Elam M, Pontén J, Wallin BG. Sympathetic muscle nerve activity, peripheral blood
flows, and baroreceptor reflexes in humans during propofol anesthesia and surgery. Anesthesiology. 1994
;80(3):534-44.
61. Thompson JP, Hall AP, Russell J, Cagney B, Rowbotham DJ. Effect of remifentanil on the haemodynamic
response to orotracheal intubation. Br J Anaesth. 1998;80(4):467-9.
62. Schüttler J, Albrecht S, Breivik H et al. A comparison of remifentanil and alfentanil in patients undergoing
major abdominal surgery. Anaesthesia 1997; 52:307-317.
63. Hall AP, Thompson JP, Leslie NAP, Fox AJ, Kumar N, Rowbotham DJ. Comparison of different doses of
remifentanil on the cardiovascular response to laryngoscopy and tracheal intubation. B J Anaesth. 2000;
84(1): 100-2.
64

65
64. Kweon TD, Nam SB, Chang CH, Kim MS, Lee JS, Shin CS, June DB. The effect of bolus administration of
remifentanil on QTc interval during induction of sevoflurane anaesthesia. Anaesthesia 2008; 63: 347-351.
65. Choi BI, Choi SH, Shin YS, Lee SJ, Yoon KB, Shin SK, Lee KY. Remifentanil prevents withdrawal
movements caused by intravenous injection of rocuronium. Yonsei M J. 2008;49(2): 211-216.
66. Stevens JB, Wheatley L. Tracheal intubation in ambulatory surgery patients: using remifentanil and propofol
without muscle relaxants. Anesth Analg. 1998 Jan;86(1):45-9.
67. Song D, Whitten CW, White PF. Use of remifentanil during anesthetic induction: a comparison with fentanyl
in the ambulatory setting. Anesth Analg. 1999 Apr;88(4):734-6.
68. Ozkose Z, Demir FS, Pampal K, Yardim S. Hemodynamic and anesthetic advantages of dexmedetomidine,
an α2-agonist, for surgery in prone position. Tohoku J Exp Med. 2006; 210: 153-60.
69. Bloor BC, Ward DS, Belleville JP, Maze M. Effects of intravenous dexmedetomidine in humans. II.
Hemodynamic changes. Anesthesiology. 1992 Dec;77(6):1134-42.
70. Basar H, Akpinar S, Doganci N, Buyukkocak U, Kaymak C, Sert O, Apan A. The effects of preanesthetic,
single-dose dexmedetomidine on induction, hemodynamic, and cardiovascular parameters. J Clin Anesth.
2008 Sep;20(6):431-6.
71. Scheinin B, Lindgren L, Randell T, Scheinin H, Scheinin M. Dexmedetomidine attenuates sympathoadrenal
responses to tracheal intubation and reduces the need for thiopentone and peroperative fentanyl. Br J
Anaesth. 1992 Feb;68(2):126-31.
72. Lawrence CJ, De Lange S. Effects of a single pre-operative dexmedetomidine dose on isoflurane
requirements and peri-operative haemodynamic stability. Anaesthesia. 1997 Aug;52(8):736-44.