Geeni- ja soluhoidot silmän takaosan sairauksien hoidossa
-
Upload
lauri-elsil -
Category
Documents
-
view
360 -
download
9
Transcript of Geeni- ja soluhoidot silmän takaosan sairauksien hoidossa

GEENI- JA SOLUHOIDOT SILMÄN TAKAOSAN SAIRAUKSIEN HOIDOSSA
Lauri Elsilä Helsingin yliopisto Farmasian tiedekunta Farmaseuttisten biotieteiden osasto Biofarmasia
Huhtikuu 2014

2
SISÄLLYS 1 JOHDANTO .................................................................................................................. 1
2 SILMÄN TAKAOSAN RAKENNE JA FARMAKOKINETIIKKAA ........................ 2
3 GEENIHOIDOT ............................................................................................................ 4
3.1. Yleistä geeniterapioista .......................................................................................... 4
3.1.1. Vektorit ........................................................................................................... 4
3.1.2. Geneettisen materiaalin muodot ..................................................................... 7
3.2. Silmän geenihoidot ................................................................................................ 8
3.2.1. Geenikorvaushoito .......................................................................................... 8
3.2.2. Neuroprotektiivinen vaikutus ....................................................................... 11
3.2.3. Optogeneettinen hoito ................................................................................... 12
4 SOLUHOIDOT ............................................................................................................ 14
4.1. Yleistä kantasoluhoidoista ................................................................................... 15
4.1.1. Hoidoissa käytettäviä kantasolutyyppejä ...................................................... 15
4.1.2. Solujen annostelusta ..................................................................................... 16
4.2. Kantasoluterapiat verkkokalvon sairauksissa ...................................................... 17
5 POHDINTA ................................................................................................................. 18
6 YHTEENVETO ........................................................................................................... 21
KIRJALLISUUSLUETTELO ........................................................................................ 22

1
1 JOHDANTO
Silmän takaosassa, erityisesti verkkokalvossa, mutta myös suonikalvossa, esiintyvät
sairaudet aiheuttavat usein selvää näön huononemista tai kokonaan näkökyvyn
menettämisen ja ovatkin yleisimpien sokeutta aiheuttavien sairauksien joukossa (Zhang
ym. 2012). Näiden sairauksien joukossa on muun muassa diabeettinen retinopatia,
silmänpohjan rappeuma, verkkokalvon rappeuma sekä glaukooma. Ihmisen tärkeimmän
aistin, näkökyvyn menettäminen ei ole ainoastaan subjektiivisesti pelätty ongelma, vaan
aiheuttaa esimerkiksi Yhdysvalloissa kymmenien miljardien dollarien edestä
terveydenhuoltomenoja (Rein ym. 2006; Zhang ym. 2012).
Ongelmalliseksi silmän takaosan sairauksien hoidon tekee alueen vaikea saavutettavuus
(Urtti 2006; del Amo ja Urtti 2008; Zhang ym. 2012). Silmän rakenteessa ja
fysiologiassa on useita esteitä, jotka vaikeuttavat lääkeaineen kulkeutumista hoitoa
vaativaan kudokseen. Systeemisesti annostelluissa lääkkeissä vaadittava lääkeainemäärä
on hyvin korkea altistaen lääkkeen haittavaikutuksille eikä silmän pinnalle annosteltu
lääke saavuta juuri koskaan silmän posteriorista osaa. Ongelma on pyritty ratkaisemaan
erilaisilla annostelumetodeilla, kuten lasiaisinjektiolla, mutta invansiiviset hoidot
sisältävät omat riskinsä eivätkä ole hoitomyöntyvyyden näkökulmasta paras vaihtoehto.
Pyrkimys pitkävaikutteisiin lääkemuotoihin on siksi nykypäivän
silmälääketutkimuksessa vallitseva suunta ja erilaiset geeni- ja kantasoluhoidot ovat
lupaavia tekniikoita, minkä lisäksi hoitojen on lisäksi teoreettisesti mahdollista olla
parantavia, mikä lisää entisestään kiinnostusta uusia hoitomuotoja kohtaan (del Amo ja
Urtti 2008; Zhang ym. 2012).
Seuraavassa esitellään sekä geeni- että kantasoluterapioita niiden perusajatuksien ja jo
tutkittujen sovellutusten kautta sekä pohditaan jo havaittuja ongelmia tutkimuksessa
sekä vaikutusta nykyiseen tutkimukseen ja tulevaan farmaseuttiseen työhön.

2
2 SILMÄN TAKAOSAN RAKENNE JA FARMAKOKINETIIKKAA
Silmän lääkinnän periaatteiden ymmärtämiseksi on ymmärrettävä silmän rakennetta ja
toimintaa, erityisesti vierasaineiden kuljetusmekanismeja. Seuraavaksi esitellään
lyhyesti silmän takaosan rakennetta ja silmän takaosan lääkehoidon kannalta oleellista
farmakokinetiikkaa.
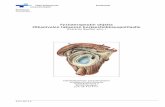
Kuva 1. Kaavakuva silmän takaosasta sekä retinan soluista ja rakenteesta. Sulkeisiin on
merkitty kyseisiin rakenteisiin vaikuttavia sairauksia.

3
Silmän posteriorinen osa eli takaosa vastaa silmään tulevan valon muuttamisesta
hermoimpulssiksi ja tämän informaation siirtämisestä aivoihin. Silmän takaosassa
sijaitsee verkkokalvo eli retina, joka koostuu valon tulosuunnasta katsottuna proteiinien
muodostamasta sisemmästä rajoittavasta kerroksesta, gangliosoluista ja niiden
näköhermoon kulkevista aksoneista, kaksisuuntaisia poikittaisyhteyksiä muodostavista
amakriinisoluista, valoreseptorisoulilta signaalia kuljettavista bipolaarisoluista,
horisontaalisoluista, valoherkistä tappi- ja sauvasoluista sekä pigmenttiepiteelistä
(Dowling 1970). Rakenne on havainnollistettu kuvassa 1. Verkkokalvon alla on
suonikalvo, joka vastaa retinan verenkierrosta. Ainoastaan pigmenttisolut on yhteydessä
verenkiertoon, joten epiteelikudos vastaa muiden retinan solujen aineenvaihdunnasta
transsytoosilla.
Veri-aivoesteen tavoin silmän ja verenkierron välissä on kudoksen muodostamia esteitä:
silmän etuosassa veri-vesieste sekä takaosan veri-retinaeste (Urtti 2006). Ensin mainittu
muodostuu suonikalvon epiteelisoluista ja estää pääasiassa plasman albumiinin
siirtymisen kammionesteeseen, mutta toimii esteenä myös hydrofiilisille
lääkemolekyyleille. Veri-retinaesteen muodostavat yhdessä verkkokalvon
pigmenttiepiteelin (retinal pigment epithelium, RPE) solut sekä retinan kapillaarien
tiiviit seinämät. Veri-retinaesteen soluissa on havaittu olevan aktiivista
kuljetustoimintaa, joka poistaa potentiaalisesti haitallisia aineita lasiaisesta ja retinan
solun ulkoisesta nesteestä (Cunha-Vaz 2003). RPE-solut kuljettavat muun muassa
ioneja ja glukoosia veren ja retinan solujen välillä ja muuttavat sauva- ja tappisolujen
valoa absorboineen retinaalin all-trans-tilasta valoaktiiviseen 11-cis-muotoon ollen näin
tärkeässä osassa valoreseptorisolujen aistitoiminnoissa (Strauss 2005). RPE-solut myös
fagosytoivat valoreseptorisolujen uloimpia osia ja kierrättävät näiden osien tärkeät
aineet, kuten retinaalin, uusiokäyttöön sekä erittävät immunosuppressiivisia aineita,
millä voi molemmilla olla vaikutuksia lääkehoitoihin silmän takaosassa.
Lasiaisen ja retinan välillä on myös immunosytokemiallisesti havaittava,
proteiinimatriiseista muodostuva tyvikalvo, jota kutsutaan sisemmäksi rajoittavaksi
kalvoksi (Inner limiting membrane, ILM) (Halfter ym. 2008). Kalvo ei vaikuta
pienimolekyylisten lääkeaineiden kulkeutumiseen, mutta estää suurempien

4
molekyylien, kuten proteiinien ja virusten, siirtymistä lasiaisesta verkkokalvoon, mikä
voi vaikuttaa esimerkiksi biologisten lääkehoitojen onnistumiseen (Dalkara ym. 2009).
3 GEENIHOIDOT
Geenihoito terminä sisältää joukon hyvin erilaisia tekniikoita, joita yhdistää
perintömateriaalin käyttö ja sen siirtäminen. Seuraavassa esitellään geenitekniikoiden ja
-terapioiden pääpiirteitä siirroissa käytettävistä kuljettimista geneettisen materiaalin
muotoihin ja myöhemmin geenihoitoja esimerkkitutkimusten kautta.
3.1. Yleistä geeniterapioista
3.1.1. Vektorit
Virukset ovat yleisimmin käytetty geenimateriaalin kuljetusmekanismi eli vektori
kliinisten kokeiden tasolla olevissa geenihoitotutkimuksissa (Walther ja Stein 2000).
Virusvektorin perimmäinen ajatus on hyödyntää viruksille ominaista infektioreittiä
aiheuttamatta kuitenkaan virusinfektiota itsessään (Thomas ym. 2003). Vektorina
käytettävistä viruksista poistetaan kaikki tai lähes kaikki viruksen oma perimäaines ja
korvataan se halutulla, siirrettävällä geenillä. Jäljelle jätetään yleensä koodaamattomat,
virusten kapseloitumista ohjaavat osat virusgenomin päissä. Mikäli kaikki viruksen
geneettinen materiaali joudutaan poistamaan, lisätään usein kapseloitumista ja
kopioitumista ohjaavat osuudet siirrettävän geenin lisäksi virukseen erillisenä
plasmidina. Virus siirretään valmistuksessa bioreaktorina toimivalle solualustalle
monistumaan. Näin tuotetaan rekombinanttiviruksia, jotka ovat puhdistamisen jälkeen
valmiita geeninsiirtokäyttöön (Kuva 2).
Virusvektorien suurimpia etuja on niiden kyky transfektoida kohdesoluja, eli siirtää
sisältämänsä trangeeninen materiaali kohdesolujen genomiin, hyvin tehokkaasti (Patil
ym. 2005). Laajempaa käyttöä estää kuitenkin virusten toksisuusriski, jota havaitaan
edelleen useissa eläinmalleissa. Ongelma on havaittu myös kliinisissä kokeissa

5
adenovirusvektorin aikaansaaman tulehdusreaktion aiheutettua potilaan kuoleman
vuonna 1999 (NIH 2002). Virukset ovat myös rajallisen kokoisia, mistä aiheutuu niiden
rajoitettu kyky kantaa siirrettävää geneettistä materiaalia (Taulukko 1) (Patil ym. 2005)
Vektoreina käytetään useita erilaisia viruksia. Eri virusvektoreita ja niiden
ominaisuuksia on tarkasteltu tarkemmin taulukossa 1. Silmän geenihoidoissa
yleisimmin käytettyjä vektoreita ovat lentivirukset, adenovirukset sekä parvoviruksiin
kuuluva AAV (adeno-associated virus), joista viimeisin on yleisesti geenitutkimuksessa
suurta mielenkiintoa herättävä useiden hyvien ominaisuuksiensa ja vähäisen
patogeenisyytensä vuoksi (Colella ja Auricchio 2012).
Taulukko 1. Erilaisten virusvektoreiden hyötyjä ja haittoja. Taulukossa mainitulla kantokyvyllä tarkoitetaan paljonko geenimateriaalia vektorin sisälle mahtuu (kb, kilo-base pair, 1000 emäsparia). AAV = adeno-associated virus (Walther ja Stein 2000). Vektori Edut Haasteet
Retrovirus Suurehko kantokyky (7–8 kb), helppo muokattavuus
Vaikea kohdentaa, epävakaa, satunnainen genomi-integraatio kohdesolussa
Lentivirus Laaja transfektiokyky, vakaa geeniekspressio, hyvä kantokyky (10 kb)
Geneettisen materiaalin pakkaaminen vaikeaa, mutageeninen
Adenovirus Korkea ekspression taso, melko suuri kantokyky (7–8 kb)
Aiheuttaa herkästi immuunivasteita, geeniekspressio ohimenevää, ei integroidu kohdesolun genomiin
AAV
Laaja transfektiokyky, ohjattavuus, ei patogeeninen, hyvin vähän immuunivasteita
Pieni kantokyky (4 kb), vaikea tuottaa
Herpesvirus
Korkea kantokyky (50 kb), transfektoi laajasti erilaisia solutyyppejä, luonnollinen tarttumisominaisuus hermosoluihin
Toksisuusriski korkea, ei integroitumista kohdesolun DNA:han

6
Virusvektoreiden ongelmia on pyritty kiertämään valmistamalla kemiallisesti ei-
viraalisia vektoreita (Abdallah ym. 1995). Lähtökohtana on ollut välttää patogeenisyys
ja virusten kapsidista johtuva rajallinen kantokyky samalla säilyttäen virusten
ohjautuvuus haluttuun kohdekudokseen ja geeninsiirtokyky. Yleisimmin käytetyt
kemialliset vektorit voidaan jakaa kahteen pääryhmään: polymeerirakenteisiin ja
liposomaalisiin vektoreihin (Patil ym. 2005).
Lipidipohjaiset vektorit rakennetaan usein kationisista lipideistä, jolloin negatiivinen
DNA muodostaa lipidien kanssa yhtenäisen kompleksin, niin sanotun lipopleksin (Li ja
Huang 2000; Patil ym. 2005). DNA voidaan myös sijoittaa liposomin ytimeen.
Kationisten liposomien on kuitenkin useammissakin kokeissa havaittu oleva
sytotoksisia ja aiheuttavan kudostoksisia reaktioita, mikä vähentää terapeuttisia
mahdollisuuksia (Lappalainen ym. 1994; Filion ja Phillips 1997; Dokka ym. 2000).
Kationisten liposomien transfektiokyky on myös virusvektoreihin verrattuna hyvin
heikko ja niiden kulkeutuminen haluttuihin retinan soluihin estyy usein, mikä tekee
liposomivektoreista toistaiseksi tehottomia geeninsiirrossa (Pitkänen ym. 2003; Patil
ym. 2005). Korvaavaksi tekniikaksi on kaavailtu anionisia liposomeja, joiden kohdalla
kationisten vastineiden kaltaista toksisuutta ei ole havaittu (Dokka ym. 2000).
Negatiivisesti varautuneen DNA:n ja negatiivisten lipidien yhteenliittämisessä on
kuitenkin havaittu vaikeuksia. Voimakkaasti transfektoivasta ja toksisesta näkökulmasta
turvallisesta anionisesta lipopleksista on raportoitu tutkimuksissa, mikä takaa
mielenkiintoa jatkotutkimuksiin lipidi-DNA-interaktion haasteista huolimatta (Patil ym.
2004).
Polymeerivektorien perusidea on hyvin samankaltainen kuin liposomeissa: kationisen
polymeerirungon ja negatiivisen DNA:n elektrostaattisen vuorovaikutuksen kautta
muodostuu kompleksi, polymeerien tapauksessa polypleksi (Patil ym. 2005).
Polypleksin positiivinen varaus auttaa myös soluunotossa negatiivisesti varautuneella
solun pinnalla. Polymeerivalinnalla voidaan vaikuttaa monipuolisesti polypleksin
fysikokemiallisiin ominaisuuksiin, ja siten DNA:n sitoutumiseen ja soluunottoon. Myös
polymeereihin kiinnitettävillä sokeriosilla ja vasta-aineilla voidaan vaikuttaa
polypleksin kohdentamiseen haluttuun kudokseen. Liposomien tavoin heikko

7
transfektiokyky sekä haasteet laadunvarmistuksessa, kuten tasakokoisten partikkelien
syntetisoimisessa, ja kulkeutumisessa ovat toistaiseksi esteitä polymeerivektorien
tehokkaalle käytölle geenisiirtovektoreina. (Pitkänen ym. 2003; Patil ym. 2005)
Myös pelkän suolaliuokseen sekoitetun DNA:n annostelua geenisiirtomenetelmänä on
tutkittu ja se on havaittu toimivaksi erityisesti lihaskudoksissa (Abdallah ym. 1995).
Tutkimuksissa on havaittu paljaan DNA:n transfektoivan myös hermokudosta ja
plasmidina silmään injisoituna toimivan uveiitin hoidossa (Schwartz ym 1996; Lee ym.
2009).
3.1.2. Geneettisen materiaalin muodot
Siirrettävä geenimateriaali on usein vektorin sisällä plasmidina, joka on tiettyä
proteiinia koodaava kaksijaosteinen DNA-molekyyli (Patil ym. 2005). Plasmidi siirtyy
solun sisällä endosomista tumaan, jossa se solun transkriptio- ja translaatiomekanismeja
hyväksikäyttäen saa aikaan transgeenisen proteiinin tuotannon. Juuri tumaan
siirtyminen on plasmidien kannalta hoidollisesti haastavin osa, sillä tumaan siirtymätön
plasmidi ei saa aikaan minkäänlaista vastetta solussa (Brunner ym. 2000). Plasimidien
avulla voidaan korjata mutaation vaurioittamia tai korvata kokonaan puuttuvia geenejä
sekä saada solu valmistamaan haluttua proteiinia (Patil ym. 2005).
Oligonukleotidit ovat lyhyitä, yksijuosteisia DNA-jaksoja, jotka solun sisällä
muodostavat mRNA:n kanssa dupleksin estäen proteiinin biosynteesin (Patil ym. 2005).
Oligonukleotidit voivat myös siirtyä solun tumaan ja muodostaa vastaavan DNA-
juosteen kanssa tripleksirakenteen estäen näin jo mRNA:n muodostumisen, jolloin
hiljennettäviä kohteita on jokaisessa solussa vähemmän. Muokkaamalla
oligonukleotidin pituutta, emäsjärjestystä ja konformaatiota voidaan toiminta kohdentaa
hyvinkin tarkasti haluttuun geeniin.
Samankaltaisella toimintaperiaatteella käytetään siRNA:ta (small interfering RNA),
kaksijuosteista RNA-ketjua, joka sitoutumalla RISC-kompleksin (RNA Induced
Silencing Complex) kanssa pilkkoo kohde-RNA:n pieniksi palasiksi estäen translaation

8
(Kaiser ym. 2010). siRNA:n on myös havaittu estävän kromosomitasolla
proteiinisynteesiä metyloimalla DNA:ta, vaikuttamalla inertin heterokromatiinin
muodostumiseen tai suoraan DNA:n eliminaatiolla (Agrawal ym. 2003). Mielenkiintoa
jatkotutkimuksille on herättänyt siRNA:n toiminta solunesteessä tuman sijaan, mikä
vähentää vektorin kohdennusominaisuuksien tarvetta, sekä molekyylin pieni koko,
jolloin useamman siRNA:n pakkaamalla yhteen vektoriin voisi mahdollisesti hiljentää
useita geenejä samanaikaisesti (Patil ym. 2005). siRNA on myös spesifisempi kuin
oligonukleotidit eivätkä aiheuta immuunivastetta, mikä tekee tekniikasta suhteellisesti
turvallisen.
Muita käytettyjä menetelmiä ovat geenihiljentämiseen käytetty RNA-juosteinen
ribotsyymi, sekä sen biologisesti kestävämpi DNA-versio DNAtsyymi (Patil ym. 2005).
Silmälääkintään FDA:n markkinoillekin hyväksymä menetelmä on hiljentää jo
muodostuneiden proteiinien toimintaa lyhyillä nukleotidijuosteilla, aptameereilla (Patil
ym. 2005; FDA 2004). Kohdennus voidaan tehdä suoraan sairauden ilmentämiin
proteiineihin tai kyseisten proteiinien translaatiossa ja transkriptiossa mukana oleviin
entsyymeihin ja muihin proteiineihin.
3.2. Silmän geenihoidot
3.2.1. Geenikorvaushoito
Geenikorvaushoito on kliinisten kokeiden tasolla yleisin silmän sairauksiin kohdennettu
geenihoito (NIH 2014). Geenikorvaushoidot tulevat kyseeseen mutaatiosta
riippuvaisissa, usein perinnöllisissä sairauksissa (Boye ym. 2013; Sahel ja Roska 2013).
Mutaatiosta johtuva verkkokalvon solujen toimintahäiriö aikaansaa rappeumaan
johtavan tapahtumaketjun, johon pyritään puuttumaan palauttamalla mutatoitumattoman
geenin siirrolla solujen normaali toimintakyky.
Leberin synnynnäisessä amauroosissa on havaittu retinan pigmenttiepiteelisolujen
RPE65-geenin mutaatio (Redmond ym. 2005). RPE65 ekspressoituu nimensä

9
Kuva 2. Geenihoidon perusperiaate virusvektorilla. (1) Viruksesta poistetaan viruksen oma geneettinen materiaali ja se korvataan halutulla geenillä. (2) Viruksella transfektoidaan kasvatusalustan solut, jotka tuottavat uutta, rekombinanttivirusta. (3) Rekombinanttivirus siirretään elimistöön, jossa se siirtyy kohdesolun sisälle. (4) Vektoriin pakattu geeni siirtyy solun tumaan tai reagoi muuten proteiinisynteesiin osallistuvan mekanismin kanssa. Valmistuva proteiini voi toimia solukalvolla kalvoproteiinina (optogenetiikka, 5A), osallistua solun sisällä erilaisiin metabolia reaktiohin tai solun tukirankaan (geenikorvaushoito, 5B) tai solu voi erittää muodostuneen proteiinin, esimerkiksi kasvutekijän (neuroprotektio, 5C).
mukaisesti RPE-soluissa retinoidi-isomeraasientsyyminä, joka on mukana all-trans-
retinoidin palauttamisessa valoaktiiviseen 11-cis-muotoon (Moiseyev ym. 2005).
Mutaatio RPE65:ssä aiheuttaa entsyymin toimintavirheen, jonka seurauksena retinoidi
jää inerttiin all-trans-muotoonsa, valoreseptorisolut eivät aktivoidu valon kautta

10
normaalisti ja kertyvä trans-retinoidi johtaa retinan kudosrappeumaan (Redmond ym.
2005). Retinan toimintakyvyn palauttamista luonnollisen RPE56-geenin siirrolla on
tutkittu useilla eläinmalleilla ja tutkimuksissa on saatu hyvin lupaavia ja
pitkäaikaisiakin tuloksia (Boye ym. 2013). Acland ryhmineen (2001, 2005) siirsivät
Leberin amauroosin koiramalliin AAV-vektorilla rekombinantti-RPE65-geeniä
subretinaalitilaan injektoimalla ja saivat palautettua verkkokalvon valoaktiivisuutta 23
koeläimessä 26:sta. Toisessa kokeessaan he seurasivat samalla tavalla hoidettuja koiria
kolme vuotta ja havaitsivat 11-cis-retinoidia muodostuvan normaalia vastaavalla tavalla
koko seuranta-ajan, joskin ainoastaan alueella, johon vektoria oli injisoitu.
Lupaavien eläinkokeiden tulosten jälkeen RPE65-hoitoja on viety useisiin kliinisiin
kokeisiin, joista yhdessä faasi I kokeessa AAV-RPE65-hoidolla hoidettuja potilaita
seurattiin kolmen vuoden ajan (Jacobson ym. 2012). Tuloksissa havaittiin
eläinkokeissakin esiin tullut hoidon vaikutus ainoastaan injektioalueella. Seuranta-
aikana potilaiden sauva- ja tappisoluaktiivisuus parani eikä toksisuutta havaittu.
Kokeessa todettiin myös, ettei tarkan näkemisen alueelle foveaan annettu injektio
juurikaan parantanut alueen valoaktiivisuutta, mutta aiheutti usein fovean solujen
vaurioitumista. Tarkkaa näkökykyä ei siis ainakaan nykyisellä metodilla voida palauttaa
suoralla foveaan geenisiirrolla. Vuoden 2014 tammikuussa aloitettiin ensimmäinen
faasin III kliininen koe RPE65-hoidolla (NIH 2014, NCT00999609).
Usherin syndroomaksi kutsutaan joukkoa oireyhtymiä, jotka aiheuttavat kuuroutta ja
verkkokalvorappeuman myötä sokeutta (Boye ym. 2013). Oireyhtymä jaetaan kolmeen
alaluokkaan oireiden alkamisajankohdan ja vaikeuden mukaan ja näistä vaikeimpaan
muotoon, USH1:een, on tutkittu myös geeninsiirtohoitoja. Tutkimuksissa on havaittu
poikkeama aktiinipohjaista moottoriproteiinia koodittavassa geenissä myosinVIIa
(MYO7A), jonka ekpressoimat proteiinit toimivat retinan epiteelisoluissa ja
valoreseptorisoluissa solun sisäisessä kuljetuksessa ja solujen adheesiossa (Weil 1996,
Wolfrum 2003). Geeninsiirtohoidon konseptin todistaneissa hiirikokeissa havaittiin
hoidetun retinan RPE-solujen sijainnin kudoksessa ja opsiinin kuljetusmekanismien
vastaavan normaaleja fysiologisia malleja. Tulosten myötä käynnistettiin faasin 1
kliininen koe, jossa ajatuksena oli käyttää eläinkokeiden tapaan lentivirusvektoria

11
(Hashimoto ym. 2007; NIH 2014, NCT01505062). Yhdysvaltalaisen Oxford
BioMedican UshStat-valmisteellaan suorittamat kliiniset kokeet ovat kuitenkin edelleen
kesken eikä muille kokeille vielä toistaiseksi ole annettu lupia.
Kliinisissä kokeissa on useita silmän geeninsiirtohoitoja. Oxford BioMedicalla on
kehitteillä lentivirusvektoriin pohjautuva geenisiirtotekniikka resessiivisesti periytyvään
Stargardtin tautiin faasin I/II kokeissa Kongin ryhmineen (2008) toteutettua vastaava
hoito ensin onnistuneesti hiirillä. Hoitoja tutkitaan ja on tutkittu kliinisesti myös
silmänpohjan rappeumaan ja koroidermiaan (Boye ym. 2013)
3.2.2. Neuroprotektiivinen vaikutus
Geeninsiirrolla voidaan myös suojata vielä toimintakykyistä kudosta degeneraatiolta ja
näin ylläpitää olemassa olevaa näkökykyä (Sahel ja Roska 2013). Erilaisten
kasvutekijöiden kautta toteutettavaa tekniikkaa kutsutaan neuroprotektiiviseksi
vaikutukseksi. Tekniikan perusajatus on siirtää vektorin avulla haluttu kasvutekijägeeni
kohdesoluihin, jotka tämän jälkeen alkavat tuottaa ja erittää kyseistä proteiinia
ylläpitäen ympäröivää kudosta (Kuva 2). Yleisimmin silmäsairauksien hoitokäyttöön
tutkittuja kasvutekijöitä ovat CNF (ciliary neurotrophic factor), BDNF (brain derived
neurotrophic factor), FGF (fibroblast growth factor) ja GDNF (glial-cell derived
neurotrophic factor).
GDNF:n on todettu viivästyttävän retinan toimintakyvyn laskua ja edesauttavan
valoreseptorisolujen selviämistä eläinmallilla (Touchard ym. 2012). Kokeessa
verkkokalvorappeumaa mallintavan Royal College of Surgeons -rotan verkkokalvoon
siirrettiin elektroporaation avulla GDNF-plasmidi, mikä aikaansai GDNF:n tuotannon.
Tulokset olivat kahtiajakoisia: GDNF:n todettiin toisaalta hyvin selkeästi ylläpitävän
retinan soluja, mutta samalla havaittiin suurten GDNF-annosten nopeuttavan
rappeutumista, mikä herättää kysymyksen kasvutekijän toksisuudesta ja mahdollisesta
kapeasta terapeuttisesta leveydestä. Toisessa, GDNF:n pitkäaikaista turvallisuutta
tarkastelleessa tutkimuksessa ei transfektoiduissa koe-eläimissä havaittu retinan soluissa
morfologisia poikkeamia (Wu ym. 2005). Kokeessa vuoden ajan vapautuneen GDNF:n

12
taso pysyi kuitenkin tasaisena, mikä edelleenkin viittaa GDNF:n toksisuuteen
ainoastaan suurilla annoksilla. Tämä tuo haasteita GDNF:ää hyödyntävien
neuroprotektiivisten geenihoitojen suunnitteluun, sillä muiden kapean terapeuttisen
leveyden omaavien lääkehoitojen, kuten digoksiinin, annostusta voidaan pienentää,
mutta kertaalleen hermokasvutekijää ylimäärin tuottamaan transfektoitua kudosta on
vaikeampi saada pienentämään eritystään.
Koska oksidatiivisen stressin ja metaboliareittien häiriöiden on todettu olevan osa
retinan rappeumasairauksia, terveissä metaboliareiteissä mukana olevien
kasvutekijöiden ja proteiinien erittäminen sairaassa silmässä on mielenkiintoinen uusi
tutkimussuunta (Punzo ym. 2012). Sauvasoluista peräisin oleva kasvutekijä RdCVF
(rod-derived cone viability factor) on herättänyt suurta mielenkiintoa rappeutuvan
verkkokalvon toimintakyvyn ylläpidossa (Yang ym. 2009). Geeni, joka koodittaa
RdCVF:ää, ekspressoituu myös toisena proteiinina, entsyyminä, joka on mukana
valoreseptorisolujen metaboliassa ja oksidatiivisen stressin aiheuttamassa
solukuolemassa (Fridlich ym. 2009). Tutkimustulosten myötä on nähty potentiaalia
kehittää metaboliareitteihin kohdistuvia hoitoja silmän rappeumasairauksiin, joskin
tutkimus on vasta aluillaan.
3.2.3. Optogeneettinen hoito
Niin kutsuttu optogeneettinen hoito perustuu ajatukseen, jossa hyödynnetään
verkkokalvon ehjänä säilyneitä hermoverkkoja ja tuhoutuneiden valoreseptorisolujen
sijaan retinan muista soluista tehdään valoaktiivisia (Busskamp ym. 2011).
Geenitekniikan avulla retinan solut saadaan ilmentämään valoaktiivisia proteiineja,
kuten kanavarodopsiini-2:a (channelrhodopsin, ChR2) ja halorodopsiinia
(Natronobacterium pharaonis halorhodopsin, NpHR). Halorodopsiini on solukalvon
kloridipumppuproteiini, joka aktivoituu valon avulla ja aikaansaa solun
hyperpolarisaation (Schobert ja Lanyi 1982). ChR2 puolestaan toimii epäselektiivisenä
kationikanavana ja aktivoiduttuaan aikaansaa siis solun depolarisaation (Nagel ym.
2003). Hyperpolarisaation ja depolarisaation vaihteluihin perustuu myös terveen
verkkokalvon soluissa tapahtuva hermoimpulssin syntyminen: bipolaarisoluissa ja

13
amakriinisoluissa on valoreseptorin aktivaatiosta hyperpolarisoituvia OFF-mallisia
soluja ja depolarisoituvia ON-soluja (Kolb 1994; Busskamp ym. 2011).
Valoaktiivisten proteiinien ilmentäminen voidaan kohdentaa tiettyihin soluihin tai
vaihtoehtoisesti voidaan pyrkiä saamaan aikaan mahdollisimman laaja valoherkkä alue
vaurioituneeseen retinaan, jolloin siirrettävään geeniin sijoitetaan niin kutsuttuja
promoottorijaksoja (Sahel ja Roska 2013). Busskamp ryhmineen (2010) käyttivät AAV-
vektoria siirtämään NpHR-geeniä kahteen verkkokalvorappeuman (Retinitis
pigmentosa, RP) eläinmalliin käyttäen soluspesifisiä promoottoreita - ihmisen
rodopsiinia, ihmisen punaopsiinia ja hiiren tappisolujen arrestiini-3:a. Knock-out-hiiret
mallinsivat verkkokalvorappeumaa, jossa sauvasolut tuhoutuvat ja tappisolut jäävät
jäljelle menettäen kuitenkin ajan myötä valoherkkyyttään. Promoottoreilla pystyttiin
kohdistamaan haluttu geeniekspressio nimenomaisesti jäljellä oleviin tappisoluihin.
Eläinmalleissa havaittiin retinan toiminnan palautumista, aktiivisuutta aivojen
näköalueilla sekä käytösmuutoksia valoherkkyyskokeissa. Ryhmä totesi onnistuneen
transfektion myös ex vivo ihmissilmissä ja näkee potentiaalia verkkokalvorappeuman
hoidossa. Soluihin kohdennettaessa tulee kuitenkin tuntea hoitoa saavan potilaan retinan
solujen tila ja osata kohdentaa ilmennettävät proteiinit oikeanlaisiin soluihin, mikä tekee
kohdennetun hoidon kliinisestä sovelluksesta toistaiseksi hyvin haastavaa.
Ivanova ja hänen tutkimusryhmänsä (2010) puolestaan käyttivät kokeessaan
silkkiapinamallia. Tutkimuksessa apinoiden lasiaiseen injisoitiin serotyypin 2
rekombintantti AAV-vektorilla (rAAV2) ChR2-geeniä kahden yleispromoottorin,
CMV:n (human cytomegalovirus immediate-early gene promoter) ja CAG:n (hybridi
CMV/kanan B-aktiini promoottori), kanssa. Tuloksissa transfektoituneita soluja
havaittiin lähes jokaisessa osassa retinaa, mutta transfektio oli voimakkainta foveassa ja
silmän periferiassa - alueilla, joissa sisempi rajoittava kalvo on ohuimmillaan. Ryhmä
päätteli yleispromoottoreilla ja rAAV-vektorilla saavutettavan hyvä transfektio
valoaktiiviselle ChR2:lle, mutta havaitsi samalla sisemmän rajoittavan kalvon olevan
hyvin voimakas este rAAV-geenihoidolle.

14
Tilanteessa, jossa sekä tappi- että sauvasolut ovat tuhoutuneet, on todistetusti pystytty
palauttamaan valoaktiivisuutta transfektoimalla retinan soluja sekä ChR2:lla että
NpHR:llä (Zhang ym. 2009). Ryhmä injisoi kahden eri knock-out-hiiriryhmän
lasiaiseen rAAV2-vektorilla ChR2-NpHR-värileima-hybridigeeniä käyttäen
yleispromoottoreita. Kokeessa todettiin transfektoidun retinan soluissa muodostuvan
valoa projisoitaessa fysiologisesti normaalin kaltaisia ON-, OFF- ja ON-OFF-vasteita.
Vasteet kuitenkin vaihtelivat voimakkaasti valon aallonpituuden vaihdellessa. Ryhmä
totesi tekniikan olevan sopimaton sellaisenaan ilman erillisiä laitteita kliinisiin
sovelluksiin, koska käytettyjen proteiinien valoaktivaatiokynnys on huomattavasti
korkeampi verrattuna luonnollisiin valoreseptorisoluihin.
4 SOLUHOIDOT
Kantasoluhoidossa pääajatuksena on korvata ja korjata toimimattomia retinan soluja
(Ong ja da Cruz 2012). Erilaistumiskykyisiä kantasoluja siirretään vaurioituneelle
alueelle ja ne erikoistuvat halutuiksi soluiksi ympäristön kasvutekijöiden avustamana
muodostaen uutta, toimivaa kudosta vaurioituneen tilalle. Myös kantasoluista in vitro
muokattua, hoidettavan kudoksen kaltaista solumateriaalia voidaan siirtää sairaan
kudoksen tilalle. Korjausmekanismin lisäksi on olemassa mahdollisuus hyödyntää jo
aikaisemmin kuvattua neuroprotektiivista vaikutusta myös kantasolujen avulla.
Seuraavassa käsitellään lyhyesti retinan hoidossa käytettyjä kantasolu- ja
annosteluvaihtoehtoja ja myöhemmin erilaisia hoitomenetelmiä esimerkkitapauksien
avulla.

15
4.1. Yleistä kantasoluhoidoista
4.1.1. Hoidoissa käytettäviä kantasolutyyppejä
Hoidoissa ja niiden tutkimuksissa käytettäviä kantasoluja on pääasiassa kolmenlaisia:
embryonaaliset kantasolut, mesenkymaaliset kantasolut sekä indusoidut pluripotentit
kantasolut (Ong ja da Cruz 2012). Embryonaaliset eli alkion kantasolut (ESC,
embryonic stem cell), ovat blastokystivaiheessa olevan alkion sisemmästä solumassasta
eristettäviä, hyvin laajan erikoistumiskyvyn omaavia soluja. Blastokystivaihe
saavutetaan alkionkehityksessä viisi päivää hedelmöityksen jälkeen, mistä aiheutuu
embryonaalisten kantasolujen ympärillä käytävä eettinen keskustelu, johon liittyy usein
uskonnollisia lähtökohtia (Sandel 2004; Nisbet 2005). Ongelmalliseksi on myös
havaittu tietyksi solutyypiksi erikoistumiseen vaadittavien, hyvin spesifisten
kasvuympäristöjen tarve, ihmisestä eristettyjen embryonaalisten kantasolujen taipumus
aiheuttaa teratoomia ja muita kasvaimia sekä usein havaittava, immunosuppressiota
vaativa hylkimisreaktio (Brickman ja Burdon 2002; Hentze ym. 2006).
Embryonaalisten kantasolujen eettiset ongelmat sekä kasvainmuodostus pystytään
välttämään aikuisen luuytimestä ja keskushermostosta sekä napanuorasta ja silmän
sädelihaksen alueelta eristettävillä mesenkymaalisilla kantasoluilla (MSC, mesenchymal
stem cell) (Tropepe ym. 2000; Ong ja da Cruz 2012). Mesenkymaalisten kantasolujen
erikoistumiskyky ei ole yhtä laaja kuin embryonaalisilla kantasoluilla, mutta niiden
jakautumis- eli proliferaatiokyky on hyvä ja ratkaisevien kehitysaskeleiden ylittäneiden
mesenkymaalisten kantasolujen saattaa olla jopa helpompi erikoistua halutuiksi
kudoksiksi. Mesenkymaaliset kantasolut mahdollistavat myös solujen siirron potilaasta
itsestään, mikä vähentää hylkimisreaktioita ja näin ollen tarvetta immunosuppressiolle.
Kolmantena vaihtoehtona ovat indusoidut pluripotentit kantasolut (iPSC, induced
pluripotent stem cell) eli somaattisista soluista soluteknologisesti embryonaalisen
kantasolun kaltaisiksi muokatut solut (Ong ja da Cruz 2012). Indusoidut kantasolut ovat
erikoitumiskyvyltään embryonaalisten kantasolujen tavoin monipuolisia (Taulukko 2),

16
mutta haittapuolena on havaittu alkiokantasolujen kaltaista tuumorigeneesiä.
Ongelmaan on kuitenkin pystytty puuttumaan geeniteknologian avulla (Nakagawa ym.
2008).
Taulukko 2. Kantasolujen ominaisuuksia (Porkka 2004).
Nimeke Määritelmä
Totipotentti Pystyy muodostamaan koko yksilön. Pluripotentti Pystyy muodostamaan kaikkia kudoksia,
rajaton uusiutumiskyky. Multipotentti Voi tuottaa useita solutyyppejä ja uusiutua
koko yksilön eliniän. Progenitorisolu Voi tuottaa rajallisen määrän
solutyyppejä, rajallinen uusiutumiskyky.
4.1.2. Solujen annostelusta
Kantasolujen annostelussa helpoin tapa on soluista ja suolaliuoksesta muodostetun
suspension injisointi lasiaiseen (Ong ja da Cruz 2012). Sisempi rajoittava kalvo
aiheuttaa kuitenkin myös kantasoluannostelulle esteen lasiaisen ja retinan välillä ja vain
noin 1 % injisoiduista kantasoluista pääsee vapaasti verkkokalvolle asti, loput jäävät
bolukseksi lasiaiseen (Nishida ym. 2000; Ong ja da Cruz 2012). Kalvon hajoaminen
sairauden myötä tai kuoriminen annostelun yhteydessä parantaa solujen kulkeutumista
(Nishida ym. 2000; Johnson ym. 2010).
Kantasoluja voidaan myös siirtää kirurgisesti suoraan subretinaalitilaan (Ong ja da Cruz
2012). Invansiivinen toimenpide on kuitenkin huomattavasti injektiota haastavampi
toimenpide ja sisältää suurempia riskejä, kuten verkkokalvon vaurioituminen ja
tulehdusreaktiot, joista pyritään silmän takaosan sairauksien hoidoissa pääsemään
eroon. Hyvänä puolena tekniikassa on siirrettyjen kantasolujen saaminen lähelle retinaa,
jolloin solujen kulkeutuminen ja integraatio tapahtuvat lasiaisinjektiota helpommin.
Kolmantena vaihtoehtona on systeeminen annostelu esimerkiksi suonensisäisellä
injektiolla (Wang ym. 2010; Ong ja da Cruz 2012). Systeemisen annostelun hyvinä
puolina on pidetty mahdollisuutta hoitaa koko retinaa suppean injektio- tai

17
siirroskohdan sijaan sekä annostelun uusimisen helppous. Ongelmiksi muodostuvat
kuitenkin samat haasteet kuin retinan systeemilääkinnässä pienmolekyylisilläkin
lääkkeillä: silmän suonikalvoon kulkeutuva verimäärä on suhteessa hyvin pieni, jolloin
kohdekudokseen kulkeutuvien kantasolujen määrä on pieni, ja ympäri elimistöä
kulkevat kantasolut voivat integroitua muihin kudoksiin, mikä ei ole tavoiteltavaa.
4.2. Kantasoluterapiat verkkokalvon sairauksissa
Kantasoluhoidoilla on silmässä tähän asti ollut kolme pääkohdetta: retinan
pigmenttiepiteeli, valoreseptorisolut ja gangliosolut (Ong ja Cruz 2012). RPE-solut ovat
jatkuvana yksikerroksisena kudoksena helpohko korjattava kohde ja epiteelikudoksen
osallistuessa monipuolisesti verkkokalvon metaboliaan ja näkemiselle oleellisiin
prosesseihin sitä on pidetty tärkeänä tutkimus- ja hoitokohteena. Useammankin ryhmän
on onnistunut muodostaa ihmisen embryonaalisista kantasoluista aikuisen RPE-
kudoksen kaltaisia solukerroksia (Lund ym. 2006; Vugler ym. 2008; Subrizi ym 2012).
Solut ovat morfologisesti samanlaisia kuin terveet aikuisen RPE-solut, mutta myös
niiden toiminta, kuten valoreseptorifagosytoosi, vastaa normaalia fysiologista toimintaa.
Royal College of Surgeons -mallirotille on useissa tutkimuksissa siirretty
subretinaalitilaan ihmisperäisistä embryonaalisista kantasoluista muokattuja RPE-soluja
ja tuloksena eläinmallien näkökykyä pystyttiin palauttamaan, valoreseptorisoluja
pelastamaan eikä tuumorigeneesiä havaittu (Whitley ym. 1996; Sauvé ym. 2002; Lu
ym. 2009). Hoidoille on myös myönnetty lupia kliinisiin kokeisiin: Stargardtin taudin
hoitoa tutkivia faasin I/II kokeita on kaksi samoin kuin silmänpohjan rappeumaa
tutkivia faasin I/II tutkimuksia (NIH 2014; NCT01344993, NCT01674829,
NCT01469832, NCT01345006). Myös indusoiduista pluripotenteista kantasoluista on
saatu muodostettua toimivia RPE-soluja, mutta koe-eläimissä aiheutuneiden
immuunivasteiden vuoksi kliinisiä kokeita ei ole vielä aloitettu ihmisillä (Buchholz ym.
2009; Carr ym. 2009).
Myös valoreseptorisolun korvaaminen on teoreettisesti helppo toimenpide, sillä
kyseessä on yksisuuntainen reseptorisolu, jossa on vain yksi, hyvin lyhyt synaptinen
yhteys (Ong ja da Cruz 2012). Keskushermostosta eristettyjä neuraalisia

18
progenitorisoluja on siirretty onnistuneesti eläinmalleille, mutta havaitusta integraatiosta
huolimatta erilaistumista verkkokalvon soluiksi ei tapahtunut, minkä uskotaan johtuvan
aikuisen silmän epäedullisesta kasvuympäristöstä (Young ym. 2000; Van Hoffelen ym.
2003; MacLaren ym. 2006). MacLarenin onnistui kuitenkin ryhmineen (2006)
muodostaa toimivia sauvasoluja silmästä eristetyistä valoreseptorien progenitorisoluista.
Vastaavanlaisia progenitorisoluja on myös pystytty valmistamaan embryonaalisista
kantasoluista (Ikeda ym. 2005).
Kolmas kohdesolu, gangliosolu, vaurioituu erityisesti glaukoomassa (Osborne ym.
1999). Silmän sisäisen paineen kasvu vaurioittaa näköhermon gangliosoluja, mikä
johtaa näkökyvyn heikkenemiseen. Nykyiset hoidot perustuvat pitkälti silmänpaineen
alentamiseen eivätkä pysäytä gangliosolujen rappeutumista tai korvaa jo vaurioitunutta
kudosta (Ong ja da Cruz 2012). Gangliosolujen korvaaminen kantasoluilla tai in vitro
erilaistetuilla gangliosoluilla on erityisen haastavaa niiden hyvin haaroittuneen
rakenteen ja pitkien, näköhermon kautta aivoihin projisoituvien hermoyhteyksien
vuoksi. Useammassa tutkimuksessa on kuitenkin onnistuneesti käytetty kantasoluja
neuroprotektiivisen vaikutuksen aikaansaamiseksi (Bull ym. 2009; Johnson ym. 2010).
Bullin ryhmä käytti kokeessaan mesenkymaalisia kantasoluja kun taas Johnsonin ryhmä
siirsi koe-eläinten lasiaiseen oligodendrosyyttien prekursorisoluja (OPC,
oligodendrocyte prceursor cell). Molempien kokeiden tuloksissa havaittiin selvästi
kontrolliryhmiä parempaa gangliosolujen aksonien selviämistä, muttei kuitenkaan
siirrettyjen solujen integraatiota vaurioituneeseen kudokseen, mikä viittaa vaikutuksen
välittyvän erittyvien kasvutekijöiden kautta. Sekä mesenkymaalisten kantasolujen että
OPC:n on myös aikaisemmin todistettu tuottavan hermokasvutekijöitä, kuten GDNF:a
(Labouyrie ym. 1999; Yu ym. 2006).
5 POHDINTA
Lupaavien konseptiensa myötä geeni- ja kantasoluhoitoja on tutkittu hyvin paljon, mutta
arkipäivän kliinisiin hoitosovelluksiin on vielä matkaa eikä näkökykyä täysin
palauttavia tai parantavia hoitoja ole vielä kuvattu eläinmalleissakaan. Useissa

19
tutkimuksissa on pystytty todistamaan hoitojen onnistuminen teoreettisella tasolla,
mutta useat pienet yksityiskohdat aiheuttavat edelleen päänvaivaa.
Kaksi merkittävää ongelmaa, hoitojen kohdennus sekä silmän rakenteelliset ja
fysiologiset esteet, nivoutuvat tietyissä määrin yhteen ja ratkaisua voidaan hakea
farmaseuttisesta tutkimuksesta. Kuten aikaisemmin tutkielmassa todettiin,
useammassakin tutkimuksessa on todettu sisemmän rajoittavan kalvon olevan
merkittävä este solujen ja viruksien kulkeutumiselle lasiaisesta verkkokalvolle (Nishida
ym. 2000; Ivanova ym 2010). Tämän kiertämiseksi on esitetty kalvon kirurgista
kuorintaa annostelun yhteydessä, entsymaattista hajottamista, mikä voisi onnistua sekä
entsyymiä että haluttua hoitomuotoa sisältävällä valmisteella, sekä Müllerin solujen
toiminnan hiljentämistä, mikä voitaisiin saada myös aikaan yhdistelmävalmisteella
(Johnson ym. 2010). Sisempi rajoittava kalvo pystyttäisiin myös kiertämään
systeemisellä annostelulla, mikäli solut ja vektorit pystyttäisiin kohdentamaan vain
retinaan. Farmaseuttisessa tutkimuksessa liposomeja ja polymeerirakenteita on
päällystetty erilaisilla vasta-aineilla ja proteiineilla, polymeereillä, kuten
polyetyleeniglykolilla sekä hiilihydraateilla lääkevalmisteiden kohdentamiseksi jo
vuosia (Hornof ym. 2008; Lehtinen ym. 2012; Hu ym. 2013). Kohdentaminen
pohjautuu kohdesolun- tai kudoksen mikroympäristön ja sen erityispiirteiden
tuntemukseen: ainoastaan solun pinnalla oleva reseptori laukaisee soluunoton,
kasvaimen hapan ympäristö hajottaa kantajan tai kudoksen tuottama proteiini saa
kantajapartikkelin hajoamaan. Ymmärtämällä paremmin retinan mikroympäristöä ja sen
muutoksia erilaisten sairauksien myötä ja sen erityispiirteitä hyväksikäyttäen
muokkaamalla kantasoluja ja geenivektoreita voidaan hoito ohjata haluttuihin soluihin.
Uutena mielenkiintoisena kohdennusmenetelmänä lääkealalla on niin kutsuttu DNA-
tietokone, jossa nukleiinihappoja ei käytetä perimäaineksena vaan
rakennusmateriaalina, joka pystyy havaitsemaan muutoksia ympäristössään (Kahan ym.
2008; Andersen ym. 2009). Tämä saattaa olla tulevaisuuden mahdollisuus myös solujen
ja geenivektoreiden ohjauksessa.
Koska geeni- ja kantasoluhoitojen tarkoitus on mahdollistaa parantava hoito silmän
takaosan sokeuttaviin sairauksiin, avohoidon apteekkityössä ei välttämättä

20
tulevaisuudessakaan tulla näkemään monia geeni- tai kantasoluvalmisteita vaan hoito
toteutetaan lääkärin vastaanotolla tai klinikassa. Tällaisten lääkkeiden käyttö kuitenkin
tulee varmasti lisääntymään, vaikka hoitoja annettaisiinkin sairaalaolosuhteissa, minkä
vuoksi myös apteekkityössä olevan farmasistin tulee ymmärtää perusteet geeni- ja
kantasolumuotoisista hoitotekniikoista antaakseen potilasneuvontaa ja ymmärtääkseen
mahdolliset vaikutukset muiden lääkehoitojen kanssa. Virus- ja liposomivektoreiden
taloudellisesti tehokas tuottaminen ja erityisesti kantasolujen erilaistumiseen liittyvien
ympäristöolosuhteiden ja kasvutekijöiden huono tuntemus ovat paitsi ongelma
perustutkimuksessa, myös este tehokkaalle teollisen mittakaavan lääkevalmistukselle,
mikä varmasti lisää viivettä aktiivisten hoitorutiinien alkamiseen ja avohoidon
apteekkityössä näkymiseen (Andreadis ym. 1999; Prather ym. 2003; Wagner ja
Vorauer-Uhl 2011).
Myös immuunivasteet ja toksiset reaktiot rajoittavat tällä hetkellä sekä geeni- että
soluterapioiden kehittämistä. Kantasoluhoidoissa immuunivasteen todennäköisyys on
havaittu olevan huomattavasti pienempi, mikäli hoidossa voidaan käyttää potilaasta
itsestään peräisin olevia kantasoluja (Levin ym. 2004). Potilaasta itsestään siirrettävät
kantasolut saattavat kuitenkin kantaa mutatoitunutta geeniä, joka on alun perinkin ollut
syy tai osasyy silmäsairauteen, jolloin tavoiteltua hoidollista hyötyä ei saavuteta.
Toisesta ihmisestä tai eläimestä siirretyissä kantasoluissa voidaan varmistua
mutatoitumattoman geenin olemassaolosta, mutta erityisesti toisesta eläinlajista siirretyt
solut aiheuttavat helposti hylkimisreaktion elimistössä, ja vaikka niiden hillintä on
mahdollista immunosuppressiivisilla lääkeaineilla, immunosuppressio altistaa
infektioille ja mahdollisuus haittavaikutuksille kasvaa kasvavan lääkemäärän myötä
(Swijnenburg ym. 2008). Geenihoidoissa immuunivaste on helpompi välttää
kehittämällä entisestään sekä kemiallisia vektoreita että ei-patogeenista AAV-vektoria
(Abdallah ym. 1995; Walther ja Stein 2000; Colella ja Aurichio 2012).
Tutkimustulosten valossa sekä geenihoidot että soluterapiat ovat lupaavia, parantavia
hoitomuotoja silmän takaosan sokeuttaviin sairauksiin. Kantasoluhoidot vaativat vielä
perustutkimustietoa erilaisten solujen erilaistumisprosessien ymmärtämiseksi, mutta
myös soveltavammalla tutkimuksella, kuten farmaseuttisella materiaalitutkimuksella ja

21
biotekniikalla on paljon annettavaa alan kehittymisessä. Herättelevä ajatus on myös
nostettava eläinkokeiden ja ihmisillä toteutettavien kliinisten kokeiden vastaavuudesta:
koe-eläinten ja ihmisen fysiologia eroavat lopulta merkittävästi toisistaan ja eläimillä
saavutetut hoitovasteet eivät välttämättä toteudu ihmisillä tai osoittautuvatkin
vaarallisiksi (Perel ym. 2006; Hackam ja Redelmeier 2006; Shuaib ym. 2007). Tästä
syystä kliinisten kokeiden tuloksia vailla olevien tekniikoiden kohdalla tulee myös olla
hieman varovainen odotuksien suhteen.
6 YHTEENVETO
Sokeuttaviin silmän takaosan sairauksiin on ollut jo pidempään tarve kehittää
lääkehoitoja ja geeniteknologiat ja kantasolut ovat tuoneet tähän mielenkiintoisen
mahdollisuuden. Sekä kantasoluihin että geenitekniikoihin pohjautuvia hoitomenetelmiä
on kehitetty monia ja niiden tulokset in vitro ja eläinkokeissa ovat olleet lupaavia.
Ihmisillä tehdyistä kliinisistä kokeista ei kuitenkaan ole vielä kovin monia tuloksia ja
molemmissa tekniikoissa on useita kehittämiskohteita ennen yleiseen kliiniseen
käyttöön ottamista. Näiden ongelmakohtien ratkaisussa on oma paikkansa sekä
perustutkimuksella koskien esimerkiksi kantasolujen erikoistumista ja geneettisen
materiaalin muokkaamista että soveltavammalla, farmaseuttisellakin tutkimuksella
esimerkiksi biotekniikan ja materiaalitieteen aloilla. Tällä hetkellä käynnissä olevien ja
tulevien kliinisten tutkimusten tulokset vaikuttavat hyvin paljon geeni- ja
soluteknologioiden tutkimuksen suuntaan.

22
KIRJALLISUUSLUETTELO
Abdallah B, Sachs L, Demeneix BA: Non-viral gene transfer: Applications in developmental biology and gene therapy. Biol Cell 85: 1 – 7, 1995 Acland GM, Aguirre GD, Ray J, Zhang Q, Aleman TS, Cideciyan AV, Pearce-Kelling SE, Anand V, Zeng Y, Maguire AM, Jacobson SG, Hauswirth WW, Bennet J: Gene therapy restores visioin in a canine model of childhood blindness. Nat Gene 28: 92 – 95, 2001 Acland GM, Aguirre GD, Bennet J, Aleman TS, Cideciyan AV, Bennicelli J, Dejneka NS, Pearce-Kelling SE, Maguire AM, Palczewski K, Hauswirth WW, Jacobson SG: Long-term restoration of rod and cone vision by single dose rAAV-mediated gene transfer to the retina in a canine model of childhood blindness. Mol Ther 12(6): 1072 – 1082, 2005 Agrawal N, Dasarandhi PVN, Mohammed A, Malhotra P, Bhatnagar RK, Mukherjee SK: RNA interference: biology, mechanism and applications. Microbiol Mol Biol R 67(4): 657 – 685, 2003 Andersen ES, Dong M, Nielsen MM, Jahn K, Subramani R, Mmdouh W, Golas MM, Sander B, Stark H, Oliviera CLP, Pedersen JS, Birkedal V, Besenbacher F, Gothelf KV, Kjems J: Self-assembly of a nanoscale DNA box with a controllable lid. Nature 459: 73 – 77, 2009 Andreadis ST, Roth CM, Le Doux JM, Morgan JR, Yarmush ML: Large-scale processing of recombinant retroviruses for gene therapy. Biotechnol Prog 15: 1 – 11, 1999 Boye SE, Boye SL, Lewin AS, Hauswirth WW: A comprehensive review of retinal gene therapy. Mol Ther 21(3): 509 – 519, 2013
Brickman JM, Burdon TG: Pluripotency and tumorigenecy. Nat Gen 32: 557 – 558, 2002 Brunner S, Sauer T, Carotta S, Cotton M, Altik M, Wagner E: Cell cycle dependence of gene transfer by lipoplex, polyplex and recombinant adenovirus. Gene Ther 7: 401 – 407, 2000 Buchholz DE, Hikita ST, Rowland TJ, Friedrich AM, Hinman CR, Johnson LV, Clegg DO: Derivation of functional retinal pigmented epithelium from induced pluripotent stem cells. Stem Cells 27: 2427 – 2434, 2009 Bull ND, Irvine K-A, Franklin RJ, Martin KR: Transplanted oligodendrocyte precursor cells reduce neurodegeneration in a model of glaucoma. Invest Ophth Vis Sci 50(9): 4244 – 4253, 2009

23
Busskamp V, Duebel J, Balaya D, Fradot M, Viney TJ, Siegert S, Groner AC,Cabuy E, Forester V, Seeliger M, Biel M, Humphries P, Paques M, Mohand-Said S, Trono D, Deisseroth K, Sahel J-A, Picaud S, Roska B: Genetic reactivation of cone photoreceptors restores visual responses in retinitis pigmentosa. Science 329: 413 – 417, 2010 Busskamp V, Picaud S, Sahel J-A, Roska B: Optogenetic therapy for retinitis pigmentosa. Gene Ther 19(2): 169 – 175, 2011 Carr A-J, Vugler AA, Hikita ST, Lawrence JM, Gias C, Chen LL, Buchholz DE, Ahmando A, Semo M, Smart MJK, Hasan S, da Cruz L, Johnson LV, Clegg DO, Coffey PJ: Protective effects of human iPS-derived retinal pigment epithelium cell transplantation in the retinal dystrophic rat. PloS ONE 4(12): 1 – 12, 2009 Colella P, Auricchio A: Gene therapy of inherited retinopathies: a long and successful road from viral vectors to patients. Hum Gene Ther 23: 796 – 807, 2012 Cunha-Vaz JG: The blood–retinal barriers system: Basic concepts and clinical evaluation. Exp Eye Res 78: 715 – 721, 2004 Dalkara D, Kolstad KD, Caporale N, Visel M, Klimczak RR, Schaffer DV, Flannery JG: Inner Limiting Membrane Barriers to AAV-mediated Retinal Transduction From the Vitreous, Mol Ther 17(12): 2096 – 2102, 2009 del Amo EM, Urtti A: Current and future ophthalmic drug delivery systems: A shift to the posterior segment. Drug Discov Today 13 (3/4): 135 – 143 Dokka S, Toledo D, Shi X, Castranova V, Rojanasakul Y: Oxygen radical-mediated pulmonary toxicity induced by some cationic liposomes. Pharm Res 17(5): 521 – 525, 2000 Dowling JE: Organization of vertebrate retinas. Invest Ophth Visual 9:655 – 680, 1970 FDA – Food and Drug Administration: Highlights of prescribing information: Macugen. NDA 21-756/S018: 3-12, 2004 Filion MC, Phillips NC: Toxicity and immunomodulatory activity of liposomal vectors formulated with cationic lipids toward immune effector cells. Biochim Biophys Acta 1329: 345 – 365, 1997 Fridlich R, Delelande F, Jaillard C, Lu J, Poidevin L, CroninT, Perrocheau L, Millet-Puel G, Niepon M-L, Poch O, Holmgren A, van Dorsselaer A, Sahel J-A, Léveillard T: The thioredoxin-like protein rod-derived cone viability factor (RdCVFL) interacts with TAU and inhibits its phosphorylation in the retina. Mol Cell Proteomics 8: 1026 – 1218, 2009 Hackman DG, Redelmeier DA: Translation of research evidence from animals to humans. J Am Med Assoc 296(14): 1731 – 1732, 2006

24
Halfter W, Dong S, Eller AW, Nischt R: Origin and turnover of ECM proteins from the inner limiting membrane and vitreous body. Eye 22: 107 – 1213, 2008 Hashimoto T, Gibbs D, Lillo C, Azarian SM, Legacki E, Zhang X-M, Yan X-J Williams DS: Lentiviral gene replacement therapy of retinas in a mouse model for Usher syndrome type 1B. Gene Ther 14: 584 – 594, 2007 Hentze H, Graichen R, Coman A: Cell therapy and the safety of embryonic stem cell-derived grafts. Trends Biotechnol 25(1): 24 – 32, 2006 Hornof M, de la Fuente M, Hallikainen M, Tammi RH, Urtti A: Low molecular weight hyaluronan shielding of DNA/PEI polyplexes facilitates CD44 receptor mediated uptake in human corneal epithelial cells. J Gene Med 10: 70 – 80, 2008 Hu Q, Gao X, Kang T, Feng X, Jiang D, Tu Y, Song Q, Yao Lei, Jiang X, Chen H, Chen J: CGKRK-modified nanoparticles for dual-targeting drug delivery to tumor cells and angiogenic blood vessels. Biomaterials 34: 9496 – 9508, 2013 Ikeda H, Osakada F, Watanabe K, Mizuseki K, Haraguchi T, Miyoshi H, Kamlya D, Honda Y, Sasai N, Yoshimura N, Takahashi M, Sasai Y: Generation of Rx/Pax6 neural retinal precursors from embryonic stem cells. P Natl Acad Sci-Biol 102(32): 11331 – 11336, 2005 Ivanova E, Hwang G-S, Pan Z-H, Troilo D: Evaluation of AAV-mediated expression of Chop2-GFP in the marmoset retina. Invest Ophth Vis Sci 51(10): 5288 – 5295, 2010 Jacobson SG, Cideciyan AV, Ratnakaram R, Heon E, Schwartz SB, Roman AJ, Peden MC, Aleman TS, Boye SL, Sumaroka A, Conlon TJ, Calcedo R, Pang J, Erger KE, Oliveras MB, Mullins CL, Swider M, Kaushal S, Feuer WJ, Iannaccone A, Fishman GA, Stone EM, Byrne BJ, Hauswirth WW: Gene therapy for leber congenital amaurosis caused by RPE65 mutations: safety and efficacy in fifteen children and adults followed up to three years. Arch Opthalmol 10(1): 9 – 24, 2012 Johnson TV, Bull ND, Martin KR: Identification of barriers to retinal engraftment of transplanted stem cells. Invest Ophth Vis Sci 51(2): 960 – 970, 2010 Kahan M, Gil B, Adar R, Shapiro E: Towards molecular computers that operate in a biological environment. Physica D 237: 1165 – 1172, 2008 Kaiser PK, Symons RCA, Shah SM, Quinlan EJ, Tabaneh H, Do DV, Reisen G, Lockridge JA, Short B, Guerciolini R, Nguyen QD: RNAi-based treatment for neovascular age-related macular degeneration by Sirna-027. Am J Ophthalmol 150: 33 – 9, 2010 Kolb H: The architecture of functional neural circuits in the vertebrate retina. Invest Ophth Vis Sci 35(5): 2385 – 2404, 1994

25
Labouyrie E, Dubus P, Groppi A, Maihon FX, Ferrer J, Parrens M, Reiffers J, de Mascarel A, Merlio JP: Expression of neurotrophins and their receptors in human bone marrow. Am J Physiol 154(2): 405 – 415, 1999 Lappalainen K, Urtti A, Söderling E, Jääskeläinen I, Syrjänen K, Syrjänen S: Cationic liposomes improve stability and intracellular delivery of antisense oligonucleotides into CaSki cells. Biochim Biophys Acta 1196(2): 201 – 208, 1994 Lee DJ, Biros DJ, Taylor AW: Injection of an alpha-melanocyte stimulating hormone expression plasmid is effective in suppressing experimental autoimmune uveitis. Int Immunopharmacol 9: 1079 – 1086, 2009 Lehtinen J, Raki M, Bergstöm K, Uutela P, Lehtinen K, Hiltunen A, Pikkarainen J, Liang H, Pitkänen S, Määttä A-M, Ketola RA, Yliperttula M, Wirth T, Urtti A: Pre-targeting and direct immunotargeting of liposomal drug carriers to ovarian carcinoma. PloS ONE 7(7): 1 – 10, 2012 Levin LA, Ritch R, Richards JE, Borrâs T: Stem cell therapy for ocular disorders. Arch Ophthalmol 22: 621 – 627, 2004 Li S, Huang L: Nonviral gene therapy: promises and challenges. Gene Ther 7: 31 – 34, 2000 Lu B, Malcut C, Wang S, Girman S, Francis P, Lemieux L, Lanza R, Lund R: Long-term safety and function of rpe from human embryonic stem cells in preclinical models of macular degeneration. Stem Cells 27: 2126 – 2135, 2009 Lund RD, Wang S, Klimanskaya I, Holmes T, Ramos-KLsey R, Lu B, Girman S, Bischoff N, Sauvé Y, Lanza R: Human embryonic stem cell–derived cells rescue visual function in dystrophic RCS rats. Cloning Stem Cells 8(3): 189 – 199, 2006 MacLaren RE, Pearson RA, MacNeil A, Douglas RH, Salt TE, Akimoto M, Saroop A, Sowden JC, Ali RR: Retinal repair by transplantation of photoreceptor precursors. Nature 44(9): 203 – 207, 2006 Nagel G, Szellas T, Huhn W, Kateriya S, Adeishvili N, Beerthold P, Ollig D, Hegmann P, Bamberg E: Channelrhodopsin-2, a directly light-gated cation-selective membrane channel. P Natl Acad Sci-Biol 100(24): 13940 – 13945, 2003 NIH - National Institutes of Health: Assessment of adenoviral vector safety and toxicity: report of the national institutes of health recombinant DNA advisory committee. Hum Gene Ther 13: 3 – 13, 2002 NIH – National Institutes of Health, www.clinicaltrials.gov, (viitattu 30.4.2014), 2014 Nisbet MC: The competition for worldviews: values, information, and public support for stem cell research. Int J Public Opin R 17(1): 90 – 112, 2005

26
Nishida A, Takahashi M, Tanibara H, Nakamo I, Takahashi JB, Mizoguchi A, Ide C, Honda Y: Incorporation and differentiation of hippocampus- derived neural stem cells transplanted in injured adult rat retina. Invest Ophth Vis Sci 41(13): 4268 – 4274, 2000 Ong JM, da Cruz L: A review and update on the current status of stem cell therapy and the retina. Brit Med Bull 102: 133 – 146, 2012 Osborne NN, Wood JPM, Childlow G, Bae J-H, Melena J, Nash MS: Ganglion cell death in glaucoma: what do we really know? Br J Ophthalmol 83: 980 – 986, 1999 Patil SD, Rhodes DG, Burgess DJ: Anionic liposomal delivery system for DNA transfection. AAPS J 6(4): 1 – 10, 2004 Patil SD, Rhodes DG, Burges DJ: DNA-based therapeutics and DNA delivery systems: A Comprehensive Review. AAPS J 7(1): 61 – 77, 2005 Perel P, Sena E, Wheble P, Briscoe C, Sandercock P, Macleod M, Mignini LE, Jayara P, Khan KS: Comparison of treatment effects between animal experiments and clinical trials: systematic review. Brit Med J 334: 1 – 6, 2006 Pitkänen L, Ruponen M, Nieminen J, Urtti A: Vitreous is a barrier in noviral gene transfer by cationic lipids and polymers. Prharm Res 20(4): 576 – 583, 2003 Porkka K, Kantasolujensiirrot. Duodecim 120: 1391 – 1399, 2004 Prather KJ, Sagar S, Murphy J, Chartrain M: Industrial scale production of plasmid DNA for vaccine and gene therapy: plasmid design, production, and purification. Enzyme Microb Tech 33: 865 – 883, 2003 Punzo C, Xiong W, Cepko CL: Loss of daylight vision in retinal degeneration: are oxidative stress and metabolic dysregulation to blame? J Biol Chem 287(3): 1642 – 1648, 2012 Redmond MT, Poliakov E, Yu S, Tsai J-Y, Lu Z, Gentleman S: Mutation of key residues of RPE65 abolishes its enzymatic role as isomerohydrolase in the visual cycle. P Natl Acad Sci-Biol 102(38): 13658 – 13663, 2005 Rein DB, Zhang P, Wirth KE, Lee PP, Hoerger TJ, McCall N, Klein R, Tielsch JM, Vijan S, Saaddine J: The Economic Burde of Major Adult Visual Disorders in the united States. Arch Ophthalmol 124:1754–1760, 2006 Sahel J-A, Roska B: Gene theraoy for blindness. Annu Rev Neurosci 36: 467 – 488, 2013 Sandek MJ: Embryo ethics – the moral logic of stem-cell research. N Engl J Med 351(3): 207 – 209, 2004

27
Sauvé Y, Girman SV, Wang S, Keegan DJ, Lund RD: Preservation of visual responsiveness in the superior colliculus of RCS rats after retinal pigment epithelium cell transplantation. Neuroscience 114(2): 389 – 401, 2002 Schobert B, Lanyi JK: Halorhodopsin is a light-driven chloride pump. J Biol Chem 257(17): 10306 – 10313, 1982 Schwartz B, Benoist C, Abdallah B, Rangara R, Hassan A, Scherman D, Demeneix BA: Gene transfer by naked DNA into adult mouse brain. Gene Ther 3(5): 405 – 411, 1996 Shuaib A, Lees K, Lyden, P, Grotta J, Davalos A, Davis SM, Diener H-C, Ashwood T, Wasiewski WW, Emeribe U: NXY-059 for the treatment of acute ischemic stroke. New Engl J Med 357: 562 – 571, 2007 Strauss O: The Retinal Pigment Epithelium in Visual Function. Physiol Rev 85: 845 – 881, 2005 Subrizi A, Hiidenmaa H, Ilmarinen T, Nymark S, Dubruel P, Uusitalo H, Yliperttula M, Urtti A, Skottman H: Generation of hESC-derived retinal pigment epithelium on biopolymer coated polyimide membranes. Biomaterials 33: 8047 – 8054, 2012 Swijnenburg R-J, Schrepfer S, Govaert JA, Cao F, Ranshoff K, Selkh A, Haddad M, Connolly AJ, Davis MM, Robbins RC, Wu JC: Immunosuppressive therapy mitigates immunological rejection of human embryonic stem cell xenografts. P Natl Acad Sci-Biol 105(35): 12991 – 12996, 2008 Thomas CE, Ehrhardt A, Kay MA: Progress and problems with the use of viral vectors for gene therapy. Nat Rev Gen 4:246 – 258, 2003 Touchard E, Heiduschka P, Berduugo M, Kowalczuk L, Bigey P, Chahory S, Gandolphe C, Jeanny J-C, Behar-Cohen F: Non-viral gene therapy for GDNF production in RCS rat: the crucial role of the plasmid dose. Gene Ther 19: 886 – 898, 2012 Tropepe V, Coles BLK, Chiasson BJ, Horsford DJ, Elia AJ, Mcinnes R, van der Kooy D: Retinal stem cells in the adult mammalian eye. Science 287, 20132 – 2036, 2000 Urtti A: Challenges and obstacles of ocular pharmacokinetics and drug delivery. Adv Drug Deliver Rev 58, 111 – 1135, 2006 Wagner A, Vorauer-Uhl K: Liposome technology for industrial purposes. J Drug Deliv 2011: ID 591325 s. 1 – 9, 2011 Walther W, Stein U: Viral Vectors for Gene Transfer: A Review of Their Use in the Treatment of Human Diseases. Drugs 60(2): 249 – 271, 2000

28
Van Hoffelen SJ, Young MJ, Shatos A, Sakaguchi DS: Incorporation of murine brain progenitor cells into the developing mammalian retina. Invest Ophth Vis Sci 44(1): 426 – 434, 2003 Wang S, Lu b; Girman S, Duan J, McFarland T, Zhang Q-S, Grompe M, Adamus G, Appukuttan B, Lund R: Non-invasive stem cell therapy in a rat model for retinal degeneration and vascular pathology. PLoS ONE5(2): 1 – 9, 2010 Weil D, Lévy G, Sahly I, Lévi-Acobas F, Blanchard S, El-Amraoui A, Crozet F, Philippe H, Abitbol M, Pett C: Human myosin VIIA responsible for the Usher 1B syndrome: A predicted membrane-associated motor protein expressed in developing sensory epithelia. P Natl Acad Sci-Biol 93: 3232 – 3237, 1996 Whitley SJO, Litchfield TM, Coffey PJ, Lund RD: Improvement of the pupillary light reflex of Royal College of Surgeons rats following RPE cell grafts. Exp Nurol 140: 100 – 104, 1996 Wlfrum U: The cellular function of the Usher gene product myosin VIIA is specified by its ligands. Kirjassa: Retinal Degeneration: Mechanisms and Experimental Therapy. s. 133 – 142 Toim. LaVail M, Hollyfield JG, Andersson RE. Kluwer Academic, Plenum Publishers, New York, 2003 Wu W-C, Lai C-C, Chen S-L, Sun M-H, Xiao X, Chen T-L, Lin K-K, Kuo S-W, Tsao Y-P: Long-term safety of GDNF gene delivery in the retina. Curr Eye Res 30: 715 – 722, 2005 Vugler A, Carr A-J, Lawrenve J, Chen LL, Burell K, Wright A, Lundh P, Semo M, Ahmado A, Gias C, da Cruz L, Moore H, Andrews P, Walsh J, Coffey P: Elucidating the phenomenon of HESC-derived RPE: Anatomy of cell genesis, expansion and retinal transplantation. Exp Neurol 214: 347 – 361, 2008 Yang Y, Mohand-Said S, Danan A, Simonutti M, Fontaine V, Clerin E, Picaud S, Lévellard T, Sahel J-A: Functional cone rescue by RdCVF protein in a dominant model of retinitis pigmentosa. Mol Ther 17(5): 787 – 795, 2009 Young MJ, Ray J, Whiteley SJO, Klassen H, Gage FH: Neuronal differentiation and morphological integration of hippocampal progenitor cells transplanted to the retina of immature and mature dystrophic rats. Mol Cell Neurosci 16: 197 – 205, 2000 Yu S, Tanabe T, Dezawa M, Ishikawa H, Yoshimura N: Effects of bone marrow stromal cell injection in an experimental glaucoma model. Biochem Bioph Res Co 344: 1071 – 1079, 2006 Zhang K, Zhang L, Weinreb RN: Ophthalmic drug discovery: novel targets and mechanisms for retinal diseases and glaucoma. Nat Rev Drug Discov 11:541–559, 2012

29
Zhang Y, Ivanova E, Bi A, Pan Z-H: Ectopic expression of multiple microbial rhodopsins restores ON and OFF light responses in retinas with photoreceptor degeneration. J Neurosci 29(29): 9186 – 9196, 2009