Faktor Resiko , Patofisiologi Dan MK CA Colorectal
-
Upload
suci-asnatasia-ramadhini -
Category
Documents
-
view
67 -
download
5
Transcript of Faktor Resiko , Patofisiologi Dan MK CA Colorectal

Faktor Resiko
1. Polip
Polip telah diketahui potensial untuk menjadi kanker kolorektal. Evolusi dari kanker itu
sendiri merupakan sebuah proses yang bertahap, dimana proses dimulai dari hiperplasia sel mukosa,
pembentukan adenoma, perkembangan dari displasia menuju transformasi maligna dan invasif
kanker . Aktifasi onkogen, inaktifasi tumor supresi gen, dan kromosomal deletion memungkinkan
perkembangan dari formasi adenoma, perkembangan dan peningkatan displasia dan invasif
karsinoma.8
Ada tiga kelompok utama gen yang terlibat dalam regulasi pertumbuhan sel yaitu proto-
onkogen, gen penekan tumor (Tumor Suppresor Gene = TSG), dan gen gatekeeper. Proto-onkogen
menstimulasi dan meregulasi pertumbuhan dan pembelahan sel. TSG menghambat pertumbuhan sel
atau menginduksi apoptosis (kematian sel yang terprogram). Kelompok gen ini dikenal sebagai
anti-onkogen, karena berfungsi melakukan kontrol negatif pada pertumbuhan sel. Gen p53
merupakan salah satu dari TSG yang menyandi protein dengan berat molekul 53 kDa. Gen p53 juga
berfungsi mendeteksi kerusakan DNA, menginduksi reparasi DNA. Gen gatekeeper berfungsi
mempertahankan integritas genomik dengan mendeteksi kesalahan pada genom dan
memperbaikinya. Mutasi pada gen-gen ini karena berbagai faktor membuka peluang terbentuknya
kanker.
Pada keadaan normal, pertumbuhan sel akan terjadi sesuai dengan kebutuhan melalui siklus
sel normal yang dikendalikan secara terpadu oleh fungsi proto-onkogen, TSG, dan gen gatekeeper
secara seimbang. Jika terjadi ketidakseimbangan fungsi ketiga gen ini, atau salah satu tidak
berfungsi dengan baik karena mutasi, maka keadaan ini akan menyebabkan penyimpangan siklus
sel. Pertumbuhan sel tidak normal pada proses terbentuknya kanker dapat terjadi melalui tiga
mekanisme, yaitu perpendekan waktu siklus sel, sehingga akan menghasilkan lebih banyak sel
dalam satuan waktu, penurunan jumlah kematian sel akibat gangguan proses apoptosis, dan
masuknya kembali populasi sel yang tidak aktif berproliferasi ke dalam siklus proliferasi. Gabungan
mutasi dari ketiga kelompok gen ini akan menyebabkan kelainan siklus sel akibatnya sel akan
berkembang tanpa kontrol (yang sering terjadi pada manusia adalah mutasi gen p53). Akhirnya
akan terjadi pertumbuhan sel yang tidak diperlukan, tanpa kendali dan karsinogenesis dimulai.
Secara histologi polip diklasifikasikan sebagai neoplastik dan non neoplastik. Non
neoplastik polip tidak berpotensi maligna, yang termasuk polip non neoplastik yaitu polip
hiperplastik, mukous retention polip, hamartoma (juvenile polip), limfoid aggregate dan inflamatory
polip.7
Neoplastik polip atau adenomatous polip berpotensial berdegenerasi maligna; dan
berdasarkan WHO diklasifikasikan sebagai tubular adenoma, tubulovillous adenoma dan villous

adenoma. Tujuh puluh persen dari polip berupa adenomatous, dimana 75%-85% tubular adenoma,
10%-25% tubulovillous adenoma dan villous adenoma dibawah 5%.8
Gambar Adenomatous Polip
Displasia dapat dikategorikan menjadi low atau high grade. Enam persen dari adenomatous
polip berupa high grade displasia dan 5% didalamnya berupa invasif karsinoma pada saat
terdiagnosa. Potensi malignansi dari adenoma berkorelasi dengan besarnya polip, tingkat displasia,
dan umur. Polip yang diameternya lebih besar dari 1 cm, berdisplasia berat dan secara histologi
tergolong sebagai villous adenoma dihubungkan dengan risiko tinggi untuk menjadi kanker
kolorektal. Polip yang berukuran kecil (<1 cm) tidak berhubungan dengan meningkatnya timbulnya
kanker kolorektal. Insiden dari kanker meningkat dari 2,5-4 kali lipat jika polip lebih besar dari 1
cm, dan 5-7 kali lipat pada pasien yang mempunyai multipel polip. Waktu yang dibutuhkan untuk
menjadi malignansi tergantung beratnya derajat displasia.8
Gambar Polip Neoplastik

Keterangan : (A) tubular adenoma, (B) villous adenoma, (C) tubulovillous adenoma, (D) karsinoma
pada tangkai tubular adenoma, (E) karsinoma invasif yang muncul dari sebuah villous adenoma.
2. Idiopathic Inflammatory Bowel Disease
2.1 Ulseratif Kolitis
Ulseratif kolitis merupakan faktor risiko yang jelas untuk kanker kolon, sekitar 1% dari
pasien yang memiliki riwayat kronik ulseratif kolitis. Risiko perkembangan kanker pada pasien ini
berbanding terbalik pada usia terkena kolitis dan berbanding lurus dengan keterlibatan dan
keaktifan dari ulseratif kolitis. Risiko kumulatif adalah 2% pada 10 tahun, 8% pada 20 tahun, dan
18% pada 30 tahun. Pendekatan yang direkomendasikan untuk seseorang dengan risiko tinggi dari
kanker kolorektal pada ulseratif kolitis dengan mengunakan kolonoskopi untuk menentukan
kebutuhan akan total proktokolektomi pada pasien dengan kolitis yang durasinya lebih dari 8 tahun.
Strategi yang digunakan berdasarkan asumsi bahwa lesi displasia bisa dideteksi sebelum
terbentuknya invasif kanker. Diagnosis dari displasia mempunyai masalah tersendiri pada
pengumpulan sampling spesimen dan variasi perbedaan pendapat antara para ahli patologi anatomi.5
2.2 Penyakit Crohn’s
Pasien yang menderita penyakit crohn’s mempunyai risiko tinggi untuk menderita kanker
kolorektal tetapi masih kurang jika dibandingkan dengan ulseratif kolitis.8
Keseluruhan insiden dari kanker yang muncul pada penyakit crohn’s sekitar 20%. Pasien
dengan striktur kolon mempunyai insiden yang tinggi dari adenokarsinoma pada tempat yang terjadi
fibrosis. Adenokarsinoma meningkat pada tempat strikturoplasty menjadikan sebuah biopsy dari
dinding intestinal harus dilakukan pada saat melakukan strikturoplasty. Telah dilaporkan juga
bahwa squamous sel kanker dan adenokarsinoma meningkat pada fistula kronik pasien dengan
crohn’s disease.5
3. Faktor Genetik
3.1 Riwayat Keluarga
Sekitar 15% dari seluruh kanker kolon muncul pada pasien dengan riwayat kanker
kolorektal pada keluarga terdekat. Seseorang dengan keluarga terdekat yang mempunyai kanker
kolorektal mempunyai kemungkinan untuk menderita kanker kolorektal dua kali lebih tinggi bila
dibandingkan dengan seseorang yang tidak memiliki riwayat kanker kolorektal pada keluarganya.6

3.2 Herediter Kanker Kolorektal
Abnormalitas genetik terlihat mampu memediasi progresi dari normal menuju mukosa kolon
yang maligna. Sekitar setengah dari seluruh karsinoma dan adenokarsinoma yang besar
berhubungan dengan mutasi. Langkah yang paling penting dalam menegakkan diagnosa dari
sindrom kanker herediter yaitu riwayat kanker pada keluarga. Mutasi sangat jarang terlihat pada
adenoma yang lebih kecil dari 1 cm. Allelic deletion dari 17p ditunjukkan pada ¾ dari seluruh
kanker kolon, dan deletion dari 5q ditunjukkan lebih dari 1/3 dari karsinoma kolon dan adenoma
yang besar.2 Dua sindrom yang utama dan beberapa varian yang utama dari sindrom ini
menyebabkan kanker kolorektal telah dikenali karakternya. Dua sindrom ini, dimana mempunyai
predisposisi menuju kanker kolorektal memiliki mekanisme yang berbeda, yaitu familial
adenomatous polyposis (FAP) dan hereditary non polyposis colorectal cancer (HNPCC).7
FAP
Gen yang bertanggung jawab untuk FAP yaitu gen APC, yang berlokasi pada kromosom
5q21. Adanya defek pada APC tumor supresor gen dapat menggiring kepada kemungkinan
pembentukan kanker kolorektal pada umur 40 sampai 50 tahun.2 Pada FAP yang telah berlangsung
cukup lama, didapatkan polip yang sangat banyak untuk dapat dilakukannya kolonoskopi
polipektomi yang aman dan adekuat. Ketika hal ini terjadi, direkomendasikan untuk melakukan
prophylactic subtotal colectomy diikuti dengan endoskopi pada bagian yang tersisa. Idealnya
prophylactic colectomy harus ditunda kecuali terdapat terlalu banyak polip yang dapat ditangani
dengan aman. Prosedur pembedahan elektif harus sedapat mungkin dihindari ketika
memungkinkan. Screening untuk polip harus dimulai pada saat usia muda. Pasien dengan FAP yang
diberi 400 mg celecoxib, dua kali sehari selama enam bulan mengurangi rata rata jumlah polip
sebesar 28%. Tumor lain yang mungkin muncul pada sindrom FAP adalah karsinoma papillary
thyroid, sarcoma, hepatoblastomas, pancreatic carcinomas, dan medulloblastomas otak. Varian dari
FAP termasuk gardner’s syndrom dan turcot’s syndrom.7
HNPCC
Pola autosomal dominan dari HNPCC termasuk lynch’s sindrom I dan II. Generasi multipel
yang dipengaruhi dengan kanker kolorektal muncul pada umur yang muda (±45 tahun), dengan
predominan lokasi kanker pada kolon kanan. Abnormalitas genetik ini terdapat pada mekanisme
mismatch repair yang bertanggung jawab pada defek eksisi dari abnormal repeating sequences dari
DNA, yang dikenal sebagai mikrosatellite (mikrosatellite instability). Retensi dari squences ini
mengakibatkan ekspresi dari phenotype mutator, yang dikarakteristikkan oleh frekuensi DNA
replikasi error (RER+ phenotype), dimana predisposisi tersebut mengakibatkan seseorang memiliki
multitude dari malignansi primer. Pasien dengan HNPCC mungkin juga memiliki adenoma
sebaceous, carcinoma sebaceous, dan multipel keratocanthoma, Termasuk kanker dari

endometrium, ovarium, kandung kemih, ureter, lambung dan traktus biliaris. Jika dibandingkan
dengan sporadic kanker kolorektal, tumor pada HNPCC seringkali poorly differentiated, dengan
gambaran mucoid dan signet-cell, reaksi yang mirip crohn’s (nodul lymphoid, germinal centers,
yang berlokasi pada perifer inflitrasi kanker kolorektal), kehadiran infiltrasi lymphocytes diantara
tumor. Karsinogenesis yang terakselerasi muncul pada HNPCC, pada keadaan ini adenoma kolon
yang berukuran kecil dapat menjadi karsinoma dalam 2-3 tahun, bila dibandingkan dengan proses
pada rata-rata kanker kolorektal yang membutuhkan waktu 8-10 tahun. Ketika kriteria amsterdam
digunakan untuk menentukan proporsi dari kanker kolorektal yang dikarenakan HNPCC, estimasi
keakurasiannya sekitar 1-6 %.
Pasien dengan HNPCC mempunyai kecenderungan untuk menderita kanker kolorektal pada
umur yang sangat muda, dan screening harus dimulai pada umur 20 tahun atau lebih dini 5 tahun
dari umur anggota keluarga yang pertama kali terdiagnosa kanker kolorektal yang berhubungan
HNPCC. Angka rata-rata pasien dengan HNPCC yang didiagnosa menderita kanker kolorektal pada
umur 44 tahun, dibandingkan dengan pasien kontrol yang menderita kanker kolorektal pada umur
68 tahun. Prognosis dari pasien HNPCC terlihat lebih baik daripada pasien dengan sporadic kanker
kolon. Dari penelitian menunjukkan bahwa pasien dengan HNPCC kurang mendapat manfaat dari
adjuvant kemoterapi berdasarkan kombinasi fluorourasil daripada pasien tanpa kelainan ini.7
4. Diet
Masyarakat yang diet tinggi lemak, tinggi kalori, daging dan diet rendah serat
berkemungkinan besar untuk menderita kanker kolorektal pada kebanyakan penelitian, meskipun
terdapat juga penelitian yang tidak menunjukkan adanya hubungan antara serat dan kanker
kolorektal. Ada dua hipotesis yang menjelaskan mekanisme hubungan antara diet dan resiko kanker
kolorektal. Teori pertama adalah pengakumulasian bukti epidemiologi untuk asosiasi antara
resistensi insulin dengan adenoma dan kanker kolorektal. Mekanismenya adalah menkonsumsi diet
yang berenergi tinggi mengakibatkan perkembangan resistensi insulin diikuti dengan peningkatan
level insulin, trigliserida dan asam lemak tak jenuh pada sirkulasi. Faktor sirkulasi ini mengarah
pada sel epitel kolon untuk menstimulus proliferasi dan juga memperlihatkan interaksi oksigen
reaktif. Pemaparan jangka panjang hal tersebut dapat meningkatkan pembentukan kanker
kolorektal. Hipotesis kedua adalah identifikasi berkelanjutan dari agen yang secara signifikan
menghambat karsinogenesis kolon secara experimental. Dari pengamatan tersebut dapat
disimpulkan mekanismenya, yaitu hilangnya fungsi pertahanan lokal epitel disebabkan kegagalan
diferensiasi dari daerah yang lemah akibat terpapar toksin yang tak dapat dikenali dan adanya
respon inflamasi fokal, karakteristik ini didapat dari bukti teraktifasinya enzim COX-2 dan stres
oksidatif dengan lepasnya mediator oksigen reaktif. Hasil dari proliferasi fokal dan mutagenesis

dapat meningkatkan resiko terjadinya adenoma dan aberrant crypt foci. Proses ini dapat dihambat
dengan (a) demulsi yang dapat memperbaiki permukaan lumen kolon; (b) agen anti-inflamasi; atau
(c) anti-oksidan. Kedua mekanisme tersebut, misalnya resistensi insulin yang berperan melalui
tubuh dan kegagalan pertahanan fokal epitel yang berperan secara lokal, dapat menjelaskan
hubungan antara diet dan resiko kanker kolorektal.8
5 Gaya Hidup
Pria dan wanita yang merokok kurang dari 20 tahun mempunyai risiko tiga kali untuk
memiliki adenokarsinoma yang kecil, tapi tidak untuk yang besar. Sedangkan merokok lebih dari 20
tahun berhubungan dengan risiko dua setengah kali untuk menderita adenoma yang berukuran
besar. Pemakaian alkohol juga menunjukkan hubungan dengan meningkatnya risiko kanker
kolorektal.
Pada berbagai penelitian telah menunjukkan hubungan antara aktifitas, obesitas dan asupan
energi dengan kanker kolorektal. Pada percobaan terhadap hewan, pembatasan asupan energi telah
menurunkan perkembangan dari kanker. Interaksi antara obesitas dan aktifitas fisik menunjukkan
penekanan pada aktifitas prostaglandin intestinal, yang berhubungan dengan risiko kanker
kolorektal. The Nurses Health Study telah menunjukkan hubungan yang berkebalikan antara
aktifitas fisik dengan terjadinya adenoma, yang dapat diartikan bahwa penurunan aktifitas fisik akan
meningkatkan risiko terjadinya adenoma.8
6 Usia
Proporsi dari semua kanker pada orang usia lanjut (≥ 65 thn) pria dan wanita adalah 61%
dan 56%. Frekuensi kanker pada pria berusia lanjut hampir 7 kali (2158 per 100.000 orang per
tahun) dan pada wanita berusia lanjut sekitar 4 kali (1192 per 100.000 orang per tahun) bila
dibandingkan dengan orang yang berusia lebih muda (30-64 thn). Peningkatan resiko kanker
kolorektal meningkat sesuai dengan usia.7
Menurut WHO, faktor resiko kanker kolorektal :5
1. Berusia > 50 tahun
2. Sindroma adenomatous popilposis ( familial, hamartomatous poliposis dan Peutz jagers sindrom)
3. Riwayat kanker kolorektal pada keluarga
4. Inflamatory bowel disease
5. Riwayat menderita kanker kolorektal
6. Riwayat menderita polip kolrektal

Patofisiologi
Penyebab dari kanker kolorektal masih terus diselidiki. Mutasi dapat menyebabkan aktivasi
dari onkogen (k-ras) dan atau inaktivasi dari gen supresi tumor ( APC, DCCà deleted in colorectal
carcinoma, p53). Karsinoma kolorektal merupakan perkembangan dari polip adenomatosa dengan
akumulasi dari mutasi ini.
Gambar 2.6 Perkembangan menuju karsinoma8
Defek pada gen APC yang merupakan pertama kali dideskripsikan pada pasien dengan FAP.
Dengan meneliti dari populasi ini, maka karakteristik mutasi dari gen APC dapat diidentifikasi.
Mereka sekarang diketahui ada dalam 80% kasus sporadik kanker kolorektal. Gen APC merupakan
gen supresi tumor. Mutasi pada setiap alel diperlukan untuk pembentukan polip. Mayoritas dari
mutasi ialah prematur stop kodon yang menghasilkan truncated APC protein. Inaktivasi APC
sendiri tidak menghasilkan karsinoma. Akan tetapi, mutasi ini menyebabkan akumulasi kerusakan
genetik yang menghasilkan keganasan. Tambahan mutasi pada jalur ini ialah aktivasi onkogen K-
ras dan hilangnya gen supresi tumor DCC dan p53.
K-ras diklasifikasikan sebagai proto onkogen karena mutasi 1 alel siklus sel. Gen K-ras
menghasilkan produk G protein yang akan menyebabkan transduksi signal intraceluler. Ketika aktif,
K-ras berikatan dengan guanosine triphosphate (GTP) yang dihidrolisis menjadi guanosis
diphosphate (GDP) kemudian menginaktivasi G protein. Mutasi K-ras menyebabkan
ketidakmampuan dalam hidrolisis GTP yang menyebabkan G protein aktiv secara permanen. Hal
ini yang menyebabkan pemecahan sel yang tidak terkontrol.
DCC ialah gen supresi tumor dan kehilangan semua alelnya diperlukan untuk degenerasi
keganasan, mutasi DCC terjadi pada lebih dari 70% kasus karsinoma kolorektal dan memiliki
prognosis negatif. Gen supresi tumor p-53 sudah banyak dikarakteristikan dalam banyak keganasan.

Protein p53 penting untuk menginisiasi apoptosis dalam sel pada kerusakan genetik yang tidak
dapat diperbaiki. Mutasi p53 diperlihatkan dalam 75% kasus.
Gambar 2.7 Perubahan genetik dan gambaran klinis9
Jalur genetik
Terdapat 2 jalur utama dalam inisasi dan progesi dari tumor yaitu jalur LOH dan jalur
replication error (RER). Jalur LOH dikarakteristikan dengan delesi pada kromosom dan tumor
aneuploidi. 80% dari karsinoma kolorektal merupakan mutasi dari jalur LOH, sisanya merupakan
mutasi jalur RER yang dikarakteristikan dengan kesalahan pasangan sewaktu replikasi DNA.
Beberapa gen sudah diidentifikasi sebagai sesuatu yang penting dalam mengenali dan memperbaiki
kesalahan replikasi. Kesalahan pencocokan gen yaitu include hMSH2, hMLH1, hPMS1, hPMS2,
dan hMSH6/GTBP. Mutasi satu dari beberapa gen ini merupakan predisposisi dalam mutasi sel
yang dapat terjadi pada proto onkogen ataupun gen supresi tumor.
Jalur RER berhubungan dengan instabilitasi mikrosatelit. Tumor dengan instabilitas
mikrosateliti memiliki karakteristik yang berbeda dari jalur LOH. Tumor ini lebih banyak terdapaat

pada bagian kanan dan memiliki prognosis yang lebih baik. Tumor yang berasal dari LOH terjadi
pada kolon distal dan berprognosis lebih buruk.6
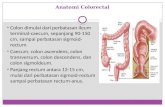
Kanker kolon dan rectum terutama (95%) adenokarsinoma (muncul dari lapisan epitel usus)
dimulai sebagai polip jinak tetapi dapat menjadi ganas dan menyusup serta merusak jaringan
normal serta meluas ke dalam struktur sekitarnya. Sel kanker dapat terlepas dari tumor primer dan
menyebar ke dalam tubuh yang lain (paling sering ke hati).
Neoplasma primer à adenokarsinoma
Secara makroskopik terdapat tiga tipe karsinoma kolon dan rektum, yaitu :
1. Tipe polipoid atau vegetatif yang tumbuh menonjol kedalam lumen usus, berbentuk kembang
kol dan ditemukan terutama di daerah sekum dan kolon asendens.
2. Tipe skirus mengakibatkan penyempitan sehingga terjadi stenosis dan gejala obstruksi,
terutama ditemukan di daerah kolon desendens, sigmoid dan rektum.
3. Bentuk ulseratif terjadi karena nekrosis di bagian sentral terdapat di rektum.
Pada tahap lanjut sebagian besar karsinoma kolon mengalami ulserasi menjadi tukak
maligna.6
Berbagai varian gambaran histopatologi kanker kolorektal berdasarkan klasifikasi World
Health Organization:
- Mucinous adenocarcinoma
- Signet ring cell adenocarcinoma
- Adenoskuamous carcinoma
- Squamous carcinoma
- Choriocarcionma
- Medullary carcinoma10
Manifestasi klinis
Usus besar secara klinis dibagi menjadi belahan kiri dan kanan sejalan dengan suplai darah
yang diterima. Arteri mesenterika superior memperdarahi belahan bagian kanan (caecum, kolon
ascendens dan duapertiga proksimal kolon transversum), dan arteri mesenterika inferior yang
memperdarahi belahan kiri (sepertiga distal kolon transversum, kolon descendens dan sigmoid, dan
bagian proksimal rektum). Tanda dan gejala dari kanker kolon sangat bervariasi dan tidak spesifik.
Keluhan utama pasien dengan kanker kolorektal berhubungan dengan besar dan lokasi dari tumor.
Kolon kanan memiliki kaliber yang besar, tipis dan dinding distensi serta isi fecal ialah air.
Karena fitur anatomisnya, karsinoma kolon kanan dapat tumbuh besar sebelum terdiagnosa. Pasien

sering mengeluh lemah karena anemia. Darah makroskopis sering tidak tampak pada feses tetapi
dapat mendeteksi tes darah samar. Pasien dapat mengeluh ketidaknyamanan pada kuadran kanan
perut setelah makan dan sering salah diagnosa dengan penyakit gastrointestinal dan kandung
empedu. Jarang sekali terjadi obstruksi dan gangguan berkemih.
Kolon kiri memiliki lumen yang lebih kecil dari yang kanan dan konsistensi feses ialah
semisolid. Tumor dari kolon kiri dapat secara gradual mengoklusi lumen yang menyebabkan
gangguan pola defekasi yaitu konstipasi atau peningkatan frekuensi BAB. Pendarahan dari anus
sering namun jarang yang masif. Feses dapat diliputi atau tercampur dengan darah merah atau
hitam. Serta sering keluar mukus bersamaan dengan gumpalan darah atau feses.
Pada kanker rektum, gejala utama yang terjadi ialah hematokezia. Perdarahan seringkali
terjadi persisten. Darah dapat tercampur dengan feses atau mukus. Pada pasien dengan perdarahan
rektal pada usia pertengahan atau tua, walaupun ada hemoroid, kanker tetap harus dipikirkan.
Gejala akut dari pasien biasanya adalah obstruksi atau perforasi, sehingga jika ditemukan
pasien usia lanjut dengan gejala obstruksi, maka kemungkinan besar penyebabnya adalah kanker.
Obstruksi total muncul pada < 10% pasien dengan kanker kolon, tetapi hal ini adalah sebuah
keadaan darurat yang membutuhkan penegakan diagnosis secara cepat dan penanganan bedah.
Pasien dengan total obstruksi mungkin mengeluh tidak bisa flatus atau buang air besar, kram perut
dan perut yang menegang. Jika obstruksi tersebut tidak mendapat terapi maka akan terjadi iskemia
dan nekrosis kolon, lebih jauh lagi nekrosis akan menyebabkan peritonitis dan sepsis. Perforasi juga
dapat terjadi pada tumor primer, dan hal ini dapat disalah artikan sebagai akut divertikulosis.
Perforasi juga bisa terjadi pada vesika urinaria atau vagina dan dapat menunjukkan tanda tanda
pneumaturia dan fecaluria. Metastasis ke hepar dapat menyebabkan pruritus dan jaundice, dan yang
sangat disayangkan hal ini biasanya merupakan gejala pertama kali yang muncul dari kanker kolon.

Gambar Distribusi kanker kolorektal menurut lokasi sebanyak 73% dapat dideteksi dengan
pemeriksaan rektosigmoidoskopi (data unit endoskopi, Divisi Departemen Ilmu penyakit Dalam
FKUI/RSCM, Jakarta 2005)
Gejala-gejala yang timbul pada karsinoma kolorektal
Kolon kanan :
- Kelemahan yang tidak dapat dijelaskan / anemia
- Tes darah samar pada feses
- Gejala dispepsia
- Ketidaknyamanan abdomen kanan persisten
- Teraba massa abdominal
Kolon kiri :
- Gangguan pola buang air besar
- Darah makro pada feses
- Gejala obstruksi
Rektum :
- Pendarahan per rektal
- Gangguan pola buang air
- Adanya sensasi tidak lampias
- Teraba tumor intrarectal5
Tabel Gambaran klinis karsinoma kolorektal
KOLON KANAN KOLON KIRI REKTUM
ASPEK KLINIS Kolitis Obstruksi Proktitis
NYERI Karena penyusupan Obstruksi Obstruksi
DEFEKASI Diare/diare berkala Konstipasi progresif Tenesmi terus menerus
OBSTRUKSI Jarang Hampir selalu Hampir selalu
DARAH PADA
FESES
Samar Samar/makroskopik Makroskopik
FESES Normal/diare berkala Normal Perubahan bentuk
DISPEPSIA Sering Jarang Jarang
ANEMIA Hampir selalu Lambat Lambat
MEMBURUKNYA Hampir selalu Lambat Lambat

KEADAAN UMUM
Staging tumor menurut TNM
Prognosis dari pasien dari pasien kanker kolorektal berhubungan dengan dalamnya penetrasi
tumor ke dinding kolon, keterlibatan kelenjar getah bening regional atau metastasis jauh. Semua
variabel ini digabung sehingga dapat ditentukan sistem staging yang awalnya diperhatikan oleh
Dukes.
Dan diaplikasi dalam metode klasifikasi TNM dalam hal ini, T menunjukkan kedalaman
penetrasi tumor, N menandakan keterlibatan kelenjar getah bening dan M ada tidaknya metastase
jauh.
Lesi superfisial yang tidak mencapai lapisan muskularis atau kelenjar getah bening (KGB)
dianggap sebagai stadium A (T1N0M0). Bila tumor yang masuk lebih dalam namun tidak menyebar
ke KGB dikelompokkan sebagai stadium B1 (T2N0M0). Bila tumor terbatas sampai lapisan
muskularis disebut stadium B2 (T3N0M0). Bila tumor menginfiltrasi serosa dan KGB disebut
stadium C (TXN1M0), bila terdapat status anak sebar di hati, paru, atau tulang mempertegas stadium
D (TXNXM1). Bila status metastasis belum dapat dipastikan maka sulit menentukan stadium. Oleh
karena itu, pemeriksaan mikroskopik terhadap spesimen bedah sangat penting dalam menentukan
stadium. Umumnya rekurensi kanker kolorektal terjadi dalam 4 tahun setelah pembedahan sehingga
harapan hidup rata-rata 5 tahun dapat menjadi indikator kesembuhan. Indikator buruknya prognosis
prognosis kanker kolorektal setelah menjalani operasi.
Kanker kolorektal umumnya menyebar ke kelenjar getah bening regional atau ke hati
melalui sirkulasi vena portal. Hati merupakan organ yang paling sering mendapat anak sebar
kelenjar getah bening. Sepertiga kasus kanker kolorektal yang rekuren disertai metastase ke hati dan
duapertiga pasien kanker kolorektal ditemukan metastase ke hati pada waktu meninggal. Kanker
kolorektal jarang bermetastasis ke paru. KGB superklavikula tulang atau otak tanpa ditemukan anak
sebar di hati terlebih dahulu. Pengecualian terjadi bilamana tumor dapat terletak di distal rektum, sel
tumor dapat menyebar melalui pleksus vena paravertebra kemudian dapat mencapai paru atau KGB
superklavikula tanpa melalui sistem vena porta. Rata-rata harapan hidup setelah ditemukan
metastase berkisar 6 – 9 bulan (hepatomegali dan gangguan pada hati) atau 20-30 bulan (nodul kecil
di hati yang ditandai oleh peningkatan CEA dan gambaran CT-scan).
T – Tumor primer
Tx: Tumor primer tidak dapat dinilai
T0: Tidak ada tumor primer
Tis: Karsinoma insitu, invasi lamina propia atau intraepitelial
T1: Invasi tumor di lapisan sub-mukosa

T2: Invasi tumor di lapisan otot propria
T3: Invasi tumor melewati otot propria ke subserosa atau masuk ke perikolik yang
tidak dilapisi peritoneum atau perirektal
T4: Invasi tumor terhadap organ/struktur sekitarnya dan/atau peritoneum viseral.
Gambar 2.9 Gambaran kedalaman tumor
N – Kelenjar limfe regional
Nx: Kelenjar limfe regional tidak dapat dinilai
N0: Tidak didapatkan kelenjar limfe regional
N1: Metastase di 1 – 3 kelenjar limfe perikolik atau perirektal
N2: Metastase di 4 atau lebih kelenjar limfe perikolik atau perirektal
N3: Metastase pada kelenjar limfe sesuai nama pembuluh darah dan atau pada
kelenjar apikal (bila diberi tanda oleh ahli bedah).
M – Metastase jauh
Mx: Metastase jauh tidak dapat dinilai
M0: Tidak ada metastase jauh
M1: Terdapat metastase jauh6
Tabel 2.3. Stadium dan Prognosis Kanker Kolorektal6,7
Stadium Deskripsi histopatologis
Bertahan 5 tahun (%)Dukes TNM Derajat
A T1N0M0 I Kanker terbatas pada
mukosa/submukosa
>90
B1 T2N0M0 I Kanker mencapai muskularis
85
B1 T3N0M0 II Kanker cenderung masuk atau
melewati lapisan
70-80

serosaC TxN1M0 III Metastasis 35-65D TxNxM1 IV 5