El Amaranthus palmeri (S. Wast) ya está con nosotrosINTA Centro Regional Chaco Formosa Estación...
Transcript of El Amaranthus palmeri (S. Wast) ya está con nosotrosINTA Centro Regional Chaco Formosa Estación...

INTA Centro Regional Chaco Formosa Estación Experimental Agropecuaria Sáenz Peña Ruta 95 km 1108. Provincia de Chaco. CP 3700. Argentina. www.inta.gob.ar/saenzpena
1
El Amaranthus palmeri (S. Wast) ya está con nosotros
Recopilación: Ing. Agr. Graciela Guevara Especialista en malezas. Grupo Agronomía, Área Investigación en Recursos Naturales.1
Introducción La introducción y difusión de especies no deseadas en los campos se debe al movimiento de propágulos (semillas, rizomas, bulbos, estolones) por medio del agua, animales (aves, artrópodos, pequeños mamífero) y por la actividad del hombre mediante el uso de la maquinaria agrícola, como sembradoras, cosechadoras y la siembra del cultivo con presencia de semillas de malezas. En la campaña 2011/12 se detectó en el SW de Córdoba, la presencia de A. palmeri, presumiblemente introducida con semilla de alfalfa de los Estados Unidos. A pesar de ser una especie exótica, presentó rápida difusión, debido a la difícil identificación al estado de plántula de los otros Amaranthus presentes en nuestros sistemas agrícolas. Durante la campaña 2014/15 ya ha sido detectada y confirmada la presencia de la especie en la provincia del Chaco. Esta especie como los otros “yuyos colorado”, pertenece a la familia de las Amarantaceas. Originaria del hemisferio Norte, Desierto de Sonora y valle del Río Grande (Texas) (Ehleringer, 1983; Keely, 1987), muy difundida en los Estados del Sur de Estados Unidos en cultivos de algodón, soja y maíz. Especie muy adaptable e invasiva. Anual se multiplica por semillas. A diferencia de las especies de Amaranthus presentes en el país, es una especie diclino dioica (flores femeninas y masculinas en distintas plantas). El primer paso y más crítico en un programa de manejo de malezas es identificar las especies presentes en el lote, debido al comportamiento diferencial a los herbicidas empleados. El A. palmeri, es difícil identificarlo a simple vista de las otras especies del género. Para su correcta identificación a continuación se describen diferentes características de la especie. Que si bien, ayudan a su identificación, muchas veces pueden variar dentro de una misma especie; incluso dentro de la misma población; por lo tanto, siempre se debe observar más de un individuo. Para la diferenciación de la especie existen varias características a tener presente:
• Presencia de pelos • Forma de la hoja • Longitud del pecíolo • Patrón de crecimiento del meristema apical • Estructuras florales • Manchas en las hojas • Presencia de un pelo en la parte apical de la hoja.
La comprensión de estas característica permitirá la correcta identificación de la especie y sobre todo a diferenciar al A. hybridus, también con resistencia a glifosato confirmada, para luego determinar las estrategias de manejo más apropiadas.
1 [email protected] Tel: (0364) 4438141.

INTA Centro Regional Chaco Formosa Estación Experimental Agropecuaria Sáenz Peña Ruta 95 km 1108. Provincia de Chaco. CP 3700. Argentina. www.inta.gob.ar/saenzpena
2
Descripción de la especie
Presencia de pelos
Amaranthus palmeri sin pubescencia Amaranthus hybridus con pubescencia
Plántula: Cotiledones estrechos y verdes en la cara superior y rojizo en el envés.
Hipocotilo (porción del tallo por debajo de los cotiledones) liso o ligeramente
pubescente. Figuras 1 y 2
Estado vegetativo: El aspecto es muy variable.
Hojas redondeadas, con pecíolo más largo que la lámina de la hoja, Figura 3, agrupadas
en la parte superior como resultado del patrón de crecimiento del meristema apical,
que crece de forma tal, de
captar la mayor cantidad de luz
posible. Presenta una
apariencia de roseta Figura 4.
Las hojas pueden presentar o
no una mancha blanca en
forma de V. Figura 5 y presencia
de pelo en el ápice Figura 6.
Figura 3. Pecíolo de la hoja más largo que la lámina
Figura 1. Plántula
Figura 2. Plántula

INTA Centro Regional Chaco Formosa Estación Experimental Agropecuaria Sáenz Peña Ruta 95 km 1108. Provincia de Chaco. CP 3700. Argentina. www.inta.gob.ar/saenzpena
3
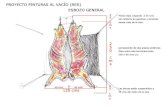
Planta adulta: Tallos erectos de 0,5-1,5 m de altura, ramas ascendentes. Inflorescencias terminales, espigas lineales en panículas colgantes, de vez en cuando levantadas, sobre todo las jóvenes Figura 7. Semillas marrón rojizo oscuro a marrón, brillantes que puede alcanzar hasta 600.000 semillas por planta
Como característica distinguible, presenta flores femeninas y masculinas en distintas plantas. Inflorescencia largas y casi sin ramificaciones. Las femeninas con brácteas espinosas al tacto hasta de 90 cm de longitud Figura 8 y las masculinas suaves al tacto que desprenden abundante polen cuando se las mueve Figura 9
Planta femenina
Planta masculina
Figura 4. Hábito de crecimiento Figura 5. Individuos con hojas con manchas blancas
Figura 6. Pelo en el ápice de la lámina

INTA Centro Regional Chaco Formosa Estación Experimental Agropecuaria Sáenz Peña Ruta 95 km 1108. Provincia de Chaco. CP 3700. Argentina. www.inta.gob.ar/saenzpena
4
Figura 7. A la izquierda inflorescencia femeninas y a la derecha las masculinas
Figura 8. Flores femeninas con brácteas Figura 9. Flores masculinas Espinosas Características fisiológicas que la hacen muy efici ente y competitiva Especie adaptada a altas temperaturas y precipitaciones escasas e imprevisibles (Ehleringer, 1983). Vía fotosintética C4 con muy alta tasa metabólica (incluso más alto que la mayoría de las otras especies C4). La temperatura óptima de fotosíntesis es de 35 a 46ºC, muy resistente a sequía y eficiente en el uso del agua, el movimiento diurno de las hojas mantiene a la lámina perpendicular al sol para la máxima fijación de carbono. En condiciones ideales de crecimiento puede alcanzar entre los 5 y 8 cm por día.
Las semillas son pequeñas y las condiciones de siembra directa les favorecen porque permanecen en los primeros 2,5 cm del suelo. La rápida germinación, le permite emerger, crecer y completar el ciclo de vida con la humedad disponible al momento de la germinación (Ehleringer, 1983). En pruebas de laboratorio, germinan en 1-2 días en una amplia gama de temperatura entre 15-40,5ºC, con el mayor porcentaje entre los 30-35ºC (Steckel et al, 2004; Guo y Al-Khatib, 2003). Al ser una especie desértica, el requisito fundamental para germinar es la humedad. Experiencias en Alabama y Georgia (Langcuster, 2008) demostraron que las semillas pierden viabilidad a los 3 años de ser enterradas.
Los individuos detectados en la Argentina, muestran resistencia a herbicidas
inhibidores de ALS (sulfonilureas, imidazolinonas, triazolpirimidinas), aunque en Estados Unidos tiene resistencia múltiple a inhibidores de EPSPS (glifosato), ALS, fotosistema II (triazinas, ureas sustituidas).
Al ser una especie dioica se facilita el cruzamiento y la diversidad genética, que le
permite la habilidad de una rápida adaptación y dispersión de los genes de resistencia cuando se aplica una presión de selección.
Impacto de Amaranthus palmeri en la producción agrí cola
• Reducción significativa de rendimientos en todos los cultivos, fundamentalmente cuando emerge antes o conjuntamente con el cultivo (algodón, soja, maíz).
• Efecto alelopático sobre algunos cultivos. • Incrementa la complejidad y los costos de control de malezas. • Compromete el éxito de la siembra directa.

INTA Centro Regional Chaco Formosa Estación Experimental Agropecuaria Sáenz Peña Ruta 95 km 1108. Provincia de Chaco. CP 3700. Argentina. www.inta.gob.ar/saenzpena
5
Manejo
• Usar herbicidas con diferentes mecanismos y modo de acción, para disminuir la presión de selección y con poder residual.
• Rotación de cultivos, para cortar el ciclo de la maleza. • Entierro de semillas, dado que pierden viabilidad rápidamente. • Cultivos de cobertura. • Eliminación manual de individuos que aparecen inicialmente o que escapan al control
para evitar la producción de semilla que incrementan el banco de semillas del suelo. • Monitorear áreas no cultivadas (banquinas y alambrados). • Carpida de plantas aisladas antes de la producción de semillas. • Cosechar al final los lotes con alta infestación de la maleza. • Tolerancia cero.
Herbicidas que controlan Amaranthus palmeri A continuación se mencionan los diferentes herbicidas para los cultivos más representativos de la región con sus mecanismos de acción. Herbicidas para Algodón
Principio Activo Nombre Comercial Sitio de Acción
Presiembra Quemado Flumioxazin amaranto < 2,5 cm Sumisoya Inhibidor PPO Diuron amaranto < 12 cm y al menos 10 días antes de siembra
Varios Fotosistema II
Diuron + Flumioxazin amaranto de 2,5 a 12 cm
Varios Sumisoya
Fotosistema II Inhibidor PPO
Pre-emergencia
Acetoclor + Diuron Varios Inhibidor de Ac. grasos de cadena larga Fotosistema II
S-Metolaclor + Diuron Inhibidor de Ac. grasos de cadena larga Fotosistema II
Fomesafen + S-Metolaclor Eddus Inhibidor de PPO Inhibidor de Ac. grasos de cadena larga
Fomesafen + Diuron Flex Varios
Inhibidor PPO Fotosistema II
Post -emergencia
Glifosato + S-Metolaclor Varios Inhibidor EPSP Inhibidor de Ac. grasos de cadena larga
Glifosato + Acetoclor Varios Inhibidor EPSP Inhibidor de Ac. grasos de cadena larga
PREVENCIÓN es mucho mejor que erradicación

INTA Centro Regional Chaco Formosa Estación Experimental Agropecuaria Sáenz Peña Ruta 95 km 1108. Provincia de Chaco. CP 3700. Argentina. www.inta.gob.ar/saenzpena
6
Herbicidas para Soja Mezcla de herbicidas para el quemado en presiembra Principio Activo Nombre Comercial Sitio de Acción
Glifosato + 2,4-D Varios Inhibidor enzima EPSPS, regulador de crecimiento
Glifosato + Dicamba Varios Inhibidor enzima EPSPS, regulador de crecimiento
Paraquat + Metribuzin Varios Fotosistema I Fotosistema II
Glufosinato Liberty Inhibición enzima glutamino sintetasa.
Saflufenacil Heat Fotosistema I Flumioxazin Sumisoya, otros Inhibidor PPO Herbicidas Pre -emergentes Sulfentrazone Varios Inhibidor PPO
Metribuzin + Clorimuron etil Sencorex Duo Fotosistema II Inhibición enzima ALS
Flumioxazin Sumisoya Inhibidor PPO Fomesafen Flex Inhibidor PPO
Fomesafen + S-metolaclor Eddus Inhibidor PPO Inhibidor de Ac. grasos de cadena larga
Herbicidas de Post -emergencia Fomesafen Flex Inhibidor PPO
Fomesafen + S-metolaclor Eddus Inhibidor PPO Inhibidor de Ac. grasos de cadena larga
Lactofen Cobra Inhibidor PPO Glufosinato de Amonio Liberty Inhibición glutamino sintetasa Herbicidas para Maíz Principio Activo Nombre Comercial Sitio de Acción Preemergencia Atrazina Varios Fotosistema II Isoxaflutole Fordor Inhibidor de pigmentos Isoxaflutole+Thiencarbazone metil+Cyprosulfamide Adengo
Inhibidor de pigmentos Inhibidor ALS
Atrazina +S-Metolaclor Bicepack Gold Fotosistema II Inhibidor de ac. Grasos de cadena larga
S-Metolaclor Varios Inhibidor de Ac. grasos de cadena larga
Post -emergencia 2,4-D Varios Regulador de crecimiento Dicamba Varios Regulador de crecimiento Mesotrione Callisto Inhibidor de pigmentos Tropamezone Convey Inhibidor de pigmentos
Glufosinato Liberty, otros Inhibición enzima glutamino sintetasa.

INTA Centro Regional Chaco Formosa Estación Experimental Agropecuaria Sáenz Peña Ruta 95 km 1108. Provincia de Chaco. CP 3700. Argentina. www.inta.gob.ar/saenzpena
7
Referencias Aaron Hager. Renam vigilant for Palmer Amaranth. The Bulletin pest management and crops development
information for Illinois. http://bulletin.ipm.illinois.edu/?p=2754 Amaranthus plameri. Http://www.aapresid.org.ar/rem/amaranthus-palmeri/. Ackley Bruce, Mark Loux. Quick Identification of Pigweed/Amaranth in Ohio.
http://www.chesco.org/DocumentCenter/View/13996 de Andrade Edson Ricardo Junior, Aderson Luis Cavenahi, Sabastião Carneiro Guimarãres, Saul Jorge
Pinto de Carvalho. Primeiro relato de Amaranthus palmeri no Brasil em áreas agrícolas no estado de Mato Grosso. Circular Técnica IMATmt. Instituto Mato-Grossense do algodão. http://www.hrac-br.com.br/wordpress/wp-content/uploads/2015/06/CircularTecnica19IMAmt.pdf
Bond Jason, Ton Enbark, Ken Smith and Bob Scott. Glyphosate-Resistant Palmer Amaranth and
Ryegrass management. Mafes – University Arkansas Division of Agriculture. http://msucares.com/pubs/ubfisgeets_research/i1351.pdf.
Glyphosate-Resistant Population of Amanthus palemri prove difficult to control in the Southern United
State. http://www.cottonic.com/fiber/AgriculturalDisciplines/Weed-Management/glyphosate-Resistan-Poplations/vs-gluphosat-Resistant-Populations.pdf.
Hager Aarib G. Management of Palmer amaranth in Illinois. University of Illinois. Weed Science. Department of crops science. http://bulletin.ipm.illinois.edu/wp-content/uplloads/2014/05/PalmerAmaran-2014-HI.pdf.
Hartzler Bob, Meaghan Bryan.2013 Palmer Amanatnht. A new threat.
http://www.weeds.iastate.edu/mgmt/2013/palmerposterB.pdf Hopkins Matt Undestanding the trhreat of Palmer Amaranth Managemente Recommendations for the 2014
season. http://www.croplife.com/crop-imputs/herbicides/undestanding-thethreat-of-palmer-amaranth-management-recomendations-forthe2014-season.
Johnson Bill and Travis Lagleiter and. Palmer Amaranth Identificacion. Purdue University.
https://www.youtube.com/watch?v=aVbgPGg0GO0. Legleiter Travis and Bill Johnson. Scout and identify pigweed species now. Purdue Weed Science.
http://articles.extensión.org/pages/65209/palmer-amaranth-amaranthus-palmeri. Legleiter Travis, Bill Johnson. Palmer Amaranth biology, identification, and management. Purdue
Extension. WSSI. https://www.extension.purdue.edu/extmedia/WS/WS-51-W.pdf Morichetti Sergio, Jason Ferrell y Ramon Leon. Amaranthus palmeri: Palmer Amaranth. University of
Florida. IFAS Extension. SS-AG-336. https://edis.ifas.ufl.edu/pdffiles/AG/AG34600.pdf MP44 Arkansas 2016. Recommended chemicals for weed and brush control. Division of Agriculture
Research & Extension- University of Arkansas System Cotton 34-42 pp. https://www.uaex.edu/publications/pdf/mp44/mp44.pdf
Palmer Amaranth: Amaranthus palmeri. Virginia Tech Weed Identification Guide. http://oak.ppws.vt.edi/~flessner/weedguide/amapa.htm.
Pratt Donald B., Micheal D.K.Owen, Lynn G. Clark, Anna Gardnes. Identification of the wedy pigweeds
and waterhemps of Iowa. PM 1786.pdf. http://store.extension.iastate.edu/.../1786.pdf. Schonbeck Mark. Palmer Amaranth (Amaranthus palmeri).
http://articles.extensión.org/pages/65209/palmer-amaranth-amaranthus-palmeri. Schonbeck Mark. Weed profile: Pigweeds (Amaranthus spp.).
http://article.extension.org/pages/65208/weed-profile:-pigweeds-amarnthus-spp. Schonbeck Mark. Redrood Pigweed (Amaranthus retroflexus), Smooth Pigweed (A. hybridus) and Powell
Amaranth (A. powelli). Virginia Extension. http://article.extension.org/pages/68434/redroot-pigweed-amaranthus-retroflexus-smoth-pigweed-a-hybridus-and-powell-amaranth-apowelli.
Show David R., Stanley Culpepper, Michel Owen, Andrew Price. 2013. Las Malezas resistentes de
herbicidas son una amenaza para los avances logrados en la conservación del suelo: Cómo encontrar un equilibrio para la sustentabilidad del suelo y los predios agrícolas. CAST, Issue. Paper Número 49 SPA. www.sej.org/.../malezas-resistentes-hherbicida-amenaza.

INTA Centro Regional Chaco Formosa Estación Experimental Agropecuaria Sáenz Peña Ruta 95 km 1108. Provincia de Chaco. CP 3700. Argentina. www.inta.gob.ar/saenzpena
8
Sosnoskie Lynn M.; Theodore M. Webster, A. Stanley Culpepper, Jeremy Kichler. The biology and
Ecology of Palmer Amaranth. Implications for control. UGA Extension. http://extension.uga.edu/publications/files/pdf/C%201000_2.PDF
Steckel Larry. Mature pigweed identification cv Extension w072.
http://extension.tennessee.edu/publications/Documents/W072.pd The rise of superweeds-and what to do about it (2013). Union of Concerned Scientists. Diciembre 2013.
http://www.ncsusa.org/food_and_agriculture/our-failing-food-system/industria-agriculture/the-rise-of-superweeds
Tuesca Daniel, Juan Carlos Papa y Sergio Morichetti. Amaranthus palmeri, una malezas arribada a
nuestro país desde e hemisferios norte. http://inta.gob.ar/sites/default/files/scruot-temp-inta-alerta-amaranthus-palmeri
2013 Weed control manual for Tennessee. Field cops-Forage crops- Pastures – Farmer Pigweed
identification. A pectorial guide to the common pigweed of the great plains. Kansas State University Agricultural Experimental Station and Coopeativa Extension Service. http://www.boskstore.ksre.ksn.edu/pubs/s80.pdf.
2016 Weed control manual for Tennessee. Field crop Forage crops Pastures Farm ponds Harvest aid.
Cotton 27-36. http://extension.tennessee.edu/publication/Documents/PB1580.pdf