Développement et maturation des cellules lymphocytaires I- Les cellules B.
-
Upload
chretien-roche -
Category
Documents
-
view
114 -
download
0
Transcript of Développement et maturation des cellules lymphocytaires I- Les cellules B.

Développement et maturation des cellules lymphocytaires
I- Les cellules B

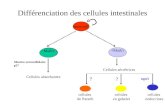
Développement des cellules B dans la moelle osseuse
BRégule la construction d’un récepteur antigène
Vérifie que chaque cellule n’a qu’une seule spécificitéB
Vérifie que les cellules B ne sont pas auto-réactives
B
Exporte des cellules à la périphérieB
Site de production d’anticorpsB

Cellules B Immatures & matures
Sinus Central
Progéniteurs Pré-B
Cellules du Stroma
X
X
X
Endoosteum
Macrophage
Schéma du développement des cellules B

Sécrétion de facteurs de croissance CYTOKINES
2. Sécrétion de cytokines par les cellules du stroma
B
Les cellules du stroma nourrissent les cellules B en développement
Différents contacts cellulaires et différents types de cytokines sont nécessaires à chaque étape de la
différentiation
Cellules du stroma
1. Contact cellulaire spécifique entre les cellules du stroma et les cellules B
Contact cellulaire

Cellules du stroma
Cellules B en développement

B
B
Stromal cell

Périphérie
Les étapes de la maturation des cellules B
Cellules souches
pro-B précoces
pro-B tardifs
grandes pré-B
petites pré-B Immature B Cellules B matures
Chaque étape du développement est définit par des réarrangements des gènes codant pour les chaînes lourdes et
légères des Ig, l’expression d’Ig de surface, l’expression de molécules d’adhésion et des récepteurs de cytokines

pro-B précoce
KitRécepteur Tyrosinekinase
Facteurde cellules souchesFacteur de croissance lié à la cellule
VLA-4(Integrine)
Cellule souche
Les différentes cytokines et les différents contacts cellulaires à chaque étape de la différentiation
Cellules du stroma
molécules d’adhésion cellulaire
VCAM-1(Ig superfamille)

pro-B précoce
récepteurInterleukin-7
Cellule du stroma
pro-B tardif
Pré-B
Interleukin-7Facteur de croissance
Les différentes cytokines et les différents contacts cellulaires à chaque étape de la différentiation

Les étapes de la différentiation sont définies par le réarrangement des gènes des Ig
CELLULES B
CONFIGURATION Des gènes IgH
cellule souche
pro-B précoce
pro-B tardif
grande pre-B
Gène original
DH - JH VH - DHJH VHDHJHExpressio
n du récepteur
Pré-B
Les gènes de chaînes légères n’ont pas encore été réarrangés

B cell receptor
Expression transitoire lorsque VHDHJH CH est réarrangé
VpreB/l5 – est nécessaire pour l’expression à la surface
Ig & Ig Impliquées dans la Transduction du signal
CH
Chaîne lourdeVHDHJH
chaîne légèreVLJLCL
VpréB
l5
Les ligands se fixant sur les récepteurs des cellules pre-B peuvent être: galectine 1, sulfate d’héparine, autre pre-BCR
Pre-

Fixation du récepteur des cellules pre-B
1. Assure une seule spécificité anticorps par cellule
Grande Pre-B
Cellule du stroma
ligand du récepteur des cellules pré-B
2. Contrôle l’entrée dans le cycle cellulaire
EXCLUSION ALLELIQUE L’expression d’un gène sur un chromosome empêche l’expression de
l’allèle sur l’autre chromosome
1. Empêche d’autre réarrangements des gènes de la chaîne lourde
2. Permet le développement des cellules pre-B possédant des jonctions VHDHJH dans un cadre de lecture correct

L’exclusion allélique empêche des réponses indésirables
Empêche d’autres réarrangements des gènes des chaînes lourdes assurant une seule et unique spécificité anticorps par cellule
Empêche l’induction d’une réponse non désirée par des pathogènes
Y Y
YYYB
S. aureus
Un récepteur Ag par cellule
Y
Y Y
Y
Y Y Y
Anticorps anti S. aureus
YY
Y YBauto antigèneExprimé par une cellule
de l’organisme (neurone)
S. aureus YY
Y
Y YY Y
YY YY Y Y
Si deux récepteurs Ag par cellule
Anticorps anti neurone Anticorps anti S. aureus

L’exclusion allélique permet la sélection clonale
Toutes les cellules doivent exprimer la même spécificité anticorps sinon la spécificité de la réponse immunitaire est compromise
Comme d’autres réarrangements de gènes de la chaîne H ne peuvent avoir lieu l’émergence d’autre spécificités anticorps dans les cellules sœurs est empêchée après la sélection clonale
S. typhiS. typhi

L’exclusion allélique permet d’avoir un répertoire complet
Ig anti-neurone
B
Exclusion des cellules B anti-neurone i.e. auto-tolérance
YYBB
Un récepteur Ag par cellule
B
Délétion Anergie
OU
B
Ig anti-neuroneET
Ig anti-S. aureusYYY
Si deux récepteurs Ag par cellule
S. aureus
Les cellules B anti S. aureus seront exclues laissant un répertoire incompletYYY
BB

Fixation du récepteur des cellules pre-B
1. Assure une seule spécificité anticorps par cellule
Grande Pre-B
Cellule du stroma
ligand du récepteur des cellules pré-B
2. Contrôle l’entrée dans le cycle cellulaire
1. Empêche d’autre réarrangements des gènes de la chaîne lourde
2. Permet le développement des cellules pre-B possédant des jonctions VHDHJH dans un cadre de lecture correct

cadre de lecture 1
MKXLWFFLLLVAAPRWVLSQVHLQESGPGLGKPPELKTPLGDTTHTCPRCPEPKSCDTPPPCPRCPEPKSCDTPPPCPRCPEPKSCDTPPPCXXCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDXXVQFKWYVDGVEVHNAKTKLREEQYNSTFRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYNTTPPMLDSDGSFFLYSKLTVDKSRWQQGNIFSCSVMHEALHNRYTQKSLSLSPGK*
séquence nucléotide de IgG3 H humaine
ATGAAACANCTGTGGTTCTTCCTTCTCCTGGTGGCAGCTCCCAGATGGGTCCTGTCCCAGGTGCACCTGCAGGAGTCGGGCCCAGGACTGGGGAAGCCTCCAGAGCTCAAAACCCCACTTGGTGACACAACTCACACATGCCCACGGTGCCCAGAGCCCAAATCTTGTGACACACCTCCCCCGTGCCCACGGTGCCCAGAGCCCAAATCTTGTGACACACCTCCCCCATGCCCACGGTGCCCAGAGCCCAAATCTTGTGACACACCTCCCCCGTGCCCNNNGTGCCCAGCACCTGAACTCTTGGGAGGACCGTCAGTCTTCCTCTTCCCCCCAAAACCCAAGGATACCCTTATGATTTCCCGGACCCCTGAGGTCACGTGCGTGGTGGTGGACGTGAGCCACGAAGACCCNNNNGTCCAGTTCAAGTGGTACGTGGACGGCGTGGAGGTGCATAATGCCAAGACAAAGCTGCGGGAGGAGCAGTACAACAGCACGTTCCGTGTGGTCAGCGTCCTCACCGTCCTGCACCAGGACTGGCTGAACGGCAAGGAGTACAAGTGCAAGGTCTCCAACAAAGCCCTCCCAGCCCCCATCGAGAAAACCATCTCCAAAGCCAAAGGACAGCCCGAGGAGATGACCAAGAACCAAGTCAGCCTGACCTGCCTGGTCAAAGGCTTCTACCCCAGCGACATCGCCGTGGAGTGGGAGAGCAATGGGCAGCCGGAGAACAACTACAACACCACGCCTCCCATGCTGGACTCCGACGGCTCCTTCTTCCTCTACAGCAAGCTCACCGTGGACAAGAGCAGGTGGCAGCAGGGGAACATCTTCTCATGCTCCGTGATGCATGAGGCTCTGCACAACCGCTACACGCAGAAGAGCCTCTCC
CTGTCTCCGGGTAAATGA
Les grandes cellules pré-B nécessitent des jonctions VHDHJH dans le cadre de lecture correct pour devenir matures
cadre de lecture 2(pas de protéine)
*
cadre de lecture 3
ETXVVLPSPGGSSQMGPVPGAPAGVGPRTGEASRAQNPTW*
grandepre-B
Développement continue
récepteur Pre-B peut être activé
Arrêt du développement
Arrêt du développement

GPre-B
GPre-B
LargePre-B
LargePre-B G
Pre-BLargePre-B Large
Pre-BLargePre-B G
Pre-BG
Pre-B
Prolifération
La fixation du récepteur pré-B contrôle l’entrée dans le cycle cellulaire
grandepre-B
Nombreuses grandes pré-B
ayant des récepteurs pré-B
identiques
Large pre-B
chaîne VDJCH intracellulaireRéarrangement VL-JL
Arrêt de la prolifération récepteur Pre-B non pourvus
petite pre-B Y B
Immature
Expression de la chaîne légère : IgM à la
surface
IgM

V D J C
D JV CD J
V CD JV
Lignée germinale
Jonction DH-JH
Jonction VH-DHJH
V J C
V CJV
Lignée germinale
Jonction VL-JL
Les réarrangement des chaînes lourdes et légères génèrent des pertes
grandepré-B
petitepré-B
Deux jonctions aléatoires soit 1/9 de chance d’être dans le cadre de lecture
Une jonction aléatoire, 1/3 de chance d’être dans le cadre de lecture
Au total 1/27 de chance d’être dans le cadre de lecture
Les cellules B qui ne sont pas dans le cadre de lecture arrêtent leur maturation

Les cellules B ont plusieurs possibilités pour réarranger correctement les gènes Ig
Pro B précocePro B tardif Pré B
VH-DJHpremier
chromosome
VH-DJHsecond
chromosome
B Immature
non
oui
non
B
premierchromosome
secondchromosome
premierchromosome
secondchromosome
non
non
non
non
oui
oui
non
oui
oui
oui
oui
YIgM
B
YIgM
B
DH-JH
premierchromosome
DH-JHsecond
chromosome
ouinon

B Y
Y
Y
YB
petite pré-BPas de récepteur Ag à la surfaceIncapable de détecter un Ag dans son environnementPeut être auto-réactive
Cellule B ImmatureIg exprimée à la surfaceCapable de détecter un Ag dans son environnementL’auto-réactivité doit être testée
L’acquisition d’une spécificité antigénique nécessite de vérifier que les auto antigènes ne sont pas reconnus
1. Élimination Physique du répertoire DELETION2. Paralysie des fonctions ANERGY3. Altération de la spécificité RECEPTOR EDITING

Auto-tolérance des cellules B : délétion clonale
cellule B immature reconnaît
des auto Ag MULTIVALENT
B
délétion clonale parapoptose
YYBB
ImmatureB
petitepre-B
petite pre-BAssemble les Ig

Y
B
YY
YB
cellule B anergique
IgD normal IgM faible
cellule B immatures
Reconnaît des auto-Ag soluble
Pas dagglutination
YYBB
ImmatureB
petitepre-B
Petite pré-Bassemble Ig
IgM
IgD
IgD
IgD
Auto-tolérance des cellules B : anergie

Édition des récepteursUn réarrangement codant pour un récepteur spécifique d’un auto antigène peut être remplacé
V CD JVV V
Y
BB!!Récepteur
Reconnaît unAuto antigène!!
B Apoptoseou anergie
YBB
Le nouveau récepteur Reconnaît un antigène
différent et sera testé à nouveau
CD JVV VV
Arrêt du développementet réactivation
de RAG-1 et RAG-2

YY
Y
YY
Y
Cellule B mature exportée à la
périphérie
Y
Y
IgD and IgM normal
IgMIgD
IgD
IgD
IgD
IgMIgM
IgM
cellule B immature
Ne reconnaît aucun auto Ag
YYBB
ImmatureB
petitepre-B
petite pré-Bassemble Ig
B
Auto-tolérance des cellules B : exportation

Production simultanée d’IgM et d’IgD: épissage des ARN
Cm1 Cm2 Cm3 Cm4 Cd1 Cd2 Cd3
pA1V D J
Cm1 Cm2 Cm3 Cm4 Cd1 Cd2 Cd3V D J
AAA
ARN ,coupé et polyadenylation à pA2
V D J Cm IgM mRNA
V D J Cd IgD mRNA
Cg1Cg3CdCmV D J
Cm1 Cm2 Cm3 Cm4 Cd1 Cd2 Cd3 ADNpA1 pA2
V D J
Deux ARNm peuvent être produits par l’utilisation de sites de polyadenylation alternatifs et épissage de l’ARN
ARN épissé et polyadenylation à pA1
AAA

CD21(C3d récepteur)
CD19
CD81(TAPA-1)
IgaIgb
CD45
co-récepteur cellule B
Les co-récepteurs des cellules B

Src (kinase) se lie à CD19phosphorylé
Reconnaissance de l’antigène
Bactérie opsonisée C3d
• Ig membranaire et CD21 sont liés de manière covalente par un antigène qui a activé le complément
C3d se lie à CD21, récepteur 2 du complément (CR2)
P P
• CD21 est phosphorylé et la kinase associée au récepteur phosphoryle CD19
P P
Phosphorylation des Co-récepteurs
• CD19 phosphorylé active d’autres kinases Src
• La fixation du co-récepteur augmente le signal de 1000 -10,000 fois

Différentiation des cellules B à la périphérie
cellule B reconnaîtUn antigène
Du non-soi dans la périphérie
sécrétion d’Ig par les cellules du plasma
YY Y YY YYY Y
B
YY
Y
Y
YYY
BYY
YY
YYYB
Cellule B mature périphérique

Cellules B du plasma
Sw
itch
isot
ype
B
Bcellule B Mature
cellule B Plasma
élevé oui non oui oui oui
faible non oui non non non
Sur
face
Ig
Sur
face
MH
C II
sé
crét
ion
Ig
haut
déb
it
croi
ssan
ce
hype
rmut
atio
n
som
atiq
ue

Circulation des cellules B à travers les organes lymphoïdes
cellules B sanguines
lympheCanal efférent
Zone cellule T
Zone cellule
B

Les antigènesentrent dans les
ganglions par le canal
afférentY
Y
Y
Y
Y
YY
Y
Y
Y
Y
Y
Y
Y
YY
Y
YLes cellules B entrent dans
les ganglions viaveinules endothélialesLes cellules B
prolifèrentrapidement
CENTRE GERMINATIFstructure transitoire
d’intense prolifération
centre germinatifproduction de
cellules Bdifférentiées en
cellules du plasma
Les cellules B circulantes attrapent des antigènes étrangers dans les organes lymphoïdes

Association des antigènes avec les cellules folliculaires dendritiques (FDC)
Les antigènes entrent dans le centre germinatif Sous forme d’un complexe immun avec C3b et des anticorps attachés
récepteur 3 du complémentrécepteur Fcdes Ig
FDC surface
Les dendrites filiformes des FDC développent des perles recouvertes de fines couches de complexes immun
Le complexe immun se fixe aux récepteurs Fc et aux récepteurs du complément sur les FDC

Follicules Primaires se transforment en
follicules secondaireslorsque les centres
germinatifs se développent
zone sombre zone claire B
T
FDC sélectionne les cellules B
Micro-anatomie du centre germinatif
1. Cellules B (centroblastes) répriment les Ig de surface, proliférent et hypermutent
somatiquement leurs gènes IgMATURATION DE L’AFFINITE
2. cellules B (centrocytes) activent lesIg de surface, stoppent leur division et
reçoivent des signaux stimulant descellules T et FDC
3. Apoptose des cellules auto-réactives &
des cellules non sélectionnées
4. Les cellules sélectionnéesquittent la lymphe
soit comme cellules mémoires soit comme cellules plasmatiques

CD5
Deux lignées cellulaires pour les lymphocytes B
B
Précurseur cellule B
B
cellule B mature
cellules B B2
Cellule B du plasma
YY Y YY Y
Y
Y YPC
IgG
B
YYYYY
YYYYY
YYYY
YYYYY
Y
IgM – un seul isotype
B
précurseur cellule B distinct
?
?cellules B B1 cellules B ‘Primitives’

CD5
B
YYYY
Y
YYYY
Y
YYYY
Y
YYYY
Y
IgM
Les cellules B B-1Les IgM utilisent des régions V différentes & en nombre restreint
Reconnaissent des épitopes Ag répétés comme les phospholipides, la phosphotidyl choline & les polysaccharides
Ne font pas partie de la réponse adaptive :pas de mémoire induitepas d’augmentation lors de la 2ème infectionPrésent dès la naissance
Peu de régions de nucléotides N (aléatoires, non codés) dans les IgM
ANTICORPS NATUREL
Produisent des Ig sans l’intervention des cellules T

Comparaison des propriétées des cellules B-1 et B-2
Propriétés B-1 B-2
régions N peu beaucouprégion répertoire V Restreint DiverseLocalisation Péritoine/plèvre partoutRenouvellement auto in situ moelle osseuseproduction spontanée d’Ig élevée faibleIsotypes IgM IgM/G/A/D/ESpécificité polysaccharides oui Rarespécificité protéines Rare ouiBesoin de cellules T Non ouiHypermutation somatique Non élevédeveloppement mémoire Non oui
Oui RareRare OuiNon Oui
Spécificité polysaccharidesSpécificité protéinesBesoin de cellules T
La spécificité & la nécessite de l’aide de cellules T suggèrent que les deux types de cellules B détectent des antigènes différents

Antigènes indépendant des cellules T (TI-2)
cellules B immatures se fixant à des auto Ag
multivalents sont conduits en apoptose
Le répertoire de cellules B-2 est purgé des cellules reconnaissant les Ag
multivalents durant leur développement dans la
moelle osseuse
YYYY
Y
YYYY
Y
YYYY
Y
YYYY
Y
IgM
YYY
YY
B-1 Mature
YY
B-2 Immature
Les cellules B-1 non dérivées de la moelle osseuse sont directement
stimulées par des antigènes contenant des épitopes multivalent
Les cellule T ne sont pas nécessaires
Induisent l’expression d’anticorps naturels spécifiques des Ag TI-2
Antigène TI-2

LPS
LPS bindingProtéines (LPSBP)
CD14
Cellule B
Les lipopolysaccharides bactériens, (LPS, antigènes TI-1), se fixent sur les LPS binding protéines de l’hôte dans le plasmaLe complexe LPS/LPSBP sont capturés par CD14 sur la surface des cellules B
TLR 4
Le récepteur 4 (TLR4) interagieavec le complexe CD14/LPS/LPSBP
Activation des cellules B
Antigènes indépendant des cellules T (TI-1)

Y Y Y Y Y YB B B B B B
Y Y Y Y Y YY Y Y Y Y YY Y Y Y Y YY Y Y Y Y YY Y Y Y Y YY Y Y Y Y Y
Six cellules B différentes ont besoin de 6 antigènes différent pour être activés
A forte dose les antigènes TI-1 (LPS) vont ACTIVER DE MANIERE POLYCLONALLE toutes les cellules B cells sans respecter leur spécificité
Les antigènes TI-1 sont des MITOGENES
LPS se complexe avec CD14, LPSBP & TLR4
Antigènes indépendant des cellules T (TI-1 - LPS)

Maturation des cellules B - résumé

La réponse immunitaire



Développement et maturation des cellules lymphocytaires
II- Les cellules T

La maturation thymique

La maturation thymique
Les thymocytes exprimant les TcR qui reconnaissent les antigènes du CMH sont retenus
Sélection positive
Sélection négative
Les thymocytes exprimant les TcR qui reconnaissent des auto-antigènes présentés par des récepteurs du CMH ou qui n’ont pas d’affinité pour les auto-récepteurs du CMH sont éliminés

Le complément

• synthétisées majoritairement dans le foie
• souvent des proenzymes (ou zymogènes)– dénomination selon l’ordre de
découverte pas nécessairement selon un ordre logique (malheureusement!)
– activation par protéolyse avec séparation d’un fragment inhibiteur et d’un fragment catalytique
Les protéines du complément
• Système complexe de plus de trente protéines plasmatiques et membranaires

• Fragment inhibiteur– le plus petit– appelé ...a– action à distance sur l’activation et le
chimiotactisme des phagocytes
• Fragment catalytique (sérine protéase)– le plus gros– appelé ...b– action enzymatique locale (à la surface de
l’agent pathogène)
Les protéines du complément

La molécule effectrice la plus importante du système
Le facteur soluble le plus important du système

C4b et C3b : les systèmes d’ancrage

• Collectines : molécules ancestrales à activité lectine
• Interagit avec plusieurs ligands mais en particulier avec des ligands présents sur les immunoglobulines et en particulier sur les complexes immuns
• Activation : reconnaissance d’un antigène par un anticorps spécifique– formation d’un complexe immun
• La portion Fc d’une immunoglobuline libre (sans antigène fixé sur le Fab) est incapable de lier C1q.
Voie classique : intervention de la collectine C1q

• C1 est formé de trois molécules distinctes– C1q : dépourvu d’activité enzymatique, se
lie au domaine Fc des IgM et des IgG– C1r : sérine protéase– C1s : sérine protéase
Voie classique : le complexe C1

Le complexe C1

• Le complexe C1r2C1s2 non lié à C1q est inactif
• C’est la fixation sur C1q qui révèle l’activité enzymatique de C1r
Non fixé sur C1q
Fixé sur C1q
Domaines d’interaction
avec C1q
Voie classique : le complexe C1

C1 = protéine avec un domaine de type collagène et un domaine lectineC1 est une COLLECTINE.

• Pour que C1r2C1s2 puisse se lier à C1q, il faut que C1q subisse lui-même un changement de conformation
• La fixation de C1q, notamment sur des complexes immuns permet ce changement de conformation
Le complexe C1
• Complexes immuns à IgM– les IgM sont des pentamères– chaque molécule d’IgM possède au moins trois sites de
fixation au C1q• les IgM activent très efficacement le complément
– Les sites de fixation au C1q ne sont exposés que si l’IgM est liée à un antigène

• La liaison de C1q à deux Ig ou plus n’est possible que si ces dernières appartiennent à un même complexe immun ou si elles sont fixées sur une même surface
Le complexe C1

Liaison de C1q à des Ig

• Constitution de C1qr2s2
C1s est le substrat de C1r et est lui-
même une protéase
Liaison de C1q à des Ig

C2 et C4 sont deux substrats de C1s
C4b intervient
dans l’ancrage à
la membrane
b
C2a
2b
C4b2b
Constitution de la C3 convertase

b
C2a
2b
C4b2b
C4b intervient dans l’ancrage à
la membrane
Constitution de la C3 convertase

Liaison thioester avide d’électrons
Hydrolyse de C3 par la C3 convertase (très efficace)

Liaison covalente avec les glycoprotéines de la surface cellulaire
Hydrolyse de C3 par la C3 convertase (très efficace)

2b
Constitution de la C5 convertase

2b
Tout le C3b ne se lie pas à la membraneUne partie diffuse et se fixe sur des complexes immuns solubles et des
microorganismes : opsonisation
Génération d’une grande quantité de C3b qui couvre la surface bactérienne

Une molécule de C4b2b clive 1000 molécules de C3 en C3b!

2b
Activation du MAC (membrane attack complex) (C5-C9)

Activation du MAC (membrane attack complex) (C5-C9)

Activation du MAC (membrane attack complex) (C5-C9)

• Le MAC est important contre un nombre limité de bactéries (neisseria notamment)
• Par contre l’opsonisation par C3b est cruciale pour un grand nombre d’agents infectieux.
Importance relative du MAC et de la génération de l’opsonine C3b

La voie classique peut parfois être activée via C1q mais par autre chose que des
complexes immuns
• Certaines bactéries (certains steptocoques)• Cellules apoptotiques
Dans certains cas C1q peut se lier directement à certaines cellules
Dans d’autres cas, C1q est activé par une protéine qui n’est pas une immunoglobuline : la CRP

• Protéine de la phase aiguë de l’inflammation (acute phase protein)
• Synthétisée par le foie
• Marqueur de l’inflammation très couramment utilisé en biologie clinique
CRP : C Reactive Protein

CRP : C Reactive Protein
• Membre d’une famille de protéines très ancienne
• Se lie à la phosphocholine et aux résidus phosphocholine des polysaccharides bactériens
• Se lie aux cellules apoptotiques
• Une fois lié à son ligand, peut activer le C1q

• protéines ou glycoprotéines capable de se lier à certains résidus glucidiques
• origine non immunitaire• capable comme un anticorps d’agglutiner ou
de précipiter des cellules ou des glycoconjugués
• isolées initialement chez des végétaux mais molécules voisines (lectin-like) présentes chez les bactéries et les animaux
Lectines

Domaine de type lectine(site de la liaison au résidus
mannosyl et fucosyl)
Liaison à de nombreux microorganismesGram-, Gram+, mycobactéries,
champignons, parasites
Le récepteur au mannose et sa famille

• Fait intervenir la MBP (mannose binding protein), une collectine de la même famille que C1q
• MBL est donc l’équivalent de C1q
• Une fois liée, la MBP recrute une protéase (la mannose binding protein associated protease ou MASP) qui est l’équivalent de C1s et dont les substrats sont C4 et C2
Voie d’activation par la lectine liant le mannose (MBL)

Voie de MBL

• Non liée à la fixation d’une collectine sur un complexe immun ou sur un pathogène donc indépendante de l’immunité adaptative
• Considérée comme constituant de l’immunité naturelle
• Aboutit à l’activation du MAC (formation de C5b sans l’intervention d’anticorps)
Voie alterne

Facteur B : une fois fixé sur C3b, devient le substrat du facteur D (protéase équivalent de C1s)
C3Bb : C3 convertase de la voie alterne
Properdine : augmente la ½ viede la C3 convertase de la voie alterne(530 minutes)
Voie alterne

• Présence physiologique de petites quantités de C3b dans le plasma (hydrolyse spontanée à bas bruit de la liaison thioester instable)
• Fixation de C3b sur toutes les cellules (y compris les cellules de l’hôte)
Voie alterne

Régulation étroite de la voie alterne sur les cellules eukaryotes

• CR1 et DAF : empêchent l’interaction C3b B et déplacent C3b des complexes C3bBb déjà formés
• Facteur I : protéase plasmatique qui clive C3b en iC3b
• CR1, DAF et facteur H sont des cofacteurs du facteur I
• L’activité du facteur H dépend du contenu cellulaire en acide sialique
Régulation de la voie alterne

Voie classique Voie alterne

Voie classique vs. voie alterne

La voie alterne constitue une boucle d’amplification de la voie classique

• Classique : intervention de C1q– Via COMPLEXES IMMUNS : le plus souvent– Via CRP (polysaccharides bactériens,
cellules apoptotiques) – Directement (certaines bactéries, cellules
apoptotiques)
Les trois modes d’initiation de la cascade du complément

• Alterne : pas d’intervention de C1q– Nombreuses bactéries, champignons, virus,
cellules tumorales
• Mannose binding lectin– Microorganismes qui contiennent des
groupes mannoses terminaux
Les trois modes d’initiation de la cascade du complément

Lié à la membrane
peut se produire à la surface d’une cellule ou sur des complexes immuns!
MAC

• Attention : si le MAC est activé par des complexes immuns libres (non cellulaires), le C5b67 peut aller se fixer sur des cellules voisines (qui n’ont pas d’antigène à leur surface)– innocent bystander lysis
MAC

Lié à la membrane
C5b678 peut suffire à lyser une hématie mais pas une cellule nucléée
10 Å
MAC

100 Å
Activation du MAC (membrane attack complex) (C5-C9)

• Une activation intempestive du complément peut tuer un individu ou altérer gravement ses organes– molécules très labiles une fois activées– nombreux systèmes de contrôle
La régulation du complément

L’inhibiteur de C1 (=inhibiteur de C1 estérase)

Déficit génétique : activation intempestive de C4 ou de C2
L’inhibiteur de C1 (=inhibiteur de C1 estérase)

• Famille de protéines (toutes codées par le même chromosome) et qui régulent l’activité de la C3 convertase – voie classique : se lient à C4b
• une protéine soluble : C4BP• deux protéines membranaires : CR1 et MCP• une protéase qui inactive C4b en C4d et C4c
Les protéines RCA (regulator of complement activation)
– voie alterne : se lient à C3b• trois protéines membranaires : CR1, MCP, facteur
H• une protéase qui inactive C3b en C3c et C3dg
– inhibent sa formation – favorisent sa dissociation (decay)
• C4BP, CRI, facteur H• DAF (decay accelerating factor)


• Protéine S (vitronectine)– protéine soluble qui lie le complexe
C5b67 et l’empêche de s’insérer dans la membrane cellulaire
Inhibition du MAC

• Homologous restriction factors (spécificité d’espèce – se lient à C8)– HRF– CD59
Inhibition du MAC
Déficit d’ancrage GPI : hémoglobinurie paroxystique nocturne


Conséquences de l’activation du complément

bactéries Gram-
virus enveloppésherpesvirus, retrovirus,...
Conséquences de l’activation du complément

peu efficace contre les bactéries Gram+ et les cellules nucléées (notamment tumorales)
Conséquences de l’activation du complément

• Neutralisation de certains virus par la fixation de certains composants du complément indépendamment de l’activation du MAC
Conséquences de l’activation du complément

Principale opsonine : C3b
Conséquences de l’activation du complément

Principale opsonine : C3bRécepteur CR1
Conséquences de l’activation du complément

Le C3b et les hématies (riches en CR1) interviennent pour éliminer les
complexes immuns via les cellules
phagocytaires de la rate et du foie
Solubilisation des complexes immuns

• C3a, C4a et surtout C5a sont des anaphylatoxines, des facteurs solubles qui initient la réponse inflammatoire– provoquent la dégranulation des basophiles et des mastocytes tissulaires et la
libération d’amines vasoactives (en particulier d’histamine)• vasodilatation, augmentation de la perméabilité vasculaire, contraction des
muscles lisses bronchiques– induisent l’adhérence des neutrophiles et des monocytes au cellules
endothéliales, leur extravasation, et leur activation sur le site inflammatoire
Réponse inflammatoire

– activité régulée par une protéase la carboxypeptidase N
– les formes des-Arg ont perdu l’essentiel de leur activité
Réponse inflammatoire


Test immunologiques


















Essai immunologique