CARACTERÍSTICAS DOS TECIDOS PERIIMPLANTARES...tecido gengival que existe ao redor de dentes (para...
Transcript of CARACTERÍSTICAS DOS TECIDOS PERIIMPLANTARES...tecido gengival que existe ao redor de dentes (para...
-
8
R. Periodontia - Dezembro 2008 - Volume 18 - Número 04
INTRODUÇÃO
Os tecidos que envolvem o implante são cha-
mados de periimplantares. Estes são compostos de
uma porção de tecido duro, osso lamelar e medular,
e uma porção de tecido mole, a mucosa
periimplantar. Esta mucosa é análoga à gengiva que
circunda dente e tem como função primordial a pro-
teção do osso subjacente. A formação da mucosa
periimplantar ocorre após a instalação de implantes
em um único estágio ou após a reabertura de im-
plantes submersos e instalação do pilar ou conector
intermediário. Em resumo, imediatamente após a
instalação do componente transmucoso e sutura
(quando necessário), uma camada de coágulo, con-
tendo uma rede de fibrina, eritrócitos e neutrófilos, é
formada entre a mucosa e a superfície do implante.
Durante as duas primeiras semanas de cicatrização
este coágulo é substituído primeiramente por tecido
de granulação e depois por tecido conjuntivo.
Concomitantemente, o epitélio começa a migrar
apicalmente. Após oito semanas de cicatrização, a
mucosa periimplantar está formada (Berglundh et al.
2007).
A possibilidade de ancoragem de próteses so-
bre implantes foi demonstrada experimentalmente
por Branemark e colaboradores. Aspectos relaciona-
CARACTERÍSTICAS DOS TECIDOS PERIIMPLANTARESCharacteristics of the peri-implant tissues
Maurício Araujo1, Norberto Francisco Lubiana2
RESUMO
O objetivo da presente revisão foi descrever algumas
características dos tecidos periimplantares que envolvem o
implante e são compostos de uma porção de tecido duro,
o osso, e uma porção de tecido mole, a mucosa
periimplantar. A mucosa periimplantar clinicamente saudá-
vel apresenta-se firme e com coloração rosa.
Histologicamente, a mucosa periimplantar é constituída de
dois tecidos: epitelial e conjuntivo. Este epitélio cobre a
porção marginal do tecido conjuntivo periimplantar sepa-
rando-o da superfície do implante por uma extensão de 2
mm e termina a uma distância de 1-1,5 mm da crista ós-
sea. O tecido conjuntivo que separa a porção apical do
epitélio da barreira e a crista óssea está em íntimo contato
com a superfície do implante e contém fibras colágenas
organizadas paralelamente à superfície do implante que se
estendem da crista óssea a margem periimplantar. O teci-
do ósseo compacto e trabecular e a medula óssea que ocu-
pa o espaço entre as trabéculas sofrem agressões durante
os procedimentos de colocação dos implantes e passam
por processos de regeneração pós-cirúrgica pela ação das
células ósseas e de componentes da matriz óssea e de
outras células e substâncias que chegam ao local.
UNITERMOS:
1 Professor Associado do Departamento de Odontologia, Universidade Estadual de Maringá2 Prof. de Histologia e Embriologia da Universidade Federal do Espírito Santo
Recebimento: 07/10/08 - Correção: 02/11/08 - Aceite: 28/11/08
implantes, mucosa, epitélio, tecido con-
juntivo, osso. R Periodontia 2008; 18:08-13.
periodez08 - 14-05-09.pmd 5/14/2009, 11:30 AM8
-
R. Periodontia - 18(4):8-13
9
dos com as condições clínica e radiográfica e análise ultra-
estrutural das células epiteliais, conjuntivas, ósseas e medu-
lares foram relatados, evidenciando a ausência de alterações
dignas de nota (Branemark et al. 1969). Outras pesquisas
mostraram as possibilidades dos implantes receberem car-
gas funcionais na reabilitação do edentulismo parcial e total,
evidenciando os benefícios da osseointegração (Zarb et al.
2002).
Mucosa periimplantar
Características clínicas
A mucosa periimplantar saudável pode variar de apa-
rência de acordo com as características da mucosa do rebor-
do onde foi instalado o implante. Dessa forma, quando um
implante é instalado em um rebordo que permita que mucosa
queratinizada envolva o implante, a mucosa periimplantar
apresenta-se firme e com coloração rosa. (Fig. 1). Por outro
lado, o implante, quando instalado em uma área sem mucosa
queratinizada, vai apresentar uma mucosa periimplantar mais
avermelhada e com certa mobilidade. A presença de uma
quantidade mínima de mucosa periimplantar queratinizada
não parece influenciar as condições de saúde dos tecidos
moles ou o nível ósseo (Wennström et al. 1994, Bengazi, et
al. 1996). Por outro lado, pode-se especular que a presença
de uma mucosa periimplantar não-queratinizada fina ao re-
dor do implante pode contribuir para o surgimento de
recessão tecidual quando exposta à inflamação provocada
por acúmulo de placa ou escovação traumática ou ainda,
causar desconforto durante a higiene bucal (Salvi & Lang
2004).
Assim como o tecido gengival ao redor dente, a mucosa
periimplantar também exibe um sulco que se localiza entre
a superfície do pilar intermediário ou prótese e a mucosa.
Este sulco periimplantar pode variar muito em profundidade
mesmo em condições onde o tecido está saudável. O local
onde foi instalado o implante (região estética versus não-
estética), forma do implante, o tipo de superfície, a força
utilizada e o design da prótese são fatores que dificultam o
estabelecimento de uma profundidade padrão. Por outro
lado, a extensão da penetração da sonda em tecidos
periimplantares saudáveis quando realizada com força ade-
quada (0,2N) indica o final da barreira epitelial e o início da
barreira conjuntiva (Lang et al. 1994, Abrahamsson & Soldini
2006). Além disso, uma sondagem como força adequada
também revela que a mucosa periimplantar saudável não
sangra (Lang et al. 1994).
Características histológicas
As características estruturais da mucosa periimplantar
foram descritas em diversos estudos e comparadas com o
tecido gengival que existe ao redor de dentes (para revisão,
consultar Berglundh 1993). Como ocorre no tecido gengival,
a mucosa periimplantar é constituída de dois tecidos, epitelial
e conjuntivo (Fig. 2). O tecido conjuntivo periimplantar é
coberto na sua porção externa (voltada para a boca) por um
epitélio pavimentoso estratificado queratinizado que está em
direta continuidade com um fino epitélio não queratinizado
com poucas camadas celulares voltado para a superfície do
implante. Este último epitélio é análogo ao epitélio juncional
que ocorre ao redor de dentes e é denominado barreira
epitelial. Este epitélio está (i) ligado à superfície do implante
via hemi-desmossomas (Gould et al. 1984), (ii) cobre o teci-
do conjuntivo periimplantar separando-o da superfície do
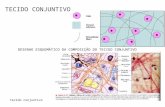
Fig. 2. Fotomicrografia de um corte vestíbulo-lingual dos tecidos periimplantares. Note o epitéliooral em continuidade com o fino epitélio da barreira e o tecido conjuntivo subjacente em íntimocontato com a superfície do implante. Coloração; Ludewig; aumento original: 5x.
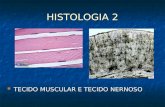
Fig. 1. Fotografia ilustrando o aspecto clínico da mucosa periimplantar ao redor coroa protéticano incisivo central superior direito.
periodez08 - 14-05-09.pmd 5/14/2009, 11:30 AM9
-
R. Periodontia - 18(4):8-13
10
implante por uma extensão de 2 mm e (iii) termina a uma
distância de 1-1,5 mm da crista óssea.
A extensão de tecido conjuntivo que separa a porção
apical do epitélio da barreira e a crista óssea é denominada
barreira conjuntiva e é análoga a inserção a conjuntiva que
ocorre ao redor de dentes. A barreira conjuntiva apresenta
características diferentes da inserção conjuntiva. Enquanto
no dente as fibras colágenas da inserção conjuntiva se inse-
rem no cemento radicular, as fibras colágenas da barreira
conjuntiva estão organizadas paralelamente a superfície do
implante e estende-se da crista óssea a margem periimplantar.
Estas dimensões da barreira epitelial e conjuntiva parecem
representar dimensões biológicas mínimas que se estabele-
cem na mucosa periimplantar saudável (Berglundh & Lindhe
1996). Estas dimensões são independentes do sistema de
implante e do tipo de instalação (um ou dois estágios) usa-
do (Abrahamsson et al. 1999). A composição do tecido con-
juntivo ao redor do implante difere da composição do tecido
conjuntivo ao redor do dente pelo seu maior conteúdo de
fibras colágenas e menor conteúdo de células e vasos san-
guíneos. (Berglundh et al. 1991). Esta composição, no en-
tanto, pode variar de acordo com o tipo de material e super-
fície do pilar ou conector intermediário com o qual o tecido
conjuntivo está em direto contato (Abrahanssom et al. 1998,
Wellander et al. 2008).
Tecido ósseo
O tecido ósseo é um tecido conjuntivo mineralizado cuja
função principal é servir de suporte para estruturas como os
músculos, cuja contração transforma os ossos em um siste-
ma de alavancas, permitindo a locomoção. O tecido ósseo
protege estruturas importantes como o cérebro, estruturas
torácicas e armazena nos espaços entre as trabéculas do
osso esponjoso a medula óssea vermelha, que produz célu-
las sanguíneas, ou a medula amarela ou adiposa. Nos ossos
maxilares na idade adulta prevalece a medula amarela entre
os espaços trabeculares (Bhaskar 1989). Uma das funções
mais importantes do tecido ósseo é a de servir como reserva
de cálcio para o organismo, necessário para a contração
muscular, adesão celular e a fisiologia de diversos sistemas
orgânicos. A calcemia depende da liberação ou
armazenamento de íons cálcio pela ação principalmente do
paratormônio e calcitonina. Se a concentração de cálcio está
baixa, o paratormônio é liberado, induzindo ação
osteoclástica, aumentando os íons na circulação. Se as ta-
xas estão altas, a calcitonina é liberada, estimulando
osteoblastos que retiram cálcio da circulação para mineralizar
o novo osso.
Células ósseas
Os osteoblastos, derivados de células mesenquimais, têm
função principal de sintetizar e mineralizar a matriz orgânica
do tecido ósseo (osteóide), composta de colágeno e proteí-
nas não colagênicas. Osteocalcina, osteogenina, proteínas
morfogenéticas ósseas, osteopontina e sialoproteina óssea
são algumas das proteínas não colagênicas. Após a
reabsorção óssea pelos osteoclastos algumas proteínas não
colagênicas funcionam como fatores locais de indução para
a formação de novos osteoblastos que irão produzir novo
tecido ósseo. A implantação de matriz óssea desmineralizada
em tecido subcutâneo e em tecidos musculares esqueléticos
provocou a liberação das proteínas morfogenéticas ósseas
induzindo formação de condroblastos nestas áreas, forman-
do cartilagens que foram substituídas por tecido ósseo pelo
Fig. 4. Radiografia mostrando condensação óssea próxima ao implante após 8 meses de cargafuncional, indicando remodelação óssea.
Fig. 3. Osso trabecular seco, mostrando espaços vazios entre as trabéculas que no indivíduo vivosão preenchidos por medula óssea adiposa ou hematopoiética.
periodez08 - 14-05-09.pmd 5/14/2009, 11:30 AM10
-
R. Periodontia - 18(4):8-13
11
processo de ossificação endocondral (Urist et al. 1970).
Osteoclastos são células multinucleadas formadas pela
fusão de monócitos que, via corrente sanguínea chegam aos
locais onde há a necessidade de reabsorção óssea. Os
osteoclastos se unem à matriz óssea por meio de seu
citoplasma periférico formando um compartimento fechado
onde liberam substâncias que quebram as ligações quími-
cas existentes entre o cálcio, fosfato e as hidroxilas da
hidroxiapatita, e também as moléculas do colágeno e as pro-
teínas não colagênicas da matriz orgânica, dissociando-as,
provocando a desintegração do tecido ósseo.
Os osteócitos são antigos osteoblastos que ficaram apri-
sionados dentro do tecido ósseo pela própria matriz. Apre-
sentam prolongamentos citoplasmáticos formando uma rede
de canalículos no interior do tecido ósseo. Os canalículos e
os prolongamentos citoplasmáticos permitem a passagem
de nutrientes e a drenagem dos produtos do metabolismo
das células, sendo sua função a manutenção do tecido ós-
seo. As células osteoprogenitoras são derivadas de células
mesenquimais indiferenciadas que irão completar a sua di-
ferenciação em osteoblastos, quando necessário, para a for-
mação de novo osso.
Interface osso/implante
A colocação de implantes requer o corte no tecido ós-
seo com instrumentos rotatórios gerando riscos de aqueci-
mento e a destruição dos vasos sanguíneos existentes nos
canais de Havers e de Volkman do osso cortical e de vasos
existentes na medula óssea entre as trabéculas do osso es-
ponjoso (Fig.3). Estes dois fatores levam sempre a formação
de uma zona necrótica de osso que ficará em contato com a
superfície dos implantes. Estudos revelaram que a exposi-
ção à temperatura crítica de 47°C durante 1 minuto é
suficiente para causar necrose no tecido ósseo e que uma
temperatura acima de 60°C poderá impedir a formação
de tecido ósseo na interface osso-implante (Ericsson et al.
1994). Na clínica este problema pode ser evitado com o uso
de irrigação copiosa com solução fisiológica durante o
processo de perfuração óssea com as brocas utilizadas na
implantodontia. Alem da área necrótica, haverá a
formação de coágulo sanguíneo resultante do
extravasamento de sangue devido ao corte dos tecidos.
Uma rede de fibrina será formada pela ação de fatores
da coagulação, por produtos liberados pelo sistema com-
plemento, ativação das plaquetas, células inflamatórias e
células endoteliais. Componentes liberados da matriz de
fibrina iniciam o processo de reorganização e regeneração
por meio do recrutamento de células inflamatórias e
fibroblastos. As plaquetas liberam fatores de crescimento que
contribuem para o recrutamento de osteoblastos. Monócitos
e linfócitos presentes no local liberam leucotrienos, fatores
de crescimento derivado de plaquetas e fator de crescimen-
to transformador-â que também contribuem para o recruta-
mento de osteoblastos (Anderson, 1999). Fatores de cresci-
mento liberados dos grânulos-〈 das plaquetas são o sinalpara atração de leucócitos, l infócitos, monócitos e
macrófagos.
O meio ambiente no local da ferida é caracterizado pela
diminuição da tensão de oxigênio e do pH, condição neces-
sária para a atividade dos polimorfonucleares e macrófagos.
Inicialmente predominam os neutrófilos na área da ferida ci-
rúrgica, porém em pouco tempo os macrófagos tornam-se
as células mais numerosas. Estas células estão envolvidas
com a degradação do coágulo por mecanismos de digestão
fagocítica tanto extra como intracelular. Claramente os
macrófagos podem alcançar a superfície do implante usan-
do como apoio a rede de fibrina e podem ter um importante
papel no desenvolvimento da interface osso-implante. A pro-
liferação de novos vasos sanguíneos (angiogênese) traz os
nutrientes e oxigenação necessários à diferenciação das cé-
lulas osteogênicas com a conseqüente deposição de tecido
ósseo na superfície do implante denominada, osteogênese
de contato. (Davies e Rosseini 1999). Uma micro camada de
material amorfo, composto de glicoproteinas, e possivelmen-
te também de proteoglicanas e fosfolipídios, medindo de 20
a 50 nanômetros é formada pelos osteobastos, entre o
osso vivo e a superfície do implante (Albrektsson et al. 1986).
Experimentos com cultura celular in vitro foram realizados
para determinar os componentes desta camada amorfa.
Difração elétrica de Raios X e espectrometria fotoeletrônica
de Raios X revelaram a presença de cálcio, fosfato,
oxigênio e sódio em sua composição. Estudos com
eletroforese e auto-radiografias revelaram a presença de
sialoproteina óssea e, em maior quantidade, de osteopontina.
(Rosseini et al. 1999).
Importante frisar que a presença de acúmulo bacteriano
ao redor dos implantes ou na interface implante-abutment
pode levar ‘a inflamação e desorganização destes compo-
nentes teciduais e conseqüente perda de osso ao redor dos
implantes.(Duarte et al. 2006)
Remodelação óssea
A remoção de osso necrótico próxima ao implante é re-
alizada pelos osteoclastos e novo tecido ósseo é produzido
pelos osteoblastos. Quando a área de tecido necrótico e de
coágulo é preenchida por novo tecido ósseo, é iniciado en-
tão o processo de remodelação que seguirá os parâmetros
já bem conhecidos no tecido ósseo normal de todo o orga-
periodez08 - 14-05-09.pmd 5/14/2009, 11:30 AM11
-
R. Periodontia - 18(4):8-13
12
nismo. Osteoclastos promovem a reabsorção óssea na for-
ma de túneis de reabsorção. Tecido de granulação prolifera
acompanhando os osteoclastos, promovendo a limpeza dos
produtos do metabolismo celular, o crescimento de vasos e
a diferenciação de células mesenquimais em osteoblastos.
Estes formam lamelas concêntricas de tecido ósseo por um
processo incremental, até o fechamento do túnel. Permane-
cem no centro dos canais, vasos e endósteo, denominados
de canais de Havers. Os sistemas de Havers, formados pelas
lamelas concêntricas e canais de Havers, são uma constante
no tecido ósseo compacto permitindo maior condensação
do tecido ósseo para resistir às cargas nele aplicadas. Como
as células ósseas necessitam de um alto gral de tensão de
oxigênio e nutrientes para sobreviver, a remodelação tem
também o papel de levar estes nutrientes à profundidade do
tecido ósseo, por meio dos canais de Havers e também dos
canais de Volkman que interligam os vasos dos sistemas de
Havers. (Fig. 4). As finas trabéculas do osso esponjoso tam-
bém sofrem remodelação, porém os osteoclastos fazem a
reabsorção em forma de baias na superfície, sem a forma-
ção dos túneis de reabsorção já que a nutrição das trabéculas
é possível apenas pela difusão dos nutrientes via canalículos
ósseos formados pelos prolongamentos citoplasmáticos dos
osteócitos (Ten Cate 2001).
CONCLUSÃO
Os tecidos periimplantares são constituídos de mucosa
periimplantar e osso. Estes tecidos estão localizados ao re-
dor do implante e tem como função primordial a proteção
do osso subjacente (via mucosa periimplantar) e a sustenta-
ção do implante (via osso). A mucosa periimplantar é revestida
de epitélio oral queratinizado em continuidade com um fino
epitélio (barreira epitelial) lateral à superfície do implante. Entre
o epitélio e o tecido ósseo, um tecido conjuntivo altamente
colagenizado e pouco vascularizado se estabelece (barreira
conjuntiva). O osso ao redor do implante é do tipo
mineralizado e não-mineralizado. Este osso se liga a superfí-
cie do implante através de um processo chamado
osseointegração que permite que o implante fique apto a
sustentar a prótese e as cargas oclusais.
ABSTRACT
The aim of the present review was to describe some
features characteristic of the peri-implant tissues. The peri-
implant tissues surround the implant and are made of hard
tissue, bone, and soft tissue portions, peri-implant mucosa.
Clinically, the healthy peri-implant mucosa is firm and exhibits
a pink appearance. Histologically, the peri-implant mucosa
is occupied by to 2 tissues: epithelial and connective. The
epithelium covers the marginal portion of the peri-implant
connective tissue which is separated from the implant surface
by a length of 2 mm. The apical portion of the epithelium is
located 1-1.5 mm from the bone crest. The connective tissue
which separates the epithelium from the bone crest is in direct
contact with the implant surface and contains collagen fibers
running in a parallel course from the bone crest to the peri-
implant margin. The trabecular and compact bone tissue and
the bone marrow which is located between the trabeculae
are exposed to injury during the implant installation
procedure. Subsequently, the bone tissue is regenerated
through the action of bone cells and other cells, bone matrix
components and, substances that penetrate the wound.
UNITERMS: implants, mucosa, epithelium, connective
tissue, bone.
periodez08 - 14-05-09.pmd 5/14/2009, 11:30 AM12
-
R. Periodontia - 18(4):8-13
13
REFERÊNCIAS BIBLIOGRÁFICAS
1- Abrahanssom, I, Berglundh, T, Glantz, PO, Lindhe, J The mucosal
attachment at different abutments. An experimental study in dogs. J
Clin Periodontol 1998; 25: 721-727.
2- Abrahanssom, I, Berglundh, T, Moon, IS, Lindhe, J Peri-implant tissues
at submerged and non-submerged titanium implants. An experimental
study in dogs. J Clin Periodontol 1999; 26: 600-607.
3- Abrahansson, I, Soldini, C Probe penetration in periodontal and peri-
implant tissues. Clin Oral Implant Res 2006; 17: 601-605.
4- Albrektsson, T, Janson ,T, Lekholm, U Osseointegrated Dental Implants.
Dent Clin North Amer 1986; 30:151-175
5- Anderson JM, The cellular cascades of would healing, in Bone
Engeineering, Davies ed 1999; 881-892
6- Bengazi, F, Wenneström, JL, Lekholm, U Recession of the soft tissue
margin at oral implants. A 2-year longitudinal prospective study. Clin
Oral Implant Res1996; 7: 303-310.
7- Berglundh, T & Lindhe, J, Ericsson, I, Marinello, CO, Liljenberg, B,
Thomsen, P The soft tissue barrier at implants and teeth. Clin Oral
Implant Res 1991; 2: 81-90.
8- Berglundh, T. Studies on gingival and periimplant mucosa in the dog
[tese]. Gotemburgo:Universidade de Gotemburgo; 1993.
9- Berglundh, T, Lindhe, J Dimensions of the peri-implant mucosa. Biological
width revised. J Clin Periodontol 1996; 23: 971-973.
10- Bhaskar, NS Histologia e Embriologia Oral de Orban. Artes
Médicas;1989;10ª Edição
11- Berglundh, T, Abrahansson, I, Welander, M, Lang, K, Lindhe, J
Morphogenesis of the peri-implant mucosa: an experimental study in
dogs. Clin Oral Implant Res 2007; 18: 1-8.
12- Branemark PI, Adell R, Breine U, Hansson BO, Lindstron J, Ohlson A.
intra Osseous Anchorage of Dental Prosthesis I –Experimental studies.
Scand J Plast Reconstr Surg 1969; 3: 81-100.
13- Davies JE. Rosseini MM, Histodynamicso of Endosseous Wound
Healling, in Bone Engineering, Davies ed 1999; 1-14
14- Duarte ARC, Rossetti PHO, Rossetti LMN,Torres SA, Bonachela WC. In
Vitro Sealing Ability od Two Materials At Five Different Implants-
Abutment Surfaces. J Periodontol 2006; 77: 1-5
15- Ericsson RA, Albrektson T, Magnusson B, Assessment of bone viability
after heat trauma: A histological, histochemical and vital microscopy
study in the rabbit Scand J Plast Reconstr Surg 1984; 18: 261-268.
16- Gould, TRL, Westbury, L, brunette, DM Ultrastructural study of the
attachment of human gingival to titanium in vivo. J Prost Dent 1984;
52: 418-120.
17- Lang, K, Wetzel, AC, Stich, H, Caffesse, R Histologic probe penetration
in healthy and inflamed peri-implant tissues. Clin Oral Implant Res 1994;
Endereço para correspondência:
Rua Misael Pedreira da Silva, 48/904 - Santa Lúcia
CEP: 29052-270 - Vitória - ES
5: 191-201.
18- Rosseini J, Sodek R, Franke RP, Davies JE, The Struture and Composition
of the Bone-Implant Interface. In Bone Engineering, Davies ed 1999;
295-304
19- Salvi, G & Lang, K Diagnostic parameters for monitoring peri-implant
conditions. Int J Oral Maxillofac Implants 2004; 19(suppl): 116-127.
20- Ten Cate AR, Histologia Bucal-Desenvolvimento, Extrutura e Função.5
ª Ed Guanabara Koogan 2001.
21- Urist MR, Jurist JM Jr, Dubuc FL, Strates BL, Quantitation of new bone
formation in intramuscular implants of bone matrix in rabbits. Clin
Orthop 1970; 68:279, 293.
22- Wellander, M, Abrahanssom, I, Berglundh, T The mucosa barrier at
implant abutment of different materials. Clin Oral Implant Res 2008;
19: 635-641.
23- Wenneström, JL, Bengazi, F, Lekholm, U The influence of the
mastigatory mucosa on the peri-mimplant soft tissue condition. Clin
Oral Implant Res 1994; 7: 1-8.
24- Zarb G, Lekholm U, Albrektson T, Tenenbaum H Introduction: Clinical
Considerations for Implant-Supported Prostheses en Elderly Patients-
in Aging Osteoporosis, and Dental Implants Quintessence Publishing
Co Inc 2002.
periodez08 - 14-05-09.pmd 5/14/2009, 11:30 AM13