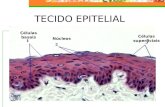
TECIDO EPITELIAL Núcleos Células superficiais Células basais.
CÂNCER - einsteinlimeira.com.br · -Fibrócitos: fibroma-Células adiposas: lipoma-Células...
Transcript of CÂNCER - einsteinlimeira.com.br · -Fibrócitos: fibroma-Células adiposas: lipoma-Células...


CÂNCER
•1 em cada 8 óbitos é devido a um tumor maligno
•2a. Principal causa de morte (20% das mortes)
•INCA (2006): 472.050 casos novos
HOMENS:
Próstata
Pulmão
Estômago
MULHERES:
Mama
Colo Útero

O que é Câncer?
Karkinos: origem grega, carcinoma = caranguejo
Cancer é um neoplasma maligno ou tumor.
Neoplasma (neo = novo, plasma =crescimento ): um
crescimento novo e anormal de células
Tumor ou câncer: sinônimo de neoplasma
massa celular com características distintas do tecido normal
Maligno: quando as células invadem os tecidos
adjacentes (metástases) são considerados
câncer.
Benigno: as células tumorais permanecem no
tecido original (agregadas) não invadem (não
metastizam)

Terminologia do Câncer: conforme os tecidos e os tipos
celulares dos quais eles derivam
1. Benignos: adicionado “oma” ao tipo celular
-Fibrócitos: fibroma
-Células adiposas: lipoma
-Células glândulares: adenoma
2. Malignos: conforme origem do tecido afetado
a) Células de origem epitelial: carcinomas (> 90% dos cânceres são
carcinomas)
Ex.: carcinoma de pulmão, de mama, de cólon
b) Células de origem mesenquimal (tecido conjuntivo: incluindo osso,
músculo, cartilagem ou tecido fibroso): Sarcomas (Sarcomas são
relativamente raros, < 2% dos cânceres)
Ex.: sufixo sarcoma + tipo celular
-Fibrócitos: fibrossarcoma
-Tecido adiposo: lipossarcoma
3. Leucemias e linfomas: cânceres malignos do tecido hematopoiético e
linfóide.

HIPÓTESE DA
MUTAÇÃO
SOMÁTICA DO
CÂNCER
Boveri (1914):
processo
multipasso devido
mutações
somáticas em
genes celulares
Acúmulo de ~10 mutações

Ciclo celular normal e pontos de checagem
Caminhos da célula durante a divisão celular:

O Câncer desenvolve por evolução clonal
•Desenvolve de uma única célula alterada (cerca de 10
ou mais mutações → seleção)
•Iniciação: alteração genética de uma célula (mutação)
vantagem de crescimento ou sobrevivência
•Promoção do tumor: agentes como hormônios ou
trauma, ou mudanças que aumentam a evolução
clonal, estimulam o crescimento celular.
• Evolução Clonal: base para o desenvolvimento do
câncer (anos). Evolução continuada de mais células
malignas que crescem ou sobrevivem melhor
desenvolvimento e progressão tumoral.
•Progressão tumoral: desenvolvimento do câncer
requer pequenos múltiplos passos (mutação e seleção). Cada passo confere a célula uma vantagem
adicional de sobrevivência ou crescimento
(necessidade reduzida para fatores de crescimento ou
resistência a apoptose)

Câncer de Cólon desenvolve por
progressão de múltiplos passos
•Iniciação: pode ser causada por carcinógenos
da dieta (nitrosaminas)
•células iniciadas vantagem proIiferativa: uma
via de fator de crescimento pode ser
constantemente ligada por mutação no gene K-
Ras células crescem sobre as vizinhas
(hiperplasia adenoma)
•Mutações adicionais seleção de células com
vantagem proliferativa e de sobrevivência:
inativação do gene TP53 permite uma taxa
mais rápida de mutagênese (adenoma inicial
adenoma tardio)
•Outra mutação converte adenoma em
carcinoma: mutação na produção de proteases
invasão de outros tecidos.
Ex. -18 (DCC), -17 e outros cromossomos

•Inibição dependente da densidade de
crescimento: células normais param
em G1 células cancerosas
continuam crescendo em densidade
muito maior.
•Perda da inibição por contato: células
cancerosas formam várias camadas
•Necessidade reduzida de fator de
crescimento: células cancerosas não
precisam de muito fator de crescimento
para se dividir produzem níveis
elevados de fatores de crescimento
autócrino, expressão aumentada de
receptores de fatores de crescimento.
Como as células cancerosas diferem das células normais?

Menor necessidade de adesão ao substrato: expressam menas moléculas de adesão de superfície celular permite as células moverem-se e invadirem outros tecidos
Secreção de proteases:
digerem a matriz extracelular
invasão outros tecidos e
penetrar nos vasos anguíneos
(metástases)

ETAPAS DO PROCESSO DE METÁSTASES

•Fatores de angiogênese:
desenvolvimento de novos vasos
(VEGF e VEGFR)
(Angiostatina e Endostatina:
bloqueador de angiongênese)
•Apoptose: células normais cometem
“suicídio” quando acumulam mutações
células cancerosas perdem essa
habilidade resistência a apoptose
(Terapia apoptótica)

O que causa o câncer?
•Fatores Ambientais e Genéticos (Herança Multifatorial)
•Ambientais: hábitos e estilo de vida (80-90% dos cânceres)
-Carcinógenos substâncias que causam câncer:
(químicos, radiação e vírus )
tabagismo (benzo-a-pireno)
hábitos alimentares (nitrosaminas, sal,
aflatoxina)
alcoolismo
medicamentos (ciclofosfamida, bussulfan)
fatores ocupacionais
luz UV e raios X
infecção viral
Genéticos : danos em genes específicos que participam do
controle do ciclo celular
mutações hereditárias → câncer familiar
mutações somáticas → câncer esporádico
polimorfismos/mutações em genes de
suscetibilidade (fatores genéticos e ambientais)

VÍRUS CAUSAM CÂNCER EM ANIMAIS E HUMANOS
Duas famílias de vírus são responsáveis por um grande número de
cânceres humanos (hepatite B e papilomavírus)
(HTLV)
(HPV)
(HBV) Risco: 200 x

•Papilomavirus: pequenos vírus de
DNA que infecta a pele, trato
anogenital e cabeça e pescoço
(HPVs).
•A maioria causa papilomas, mas
alguns causam câncer cervical
(linhagens 16 e 18): principal causa
de morte por câncer em mulheres
em muitos países.
•HPV: tem 7 genes genes E6 e E7
são oncogenes importantes se
ligam e inativam as proteínas Rb e
p53.

BASE GENÉTICA DO CÂNCER
Gene anômalo herdado forma hereditária do câncer (crianças e jovens)
Mutações somáticas por agentes ambientais radiação, agentes químicos e biológicos, hábito alimentar, fumo, exposição ocupacional, etc.
REPARO INEFICIENTE: mudanças na função de genes que controlam o crescimento celular

ALTERAÇÕES CROMOSSÔMICAS E CÂNCER
ABERRAÇÕES: Perda:
deleção
monossomia
Ganho:
duplicação, amplificação
trissomia
poliploidia
Relocação:
translocação
inversão
inserção

MUTAÇÕES GÊNICAS E CÂNCER
A- Genes que controlam o ciclo celular e apoptose:
Proto-oncogenes :ativação do ciclo celular
proliferação celular
Genes supressores:bloqueio do ciclo celular: perda de função
proliferação celular
B- Genes de reparo do DNA:
mutações em genes celulares (oncogenes e genes supressores) INSTABILIDADE GENÔMICA

Esquema geral para mecanismos de oncogênese:
-pela ativação de proto-oncogene,
-mutação ou perda de genes supressores tumorais,
-ativação de genes anti-apoptóticos ou perda de genes pró-apoptóticos

O QUE SÃO ONCOGENES?
Proto-oncogene: genes promotores do crescimento e
diferenciação celulares contraparte normal de um
oncogene (sem mutação).
Oncogene: genes mutados cuja expressão alterada
estimula a proliferação celular de forma anormal.
Padrão dominante Ganho de função

MAIS DE 100 ONCOGENES TÊM SIDO IDENTIFICADOS
•Os genes adquirem
habilidade oncogênica
devido dois tipos de
mudanças:
•Eles são expressados em
níveis muito elevados nas
células infectadas pelo
vírus devido a LTR.
•Eles estão frequentemente
mutados ou rearranjados
após inserção pelo vírus
podem aumentar a atividade
do produto do gene.

ONCOGENES
componentes da maquinaria que coordena o
ciclo celular: estimulam a proliferação
celular.
•fatores de crescimento
•receptores
•transdutores de sinais
•fatores de transcrição

COMO OS ONCOGENES TORNAM-SE
ATIVADOS E CAUSAM CÂNCER EM
CÉLULAS HUMANAS?
•Mutação de Ponto: proteína
estrutural e funcionalmente
aberrante
•Aberrações Cromossômicas
(Rearranjos Cromossômicos):
proteína quimérica ou expressão
elevada
•Amplificação Gênica: super
expressão de proteína
estruturalmente normal
•Inserção de DNA viral: inserção
de oncogenes-virais

MUTAÇÃO DE PONTO: ONCOGENE H-RAS
•Mutação do aminoácido 12: glicina valina (câncer bexiga, mama, cólon)
•Causa mudança na conformação da proteína ras que não pode converter
GTP GDP, que permanece ativado induzindo a proliferação celular
progressão para o câncer
GDP
Ras inativa
GTP
Ras ativa
xOncoproteína bloqueada: sinal
permanece ligado – ativa
continuamente a quinase seguinte

REARRANJOS CROMOSSÔMICOS
• Espressão desregulada de
proto-oncogenes
Translocação cromossômica:
Leucemia mielóide
crônica: t(9;22)(q34;q11)
proteína quimérica
(truncada) abl/bcr
atividade de quinase
aumentada

REARRANJOS CROMOSSÔMICOS
Linfoma de Burkitt:
t(8;14):gene c-myc é
ativado expressado em
níveis elevados
contribue para o câncer

AMPLIFICAÇÃO
Aumento do número de cópias (dezenas-centenas de vezes) de
oncogenes (erros de replicação do DNA): c-Myc, Her-2/Neu, CCND1
Double minutes (DM): DNA circular extracromossômico
Regiões Homogeneamente Coradas (HSR): intracromossômico

Oncogenes frequentemente alteram a função das vias dos
fatores de crescimento
Fatores de crescimento: super produção
crescimento continuado. Ex.: TGF-a
Receptores: mutação ou amplificação de
genes que codificam receptores aumenta
a sinalização. Ex.: ErbB-1,2
Transdução de sinal: mutações em
genes que codificam mensageiros
secundários.
Ex.: ras ou raf induz ativação
constitutiva e promove o crescimento.
Fatores de transcrição : mutação induz
ativação constante de genes imediatos e
crescimento celular.
Ex.: jun ou fos

GENES SUPRESSORES DE TUMOR
•Regulam negativamente o crescimento celular e desenvolvimento do
tumor: quando mutados ou deletados o controle do ciclo celular é perdido.
Padrão Recessivo Perda de Função
•Experimentos com fusão celular:
células normais x células tumorais
células tumorais híbridas voltam ao estado normal.

Funções Bioquímicas dos Genes Supressores de Tumor
Produção de moléculas de superfície: proteínas transmembranas transmissão de sinais negativos inibição por
contato: DCC (inibição por contato)
Moléculas que regulam a transdução de sinais: enzimas que impedem a fosforilação das proteínas da membrana relacionadas com a emissão de sinais para o núcleo: NF1 (inativa ras)
Moléculas que regulam a transcrição nuclear: p53 e RB

RETINOBLASTOMA – RB – 13q14
•Primeiro gene supressor de tumor descoberto tumor de retina
•Atuam recessivamente: ambas as cópias devem ser perdidas para a
perda da função celular
• Teoria de Knudson: “Dois Eventos de Mutação”
• primeiro alelo herdado com mutação (1o. Evento)
• alelo normal perdido ou mutado na infância (2o. Evento) células da
retina
•Perda de Heterozigosidade (LOH): perda
do alelo (frequentemente por deleção ou
monossomia)
•RB: controla a entrada do ciclo celular
regula o ponto de restrição G1 S

Ação do produto do gene RB1:

Hipótese de dois Eventos Mutacionais

Retinoblastoma bilateral
•Hereditário (40%)
•Mutação da linhagem germinativa
•Início precoce
Retinoblastoma unilateral
•Esporádico (60%)
•Mutação somática
•Início tardio
Tumor maligno de retina
Incidência: 1:20.000

GENE TP53 – GUARDIÃO DO GENOMA
•TP53 : (17p12) segundo principal gene supressor de tumor descoberto
Mutagênese aumentada:
quando a célula perde TP53
ela também perde o controle
do ciclo celular que é
necessário para reparo do
DNA lesado aumento de
células com mutações
Perda da apoptose:
importante ativador da morte
celular programada
muitas células falham em
entrar em apoptose em
resposta a lesões no DNA.

p53 E ESTABILIDADE GENÔMICA
célula normal
lesão do DNA Bloqueio em G1
APOPTOSE
REPARO DO DNAp53p53
Ativação da transcrição

Atuação da p53 no ciclo celularmutação herdada do TP53 : Síndrome de Li-Fraumeni (sarcomas, osteossarcomas, tumores de mama, cérebro, córtex adrenal e leucemia).

CÂNCER HEREDITÁRIO CAUSADO POR MUTAÇÕES EM GENES SUPRESSORES
Polipose adenomatosa do cólon (FAP): APC (5q21)
Câncer hereditário cólon não-poliposo (HNPCC): MSH2, MLH1 (2p16, 3p21)
Câncer de mama e ovário: BRCA1 (17q21)
Câncer de mama de início precoce: BRCA2 (13q12)
Síndrome de Li-Fraumeni: TP53 (17p13)
Retinoblastoma: RB1 (13q14)
Ataxia telangiectasia: ATM (11q22)
•Mutação da linhagem germinativa
•5-10% tumores sólidos
•Tumores múltiplos e bilaterais
•Início precoce

CÂNCER DE MAMA
• 5-10% - forma familiar da doença
•Início precoce (pré-menopausa) e bilateral
•Associado a risco elevado de câncer de ovário
• metade: mutações em BRCA1 (17q21) e BRCA2 (13q12-13)
•BRCA1 e BRCA2 –proteínas nucleares
• abundantes na fase S do ciclo celular: reparo de quebras
duplas (reparo recombinacional)
• BRCA1 ou BRCA2 defeituosos – desenvolvimento de câncer
de mama ou ovário

PERSPECTIVAS PARA O TRATAMENTO DO CÂNCER
Quimioterapia: resposta parcial, temporária e imprevisível
Alvos terapêuticos para apoptose: controle da proliferação e metástases: drogas ativação de caspases; regulação de genes Bcl-2
Bloqueio da angiogênese: inibidores de angiogênese marcadores de superfície nos tecidos cancerosos
Terapia Molecular: inibidores de proteínas tirosina-quinases

TERAPIA MOLECULAR: Leucêmia mielóide crônica (LMC)
Gleevec= imatinib

CÂNCER DE MAMA
HERCEPTIN (trastuzumab): anticorpo monoclonal humanizado
bloqueador do Her-2/Neu câncer de mama metastático
http://www.gene.com/gene/products/information/oncology/herceptin/moa.jsp
http://www.roche.com/pages/facets/9/herc.htm