Atomos y estructuras cristalinas
-
Upload
anakarina-medina -
Category
Documents
-
view
219 -
download
0
Transcript of Atomos y estructuras cristalinas

REPUBLICA BOLIVARIANA DE VENEZUELA.
INTITUTO UNIVERSITARIO POLITECNICO SANTIAGO MARIÑO.
EXTENSION PORLAMAR
ATOMOS Y ESTRUCTURA CRISTALINA
REALIZADO POR:
Anakarina Medina C.I 22.994.488

El Átomo
Los Átomos son la unidad básica de toda la
materia, la estructura que define a todos los
elementos y tiene propiedades químicas bien
definidas. Todos los elementos químicos de la
tabla periódica están compuestos por átomos
con exactamente la misma estructura y a su
vez, éstos se componen de tres tipos de
partículas, como los protones, los neutrones y
los electrones.

Composición
De Los
Átomos

Núcleo
Es el centro del átomo, es la parte
más pequeña del átomo y allí se
conservan todas sus propiedades
químicas. Casi que toda la masa del
átomo reside en el núcleo.
Protones
Son uno de los tipos de partículas
que se encuentran en el núcleo de
un átomo y tienen carga positiva
(masa = 1.673 x 10-24 gramos). Los
protones están compuestos de
partículas aún más diminutas
conocidas como quarks o cuarks.

Electrón
Éstas son las partículas que orbitan
alrededor del núcleo de un átomo,
tienen carga negativa y son atraídos
eléctricamente a los protones de
carga positiva (masa = 9.10 x 10-28
gramos).
Neutrones
Los neutrones son partículas
ubicadas en el núcleo y tienen una
carga neutra (masa = 1.675 x 10-24
gramos). La masa de un neutrón es
ligeramente más grande que la de
un protón y al igual que éstos, los
neutrones también se componen de
quarks.

Modelos
Atómicos

John Dalton(1803)
Fue el primer modelo atómico con bases científicas,
fue formulado en 1803 por John Dalton, quien
imaginaba a los átomos como diminutas esferas
La materia está formada por partículas muy pequeñas
llamadas átomos, que son indivisibles y no se pueden
destruir.
Los átomos de un mismo elemento son iguales entre sí,
tienen su propio peso y cualidades propias. Los átomos
de los diferentes elementos tienen pesos diferentes

Joseph John Thomson(1904)
Se determinó que la materia se componía de dos partes, una negativa y
una positiva. Para explicar la formación de iones, positivos y negativos, y
la presencia de los electrones dentro de la estructura atómica, Thomson
ideó un átomo parecido a un pastel de frutas. Una nube positiva que
contenía las pequeñas partículas negativas (los electrones) suspendidos
en ella. El número de cargas negativas era el adecuado para neutralizar la
carga positiva. En el caso de que el átomo perdiera un electrón, la
estructura quedaría positiva; y si ganaba, la carga final sería negativa. De
esta forma, explicaba la formación de iones; pero dejó sin explicación la
existencia de las otras radiaciones.

Ernest Rutherford
Este modelo fue desarrollado por el físico Ernest Rutherford a partir
de los resultados obtenidos en lo que hoy se conoce como el
experimento de Rutherford en 1911. Representa un avance sobre el
modelo de Thomson, ya que mantiene que el átomo se compone de
una parte positiva y una negativa, sin embargo, a diferencia del
anterior, postula que la parte positiva se concentra en un núcleo, el
cual también contiene virtualmente toda la masa del átomo,
mientras que los electrones se ubican en una corteza orbitando al
núcleo en órbitas circulares o elípticas con un espacio vacío entre
ellos. A pesar de ser un modelo obsoleto, es la percepción más común
del átomo del público no científico.

Niels Bohr
Este modelo es estrictamente un modelo del
átomo de hidrógeno tomando como punto de
partida el modelo de Rutherford, Niels
Bohr trata de incorporar los fenómenos de
absorción y emisión de los gases, así como la
nueva Teoría de la cuantizacion de la
energía .
o Cada órbita tiene una energía asociada. La
más externa es la de mayor energía.
o Los electrones no radian energía (luz) mientras
permanezcan en órbitas estables.
o Los electrones pueden saltar de una a otra órbita. Si lo hace desde una de
menor energía a una de mayor energía absorbe un cuanto de energía igual
a la diferencia de energía asociada a cada órbita. Si pasa de una de mayor
a una de menor, pierde energía en forma de radiación.

Schrödinger (1924)
o El modelo de Schrödinger se abandona la concepción de los
electrones como esferas diminutas con carga que giran en
torno al núcleo, que es una extrapolación de la experiencia
a nivel macroscópico hacia las diminutas dimensiones del
átomo. En vez de esto, Schrödinger describe a los
electrones por medio de una función de onda, el cuadrado
de la cual representa la probabilidad de presencia en una
región delimitada del espacio. Esta zona de probabilidad se
conoce como orbital. La gráfica siguiente muestra los
orbitales para los primeros niveles de energía disponibles
en el átomo de hidrógeno.

Estructura cristalina
La estructura cristalina es la forma
solida de cómo se ordenan y
empaquetan los átomos, moléculas o
iones. Estos son empaquetados de
manera ordenada y con patrones de
repetición que se extienden en las
tres dimensiones del espacio.

Tipos De Estructuras Cristalina

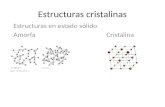
Diferencia Entre Vidrios y Cristales.
o En ocasiones la repetitividad se rompe o no es exacta,
y esto diferencia los vidrios y los cristales, los vidrios
generalmente se denominan materiales amorfos
(desordenados o poco ordenados).
o No obstante, la materia no es totalmente ordenada o
desordenada (cristalina o no cristalina) y nos
encontramos una gradación continua del orden en que
está organizada esta materia, en donde los extremos
serían materiales con estructura atómica
perfectamente ordenada y completamente
desordenada.

Estructura Cristalina Ordenada
En la estructura cristalina (ordenada) de los materiales
inorgánicos, los elementos que se repiten son átomos y
iones enlazados entre sí, de manera que generalmente no se
distinguen unidades aisladas; estos enlaces proporcionan la
estabilidad y dureza del material. En los materiales
orgánicos se distinguen claramente unidades moleculares
aisladas, caracterizadas por uniones atómicas muy débiles,
dentro del cristal. Son materiales más blandos e inestables
que los inorgánicos.