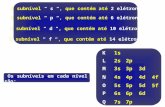
1 3.9.8: A Pressão Total no Interior de uma : Ela será a resultante das contribuições de todos...
Transcript of 1 3.9.8: A Pressão Total no Interior de uma : Ela será a resultante das contribuições de todos...

1
3.9.8: A Pressão Total no Interior de uma : Ela será a resultante das contribuições de todos as componentes: (3.72)
elétrons
núcleos
JÁ SABEMOS ESCREVER OS TERMOS ACIMA!!
»» Balanço entre Pr e Pgás:
e ;
Igualando as duas expressões, obtém-se a região limite para P:
fótons

2
Limite entre predominâncias de Pr e Pgás :
( em g/cm3 e T em K).
Isso pode ser visto na Fig. 3.6 (Maciel’s):
Pr domina
Pgás domina
não DG
DG
não-relativístico
relativístico
cristalização

3
IV: TERMODINÂMICA DO INTERIOR ESTELAR
(cf. R. REIF, “Fundamental of Statistical & Thermal Physic”, McGraw-Hill)
Introdução:
▲ Em geral, está em Equilíbrio Hidrostático, mas, nem sempre tem configuração estática. »» Durante sua evolução, sofre contrações e expansões,em pelo menos parte de suas camadas internas. Se forem suficientemente lentas, ≡ ≡ ≡ ≡ sistema em equilíbrio a qualquer momento ► ► processo quase-estático, ou reversível (i.é, pode ocorrer no sentido inverso) Processos ocorrendo corriqueiramente no interior estelar podem , assim, ser tratados como adiabáticos

4
»» Uma como um todo, deve obedecer às leis da termodinâmica dos processos irreversíveis ≡ ≡ ≡ ≡ de não-equilíbrio.
► Aproximação geralmente feita: dividir a em camadas, cada uma delas em equilíbrio.
4.1: A Lei de Stefan-Boltzmann
»» De antes: ≡≡
lei de Stefan-Boltzmann, deduzida
leis da Termodinâmica + processos quasi-estáticos:
1ª lei da termodinâmica (1LT), (4.1)

5
, sendo o calor absorvido pelo sistema, a variação da energia interna e o trabalho realizado pelo
2ª lei da termodinâmica (2LT), (4.2) ,
sendo a variação de entropia do sistema, ►
► ;
» Em geral, E = E(V,T) e deve-se escrever:
(4.3) ;
Como em geral, também S = S(V,T), ►
(4.4) ; sendo

6
E conclui-se:
(4.5) .
» Relembrando que é a densidade de energia por V,
vem que E = U(T) V. Daí,
(4.6) e (4.7) .
▲ Para um gás de fótons, e de (4.5) – (4-7),
, cuja integral ► U = const. X T4lei de Stefan-Boltzmann

7
4.2: Calores Específicos (gases perfeitos):
▲ Algumas relações termodinâmicas p/ os gases perfeitos:
»» de , com E = E(T) ► (4.8)
onde agora ≡ o volume específico.
»» Introduzamos oscalores específicos a volume constante e a pressão constante:
(4.9) e (4.10) .
(cf. Reif, cap. 3)

8
Utilizando agora a eq. de estado dos Gases Perfeitos,
considerando constante (razoável!) e
R ⁄ = constante dos gases ⁄ grama de matéria
► (4.11) .
»» Para dQ, de (4.8) e (4.11) ,
(4.12)
» O cP fica: (4.13) .
» E a razão dos calores específicos, (4.14) .

9
»» Para gás perfeito monoatômico (cf. Reif), E = 3/2 NkT , donde
e como , segue que:
(4.15) , o que nos fornece o resultado clássico
= 5/3 que vale para um gás ideal monoatômico .
► É possível mostrar que depende de f ≡ ,
f ≡ número de graus de liberdade da partícula, sendo
= 1 + 2 ⁄ f , e para f = 3, = 5 ⁄ 3

10
4.2: Expansão Adiabática de um Gás:
»» Da 1LT (p/ unidade de massa) ►
e como com se obtém
Como, para um gás ideal cP e cV são ctes.,
Integrando T V -1 = constante (4.16)
►► outras formas dessa equação:
PV = cte. , P 1- T = cte. , T = cte. -1 (4.17)
Reif

11
»» em termos das variações adiabáticas dos parâmetros, podemos escrever:
(4.18) e (4.19)
variações adiabáticas num gás perfeito não degenerado.
»» O Gradiente Adiabático é uma grandeza que aparece
amiúde no interior das s :
(4.20) .
Para um gás perfeito (eq. 4.18), (4.21) .
»» Ex.: gás perfeito monotômico ►
► = 5/3 e = 2/5
Entropia constante

12
4.4: Efeito da Pressão de Radiação
»» s + massivas : Pr pode ser importante → Pg .
Examinemos a expansão adiabática de um gás ideal, não DG e monoatômico, levando em conta Pr :
(4.21)
A energia interna ≡ energia cinética do gás:
e,
Ptotal

13
» Por outro lado, da 1ªLT,
e das eqs. anteriores,
Como a expansão é adiabática,
(4.22) , onde , e
Analogamente,
(4.23) .

14
»» Por analogia com o gás de partículas,
► define-se os
Expoentes Adiabáticos de Chandrasekhar,
de modo a conservar a forma das eqs.:
(4.24) , (4.25) e
(4.25) ; das relações acima obtém-se:
(4.26) .
»» E quanto vale para um gás com patclas. + radiação?

15
da definição do gradiente, e de
(4.27)
»» Outras relações que podem ser obtidas para os :

16
»» Exs. Práticos de valores dos e : ( )
≡ ≡ gás de partículas, sem radiação;
≡ ≡ gás só de fótons
= 5/3
= 5/3
»» Finalmente, Gradientes de T, P e podem ser deduzidos
das eqs. dT/T... e dP/P...: exs.,
Euler Lagr.

17
4.5: Gás Parcialmente Ionizado (caso + real!)
»» Se nesse gás ocorre p.ex. que
T , Grau de ionização , ≡ ≡ Grande Gasto de Energia e
Termodinâmica ≠ da de um gás neutro ou ionizado
{gás com calor específico grande}
ne ≠ constante
»» Em ET, as populações relativas de dois níveis de energia
j e k de um elemento X no estágio de ionização r são dadas
pela equação de Boltzmann,
(4.28) , sendo

18
onde
≡ pesos estatísticos dos níveis
e ≡ as energias desses níveis.
» Generalizando essa equação, obtém-se, a distribuição
dos átomos do elemento X nos diversos estágios de
ionização
(4.29), onde
= densidade de elétrons e
equação de ionização de Saha:
≡ função de partição:

19
a função de partição do átomo X no estágio de
ionização r é:
NOTA: j e k ≡ Estados de Excitação;
r ≡ Estágio de ionização
»» Em ET, equações de Boltzmann e Saha populações de cada nível e cada estágio de ionização
dos átomos do gás, conhecidos os gs , fr , H , etc...
»» P.ex., seja um gás de H puro em ET; nele ocorrem
H+ + e- H0 + H ,

20
H+ + e- H0 + H , onde H = 13,6 eV é o
potencial de ionização do nível fundamental do H
NOTA: SUPONDO UM ÚNICO NÍVEL PARA O H
» Nesse caso, a eq. de Saha será
, n+ = np, n0 = n de H neutro
(4.30)
Relações úteis:
13,6 eV

21
»» Podemos então, determinar as populações relativas
e o grau de ionização x do gás, ou seja,
a fração do gás de H puro que se encontra ionizada:
= (n+ ⁄ n) = ne ⁄ n ≡ y ,
ou seja, p/ H neutro e para H
totalmente ionizado.
» A eq. de SAHA pode então ser escrita:
(4.31)

22
»» NA VIDA REAL:
aplica-se a equação de Saha sucessivamente a todas as espécies de partículas existentes no gás grau de ionização de todos os componentes.
»» Ex. com o Sol:
(H puro)
interior, >P, >T
regiões superficiais
fig. 5.1

23
»» AINDA NA VIDA REAL: (Natureza camarada...)
a) geralmente, DOIS estágios de ionização bastam
e as zonas de ionização respectivas são separadas;
b) geralmente, apenas ALGUNS níveis atômicos
precisam ser considerados.
{cf. referências s/ o assunto em Maciel, pg. 110}
»» ALGUNS RESULTADOS (Gás de H puro,
parcialmente ionizado) :

24
1) Calores Específicos:
da definição dos mesmos
(4.32)
(4.33)
, sendo
, n = H + H+ + ne = H + 2H+ e
V ≡ volume específico = Vol./massa (cm3g-1) , e ne ,
H+ + H = Na ⁄ V , Na ≡ nº de Avogadro

25
» Variação de cP e cV com xH :
p/ H neutro, =1 e ordenada=cP/c0
p/ H ionizado, =1/2 e ord.= 2cP/c0
xH = fração do gás ionizada ≡
≡ grau de ionização do gás
nas regiões intermediárias, os c , pois precisa-se de > E
para a ionização.
cP ⁄ cV não varia com xH
c0 ci
ci = 2 c0, pois o número de ptclas. livres = 2x >
fig. 5.2

26
2) s :
»» Em geral, Mas, s ~1
A partir das definições dos
(4.35)
... e suas variações, para T≃104 K (≡ interior de
uma estrela)

27
(só H...; porém, como ele é o + abundante, a figura abaixo é bastante representativa)
3) Gradiente adiabático:
como e , também muda.
variações rápidas nas regiões
0 – 1% e 99 – 100%;
< 4/3 (~1,33) ≡ instabilidades
ISTO É,
Na > parte do tempo, a ionização age como fator desestabilizante
5 – 95%
fig. 5.3

28
»» Num gás de H puro parcialmente ionizado,
(4.36)
Ei-lo, nas camadas externas do Sol:
ou seja, se xH , ad , pois
E é gasta com ionização

29

30

31

32

33
Havera DG se:
Trans. Relat-nao rel.

34













![Download [3.72 MB]](https://static.fdocument.pub/doc/165x107/587892181a28aba5258b53fe/download-372-mb.jpg)