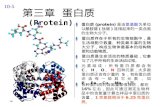
第七章食品质量检验 第一节检验制度、计划与组织 一、食品质量检验制度 讨论: 谈谈你是如何认识质量检验与质量管理的关系? 是不是可以取缔质量检验?
第三章 物质的量
description
Transcript of 第三章 物质的量

第三章 物质的量第三章 物质的量第二课时、摩尔质量第二课时、摩尔质量

引言 引言 在初中我们学习过相对原子质量。回忆 :回忆 : 什么叫相对原子质量 ? 其数学表达式如何写
?相对原子质量 =
一个某原子的质量 ( 克 )
1/12 ×× 一个 C-12 原子质量 ( 克 )
1mol 某原子的质量 ( 克 )=1/12 ×× NNAA 个 C-12 原子质量 (
克 )1mol 某原子的质量 ( 克 )=1/12 ××
结论 :1 摩尔某原子的质量以克为单位 , 在数值上正好等于该原子的相对原子质量结论 :1 摩尔某原子的质量以克为单位 , 在数值上正好等于该原子的相对原子质量
如 :1 摩尔 O 的质量为
16 克;
1 摩尔 S 的质量为
32 克;1 摩尔 Na 的质量
为23 克;
1 摩尔 H 的质量为
1 克 ;
×N×NAA
×N×NAA
12 克 1 克

填空: 填空: 1molHCl 的质量为 ( ) 克 =1molH 的质量 +1molCl 的质
量 =1克
+35.5克
36.5
数值上正好等于 HCl 的式量1molH2O 的质量为 ( ) 克 =2molH 的质量 +1molO 的质量
= 2×× 1 克 +16 克18
数值上正好等于 H2O 的式量 1 摩尔分子的质量以克为单位 , 在数值上正好等于该分子的式量 .
1molNaCl 的质量为 ( ) 克 =1molNa+ 的质量 +1molCl- 的质量
= 233 克 + 35.5 克数值上正好等于 NaCl 的式量
1 摩尔离子化合物的质量以克为单位 , 在数值上正好等于该离子化合物的式量 .
58.5

1molOH- 的质量为 ( ) 克 ; 1mol Na+ 的质量为 ( ) 克
17 23 1 摩尔分子的质量以克为单位 , 在数值上正好等于该分子的式量 .
结论: 结论: 1mol 任何物质的质量以克为单位 , 在数值上正好等于该物质的式量。
二、摩尔质量1. 定义:
2. 单位 :
1 摩尔物质具有的质量或单位物质的量的物质具有的质量。符号:用 M 表示。克 / 摩或 g/mol 或 g .mol - 1
3. 数值:等于该物质的式量。

判断: 判断:下面叙述是否正确?( 1 ) 1 摩尔硫酸的质量等于其式量 ( ); ( 2 ) 1 摩尔硫酸的质量等于 98 克 ( ); ( 3 )硫酸的摩尔质量等于98( ); ( 4 )硫酸的摩尔质量为 98 克 ( ); ( 5 )硫酸的摩尔质量为 98 克 / 摩 ( ); ( 6 ) 1 摩尔氧的质量为 32 克 ( ); ( 7 ) 1 摩尔 O 为 16 克 ( ); ( 8) 1 摩尔 O2 的质量为 32 克 ( ); ( 9 ) 1 摩尔 O2 的质量为 32 克 / 摩 ( ) .
××××
××××
×× 有了摩尔质量
3. 宏观与微观之间换算:
M
NA
.. NA
质量质量( 克 )m
物质的量物质的量 ( 摩尔 ) n
微粒数微粒数( 个 )N
.
.
M
M - 摩尔质量(克 / 摩)NA - 阿伏加德罗常数 ( 近似值 :6.02 ×× 1023)
物质的量象“桥梁”

[ 例 1] 90 克水相当于多少摩水 ?
解 : 水的式量是 18,
水的摩尔质量是 18g/mol 。
n (H2O) = 90g
18g/mol= 5 mol
答: 90 克水相当于 5mol 水。

[ 例 2] 2. 5 mol 铜原子的质量是 多 少克 ?解 : 铜的原子量是 63. 5 , 铜的摩尔质量是 63.5 g/mol 。
m (Cu) = ×× 2.5 mol63.5g/mol= 158.8g
答: 2.5mol 铜原子的质量等于 158.8g 。

[ 例 3] 4. 9 克硫酸里含有多少个硫酸分子 ?
解 : 硫酸的式量是 98,硫酸的摩尔质量是 98g/mol 。
n (H2SO4) = 4. 9 g
98g/mol = 0.05 mol
答: 4.9 克硫酸里含有 (3.01)(1022) 个硫酸分子。
N (H2SO4) = 0.05 ×× 6.02 ×× 1023
= 3.01 ××1022 (个)

[ 练习 ] 20. 2 克硝酸钾中,氧元素的质量是多少克 ?
解 : 硝酸钾的式量是 101,
硝酸钾的摩尔质量是 101g/mol 。
n (KNO3) = 20.2 g
101g/mol = 0.2 mol
答: 20.2 克硝酸钾中,氧元素的质量是 9. 6 g 。
n (O) = 0.2 mol××3 = 0.6 mol
m (O) = 0. 6 mol ××16g/mol = 9.6 g

试试看:试试看:
1 、 24.5 克硫酸的物质的量是 mol ;2 、 1.5mol 硫酸的质量是 克,其中含有 mol O ,其质量是 克;3 、 0.01 mol 某物质的质量是 1.08 克,此物质的摩尔质量为 ;4 、 71 克 Na2SO4 中含 Na+ mol,
个 .

试试看:试试看: 例题 1 、 Cl2 、 HCl 、 O2 、 H2 、 CO2 各 5 克,按其所含分子数目由多到少的顺序排列是。
H2> O2> HCl> CO2 >Cl2
例题 2 、欲使 SO2 与 SO3 中氧元素质量相等, SO2 与 SO3 的质量比为多少?6 : 5
例题 3 :下列各物质中,含氧原子个数最多的是:( ) A 、 1molKClO3 B 、 0.5molH2SO4
C 、 32 克 O2 D 、 3.01×1023 个 CO2
A

试试看:试试看: 【练习】1 、如果 1 克水中含有 m 个氢原子,则阿伏加德罗
常数是( ) A 、 m/9 B 、 9m C 、 2m D 、
m/2
B
2 、 1 个氧原子的质量为 m 克,若阿伏加德罗常数为 NA ,下列式子可表示 12C 原子的质量是( )
A 、 12/NA 克 B 、 m/16 克 C 、 3m/4 克 D 、 mNA 克
AC
3 、已知 n 个原子质量为 b 克,则 b 个该原子的原子量之和是( )
A 、 6.02×1023b2/n B 、 b2/n C 、 n /b2 D 、 6.02×1023b
A

小 结 本节课我们主要学习了摩尔质量、宏观与微观之间换算之间的换算。二、摩尔质量1. 定义:
2. 单位 :
1 摩尔物质具有的质量或单位物质的量的物质具有的质量。
或 g/mol 或 g .mol - 1
3. 数值:等于该物质的式量。4. 宏观与微观之间换算:
NA 质量质量( 克 )m
物质的量物质的量 ( 摩尔 ) n
微粒数微粒数( 个 )N
.
.
M
M - 摩尔质量(克 / 摩)NA - 阿伏加德罗常数 ( 近似值 :6.02 ×× 1023)
物质的量象“桥梁”
M.. NA
克 / 摩

同学们再见同学们再见
2004 年 10月